江西省鹰潭市第一中学人教版高中化学选修1 化学与生活 第一章 第三节 生命的基础—蛋白质(第2课时)
高中化学选修1全册教案

高中化学选修1 化学与生活全册教案第一章关注营养平衡第一节生命的基础能源----糖类教学目标:1. 使学生掌握葡萄糖、蔗糖、淀粉、纤维素的组成和重要性质,以及它们之间的相互转变和跟烃的衍生物的关系.2. 了解合理摄入营养物质的重要性,认识营养均衡与人体健康的关系。
3. 使学生掌握葡萄糖蔗糖淀粉的鉴别方法.教学重点:认识糖类的组成和性质特点。
教学难点:掌握葡萄糖蔗糖淀粉的鉴别方法教学方法:讨论、实验探究、调查或实验、查阅收集资料。
教学过程:[问题]根据P2~P3图回答人体中的各种成分。
我们已经知道化学与生活关系多么密切。
在这一章里,我们将学习与生命有关的一些重要基础物质,以及它们在人体内发生的化学反应知识。
如糖类、油脂、蛋白质、微生素和微量元素等。
希望学了本章后,有利于你们全面认识饮食与健康的关系,养成良好的饮食习惯。
[导入]讨论两个生活常识:①“饭要一口一口吃”的科学依据是什么?若饭慢慢地咀嚼会感觉到什么味道?②儿童因营养过剩的肥胖可能引发糖尿病来进行假设:这里盛放的是三个肥儿的尿样,如何诊断他们三个是否患有糖尿病?今天我们将通过学习相关知识来解决这两个问题.下面我们先来学习糖类的有关知识。
糖类: 从结构上看,它一般是多羟基醛或多羟基酮,以及水解生成它们的物质. 大部分通式Cn (H2O)m。
糖的分类: 单糖低聚糖多糖一、葡萄糖是怎样供给能量的葡萄糖的分子式: C6H12O6、白色晶体,有甜味,溶于水。
1、葡萄糖的还原性结构简式: CH2OH-CHOH-CHOH-CHOH-CHOH-CHO或CH2OH(CHOH)4CHO。
2、葡萄糖是人体内的重要能源物质C 6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)3、二糖(1)蔗糖:分子式:C12H22O11物理性质:无色晶体,溶于水,有甜味化学性质:无醛基,无还原性,但水解产物有还原性。
C 12H22O11+ H2O C6H12O6+ C6H12O6(蔗糖) (葡萄糖) (果糖)(2)麦芽糖: 物理性质: 白色晶体, 易溶于水,有甜味(不及蔗糖). 分子式: C 12H 22O 11(与蔗糖同分异构) 化学性质:(1)有还原性: 能发生银镜反应(分子中含有醛基),是还原性糖. (2)水解反应: 产物为葡萄糖一种. C 12H 22O 11 + H 2O 2 C 6H 12O 6(麦芽糖) (葡萄糖) 二、淀粉是如何被消化的 1.淀粉的存在:淀粉主要存在于 和 。
2019人教版高中化学选修1《化学与生活》全册教案

第一章化学与生活课题:第一节生命的基础能源——糖类知识与技能:1. 使学生掌握糖类的主要代表物: 葡萄糖、蔗糖、淀粉、纤维素的组成和重要性质,以及它们之间的相互转变和跟烃的衍生物的关系.2. 了解合理摄入营养物质的重要性,认识营养均衡与人体健康的关系。
3. 使学生掌握葡萄糖蔗糖淀粉的鉴别方法.过程与方法:通过日常生活中的一些事例来讲解具体的内容。
情感、态度、价值观:使学生认识到糖类物质对人的重要性。
教学重点、难点:认识糖类的组成和性质特点。
课时划分:二课时第一课时[问题]根据P2~P3图回答人体中的各种成分。
[演讲]生命本身就是一种奇迹,只要走进大自然无论是公园、农田、森林、草原,还是崇山峻岭,江河湖海,你们就会发现有多种多样的动物和植物。
生命要为生存而感激太阳,同时也要感谢把能量转化为生命物质的化学过程。
我们已经知道化学与生活关系多么密切。
在这一章里,我们将学习与生命有关的一些重要基础物质,以及它们在人体内发生的化学反应知识。
如糖类、油脂、蛋白质、微生素和微量元素等。
希望学了本章后,有利于你们全面认识饮食与健康的关系,养成良好的饮食习惯。
[导课]我们来讨论两个生活常识:①“饭要一口一口吃”的科学依据是什么?若饭慢慢地咀嚼会感觉到什么味道?②儿童因营养过剩的肥胖可能引发糖尿病来进行假设:这里盛放的是三个肥儿的尿样,如何诊断他们三个是否患有糖尿病?今天我们将通过学习相关知识来解决这两个问题.下面我们先来学习糖类的有关知识。
[板书] 第一章化学与生活第一节生命的基础能源——糖类[设问]如果有人问“今天你吃糖了吗?”你将怎样回答?[回答]学生讨论后回答:吃糖了,因为淀粉就属于糖类。
[讲述] 糖类是绿色植物光合作用的产物。
糖类是生物进行生命活动的重要物质,动物(包括人)消耗的能量大部分来自于糖类的分解。
我国居民食物构成中大约75%来自糖类,淀粉就属于糖类,淀粉就属于糖类。
[资料]表1—1含糖食物与含糖量食物蔗糖粉丝等大米、面粉、玉米等苹果、桃、葡萄等含糖量[设问]根据我们以前所学的知识,谁来回答什么是糖?哪些物质属于糖?[学生讨论] 回答:糖类是由C、H、O三种元素组成的一类有机物,糖类也叫做碳水化合物。
人教版高中化学选修1《化学与生活》全册教案

第一章化学与生活课题:第一节生命的基础能源——糖类知识与技术 :1.使学生掌握糖类的主要代表物:葡萄糖、蔗糖、淀粉、纤维素的组成和重要性质, 以及它们之间的互相转变和跟烃的衍生物的关系.2.认识合理摄取营养物质的重要性,认识营养平衡与人体健康的关系。
3.使学生掌握葡萄糖蔗糖淀粉的鉴别方法.过程与方法:经过平时生活中的一些事例来讲解详尽的内容。
感情、态度、价值观:使学生认识到糖类物质对人的重要性。
授课重点、难点:认识糖类的组成和性质特点。
课时划分:二课时第一课时[ 问题 ] 依照 P2~P3图回答人体中的各种成分。
[ 演讲 ] 生命自己就是一种奇景,只要走进大自然无论是公园、农田、森林、草原,仍是崇山峻岭,江河湖海,你们就会发现有多种多样的动物和植物。
生命要为生计而感谢太阳,同时也要感谢把能量转变成生命物质的化学过程。
我们已经知道化学与生活关系多么亲近。
在这一章里,我们将学习与生命相关的一些重要基础物质,以及它们在人体内发生的化学反响知识。
如糖类、油脂、蛋白质、微生素和微量元素等。
希望学了本章后,有益于你们全面认识饮食与健康的关系,养成优秀的饮食习惯。
[ 导课 ] 我们来讨论两个生活知识:①“饭要一口一口吃”的科学依照是什么 ?若饭慢慢地咀嚼会感觉到什么味道 ?②儿童因营养节余的肥胖可能惹起糖尿病来进行假设:这里盛放的是三个肥儿的尿样,怎样诊断他们三个可否患有糖尿病?今天我们将经过学习相关知识来解决这两个问题. 下面我们先来学习糖类的相关知识。
[板书]第一章化学与生活第一节生命的基础能源——糖类[ 设问 ] 倘如有人问“今天你吃糖了吗?”你将怎样回答?[ 回答 ] 学生讨论后回答:吃糖了,由于淀粉就属于糖类。
[ 表达 ]糖类是绿色植物光合作用的产物。
糖类是生物进行生命活动的重要物质,动物(包括人)耗资的能量大多数来自于糖类的分解。
我国居民食品组成中大体75%来自糖类,淀粉就属于糖类,淀粉就属于糖类。
高二化学选修1《化学与生活》

有多元醇和醛的性质
、烟酸、烟酰胺、
+H
有酸和酯的性质:能与碱中和、水解,与醇酯化,不易溶于水
明代李时珍《本草纲目》天然药物
治疗支气管哮喘、鼻黏膜充血引起的鼻塞,
会由于中枢神经兴奋会失眠、不安,可作兴奋剂合金一般比纯金属硬度大、熔点低
99.5%
金属与周围的接触到物质直接接触而被腐蚀的过程
玻璃、陶瓷和水泥
光导纤维、高温结构陶瓷、超硬陶瓷、生物陶瓷、超导陶瓷
四特性(耐高温、电学特性、光学特性、生物功能)主要成分合成树脂(高聚物),还含有增塑剂和防老化剂等添加剂
2CO。
高二化学选修1《化学与生活》
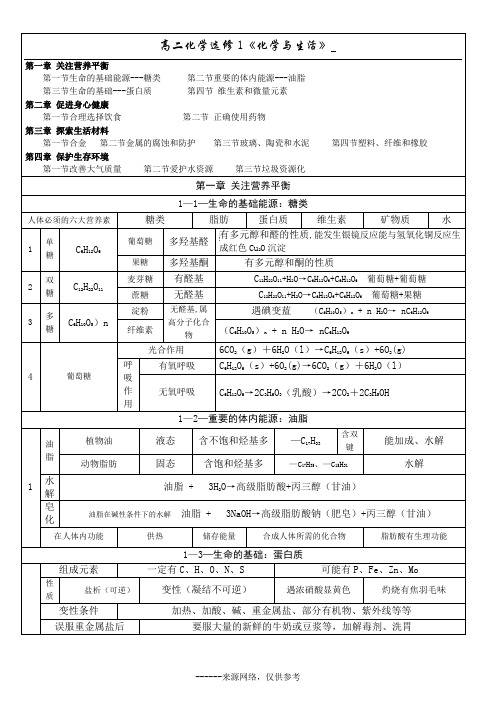
高二化学选修1《化学与生活》第一章关注营养平衡第一节生命的基础能源---糖类第二节重要的体内能源---油脂第三节生命的基础---蛋白质第四节维生素和微量元素第二章促进身心健康第一节合理选择饮食第二节正确使用药物第三章探索生活材料第一节合金第二节金属的腐蚀和防护第三节玻璃、陶瓷和水泥第四节塑料、纤维和橡胶第四章保护生存环境第一节改善大气质量第二节爱护水资源第三节垃圾资源化第一章关注营养平衡1—1—生命的基础能源:糖类人体必须的六大营养素糖类脂肪蛋白质维生素矿物质水1 单糖C6H12O6葡萄糖多羟基醛有多元醇和醛的性质,能发生银镜反应能与氢氧化铜反应生成红色Cu2O沉淀果糖多羟基酮有多元醇和酮的性质2 双糖C12H22O11麦芽糖有醛基C12H22O11+H2O→C6H12O6+C6H12O6葡萄糖+葡萄糖蔗糖无醛基C12H22O11+H2O→C6H12O6+C6H12O6葡萄糖+果糖3 多糖C6H10O5)n淀粉无醛基,属高分子化合物遇碘变蓝(C6H10O5)n + n H2O→ nC6H12O6纤维素(C6H10O5)n + n H2O→ nC6H12O64 葡萄糖光合作用6CO2(g)+6H2O(l)→C6H12O6(s)+6O2(g)呼吸作用有氧呼吸C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)无氧呼吸C6H12O6→2C3H6O3(乳酸)→2CO2+2C2H5OH1—2—重要的体内能源:油脂1 油脂植物油液态含不饱和烃基多—C17H33含双键能加成、水解动物脂肪固态含饱和烃基多—C17H35、—C15H31水解水解油脂 + 3H2O→高级脂肪酸+丙三醇(甘油)皂化油脂在碱性条件下的水解油脂 + 3NaOH→高级脂肪酸钠(肥皂)+丙三醇(甘油)在人体内功能供热储存能量合成人体所需的化合物脂肪酸有生理功能1—3—生命的基础:蛋白质组成元素一定有C、H、O、N、S可能有P、Fe、Zn、Mo性质盐析(可逆)变性(凝结不可逆)遇浓硝酸显黄色灼烧有焦羽毛味变性条件加热、加酸、碱、重金属盐、部分有机物、紫外线等等误服重金属盐后要服大量的新鲜的牛奶或豆浆等,加解毒剂、洗胃水解蛋白质多肽二肽氨基酸氨基酸官能团羧基(-COOH)有酸性、氨基(-NH2)有碱性人体必需赖氨酸蛋氨酸亮氨酸异亮氨酸缬氨酸苯丙氨酸苏氨酸色氨酸酶具有催化作用的蛋白质条件温和专一性高效性多样性1—4—维生素和微量元素1维生素:参与生物生长发育和新陈代谢所必需的一类小分子有机物分类脂溶性维生素难溶于水易溶于有机溶剂,不易排泄,内存于肝脏A、D、E、K 水溶性维生素易溶于水易吸收,多余随尿道排出,不内存,易缺乏B族、C1维生素B族B1、B2、烟酸、烟酰胺、B6、生物素、泛酸、叶酸、B12等缺乏病缺乏维生素 A会出现夜盲症、干眼病和皮肤干燥,使儿童生长受阻服鱼肝油缺乏维生素D易患佝偻病、软骨病多晒太阳缺乏维生素B1易患脚气病用粗粮缺乏维生素B2易患舌炎缺乏维生素B12易患恶性贫血缺乏维生素C易出现坏血病多吃水果维生素C抗坏血酸,多羟基不饱和酯,可以表现烯烃、醇和酯的性质,有较强的还原性2微量元素16种含量在0.01%以下Fe、Cu、Zn、Mn、Co、Mo、Se、I、Li、Cr、F、Sn、Si、V、As、B 常量元素11种含量在0.01%以上C、H、O、N、Na、Mg、Ca、P、S、K、Cl碘智力元素甲状腺和多种酶缺乏会甲状腺肿、克汀病、IDD盐中加KIO3、海带铁造血元素人体血红蛋白中含Fe2+缺乏会贫血铁强化酱油、蔬菜水果硒Se 抗癌元素氟 F 防龋齿加 NaF过多会骨质疏松锌提高免疫力第二章促进身心健康2—1—合理选择饮食1 水在人体内的作用人体重要成分良好的溶剂调节体温2 食物的酸碱性按食物在人体内代谢的最终产物的酸碱性(不是本身的性质)酸性食物由C、H、O、N等非金属元素组成的蛋白质代谢产物为弱酸性碱性食物含K、Ca、Na、Mg等金属盐的水果、蔬菜代谢产物为弱碱性人体血液的PH7.35-7.45<7.36酸中毒>7.45碱中毒尿液偏酸性叫多酸症人体细胞内酸碱平衡CO2+H2O H2CO3HCO3-H2PO4- HPO42-3食品添加剂着色剂分天然和人造胡萝卜素、胭脂红、柠檬黄、苋菜红、(苏丹红)婴儿食品不加色素调味剂食盐咸,过多会高血压,味精过多过敏口渴等,醋有酸味防腐剂食盐、糖、醋、苯甲酸钠、硝酸盐、二氧化硫、亚硝酸钠(可变成亚硝胺)营养强化剂食盐中加碘(KIO3)、酱油中加铁、粮食中加赖氨酸、食品加维生素、钙、硒、锗2—2—正确使用药物人工1解热镇痛药阿司匹林乙酰水杨酸防止心脏病、减缓视力衰退、提高免疫力合成药物水解 + H2O→ + CH3COOH有酸和酯的性质:能与碱中和、水解,与醇酯化,不易溶于水长期使用有胃肠道反应、水杨酸反应(中毒)要停药并注射NaHCO32 抗生素(英国弗莱明发现)青霉素阻止多种细菌生长有F、G、X、K、V结构骨干为青霉酸青霉素G的钠盐叫盘尼西林,良效的广谱抗生素(与原子弹、雷达为三大发明)不良反应:过敏反应(过敏性休克)要皮肤敏感试验,过度使用会无药可用3 抗酸药中和胃酸(弱碱性):NaHCO3、CaCO3、MgCO3、Al(OH)3、Mg(OH)2天然药物取自植物、动物、矿物;明代李时珍《本草纲目》天然药物1892种、药方11096个麻黄碱(麻黄中提炼)治疗作用治疗支气管哮喘、鼻黏膜充血引起的鼻塞,不良反应会由于中枢神经兴奋会失眠、不安,可作兴奋剂买药处方符号R—表示处方药OTC—表示非处方药毒品鸦片由罂粟未成熟的果实浆汁干燥得棕褐色膏状物止泻、镇痛消咳吗啡鸦片中主要的生物碱,剧烈麻醉剂海洛因由吗啡和乙酸酐反应得,叫二乙吗啡,白色粉末又称白粉、白面、毒品之王冰毒甲基苯丙胺,无色晶体,中枢神经兴奋剂药物研究的新成果药物的微囊化药物的缓释第三章探索生活材料3—1—合金合金定义由两种或两种以上金属(或与非金属)熔合而成的具有金属特性的物质优点合金一般比纯金属硬度大、熔点低,良好的物理、化学和机械的性能铁的合金生铁含碳量2%~4.3% 生铁硬度大、抗压、性脆,可铸不可锻钢0.03%~2% 有良好的延展性,机械性能好,可铸可锻钢普通钢又叫碳素钢含碳量高,硬度大;含碳量低,韧性较强特种钢又叫合金钢例:不锈钢中加Ni、Cr,不易生锈,抗腐蚀力强2 铝合金抗蚀力强,强度大,密度较小硬铝:Al中加少量Cu、Mg、Si、Mn、Zn及稀土元素3 铜合金黄铜:Cu中加Zn青铜:Cu中加Sn4 黄金合金24K(含金量99.5%以上)18K(含金量约75%)5 新型合金储氢合金吸收大量的氢气成氢货物后稍稍加热易分解钛合金密度小、强度高、耐高温和抗腐蚀,常用于制造飞机起落架耐热合金常用于制造喷气式飞机的发动机叶片形状记忆合金变形后加热到一定的跃变温度时,又可变回到原来的形状泡沫金属质轻、吸音、隔热、吸收电磁波3—2—金属的腐蚀和防护1 定义金属或合金与周围的接触到的气体或液体进行氧化还原反应而腐蚀损耗过程本质金属单质失电子而被氧化成金属阳离子的过程2 化学腐蚀金属与周围的接触到物质直接接触而被腐蚀的过程电化腐蚀不纯金属或合金与电解质溶液发生原电池反应较活泼的金属被的腐蚀3 钢铁电化析氢腐蚀水膜为弱酸性-负极Fe Fe-2e- = Fe2++正极C 2H++2e- = H2↑腐蚀吸氧腐蚀更普遍、危害大水膜为中性或弱碱性-负极Fe Fe-2e- = Fe2++正极C O2+ 2H2O + 4e- =4OH -4 防护方法改变金属的内部结构不锈钢在金属表面覆盖保护层加塑料、搪瓷、金属等电化学保护法加一块比要保护的金属活泼的金属3—3—玻璃、陶瓷和水泥1 传统无机非金属材料玻璃、陶瓷和水泥新型无机非金属材料光导纤维、高温结构陶瓷、超硬陶瓷、生物陶瓷、超导陶瓷四特性(耐高温、电学特性、光学特性、生物功能)2 硅酸盐材料玻璃纯碱、石英、石灰石Na2SiO3、CaSiO3、SiO2透明、可软化、陶瓷黏土抗氧化、酸碱、耐高温、绝缘水泥黏土、石灰石、石膏3CaO.SiO2、2CaO.SiO2、3CaO.Al2O3、有水硬性,作建材,不能长放,防潮,保质期3个月玻璃普通玻璃本身含二价铁(Fe2+)都呈淡绿色铅玻璃加入PbO光学玻璃折光率高制眼镜片、透镜硼酸盐玻璃加入B2O3或硼砂膨胀系数低.耐高温、抗化学腐蚀制高级化学反应容器有色玻璃加入Cu2O红色玻璃加入Co2O3蓝色玻璃加入AgBr和CuO成变色玻璃钢化玻璃普通玻璃加热软化后,用冷风急吹成机械强度大4-6倍,抗震裂,破碎没尖棱角陶瓷陶瓷中国陶都:江苏宜兴紫砂壶中国瓷都:江西景德镇景泰蓝彩釉在普通釉料中加一些重金属离子:Fe Cu Mn Cr Co(如唐朝的唐三彩)水泥水泥的等级01年4月中国新标准42.5、52.5、62.5三个等级,等级越高,性能越好水泥砂浆水泥、沙子、水的混合物建筑的黏合剂混凝土水泥、沙子、碎石和水的混合物建筑钢筋混凝土水泥、沙子、碎石、钢筋和水的混合物强度大,建高楼大厦、桥梁新型光导纤维高纯度的SiO2拉出的100μm的细丝光抗干扰性好、通信质量高、传输量大高温结构陶瓷Si3N4、Al2O3、SiC、ZrO2汽车的发动机、航天飞机防护片3—4—塑料、纤维和橡胶1塑料主要成分合成树脂(高聚物),还含有增塑剂和防老化剂等添加剂,一定属人工合成的热塑性塑料线形结构受热会熔化、冷却会硬化,多次使用如聚乙烯塑料,聚丙烯塑料等热固性塑料受热会交联成立体网状结构,一次使用酚醛树脂,脲醛树脂等导电聚合物聚乙炔掺杂碘后能导电抗静电添加剂、有机发光二极管等聚乙烯PE 聚氯乙烯PVC 不包食品聚丙烯 PP聚苯乙烯PS 聚甲基丙烯酸甲酯有机玻璃 PMMA脲醛塑料电玉聚四氟乙烯PTFE 塑料王2 自然界天然纤维属纤维素:棉花、麻等属蛋白质:羊毛和蚕丝等人造纤维用木材等为原料加工成的人造棉、人造丝、玻璃纸等仍属纤维素合称为化学纤合成纤维(六大纶)用石油、天然气、煤核农副产品等为原料人工合成的高分子材料锦纶(尼龙)、涤纶(的确良)、腈纶(人造羊毛)、维纶、氯纶、丙纶维3天然橡胶聚异戊二烯合成橡胶通用橡胶丁苯橡胶、氯丁橡胶、顺丁橡胶特种橡胶耐热耐酸碱的氟橡胶、耐高温耐严寒的硅橡胶一般橡胶线型结构,可塑性好,但强度和韧性差硫化橡胶加硫后通过硫桥交联成立体型的网状结构,强度和韧性高、弹性好、化学稳定4 复合材料一种作基体、一种作增强剂,结合在一起产生有特殊的性能玻璃钢:玻璃纤维熔化后拉丝加入到合成树脂中,强度大、密度小、耐腐蚀、韧性好第四章保护生存环境4—1—改善大气质量1清洁大气N2占78%O2占21%稀有气体CO2水蒸气少量其他杂质微量大气污染颗粒物硫的氧化物氮的氧化物CO碳氢化合物氟氯代烷大气污染危害危害人体健康影响动植物的生长严重时会影响地球的气候全球性三大环境问题酸雨臭氧层受损温室效应2酸雨正常雨水:PH约为5.6酸雨:PH小于5.6我国为硫酸型酸雨,烧煤炭造成硫酸型硫的氧化物转化SO2+H2O=H2SO32H2SO3+O2=2H2SO4大气中烟尘和O3作催化剂硝酸型氮的氧化物转化3NO2+H2O=2HNO3+NO↑3臭氧层自然界的臭氧90%集中在距地面15-50km的大气平流层中吸收自太阳的大部分紫外线氟氯代烷引起的Cl+O3→ClO+O2ClO+O→Cl+O2总式:O3+O→2O2Cl为催化剂 ClO为中间产物一个Cl原子能破坏10万个O3引起臭氧层受损物质氟氯代烷(致冷剂)、哈龙(含溴的灭火剂)、CCl4、N2O、NO 、核弹爆炸产物保护臭氧层公约《保护臭氧层维也纳公约》《关于消耗臭氧层物质的蒙特利尔议定书公约》4温室效应太阳短波辐射可以透过大气射入地面,而地面增暖后放出的长短辐射却被大气中的二氧化碳等物质所吸收,从而产生大气变暖的效应温室效应后果荒漠将扩大,土地侵蚀加重,森林退向极地,旱涝灾害严重,雨量将增加7-11%;温带冬天更湿,夏天更旱;热带也将变得更湿,干热的副热带变得更干旱,两极冰块将熔化,使海平面上升1米多,引起厄尔尼诺现象引起温室效应的物质CO2、CH4、N2O、氟氯代烷5 减少煤等化石燃料燃烧产生污染1、改善燃煤质量2、改进燃烧装置、技术和排烟设备3、发展洁净煤技术和综合利用4、调整和优化能源结构煤的综合利用:煤的的干馏煤的气化煤的液化煤的气化C+H2O(g)=CO+H2煤的液化CO+2H2→CH3OH煤的脱硫2CaCO3+O2+2SO2=2CaSO4+2CO26 减少汽车等机动车尾气污染尾气污染(占大气污染排出总量的40-50%)CO、NO2、NO、碳氢化合物使用无铅汽油四乙基铅作抗爆震剂铅对神经系统损害大尾气系统加催化转化器前半部2CO+2NO 2CO2+N2后半部2CO+O2 2CO2C7H16+11O27CO2+8H2O7 减少室内空气污染室内空气污染CO、CO2、NO2、NO、SO2、尼古丁;甲醛、苯、二甲苯、氡CO 与血红蛋白易结合难分离而缺氧,结合能力是O2的200-300倍甲醛 HCHO有刺激性气味气体过敏性皮炎、免疫异常、中枢神经、致癌氡 Rn无色无味放射性气体岩石、土壤、石材中肺癌,隐性杀手方法1、保持室内外空气流通2、禁止吸烟3、装修用环保材料4—2—爱护水资源1 重金属使人体的蛋白质变性,可通过食物链被富集,人通过饮水和食物摄入而中毒汞Hg 水俣病有机汞更毒镉Cd 痛痛病还有铬、铅等2 植物营养物质污染生活废水和工业废水蛋白质含N、洗涤剂和化肥中含P等植物营养素在分解时大量消耗水中的溶解氧,释放养分,使藻类和浮游生物大量繁殖颜色蓝、红、棕在江河湖泊在出现叫水华在海湾在出现叫赤潮3 改善水质方法物理法、生物法、化学法污水处理程度分一级二级三级化学方法混凝法混凝剂吸附细小悬浮颗粒,用明矾、聚羟基氯化铝、聚丙烯酰胺中和法用熟石灰中和酸性废水,用稀硫酸中和碱性废水沉淀法Hg2++S2-=HgS↓氧化还原法CN-加Cl2被氧化成N2Cr2O72-被还原成Cr3+饮用水消毒用Cl2会生成卤代烃致癌改用ClO24—3—垃圾资源化世界上没有真正的垃圾,只有放错了地方的资源1垃圾处理三原则无害化减量化资源化三方法卫生填埋堆肥焚烧卫生填埋处理量最大,最终手段浪费土地,地表水有重金属堆肥用微生物处理其中的有机物成肥料,但重金属可对土地污染焚烧高温烧成灰渣,再填埋,可发电占地少、减量大、但有空气污染物产生二恶英,其中2、3、7、8-四氯代二苯并二恶英最毒,致癌城市生活垃圾分类标志粗分6个可回收物有害垃圾大件垃圾可堆肥垃圾其他垃圾可燃垃圾细分8个织物瓶罐厨余垃圾电池纸类塑料金属玻璃2 废旧电池含汞作缓蚀剂中国2002年电池低汞化中国2006年电池无汞化医疗垃圾含多种致病菌属高危险性、高污染性废物,要焚烧,但要防产生二恶英3 白色污染废旧塑料(占垃圾5-14%)难降解引起的污染污染土壤、地下水,危害动物、焚烧放毒气处改进配方、生产工艺3R运减量Reduce 再利Reuse 再循Recycle理动化用环热塑性的塑料分类、清洗、热熔热固性的塑料粉碎、加黏合剂成填料再利用的关键塑料的分类回收热裂解法成汽油、乙烯等数据人每天摄入热能来自糖类占 75%正常人的血糖的质量分数约为 0.1%人每天需进食脂肪 50-60克成年人体内储存的脂肪约占体重 10-20%高中生每天摄入蛋白质 80-90克中学生每天需补充维生素C约 60毫克人体内碘的含量仅约占 30毫克每天需补充水约 2.5-4L成年人每天排出铁约 1毫克人体中铁的含量约 4-5克女性月经期排铁约 1-2毫克每天需补充铁约 15-20毫克生理盐水含NaCl 占 0.9%医用酒精含量 75%。
人教版高中化学选修1 化学与生活 第一章 第三节 生命的基础—蛋白质(第1课时)

课件库的建设与应用研究》 (课题编号:GDK-2012-G-72883)
2020/10/2
1
新课标人教版高中化学课件系列
选修1 化学与生活 第一章 关注营养平衡 第三节 生命的基础——油脂
第1课时
2020/10/2
2
生命的基础—蛋白质
丙氨酸(α—氨基丙酸) 苯丙氨酸( α—氨基—β苯基—丙酸)
谷氨酸(α—氨基戊二酸 )
2020/10/2
6
蛋白质的组成和结构
探究思考2:
1、氨基酸的结构式中都有哪些官能团? 氨基、羧基
2、根据官能团决定有机物的性质,推
测氨基酸应具有什么性质?
(1、两性
2、缩合)
2020/10/2
7
蛋白质的组成和结构
2020/10/2
26
蛋白质的组成和结构
氨基酸的两性:
H2N–CH2–COOH + HCl → HOOC–CH2–NH3Cl
显碱性
H2N–CH2–COOH + NaOH → H2N–CH2–COONa + H2O
显酸性 BACK
2020/10/2
27
蛋白质的组成和结构
氨基酸的缩合: O
‖
H2N–CH2–C–OH + H–NH–CH2–COOH →
谢谢大家
31
多 肽 的 一 段
11
蛋白质的组成和结构
2020/10/2
蛋 白 质 的 三 级 空 间 结 构
12
蛋白质的组成和结构
结晶牛胰岛素
1965年我国科技工作者成功合成了具有生物学活性的—结晶牛胰岛素
人教版高中化学选修1 化学与生活 第一章 第三节 生命的基础—蛋白质(第2课时)

2019/4/1
江西省鹰潭市第一中学 桂耀荣
7
酶
四、酶 酶— 特殊的蛋白质,生物制造的催化剂 酶的特性— 离开生物机体后仍具活性 酶的作用— 催化许多有机化学反应和生物体用— 食品、发酵、纺织、制药、制革等
2019/4/1
江西省鹰潭市第一中学 桂耀荣
8
酶
1、下列关于蛋白质的叙述中,正确的是 ( ) A.蛋白质溶液中加(NH4)2SO4溶液可提纯蛋白质。 B.在豆浆中加少量石膏,能使豆浆凝结为豆腐。 C.温度越高,酶对某些化学反应的催化效率越高。 D.任何结构的蛋白质遇到浓HNO3都会变成黄色。 AB
2、为了鉴别某白色纺织物成分是蚕丝还是人造丝,可以选用的方法 是( ) A.滴加浓硝酸 AD B.滴加浓硫酸 C.滴加酒精 D.灼烧
豆腐
红烧虾米豆腐
夹心儿豆腐
绿叶托豆腐
雪花蟹肉豆腐羹
鱼腩烧豆腐 西湖豆腐
2019/4/1
江西省鹰潭市第一中学 桂耀荣
16
豆腐
酸菜鱼炖豆腐汤
宝黄豆腐
麻婆豆腐
蛋美豆腐
豆腐海带汤 2019/4/1
豆腐荤杂烩
豆腐鲫鱼
红烧豆腐 17
江西省鹰潭市第一中学 桂耀荣
豆腐
研究性学习:有趣的豆腐
一、豆腐文化
二、豆腐制作
此ppt下载后可自行编辑
高中化学课件
江西省教育信息技术研究“十二五”规划2012年度课题《基于网 络的高中化学课件库的建设与应用研究》 (课题编号:GDK-2012-G-72883)
主持人:桂耀荣
2019/4/1
江西省鹰潭市第一中学 桂耀荣
3
新课标人教版高中化学课件系列
选修1 化学与生活 第一章 关注营养平衡
高中化学人教版选修一 化学与生活高中化学选修一1.1生命的基础能源—糖类 教案(1)

优质资料---欢迎下载第一章关注营养平衡第一节生命的基础能源----糖类主备教师:李天娥辅备教师:化学组课时计划:3课时一、内容及其解析:本章要学的内容基本营养物质指的是糖类、油脂和蛋白质,其核心是糖类、油脂和蛋白质的组成特点及主要性质。
理解它关键就是在学生学习了几种有机物的基础上,突出从结构角度认识糖类、油脂和蛋白质的性质,可以使学生对有机物的初步认识相对完整。
本节课的内容糖类、油脂和蛋白质就是在此基础上进一步学习有机物的相关知识。
由于它还与烃的衍生物有联系,所以在本学科有着重要的地位,并有对结构与性质的关系进一步深化认识起到重要的作用,是本学科的核心内容。
教学重点是糖类、油脂和蛋白质的组成特点及主要性质;解决重点的关键是从生活经验和通过实验初步了解有机基本反应类型,形成对有机物特殊性的认识,并能从结构认识其反应特点。
二、目标及其解析:1、目标定位:(1)使学生了解糖类的组成和分类(2)使学生掌握葡萄糖的结构简式和重要性质,了解其在人体内的储存方式和氧化分解的生理意义。
(3)使学生了解淀粉在人体内的水解吸收过程和纤维素的生理功能。
2、目标解析:(1)、糖类、淀粉的组成和结构是:都含有C、H、O元素;(2)、糖类、淀粉的共同性质与特征反应是葡萄糖的银镜反应,淀粉与碘的反应,蛋白质的颜色反应。
(3)、糖类、淀粉都会水解。
三、问题诊断分析:在本节课的教学中,学生可能遇到是葡萄糖与弱氧化剂氢氧化铜的反应;油脂的水解,产生这一问题的原因是官能团模糊,不能很好的理解有机反应特殊性。
要解决这一问题,就要从官能团及形成有机反应特殊性,其中关键是能从结构上认识其反应特点。
四、支持条件分析:在本节课基本营养物质的教学中,准备使用多媒体以及演示实验教学。
因为使用多媒体,有利于提高学生学习兴趣,实验教学有利于学生眼见为实加强学生的学习兴趣。
五、教学过程: 第一课时第一部分 自学[新课导入] “果实的事业是尊贵的,花的事业是甜美的,但还是让我绿叶的事业吧,她总是谦逊地专心地垂着绿荫的”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
江西省鹰潭市第一中学 桂耀荣
24
Thanks 谢谢您的观看!
2013-10-12
江西省鹰潭市第一中学 桂耀荣
25
江西省鹰潭市第一中学 桂耀荣
2013-10-12
7
酶
3、下列过程中,不可逆的是( C ) A.蛋白质的盐析 B.酯的水解 C.蛋白质变性 D.氯化铁的水解 4、欲将蛋白质从水中析出而又不改变它的性质 应加入( B )。 A.甲醛溶液 B.饱和Na2SO4溶液 C.CuSO4溶液 D.浓硫酸
2013-10-12
CH3CHCH2CHCOOH
CH3 NH2
—CH2CHCOOH NH2 CH2CHCOOH N H NH2
CH3CH2CH—CHCOOH CH3 NH2
2013-10-12
江西省鹰潭市第一中学 桂耀荣
4
人体必需的氨基酸
合理搭配食物的意义
不同的食物中含有的蛋白质的数量 及成分不同,即营养价值不同。合理 搭配各种食物,可以使氨基酸相互补 充,提高膳食中蛋白质的吸收与利用。
2013-10-12 江西省鹰潭市第一中学 桂耀荣 17
豆腐
一、豆腐文化 2、豆腐的好处 豆腐,不仅是人们餐桌上的美味佳肴,营养丰富, 而且具有医疗保健作用。豆腐及其制品所含的植物蛋 白,有人体必需的8种氨基酸。常食用豆腐,可以降低 血液中胆固醇的含量,减少动脉硬化机会。 豆腐中还含有大豆磷脂,是生命的重要组成部分, 对人体细胞的正常活动和新陈代谢起着重要的作用。 经常食用豆腐不仅对神经衰弱和体质虚弱的人有所裨 益,而且对高血压、动脉硬化、冠心病等患者有一定 的辅助疗效。目前豆腐已经被全球公认为“国际性保 健食品” 。
2013-10-12
江西省鹰潭市第一中学 桂耀荣
23
豆腐
二、豆腐的制作 9、成型 豆腐成型箱内,先把豆包布对角铺平,由四 角向箱内放豆脑,放豆脑前不得搅拌,豆包布拉 平盖好,然后旋压成型,旋压时应将弹簧缓慢挤 压,当弹簧有少许缝隙时,即可停止,如此反复 三次,10分钟即可成型。
2013-10-12
2013-10-12
江西省鹰潭市第一中学 桂耀荣
5
酶
四、酶
酶— 特殊的蛋白质,生物制造的催化剂 酶的特性— 离开生物机体后仍具活性 酶的作用— 催化许多有机化学反应和生物体内的复杂 反应
酶作催化剂的特点— 反应条件温和、反应快、专一 性
应用— 食品、发酵、纺织、制药、制革等
2013-10-12
江西省鹰潭市第一中学 桂耀荣
江西省鹰潭市第一中学 桂耀荣
2013-10-12
2
人体必需的氨基酸
三. 人体必需的氨基酸
蛋白质
胃蛋白酶或胰蛋白酶 水解
氨基酸
在人体内吸收 后重新组合
蛋白质
动物性蛋白质 食物中的蛋白质 植物性蛋白质
必需氨基酸(人体不能合成,共有8种只能从食物中获取)
蛋白质 非必需氨基酸(人体能合成有12种,无需食物供给)
江西省教育信息技术研究“十二五”规 划2012年度课题《基于网络的高中化学 课件库的建设与应用研究》 (课题编号:GDK-2012-G-72883)
主持人:桂耀荣
2013-10-12
江西省鹰潭市第一中学 桂耀荣
1
新课标人教版高中化学课件系列
选修1 化学与生活 第一章 关注营养平衡
第三节 生命的基础——油脂 第2课时
2013-10-12 江西省鹰潭市第一中学 桂耀荣 21
豆腐
二、豆腐的制作 4、磨豆 第一磨加水量适中,水流¢8-10毫米,加入14公 斤湿黄豆(约6公斤干豆)豆腐的加水比例1:6即36公 斤生豆浆(豆浆加水比例为1:8到1:10)。豆浆量小 于40公斤。 5、煮浆 煮浆至80度左右加入消泡剂(比例为8克/40公斤) 用长勺均匀搅拌至泡沫消失,至98度时熄灭。(豆 浆会以余下的热量加热到103度。可减少耗电量)。 6、放浆 放浆用滤架及滤网过滤,自然降温至80-85度即 可点卤。
2013-10-12
江西省鹰潭市第一中学 桂耀荣
22
豆腐
二、豆腐的制作 7、点卤 卤片加水稀释,(比例为1:1.5)制成卤水,加入 适当食盐,(有一点食盐沉淀为宜)浆的温度在80-85 度时用勺子使其在桶中上下缓慢翻动,慢慢加入卤水, 有絮状出现时卤流放小,出现80%絮状时停卤,(点 卤量约250-300毫升)并在液面上洒卤压面。 8、蹲缸 静止不动大约10分钟,让蛋白质充分凝固。
豆腐
红烧虾米豆腐
夹心儿豆腐
绿叶托豆腐
雪花蟹肉豆腐羹
鱼腩烧豆腐 西湖豆腐
2013-10-12
江西省鹰潭市第一中学 桂耀荣
14
豆腐
酸菜鱼炖豆腐汤
宝黄豆腐
麻婆豆腐
蛋美豆腐
豆腐海带汤
2013-10-12
豆腐荤杂烩
豆腐鲫鱼
红烧豆腐
江西省鹰潭市第一中学 桂耀荣
15
豆腐
研究性学习:有趣的豆腐
一、豆腐文化
二、豆腐制作
6
酶
1、下列关于蛋白质的叙述中,正确的是 ( AB ) A.蛋白质溶液中加(NH4)2SO4溶液可提纯蛋白质。 B.在豆浆中加少量石膏,能使豆浆凝结为豆腐。 C.温度越高,酶对某些化学反应的催化效率越高。 D.任何结构的蛋白质遇到浓HNO3都会变成黄色。
2、为了鉴别某白色纺织物成分是蚕丝还是人造丝,可 以选用的方法是( AD ) A.滴加浓硝酸 B.滴加浓硫酸 C.滴加酒精 D.灼烧
2013-10-12 江西省鹰潭市第一中学 桂耀荣 18
豆腐
豆腐的制作方法很简单,但做的时候却要细 心,什么时候点卤,需要什么样的豆浆, 这都是很重要的。
2013-10-12
江西省鹰潭市第一中学 桂耀荣
19
豆腐
二、豆腐的制作
制作流程: 采购→洗涤→浸豆→磨豆→煮浆→放浆→ 点卤→蹲缸→成品
2013-10-12
2013-10-12
江西省鹰潭市第一中学 桂耀荣
3
人体必需的氨基酸
人体必需氨基酸
赖氨 酸 蛋氨 酸 亮氨 酸 异亮 氨酸
H2N(CH2)4CHCOOH NH2 CH3SCH2CH2CHCOOH NH2
缬氨 酸 苏氨 酸 苯丙 氨酸 色氨 酸
CH3CH—CHCOOH CH3 NH2 CH3CH—CHCOOH OH NH2
2013-10-12
江西省鹰潭市第一中学 桂耀荣
11
豆腐
[家庭小实验] 在豆浆中加入石膏,即出现大量蛋白 质沉淀,成为豆腐脑;将豆腐脑包在纱布 中挤压去少量水分后,成为豆腐;加大压 强,挤压去大部分水分,则成为豆腐干。
2013-10-12
江西省鹰潭市第一中学 桂耀荣
12
豆腐
肥牛菇菌嫩豆腐
2013-10-12 江西省鹰潭市第一中学 桂耀荣 13
2013-10-12 江西省鹰潭市第一中学 桂耀荣 9
酶
7、下列物质可以使蛋白质变性的是( D) ①福尔马林、②酒精、③高锰酸钾溶液、④硫酸铵、 ⑤硫酸铜、⑥双氧水、⑦硝酸 A.除④⑦外 B.除③⑥ C.①②⑤ D.除④外
8、下列叙述中正确的是( BC ) A.能发生酯化反应的酸一定是羧酸 B.油脂水解后得到的醇是丙三醇 C.天然蛋白质水解的最终产物是多种α-氨基酸 D.蛋白质溶液中加入K2SO4溶液后,蛋白质从溶液中析 出,这种变化叫做变性
2013-10-12 江西省鹰潭市第一中混合物放入玻璃纸袋中,浸入 流动的温水中。相当长一段时间后,取袋内液体分别与 碘水、新制Cu(OH)2(加热)和浓硝酸(微热)作用, 其现象分别是是(C ) A.显蓝色、无现象、显黄色 B.显蓝色、红色沉淀、无现象 C.无现象、变黑色、显黄色 D.无现象、红色沉淀、无现象
江西省鹰潭市第一中学 桂耀荣
8
酶
5、氯化钡有剧毒,致死量为0.3g,万一不慎误服,应 大量吞服鸡蛋清及适量解毒剂,此解毒剂是( D) A.AgNO3 B.CuSO4 C.MgSO4 D.Na2CO3
6、(2004年北京理科综合)糖类、油脂和蛋白质是维持 人体生命活动所必需的三大营养物质。以下叙述正确的 是( B ) A.植物油不能使溴的CCl4溶液褪色 B.淀粉水解的最终产物是葡萄糖 C.葡萄糖能发生氧化反应和水解反应 D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
2013-10-12
江西省鹰潭市第一中学 桂耀荣
16
豆腐
一、豆腐文化 1、豆腐的由来 明代大药理学家李时珍在《本草纲目》二五卷 《谷部》中载:“豆腐之法,始于汉淮南王刘安”, 并详细介绍了豆腐的制作方法。公元前164年,刘安 袭父封为淮南王,建都寿春。刘安好道,为求长生不 老之药 ,招方士数千人,有名者为苏非等八人,号称 “八公”。他们常聚在楚山即今八公山谈仙论道,著 书炼丹。在炼丹中以黄豆汁培育丹苗,豆汁偶与石膏 相遇,形成了鲜嫩绵滑的豆腐。刘安炼丹未成却发明 豆腐。之后,豆腐技法传入民间。
江西省鹰潭市第一中学 桂耀荣
20
豆腐
二、豆腐的制作 1、采购 东北优质大豆,要无虫豆、霉豆、黑豆,及杂质。 2、洗涤 黄豆浸泡之前用清水洗净。 3、浸豆 1斤黄豆加4斤水浸泡。浸泡时间春天为8-10小时, 夏天6-8小时,冬天12 小 时。(如用温水泡豆,温度 不要超过35度。)豆胀后豆子不得露出水面。(豆劈 开两片时呈片状,有凹心意味着没有浸透。有泡沫意 味浸过头)
