常见阳离子的分离与鉴定
常见阳离子的分离与鉴定

生成黑色沉淀。
(1)Hg2+和Cu2+、Pb2+的分离
在所得沉淀上加5滴1 mol·L-1Na2S溶液,水浴 加热3min,并不时搅拌。再加3~4滴水,搅拌 均匀后离心分离。沉淀用Na2S溶液再处理一次, 合并清液,并编号溶液3。沉淀用饱和NH4Cl溶 液洗涤,并编号沉淀3。观察溶液3的颜色, 讨论反应历程。
[实验目的]
1、学会混合离子分离的方法, 进一步巩固离子鉴定的条件和方 法。2、熟练运用常见元素(Ag、 Hg、Pb、Cu、Fe)的化学性质。
[实验原理]
离子混合溶液中诸组分若对鉴定不 产生干扰,便可以利用特效应直接 鉴定某种离子。若共存的其它彼此 干扰,就要选择适当的方法消除干 扰。通常采用掩蔽剂消除干扰,这 是一种比较简单、有效的方法。但 在很多情况下,没有合适的掩蔽剂, 就需要将彼此干扰组分分离。沉淀 分离法是最经典的分离方法。
再用KI和HCl重复处理沉淀。合并两次离心 液,往离心液中加1滴0.2mol·L-1CuSO4和少许 Na2CO3固体,有什么生成?说明有哪种离子 存在?
反应方程式如下: HgS22-+2H+=HgS↓+H2S↑ HgS+4I-+2H+=[HgI4]2-+H2S
[HgI4]2-+Cu2+=Cu2[HgI4]↓
常 用 的 沉 淀 有 HCl 、 H2SO4 、 NaOH 、 NH3·H2O、(NH4)2CO3、(NH4)2-S溶液等。 由于元素在周期表中同时产生沉淀。这 种沉淀剂称为产生沉淀的元素的组试剂。 组试剂将元素划分为不同的组,逐渐达 到分离的目的。
(完整版)常见阳离子的分离及鉴定

2020/4/14
(8)Mn2+的鉴定 5BiO3- + 2Mn2+ + 14H+
═ 5Bi3+ + 2MnO4— (紫红色溶液)+7H2O
(9)Co2+的鉴定 Co2+ + 4SCN— = [Co(SCN)4]2—( 蓝色)
试 HCl)
(NH4)2S (NH3-NH4Cl)
(NH4)2CO3 (NH3-NH4Cl)
硫化物 难溶于水
分 组 依 据
两酸两碱系统分析法
分别检出NH4+、Na+、Fe3+、Fe2+
氯化物易溶于水
硫酸盐 难溶于水
硫酸盐易溶于水
氢氧化物难溶于水及 氨水
氨性条件下不生成沉淀
2020/4/14
(2)Pb2+的鉴定 Pb2+ + CrO42—→ PbCrO4↓(黄色沉淀) (3) Cu2+的鉴定 2Cu2++ [ Fe(CN)6]4- → Cu2Fe(CN)6↓ (红棕色)
2020/4/14
(4)Fe3+的鉴定 ①Fe3++ nSCN — == Fe(SCN)nn-3 (血红色溶液) ②K+ + Fe3++ [ Fe(CN)6]4- →[K Fe(CN)6 Fe] ↓
2020/4/14
硫化氢系统分析法
硫化物不溶于水
硫化物溶于水
在稀酸中生成硫化物沉淀
分
组
氯化物溶于热水
依 据
氯化物 不溶于 热水
常见阳离子的分离与鉴定.

6mol· L-1NO3 +
沉淀溶解
6mol· L-1NH4· H2O
☺ Zn2+的鉴定:
3滴0.2mol· L-1ZnSO4 + 2滴2mol· L-1HAc + 白色沉淀 3滴(NH4)2[(SCN)4]
11
☺ Hg2+的鉴定:
2滴0.2mol· L-1HgCl2 + 逐滴加0.5mol· L-1SnCl2 继续加
硫化氢法。 两酸两碱法是以最普通的酸 (盐酸、硫酸 ) 和碱 ( 氨水、 氢氧化钠 ) 作试剂,根据各离子氯化物、硫酸盐、氢氧化物 的溶解度不同进行分离鉴定; 硫化氢法依据各离子硫化物以及它们的氯化物、碳酸盐 和氢氧化物的溶解度不同进行分离鉴定。
3
【实验原理】
与HCl溶液反应:
Ag+、Hg22+、Pb2+等
Ag+ 、 Pb2+ 、 Cu2+ 、 Cd2+ 、 Bi3+ 、 Hg+ 、 Hg22+ 、 Sb3+、Sn2+等
5
【仪器与试剂】
仪器:
试管(10ml),离心管(10ml),离心机
试剂:
HCl、H2SO4、HNO3、HAc、NaOH、NH3· H2O、 MgCl2、CaCl2、BaCl2、AlCl3、PbNO3、SnCl2、 HgCl2、Bi(NO3)3、CuCl2、AgNO3、ZnSO4、镁试
与稀H2SO4溶液反应: Ba2+、Sr2+、Ca2+ 、Pb2+ 、Ag+ 等 与NaOH溶液反应: Al3+、Zn2+、Pb2+ 、Sb2+ 、Sn2+等 与NH3溶液反应: Ag+、 Cu2+、Cd2+ 、Zn2+等
无机化学常见阳离子分离与鉴定

离子鉴定方法备注Hg2+①Hg2+离子,可被铜置换,在铜表面析出金属汞的灰色斑点,示有Hg2+离子:Cu + Hg2+ → Cu2+ + Hg↓②在2滴试液中,加入过量SnCl2溶液,SnCl2与汞盐作用,首先生成白色Hg2Cl2沉淀,过量SnCl2将Hg2Cl2进一步还原成金属汞,沉淀逐渐变灰,说明Hg2+离子存在。
2HgCl2 + Sn2+ → Sn4+ + Hg2Cl2↓+ Cl–Sn2+ + Hg2Cl2→ 2Hg↓+ Sn4+ + 2Cl–Mg 2+取几滴试液,加入少量镁试剂(对硝基苯偶氮间苯二酚),再加入NaOH溶液使呈碱性,若有Mg 2+存在,产生蓝色沉淀。
Mg 2+离子量少时,溶液由红色变成蓝色。
加入镁试剂后,溶液显黄色,表示试剂酸性太强,应加入碱液。
Ni 2+、Co2+、Cd 2+的氢氧化物与镁试剂作用,干扰Mg 2+的鉴定。
Mn2+取1滴试液,加入数滴0.1mol·L-1HNO3溶液,再加入NaBiO3固体,若有Mn2+存在,溶液应为紫红色。
Na+取1滴试液,加入8滴乙酸铀酰锌试剂,用玻璃棒摩擦试管。
淡黄色结晶乙酸铀酰锌钠(NaCH3COO·Zn(CH3COO)2·UO2(CH3COO)2·H2O)沉淀出现,示有Na+离子存在。
①反应应在中性或乙酸酸性溶液中进行。
②大量K+离子存在干扰测定,为降低K+离子浓度,可将试液稀释2~3倍。
NH4+①在表面皿上,加入5滴6mol·L-1 NaOH,立即把一凹面贴有湿润红色石蕊试纸(或pH试纸)的表面皿盖上,然后放在水浴上加热,试纸呈碱性,示有NH4+离子存在。
②在点滴板上放1滴试液,加2滴奈斯勒试剂(K2[HgI4]与KOH的混合物),生成红棕色沉淀,示有NH4+离子存在。
NH4+离子含量少时,不生成红棕色沉淀而得到黄色溶液。
Ni2+取2滴试液,加入2滴二乙酰二肟(丁二肟)和1滴稀氨水,生成红色的沉淀,说明有Ni2+离子存在。
常见阳、阴离子的分离与鉴定
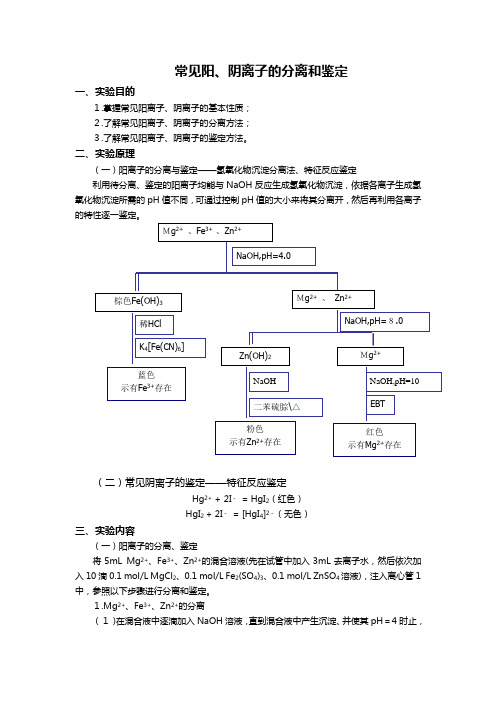
常见阳、阴离子的分离和鉴定一、实验目的1.掌握常见阳离子、阴离子的基本性质; 2.了解常见阳离子、阴离子的分离方法; 3.了解常见阳离子、阴离子的鉴定方法。
二、实验原理(一)阳离子的分离与鉴定——氢氧化物沉淀分离法、特征反应鉴定利用待分离、鉴定的阳离子均能与NaOH 反应生成氢氧化物沉淀,依据各离子生成氢氧化物沉淀所需的pH 值不同,可通过控制pH 值的大小来将其分离开,然后再利用各离子的特性逐一鉴定。
(二)常见阴离子的鉴定——特征反应鉴定Hg 2+ + 2I - = HgI 2(红色) HgI 2 + 2I - = [HgI 4]2-(无色)三、实验内容(一)阳离子的分离、鉴定将5mL Mg 2+、Fe 3+、Zn 2+的混合溶液(先在试管中加入3mL 去离子水,然后依次加入10滴0.1 mol/L MgCl 2、0.1 mol/L Fe 2(SO 4)3、0.1 mol/L ZnSO 4溶液),注入离心管1中,参照以下步骤进行分离和鉴定。
1.Mg 2+、Fe 3+、Zn 2+的分离(1)在混合液中逐滴加入NaOH 溶液,直到混合液中产生沉淀、并使其pH =4时止,Mg 2+ 、Fe 3+ 、Zn 2+Mg 2+ 、 Zn 2+棕色Fe(OH)3稀HCl NaOH,pH=4.0蓝色 示有Fe 3+存在K 4[Fe(CN)6] NaOH,pH=8.0 Zn(OH)2Mg 2+NaOH 粉色示有Zn 2+存在二苯硫腙\△ NaOH,pH=10 红色示有Mg 2+存在EBT然后离心分离。
把上清液移到另一离心管2中;沉淀用去离子水洗涤二遍后,记为沉淀1,留待下面分析。
(2)往离心管2的上层清液中继续逐滴加入NaOH溶液,直到溶液中产生沉淀、并使其pH=8时止,把上清液移到另一离心管3中;沉淀用去离子水洗涤二遍后,记为沉淀2,留待下面分析。
2.Mg2+、Fe3+、Zn2+的鉴定(1)Fe3+的鉴定取沉淀1加入去离子水及几滴盐酸,振荡试管使沉淀溶解。
实验二十六 常见阳离子的分离和鉴定-PPT精选文档

生成白色沉淀,示有Ag+存在。
8.Zn 2+
的鉴定
取3滴0.2
mol· L –1 ZnSO4试液于试管中,
加2滴2 mol· L –1 HAc溶液酸化,再加入 等体积硫氰酸汞铵(NH4)2[Hg(SCN)4]
溶液,摩擦试管壁,生成白色沉淀,示
2.K+的鉴定
在盛有0.5mL1mol· L-1
KCl溶液的试管中,
加入0.5mL饱和酒石酸氢钠NaHC4H4O6
溶液,如有白色结晶状沉淀产生,示有
K+存在。如无沉淀产生,可用玻棒摩擦 试管壁,再观察。写出反应方程式。
3.Mg 2+的鉴定
在试管中加2滴0.5mol· L-1
MgCl2溶液,
2.Sn 2+的鉴定 取5滴0.5mol· L –1
SnCl2试管中,逐滴
加入0.2mol· L –1 HgCl2溶液,边加边
振荡,若产生的沉淀由白色变为灰
色,然后变为黑色,示有Sn 2+ 存在。
二、p区和ds区部分金属离子的鉴定
1.Al 3+ 的鉴定 取2滴0.5mol· L –1 AlCl3溶液于小试管中, 加2~3滴水,2滴2mol· L –1 HAc及2滴 0.1%铝试剂,搅拌后,置水浴上加热片 刻,再加入1~2滴6mol· L –1 氨水,有红 色絮状沉淀产生,示有Al 3+存在。
三、部分混合离子①的分离和鉴定
取Ag+试液2滴和Cd 2+、Al 3+、Ba 2+、
Na+试液各5滴,加到离心试管中, 混合均匀后,按下表进行分离和鉴
常见阳离子的分离与鉴定一

• 4 Sb3+ + NO2- +H2O + 6Cl- = SbCl6- + NO3- + 2H+
• • • • • • • • • 5 Bi3+ + SC(NH2)2 = [Bi(SC(NH2)2)4]3+ 6 Cu2+ + [Fe(CN)6] 4- = Cu2 [Fe(CN)6] 7 Ag+ + Cl- = AgCl AgCl + 2NH3 = [Ag(NH3)2]+ + Cl[Ag(NH3)2]+ + Cl- + 2H+ = AgCl + 2NH4+ 8 Zn2+ + [Hg(SCN)4]2- = Zn [Hg(SCN)4] 9 Cd2+ + S2- = CdS 10 同2 三、参照前面的方程式
实验注意事项
• 二2中改为HgCl2中加入SnCl2才会出书上的 现象。 • 做分离时在离心试管中进行;每次沉淀时 沉淀剂都是稍过量的;离心后清液用专用 滴管吸出留后用,沉淀经洗涤(加水后用 尖玻棒搅动,再离心,水洗液弃去)后再 用;滴管每吸液一次后都要用去离子水清 洗(三个烧杯都分盛去离子水,每个烧杯 吸三次都弃去)!
阳离子的主要分离方法
• 氢氧化物的酸碱性:主要利用其两性。 • 配位能力:过渡元素的配位能力远强于主 族,以此将主族金属离子与过渡金属离子 分开。 • 沉淀的生成:主要利用氢氧化物(pH控制)、 硫化物(pH控制)和其它沉淀反应。 • 氧化还原性:过渡金属的氧化态变化大, 改变氧化态从而改变其性质,再进行分离。
常见阳离子的分离与鉴定
阳离子的形成方式 单原子阳离子:最常见的存在方式,通常是金属 阳离子,尤其在强酸性溶液中; 同核多原子阳离子:即离子簇,水溶液中较少见, 多见于熔盐和固体中,尤其是过渡金属易生成该 类阳离子。如Hg22+、Timn+等; 高氧化态金属与O形成的多原子阳离子,水溶液 和熔盐中均常见;如VO2+、BiO+、TiO2+等; 金属与非氧非金属形成的多原子阳离子,水溶液 中较少见,多见于熔盐中,如AlF2+等; 金属与配体形成的阳离子:很常见于配合物中; 非金属间形成的阳离子:较少见,一般是季胺类 和叔醚类,也有象NH4+和PCl4+等。
无机化学常见阳离子分离与鉴定

离子鉴定方法备注Hg2+①Hg2+离子,可被铜置换,在铜表面析出金属汞的灰色斑点,示有Hg2+离子:Cu + Hg2+ → Cu2+ + Hg↓②在2滴试液中,加入过量SnCl2溶液,SnCl2与汞盐作用,首先生成白色Hg2Cl2沉淀,过量SnCl2将Hg2Cl2进一步还原成金属汞,沉淀逐渐变灰,说明Hg2+离子存在。
2HgCl2 + Sn2+ → Sn4+ + Hg2Cl2↓+ Cl–Sn2+ + Hg2Cl2→ 2Hg↓+ Sn4+ + 2Cl–Mg 2+取几滴试液,加入少量镁试剂(对硝基苯偶氮间苯二酚),再加入NaOH溶液使呈碱性,若有Mg 2+存在,产生蓝色沉淀。
Mg 2+离子量少时,溶液由红色变成蓝色。
加入镁试剂后,溶液显黄色,表示试剂酸性太强,应加入碱液。
Ni 2+、Co2+、Cd 2+的氢氧化物与镁试剂作用,干扰Mg 2+的鉴定。
Mn2+取1滴试液,加入数滴0.1mol·L-1HNO3溶液,再加入NaBiO3固体,若有Mn2+存在,溶液应为紫红色。
Na+取1滴试液,加入8滴乙酸铀酰锌试剂,用玻璃棒摩擦试管。
淡黄色结晶乙酸铀酰锌钠(NaCH3COO·Zn(CH3COO)2·UO2(CH3COO)2·H2O)沉淀出现,示有Na+离子存在。
①反应应在中性或乙酸酸性溶液中进行。
②大量K+离子存在干扰测定,为降低K+离子浓度,可将试液稀释2~3倍。
NH4+①在表面皿上,加入5滴6mol·L-1 NaOH,立即把一凹面贴有湿润红色石蕊试纸(或pH试纸)的表面皿盖上,然后放在水浴上加热,试纸呈碱性,示有NH4+离子存在。
②在点滴板上放1滴试液,加2滴奈斯勒试剂(K2[HgI4]与KOH的混合物),生成红棕色沉淀,示有NH4+离子存在。
NH4+离子含量少时,不生成红棕色沉淀而得到黄色溶液。
Ni2+取2滴试液,加入2滴二乙酰二肟(丁二肟)和1滴稀氨水,生成红色的沉淀,说明有Ni2+离子存在。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1、学会混合离子分离的方法, 进一步巩固离子鉴定的条件和方 法。2、熟练运用常见元素(Ag、 Hg、Pb、Cu、Fe)的化学性质。
[实验原理]
离子混合溶液中诸组分若对鉴定不 产生干扰,便可以利用特效应直接 鉴定某种离子。若共存的其它彼此 干扰,就要选择适当的方法消除干 扰。通常采用掩蔽剂消除干扰,这 是一种比较简单、有效的方法。但 在很多情况下,没有合适的掩蔽剂, 就需要将彼此干扰组分分离。沉淀 分离法是最经典的分离方法。
生成黑色沉淀。
(1)Hg2+和Cu2+、Pb2+的分离
在所得沉淀上加5滴1 mol·L-1Na2S溶液,水浴 加热3min,并不时搅拌。再加3~4滴水,搅拌 均匀后离心分离。沉淀用Na2S溶液再处理一次, 合并清液,并编号溶液3。沉淀用饱和NH4Cl溶 液洗涤,并编号沉淀3。观察溶液3的颜色, 讨论反应历程。
反应方程式如下:
Ag++Cl-=AgCl↓
Pb2++2Cl-=PbCl2↓ 现象:
出现白色沉淀,沉淀为AgCl、 PbCl2,溶液中有Cu2+、Hg2+、 Fe3+。
(1)Pb2+和Ag+的分离及Pb2+的鉴定 向沉淀 1中加六滴水,在沸水浴中加热3min以上,并 不时搅动。待沉淀沉降后,趁热取清液三滴于 黑色点滴板上,加2 mol·L-1K2CrO4和2 mol·L1HAc溶液各一滴,有什么生成?加2 mol·L-1 NaOH溶液后又怎样?再加6 mol·L-1HAc溶液又 如何?取清液后所余沉淀信号为沉淀2。
反应方程式如下:
NO3-+Zn+2HAc=NO2+Zn2++H2O+2Ac-
NO2-+对氨基苯磺酸+α萘胺→玫瑰 红色
现象:
混合液生成玫瑰红色,示有 NO3-。
2.Fe3+的鉴定
取一滴试液加到白色点滴板凹穴,加 0.25 mol·L-1K4Fe(CN)6一滴。观察沉淀 的生成和颜色,该物质是何沉淀?
反应方程式如下: AgCl+2NH3=[Ag(NH3)2]++Cl[Ag(NH3)2]++Cl+2HNO3=AgCl↓+2NH+4+2NO3-
现象:
AgCl沉淀溶解生成无色配离子[Ag(NH3)2]+, [ቤተ መጻሕፍቲ ባይዱg(NH3)2]+配离子在硝酸作用下,又生成AgCl白色沉 淀,示有Ag+。
4. Pb2+、Hg2+ Cu2+和Fe3+的分离及Pb2+、 Hg2+、Cu2+的分离和鉴定
用6 mol·L-1氨水将溶液1的酸度调至中性(加 氨水约3~4滴),再加入体积约为此时溶液十
分之一的2 mol·L-1 HCl溶液(约3~4滴),将 溶 液 的 酸 度 调 至 0.2 mol·L-1 。 加 15 滴 5%CH3CSNH2 , 混 匀 后 水 浴 加 热 15min 。 然 后 稀 释一倍再加热数分钟~。静置冷却,离心沉降。
反应方程式如下: Fe3++[Fe(CN)6]4-=Fe4[Fe(CN)6]3↓ 现象:
有深蓝色沉淀生成。
3. Ag+、Pb和Cu2+、Hg2+、Fe3+的分离 及Ag+、Pb2+的分离和鉴定。
向余下试液中滴加4滴2 mol·L-1HCl,充分振动, 静置片刻,离心沉降,向上层清液中加2 mol·L-1 HCl溶液以检查沉淀是否完全。吸出上层清液, 编号溶液1。用2 mol·L-1 HCl溶液洗涤沉淀,编 号沉淀1。观察沉淀的生成和颜色,写出反应方 程式。
反应方程式如下: HgS+S2-=HgS22-
现象: 部 分 沉 淀 溶 于 Na2S 生 成 无 色
HgS22-离子。
(2)Cu2+的鉴定
向沉淀3中加入浓硝酸(约4~5滴),加热搅
拌,使之全部溶解,所得溶液编号为溶液4。 用玻棒将产物单质S弃去。取1滴溶液4于白色 点滴板上,加1mol·L-1NaAc和0.25mol·L-1 K4Fe(CN)6各1滴,有何现象?
常 用 的 沉 淀 有 HCl 、 H2SO4 、 NaOH 、 NH3·H2O、(NH4)2CO3、(NH4)2-S溶液等。 由于元素在周期表中同时产生沉淀。这 种沉淀剂称为产生沉淀的元素的组试剂。 组试剂将元素划分为不同的组,逐渐达 到分离的目的。
本次实验学习熟练运用Ag+、Hg2+、Pb2+、 Cu2+ 和 Fe3+ 元 素 的 化 学 性 质 , 进 行 分 离 和鉴定。其实验方案设计见课本P186。
[实验用品]见课本P187。
[实验内容]
1. NO3-的鉴定
取3滴混合试液,加6 mol·L-1HAc溶液酸化 后用玻棒取少量锌粒加入试液,搅拌均匀, 使溶液中NO3-还原为NO22-。加对氨基苯磺 酸与α -苯胺溶液各一滴,有何现象?
取混合溶液20滴,放入离心试管并按以下 实验步骤进行分离和鉴定。
向上层清液中加新制H2S溶液检查沉淀是 否完全。沉淀完全后离心分离,用饱和 NH4Cl溶液洗涤沉淀,所得溶液为溶液2。 通过实验判断溶液2中的离子。观察沉淀 的生成和颜色。
反应方程式如下:
Pb2++CH3CSNH2→PbS↓ Cu2++CH3CSNH2→CuS↓ Hg2++CH3CSNH2→HgS↓ 现象:
反应方程式如下: PbCl2=Pb2++2Cl-
Pb2++CrO42-=PbCrO4↓ PbCrO4+4OH-=Pb(OH)42-+CrO42-
Pb(OH)42-+4HAc+CrO42=PbCrO4↓+4H2O+4Ac-
现象:
白色沉淀溶解,生成黄色沉淀,沉淀 溶解生成配离子,又生成黄色沉淀,示 有Pb2+。
[思考题]
Pb2+的鉴定有可能现象不明显, 请 查 阅 不 同 温 度 时 PbCl2 在 水 中 的溶解度并作出解释。
(2)Ag+的鉴定 向沉淀2中加 少量6 mol·L-1 NH3·H2O,沉淀是 否溶解?再加入6 mol·L-1HNO3, 沉淀重新生成。观察沉淀的颜色,
并写出反应方程式。
反应方程式如下:
CuS+2HNO3(浓)=Cu(NO3)2+H2S↑ H2S+HNO3(浓)=NO2↑+S↓+2H2-O Cu2++[Fe(CN)6]4-=Cu2[Fe(CN)6]↓
