常见阳离子的分离与鉴定(一)
阳离子的分离与鉴定

阳离子的分离与鉴定一. 实验目的1. 掌握用两酸三碱系统分析法对常见阳离子进行分组分离的原理和方法。
2. 掌握分离、鉴定的基本操作与实验技能。
二. 实验原理阳离子的种类较多,常见的有二十多种,个别检出时,容易发生相互干扰,所以一般阳离子分析都是利用阳离子某些共同特性,先分成几组,然后再根据阳离子的个别特性加以检出。
凡能使一组阳离子在适当的反应条件下生成沉淀而与其它组阳离子分离的试剂称为组试剂,利用不同的组试剂把阳离子逐组分离再进行检出的方法叫做阳离子的系统分析。
在阳离子系统分离中利用不同的组试剂,有很多不同的分组方案。
如硫化氢分组法,两酸、两碱系统分组法。
下面介绍一种以氢氧化物酸碱性与形成配合物性质不同为基础,以HCl、H2SO4、NH3 H2O、NaOH、(NH4)2S为组试剂的两酸三碱分组方法。
本方法将常见的二十多种阳离子分为六组。
第一组:盐酸组Ag+,Hg22+,Pb2+第二组:硫酸组Ba2+,Ca2+,Pb2+第三组:氨合物组Cu2+,Cd2+,Zn2+,Co2+,Ni2+第四组:易溶组Na+,NH4+,Mg2+,K+第五组:两性组Al3+,Cr3+,Sb III、V,Sn II、IV第六组:氢氧化物组Fe2+,Fe3+, Bi3+,Mn2+,Hg2+用系统分析法分析阳离子时,要按照一定的顺序加入组试剂,将离子一组一组沉淀下来,具体分离方法如下表。
表阳离子分组步骤试液(用个别检出法鉴定NH4+、Fe2+、Fe3+)(Hg)(两性组) (氢氧化物组) (第三组硫化物) (第四组易溶组)AlO2−、Cr O42−Fe(OH)3、K+、Na+、Mg2+、NH4+SbO43−、SnO32−MnO(OH)2、NaBiO3、HgNH2Cl每组分出后,继续再进行组内分离,直至鉴定时相互不发生干扰为止。
在实际分析中,如发现某组离子整组不存在(无沉淀产生)、这组离子的分析就可省去。
从而大大简化了分析的手续。
实验常见阳离子的分离与鉴定-V1

实验常见阳离子的分离与鉴定-V1实验常见阳离子的分离与鉴定阳离子是指带正电荷的离子,常见的有盐酸中的K+、Na+、Mg2+、Ca2+等。
在实验室中对这些阳离子的分离和鉴定是一项比较常见的实验操作,下面将对此进行重新整理。
一、分离NH4+和Fe3+实验操作步骤:1.将NH4+和Fe3+混合,并加入NaOH,出现棕色沉淀;2.将沉淀过滤,并加入HCl,沉淀消失;3.将所得溶液加入HgCl2,出现白色沉淀。
实验操作目的:该实验可用于检测食品和饲料中的氨盐等。
二、分离Ba2+和Fe3+实验操作步骤:1.将Ba2+和Fe3+混合,并加入NaOH,出现棕色沉淀;2.将沉淀过滤,得到沉淀和过滤液;3.将所得沉淀加入Na2CO3,在锅炉中加热,轻轻搅拌,直到溶解;4.将溶液冷却,加入硫酸钠,出现白色沉淀。
实验操作目的:该实验可用于检测水中钙、铁的含量。
三、分离Mg2+和Fe2+实验操作步骤:1.将Mg2+和Fe2+混合,加入氨水,pH值达到9.5~10.2;2.将所得溶液加入EDTA,出现蓝色沉淀。
实验操作目的:该实验可用于检测水或者土壤中的镁和铁的含量。
四、分离Ca2+和Ba2+实验操作步骤:1.将Ca2+和Ba2+混合,加入Na2SO4;2.出现白色沉淀。
实验操作目的:该实验可用于检测食品和饲料中的钙盐。
五、分离Na+和K+实验操作步骤:1.将Na+和K+混合,并加入Na2CO3;2.加热,溶解后冷却,加入二甲基黄。
3.观察产生的沉淀,小型重沉。
实验操作目的:该实验可用于检测水中钠、钾的含量。
常见阳离子的分离与鉴定-第I组阳离子

2.第Ⅰ组阳离子的鉴定反应
(1) Ag+离子的鉴定反应 —— Ag2CrO4沉淀(稍溶于HAc,易溶于HNO3及氨水)
(2) Pb2+离子的鉴定反应 a.以K2CrO4试剂鉴定Pb2+离子 —— PbCrO4沉淀(溶于NaOH和HNO3,不溶于HAc) b.以KI试剂鉴定Pb2+离子 —— 黄色片状PbI2晶体
进一步验证Hg22+的存在: 沉淀用氨水洗涤,加浓HCl溶液5滴和浓HNO3溶液3滴,水浴加热溶解,转入 微烧杯,小火蒸发至余2~3滴。冷却,加10滴水再蒸发至余2~3滴,加4滴水。离 心分离弃去沉淀。 SnCl2试剂检验溶液中的Hg2+离子。 (5) Ag+ 的鉴定 加入6mol/L HNO3溶液数滴生成AgCl沉淀;或用KI试剂检验。
(1) 沉淀分离第Ⅰ组阳离子 阳离子混合试液1.5ml + HCl溶液→ 加热2~3min → 冷却并充分搅拌 → 离心, 检验并继续滴加HCl至沉淀完全→离心分离。 分离得的溶液中含有Ⅱ、Ⅲ组阳离子,保留待用。 (2) 分离Pb2+离子 上一步骤分离得的沉淀→ HCl溶洗涤2次→加10滴水→水浴上加热,不断 2+ 搅拌→趁热离心分离 溶液转出→鉴定Pb 离子 沉淀热水洗涤,保留待用 (3) Pb2+离子的鉴定 (4) 分离并鉴定Hg22+ 取 (2)分离所得沉淀+氨水,充分搅拌,离心分离 溶液→鉴定Ag+ 沉淀:若黑色(Hg+HgNH2Cl) 已可初步确认含有汞
常见阳离子的分离与鉴 定
第Ⅰ组阳离子的分离和鉴定
第Ⅰ组阳离子的分离和鉴定
第Ⅰ组阳离子包括Ag+、Hg22+、Pb2+ 离子 特点: 它们的氯化物难溶于水
实验二十二 常见阳离子的分离与鉴定(一)

一、实验目的 巩固和进一步掌握一些金属元素及
其化合物的性质。了解常见阳离子混合 液的分离和检出的方法以及巩固检出离 子的操作。
离子的分离和鉴定是以各离子对试剂的 不同反应为依据的。这种反应常伴随有 特殊的现象,如沉淀的生成或溶解,特 殊颜色的出现,气体的产生等等。
2.A l 3+的分离和鉴定 往(三)-1的清液中滴加6 mol·L –1 氨水至显碱
性,搅拌片刻,离心分离,把清液转移到 另一支离心试管中,按(三)-3处理。沉淀中 加入2 mol·L –1 HAc各2滴,再加入2滴铝试 剂,搅拌后微热之,产生红色沉淀,示有A l 3+存在。
3.Ba 2+的分离和鉴定
5.Bi 3+的鉴定
取1滴0.5mol·L –1 Bi(NO3)3试液于试管 中,加1滴2.5%硫脲,生成鲜黄色配 合物,示有Bi 3+存在。
6.Cu 2+ 的鉴定 取1滴0.5mol·L –1 CuCl2试液于试管中,加
1滴6mol·L-1HAc溶液酸化,再加1滴 0.5mol·L –1 亚铁氰化钾K4[Fe(CN)6]溶液, 生成红棕色Cu2[Fe(CN)6]沉淀,示有Cu 2+ 存在。
4.Ca 2+的鉴定 取0.5mL0.5mol·L-1 CaCl2溶液于离心试管中,
再加10滴饱和草酸铵溶液,有白色沉淀产 生。离心分离,弃去清液。若白色沉淀不 溶于6mol·L-1 HAc溶液而溶于2mol·L -1盐酸, 示有Ca 2+存在。写出反应式。
5.Ba 2+的鉴定
取2滴0.5mol·L –1 BaCl2于试管中,加 入2mol·L –1 HAc和2mol·L –1 NaAc各 2滴,然后滴加2滴1mol·L –1 K2CrO4, 有黄色沉淀生成,示有Ba 2+存在。 写出反应式
常见阳、阴离子的分离与鉴定
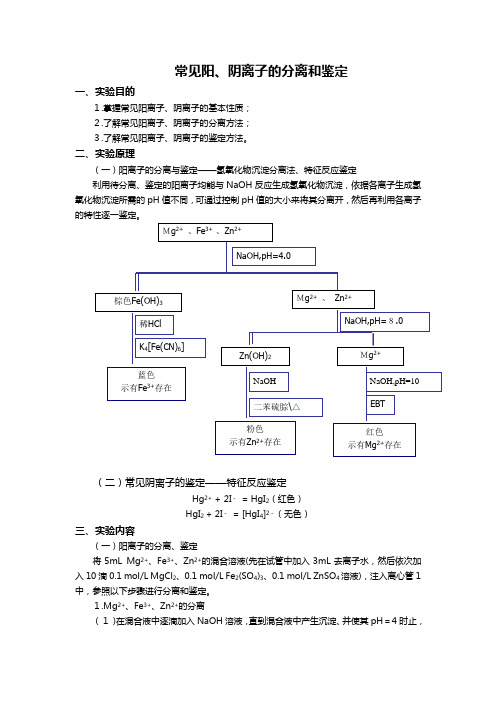
常见阳、阴离子的分离和鉴定一、实验目的1.掌握常见阳离子、阴离子的基本性质; 2.了解常见阳离子、阴离子的分离方法; 3.了解常见阳离子、阴离子的鉴定方法。
二、实验原理(一)阳离子的分离与鉴定——氢氧化物沉淀分离法、特征反应鉴定利用待分离、鉴定的阳离子均能与NaOH 反应生成氢氧化物沉淀,依据各离子生成氢氧化物沉淀所需的pH 值不同,可通过控制pH 值的大小来将其分离开,然后再利用各离子的特性逐一鉴定。
(二)常见阴离子的鉴定——特征反应鉴定Hg 2+ + 2I - = HgI 2(红色) HgI 2 + 2I - = [HgI 4]2-(无色)三、实验内容(一)阳离子的分离、鉴定将5mL Mg 2+、Fe 3+、Zn 2+的混合溶液(先在试管中加入3mL 去离子水,然后依次加入10滴0.1 mol/L MgCl 2、0.1 mol/L Fe 2(SO 4)3、0.1 mol/L ZnSO 4溶液),注入离心管1中,参照以下步骤进行分离和鉴定。
1.Mg 2+、Fe 3+、Zn 2+的分离(1)在混合液中逐滴加入NaOH 溶液,直到混合液中产生沉淀、并使其pH =4时止,Mg 2+ 、Fe 3+ 、Zn 2+Mg 2+ 、 Zn 2+棕色Fe(OH)3稀HCl NaOH,pH=4.0蓝色 示有Fe 3+存在K 4[Fe(CN)6] NaOH,pH=8.0 Zn(OH)2Mg 2+NaOH 粉色示有Zn 2+存在二苯硫腙\△ NaOH,pH=10 红色示有Mg 2+存在EBT然后离心分离。
把上清液移到另一离心管2中;沉淀用去离子水洗涤二遍后,记为沉淀1,留待下面分析。
(2)往离心管2的上层清液中继续逐滴加入NaOH溶液,直到溶液中产生沉淀、并使其pH=8时止,把上清液移到另一离心管3中;沉淀用去离子水洗涤二遍后,记为沉淀2,留待下面分析。
2.Mg2+、Fe3+、Zn2+的鉴定(1)Fe3+的鉴定取沉淀1加入去离子水及几滴盐酸,振荡试管使沉淀溶解。
常见阳离子的分离与鉴定(Ⅰ)

成白色沉淀,示有Ag+存在。
写出相应的反应方程式。
Ag++Cl-==AgCl↓AgCl+3NH3+H2O==Ag(NH3)2OH+NH4ClAg(NH3)2OH+3H++Cl-==AgCl↓+2NH4++H2O(2)Pb2+的鉴定取5滴0. 5mol/L Pb(NO3)2试液于试管中,加2滴1mol/L K2CrO4溶液,如有黄色沉淀生成,在沉淀上滴加数滴2mol/L NaOH溶液,沉淀溶解,示有Pb2+存在。
写出反应方程式。
Pb2++CrO42-==PbCrO4↓PbCrO4+4OH-==[Pb(OH)4]-+CrO42-(3)Cu2+的鉴定取1滴0. 5mol/L CuCl2试液于试管中,加1滴6mol/L HAc溶液酸化,再加1滴0. 25mol/L K4[Fe(CN)6]溶液,生成红棕色Cu2[Fe(CN)6]沉淀,示有Cu2+存在。
Cu2++[Fe(CN)6]2-==Cu2[Fe(CN)6]↓2、混合离子的分离鉴定相关反应方程式:银离子:Ag++Cl-==AgCl↓AgCl+3NH3+H2O==Ag(NH3)2OH+NH4ClAg(NH3)2OH+3H++Cl-==AgCl↓+2NH4++H2O铅离子:Pb2++S2-==PbSPbS+2H+==Pb2++H2S↑Pb2++CrO42-==PbCrO4↓PbCrO4+4OH-==[Pb(OH)4]-+CrO42-[Pb(OH)4]-+CrO42-+4HAc==PbCrO4↓+4H2O+4Ac-铜离子:Cu2++S2-==CuSCuS+2H+==Cu2++H2S↑Cu2++[Fe(CN)6]2-==Cu2[Fe(CN)6]↓铁离子:Fe3++3OH-==Fe(OH)3↓♥ NO3-的鉴定亚硝酸盐与对氨基苯磺酸作用,生成不稳定的化合物,随即与α—萘胺作用,生成红色偶氮化合物。
三、实验注意事项1、单一离子鉴定可使用点滴板鉴定,可以节约试剂的用量。
实验二十六常见阳离子的分离和鉴定-2022年学习资料
5.Ba2+的鉴定-●取2滴0.5mol.L1BaC1,于试管中,加-入2mol-L-1HAc和2mol1NaAc各-2滴,然后滴加2滴1moL-1K2Cr○4-有黄色沉淀生成,示有Ba2+存在。-写出反应式
●2.Sn2+的鉴定-取5滴0.5mol-L-1SnCl,试管中,逐滴-o.-加入0.2molL-1HgC 2溶液,边加边-振荡,若产生的沉淀由白色变为灰-色,然后变为黑色,示有Sn2+存在。
·二、p区和ds区部分金属离子的鉴定-1.A13+的鉴定-取2滴0.5mol.L1A1C13溶液于小试管中 -加2~3滴水,2滴2mol-L-1HAc及2滴-0.1%铝试剂,搅拌后,置水浴上加热片-刻,再加入1~2 6mol.L1氨水,有红-色絮状沉淀产生,示有A]3+存在。
Pb2+的'鉴定-·取5滴0.5molL1PbNO32试液于离-心试管中,加2滴1molL1KCrO4 -液,如有黄色沉淀生成,在沉淀上-滴加数滴2mol.L1NaOH溶液,沉淀-溶解,示有Pb2+存在。
。因此,除了要熟悉离子的有关性质外,还要学-会运用离子平衡(酸碱、沉淀、氧化还原、络-合等平衡的规律控制反 条件。这对于我们-进一步了解离子分离条件和检出条件的选择将-有很大帮助。-。用于常见阳离子分离的性质是指常 阳离子与-常用试剂的反应及其差异,重点在于应用这种-差异性将离子分离。
[实验用品]见教材P169。
8.Zn2+的鉴定-取3滴0.2mol-L1ZnSO试液于试管中,-加2滴2mol.L1HAc溶液酸化,再 入-等体积硫氰酸汞铵NH4HgSCN4]-溶液,-摩擦试管壁,生成白色沉淀,示-有Zn2+存在。
9.Cd2+的鉴定-·取3滴0.2molL1CdNO2试液于小-试管中,加入2滴0.5molL1Na2S溶 液,生成亮黄色沉淀,示有Cd2+存-在。
常见阳离子的分离与鉴定
(3)实验三:亚锡离子的鉴定;取3滴0.5mol/L SnCl2溶液于试管中,逐滴加入0.2mol/L HgCl2溶液,边加边振荡。
《XXXXXXXXXXXX》实验报告
专业班级:********宋体四号
学生学号:********宋体四号
学生姓名:********宋体四号
实验教师:********宋体四号
开课学期:20~20 -学期
实验序号
7
项目名称
常见阳离子的分离与鉴定
学生学号
学生姓名
专业班级
实验பைடு நூலகம்师
实验时间
实验地点
分组序号
同组人数
(5)实验五:产生白色沉淀,在沉淀中加入6mol/L氨水至沉淀完全溶解,再用6mol/L HNO3溶液酸化,再产生白色沉淀,AgNO3+HCl = AgCl+HNO3,AgCl+2NH3.H2O = [Ag(NH3)2]Cl+2H2O,[Ag(NH3)2]Cl+2HNO3= AgCl+2NH4NO3
(3)实验三:溶液中产生的沉淀由白色变成灰色,又变成黑色,2HgCl2+SnCl2= Hg2Cl2(白色)+SnCl4,Hg2Cl2(白色)+SnCl2= 2Hg(黑色)+SnCl4
(4)实验四:先产生黄色沉淀,然后沉淀溶解,Pb(NO3)2+K2C2O4= PbC2O4+2KNO3,PbC2O4+2NaOH = Pb(OH)2+Na2C2O4
常见阳离子的分离与鉴定(一)
碱式盐 蓝 碱式盐 浅绿
浓NaOH
Co(OH)2 粉红 Ni(OH)2 绿
与NH3反应
Ag+ Cu2+ Ag2O 褐 Ag(NH3)2+ 无色
(一) 生成氢氧化物、氧化物或碱式盐沉淀,能溶于过 Cu(NH3)42+ 深蓝 碱式盐 蓝绿 量氨水,生成配离子的有: Cd(OH)2 白 Cd2+ Cd(NH ) 2+ 无色
2+
BaSO4 白 SrSO4 白 H2SO4 CaSO4 白 PbSO4 白,溶于NH4Ac,生成Pb(Ac)3Hg2SO4 白
Hg22+
Al3+ Cr
3+
与NaOH 反应 Al(OH) 白
3
AlO2- 无色 CrO2- 亮绿
Cr(OH)3 灰绿
22+ ZnO 过量 Zn Zn(OH) 白 2 无色 (一)生成两性氢氧化物沉淀,能溶于过量 NaOH的有: 2 适量 NaOH 2PbO Pb(OH) 白 Pb2+ NaOH 2 无色 2
Sb3+ Sn2+ Sn
4+ 2+
SbO(OH) 白 Sn(OH)2 白 Sn(OH)4或H4SnO4 白 Cu(OH)2 浅蓝
浓NaOH,加热
SbO2- 无色 SnO22-无色 SnO32-无色 少量溶解,生成CuO22- 蓝
Cu
Mg2+ Fe
3+ 2+
与NaOH 反应 Fe(OH) 红棕
3
Mg(OH)2 白
与(NH4)2CO3反应
• Al3+、Cr3+、Sn2+、Sn4+、Sb3+与 (NH4)2CO3反应,生成氢氧化物沉淀。
实验常见阳离子的分离与鉴定(一)
实验二十二:常见阳离子的分离与鉴定(一)〔实验目的〕1.巩固和进一步掌握一些金属元素及其化合物的性质;2.了解常见阳离子混合液的分离和检出的方法及巩固检出离子的操作。
〔实验原理〕1. 与HCl反应Ag+Hg22+HNO3及H2SO4Pb2+NH4Ac、NaOH2.Ba2+4↓白色,难溶于酸Sr2+4↓白色,溶于煮沸的酸Ca2+4↓白色,溶解度较大,当Ca2+浓度很大时,才析出沉淀Pb2+4↓白色,溶于NaOH、NH4Ac、热HCl、浓H2SO4,不溶于稀H2SO4 Ag+4↓白色,在浓溶液中产生沉淀,溶于热水3.Al3+AlO2-或[Al(OH)4]-浓NaOHZn2+2-或[Zn(OH)4]2-Cu2+Cu(OH)42-Pb2+ PbO2-或[Pb(OH)4]2-ΔSb3+SbO2-或[Sb(OH)4]-Sn2+SnO22-或[Sn(OH)4]2-4. 与NH3反应AgCuCdZn6.AgPbCuCdBiHg溶于王水,Na2SHgSbSb溶于浓HCl,NaOH,Na2SSnSn溶于浓HCl,(NH4)2S x,不溶于NaOH,Zn HCl溶液,不溶于HAc溶液Al HCl溶液5. 与(NH4)2CO3反应Cu2+Cu2(OH)2CO3↓浅蓝 Cu(NH3)42+ 深蓝Ag+Ag2CO3↓白色 (NH4)2CO3Ag(NH3)2+ 无色Zn2+Zn2(OH)2CO3↓白色 (过量)Zn(NH3)42+ 无色Cd2+Cd2(OH)2CO3↓白色 Cd(NH3)42+ 无色Hg2+ Hg2(OH)2CO3↓白色Hg22+Hg2CO3↓白色→HgO↓(黄)+ Hg↓(黑)+ CO2↑Mg2+Mg2(OH)2CO3↓白色Pb2+(NH4)2CO3Pb2(OH)2CO3↓白色Bi3+(适量)(BiO) 2CO3↓白色Ca2+CaCO3↓白色Sr2+SrCO3↓白色Ba2+BaCO3↓白色Al3+Al(OH)3↓白色Sn2+Sn(OH)2↓白色Sn4+Sn(OH)4↓白色Sb3+Sb(OH)3↓白色〔实验步骤〕内容步骤现象结论(解释)一、碱金属、碱土金属离子的鉴定1. Na+的鉴定NaCl + KSb(OH)6白色结晶Na+ + Sb(OH)6-=NaSb(OH)6(s)2. K+的鉴定KCl + NaHC4H4O6白色结晶K++ HC4H4O6-= KHC4H4O6(s)3. Mg2+的鉴定 MgCl2+NaOH+镁试剂先生成白色Mg(OH)2,后生反应式见后1成蓝色沉淀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
软亲软中的反馈键
M
dd反馈键
AA
d *反馈键
配合物的生成引起物质性质变化
• 溶解度变化:增大或沉淀生成,如Zn(OH)2/NH3、 Fe3+、Fe2+/CN-
• 酸碱性变化:使酸的酸性增强,使碱的碱性增强; 如HF/Al3+、Cu(OH)2/NH3
• 颜色改变:配位场的改变引起d-d跃迁光谱变化, 配体光谱也会因此而变;如Cu2+/NH3
物质的溶解度规律
• 盐的溶解度规律: ➢ 大体积的阳离子与大体积的阴离子结合水溶性小; ➢ 小体积的阳离子与小体积的阴离子结合水溶性小; ➢ 复盐的溶解度比单盐小; ➢ 除碱金属及铵以外的盐一般强酸盐大都易溶而弱酸
盐大都难溶。
• 小分子的相溶性规律:分子间作用力的种子的分离与鉴定(一)
• 配合物的生成与软硬酸碱理论:供电子的是碱; 接受电子的是酸。
• 硬酸:正氧化态高、离子半径小、不易变形; • 硬碱:负氧化态低、原(离)子半径小、不易变形。 • 软酸:正氧化态低、价层d电子数多、易变形; • 软碱:负氧化高、半径大、易变形、有价d空轨
道或低能量的*空分子轨道。
• 二2中改为HgCl2中加入SnCl2才会出书上的 现象。
• 做分离时在离心试管中进行;每次沉淀时 沉淀剂都是稍过量的;离心后清液用专用 滴管吸出留后用,沉淀经洗涤(加水后用 尖玻棒搅动,再离心,水洗液弃去)后再 用;滴管每吸液一次后都要用去离子水清 洗(三个烧杯都分盛去离子水,每个烧杯 吸三次都弃去)!
• 6 Cu2+ + [Fe(CN)6] 4- = Cu2 [Fe(CN)6]
• 7 Ag+ + Cl- = AgCl
• AgCl + 2NH3 = [Ag(NH3)2]+ + Cl• [Ag(NH3)2]+ + Cl- + 2H+ = AgCl + 2NH4+ • 8 Zn2+ + [Hg(SCN)4]2- = Zn [Hg(SCN)4] • 9 Cd2+ + S2- = CdS • 10 同2 • 三、参照前面的方程式
常见阳离子的分离与鉴定(一)
• 离子的软硬调节方法:降低电荷变软,升 高 化态电,荷降变氧硬化,态如变NH软3,N升H氧2-化N态3-变;硬改,变如氧 Cu2+Cu+;
• 软硬酸碱结合规律:软亲软、硬亲硬,软 硬结合不稳定。
• 软硬酸碱理论的成键解释: ➢硬亲硬是由于成键键长短而稳定; ➢软亲软是因为同时形成配位键和反馈配位
➢ 高氧化态金属与O形成的多原子阳离子,水溶液 和熔盐中均常见;如VO2+、BiO+、TiO2+等;
➢ 金属与非氧非金属形成的多原子阳离子,水溶液 中较少见,多见于熔盐中,如AlF2+等;
➢ 金属与配体形成的阳离子:很常见于配合物中;
➢ 非金属间形成的阳离子:较少见,一般是季胺类 和叔醚类,也有象NH4+和PCl4+等。
• Sn2+ + Hg2Cl2 = 2Hg + 2Cl- + Sn4+
• 3 Pb2+ + CrO42- = PbCrO4 ↓
• PbCrO4 + 4OH- = Pb(OH)42- + CrO42-
• 4 Sb3+ + NO2- +H2O + 6Cl- = SbCl6- + NO3- + 2H+
• 5 Bi3+ + SC(NH2)2 = [Bi(SC(NH2)2)4]3+
• 氧化还原性变化:降低了氧化型或还原型的浓度, 氧化型浓度降低则氧化能力下降、还原型的浓度 降低则还原能力下降。如Au +O2/CN-
常见阳离子的分离与鉴定
阳离子的形成方式
➢ 单原子阳离子:最常见的存在方式,通常是金属 阳离子,尤其在强酸性溶液中;
➢ 同核多原子阳离子:即离子簇,水溶液中较少见, 多见于熔盐和固体中,尤其是过渡金属易生成该 类阳离子。如Hg22+、Timn+等;
9-17e构型:d过渡元素中氧化态未达到其价电子数者; 通常有低能量的空(n-1)d价轨道,d电子少及氧化态高 者亲氧,d电子多且电荷低者亲硫;极易形成配合物。
阳离子的主要分离方法
• 氢氧化物的酸碱性:主要利用其两性。 • 配位能力:过渡元素的配位能力远强于主
族,以此将主族金属离子与过渡金属离子 分开。 • 沉淀的生成:主要利用氢氧化物(pH控制)、 硫化物(pH控制)和其它沉淀反应。 • 氧化还原性:过渡金属的氧化态变化大, 改变氧化态从而改变其性质,再进行分离。
相关反应方程式
• 1 Na+ + [Sb(OH)6]- = Na [Sb(OH)6] ↓ • 2 K+ + HC4H4O6- = K HC4H4O6 ↓ • 3 Mg2+ + 2OH- = Mg(OH)2 ↓吸附镁试剂成蓝色 • 4 Ca2+ + C2O42- = CaC2O4 ↓ • 5 Ba2+ + CrO42- = BaCrO4 ↓ • 二1 Al3+ + 3HR + 3NH3 = AlR3 ↓ + 3NH4+ • 2 Sn2+ + 2Hg2+ + 2Cl- = Hg2Cl2 ↓
简单阳离子的电子构型及特点: 8高e氧构化型态:金包属括阳IA、离I子IA、;A无l3d+、电子f区,及亲前氧d能过力渡强元,素除的前最d
过渡元素离子外均难形成稳定配合物。
1金8属e电元子素构的型最:高包氧括化IB态(I;)、1I8IB+(I2I)e和电第子四构周型期:及包以括下第p四区 周期及以下p区金属元素的最高氧化态-2。这两类电子 构型的共同特点是d电子最多,亲氧能力差,亲硫能力 强,形成配合物能力强于8e构型而弱于9-17e构型。
