溶血性链球菌检验原始记录
溶血性链球菌

氏染色阳性,球形或卵圆形,常排列成短链状。
3.3 触酶试验 挑取可疑菌落于洁净的载玻片上,滴加适量3%
过氧化氢溶液,立即产生气泡者为阳性。β型溶血 性链球菌触酶为阴性。
3.4 链激酶试验 吸取草酸钾血浆0.2 mL于0.8 mL灭菌生理盐水中混
2 分离 将增菌液划线接种于哥伦比亚CNA血琼脂平板,
36 ℃±1 ℃厌氧培养18 h~24 h,观察菌落形态。 溶血性链球菌在哥伦比亚CNA血琼脂平板上的典
型菌落形态为灰白色、半透明、光滑、表面突起、 圆形、边缘整齐,并产生β型溶血。 3 鉴定 3.1 分纯培养
挑取可疑菌落分别接种哥伦比亚血琼脂平板和接 种TSB增菌液, 36 ℃±1 ℃培养18 h~24 h。
3.5 杆菌肽敏感试验
取可疑菌纯培养物,在0.5 mL灭菌生理盐水 中混匀,用棉签沾取TSB增菌液均匀涂布于 哥伦比亚血琼脂平板上,用灭菌镊子夹取 杆菌肽纸片,放于琼脂表面,36 ℃±1 ℃培 养18 h~24 h,如出现抑菌圈即为敏感,同 时用已知敏感菌株作为阳性对照。β型溶血 性链球菌为杆菌肽敏感。
3.6 可选择使用生化鉴定试剂盒或生化鉴定 卡对可疑菌落进行鉴定。
结果与报告
综合以上试验结果,报告每25 g(mL)检 样中检出或未检出β型溶血性链球菌
亚血琼脂代替了血琼脂平板; —— 完善了操作步骤; —— 在人血浆的基础上增加了兔血浆和绵羊血浆; —— 增加了规范性附录A。
本标准所代替的历次版本发布情况为: GB 4789.11-1984、 GB/T 4789.11-1994、 GB/T 4789.11-2003。
溶血性链球菌检验程序
Байду номын сангаас报告
溶血性链球菌的检验

预防措施
采取积极的预防措施,如 加强个人卫生、避免接触 可能的感染源等,以降低 感染风险。
病情监测
对患者进行密切监测,及 时发现并处理可能出现的 并发症和异常情况,确保 患者安全。
05
注意事项与建议
实验室安全与防护措施
实验室防护
进行溶血性链球菌检验时,实验 操作区域应保持通风,工作人员 需佩戴一次性手套、实验服、口
溶血性链球菌的检验
2023-11-10
contents
目录
• 简介 • 检验方法 • 检验流程 • 结果分析 • 注意事项与建议
01
简介
溶血性链球菌的定义
• 溶血性链球菌是一种常见的革兰氏阳性菌,其特点是在培养过 程中能产生溶血现象。它是人体常见的病原菌之一,可引起多 种感染疾病,包括扁桃体炎、咽炎、丹毒、猩红热等。
03
检验流程
样品采集与处理
采集咽拭子、血液、尿液等样 品,确保采集方法和操作规范 。
将采集的咽拭子放入适量运输 培养基中,血液和尿液可直接 接种培养基。
在运输培养基中保存样品,尽 快送至实验室进行检测。
细菌分离与培养
将咽拭子接种至5%羊血平板和 巧克力平板上,血液和尿液接种
至巧克力平板上。
在35℃、5%CO2的环境中培养 24-48小时,观察细菌生长情况
04
结果分析
数据分析与解读
实验室数据评估
对实验数据进行分析,包括细 胞形态、生化反应、药敏试验 等,以确定溶血性链球菌的特
性。
数据对比与参照
将实验数据与已知的正常值或参考 范围进行对比,以确定是否存在异 常。
综合分析
结合患者的病史、临床症状和实验 室数据,进行综合分析,以确定病 情的严重程度和可能的治疗方案。
微生物检测原始记录【范本模板】
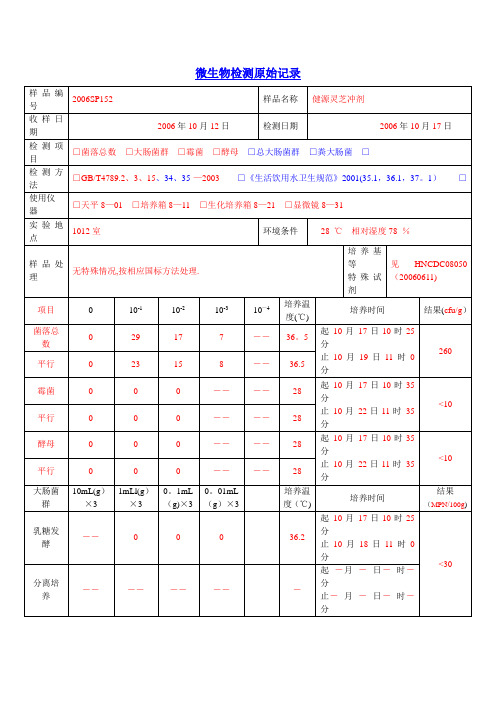
样品编号
2006SP152
样品名称
健源灵芝冲剂
收样日期
2006年10月12日
检测日期
2006年10月17日
检测项目
□菌落总数□大肠菌群□霉菌□酵母□总大肠菌群□粪大肠菌□
检测方法
□GB/T4789.2、3、15、34、35-—2003□《生活饮用水卫生规范》2001(35.1,36.1,37。1)□
沙门氏菌属
三糖铁:斜面无动力
产气-硫化氢-
5%甘棉甘靛
乳露子基
糖醇糖油质
A型---(+)-
B型-++-(+)
C型-+-(+)-
D型+++d-
生化特征为
□:痢疾志贺氏菌
□:福氏志贺氏菌
□:鲍氏志贺氏菌
□:宋内氏志贺氏菌
生化试验
甘露醇+特征为
金黄色葡萄球菌
三糖铁:斜面-产酸+
增菌与
分离
PB:36℃培养,起17日10时0分止17日14时0分,MM:42℃和SC:36℃培养起10月17日15时55分止10月18日15时0分,BS平皿:36℃培养起10月18日15时30分止10月20日14时0分。SS平皿:36℃培养起10月18日15时30分止10月20日14时0分.有/无可疑菌落
产气-硫化氢-
有动力
其它生化试验:
靛基质-甲基红+
V-P-赖氨酸+
溶血+甘露醇+
乌氨酸+精氨酸-
生化特征为
溶血性链球菌
微生物检测原始记录(致病菌)共2页第1页
HNCDC/JL09030
样品编号
2006SP152
样品名称
健源灵芝冲剂
项目
沙门氏菌
志贺氏菌
溶血性链球菌检验

【GB/T 4789.11—1994】食品卫生微生物学检验溶血性链球菌检验1 主题内容与适用范围本标准规定了食品中溶血性链球菌的检验方法。
本标准适用于食品和食物中毒样品中溶血性链球菌的检验。
2 引用标准GB 4789.28 食品卫生微生物学检验染色法、培养基和试剂3 设备和材料3.1 温箱:36±1℃。
3.2 水浴:36±1℃。
3.3 显微镜。
3.4 离心机。
3.5 试管架。
3.6 灭菌平皿。
3.7 灭菌小试管。
3.8 载玻片。
3.9 灭菌吸管:1mL、10mL。
3.10 灭菌镊子。
3.11 均质器。
3.12 酒精灯。
3.13 接种环。
4 培养基和试剂4.1 葡萄糖肉浸液肉汤:按GB 4789.28中4.1规定,在肉浸液肉汤内加入1%葡萄糖。
4.2 肉浸液肉汤:按GB 4789.28中4.1规定。
4.3 匹克氏肉汤:按GB 4789.28中4.62规定。
4.4 血琼脂平板:按GB 4789.28中4.6规定。
4.5 人血浆。
4.6 0.25%氯化钙。
4.7 灭菌生理盐水。
4.8 杆菌肽药敏纸片(含0.04单位)。
5 检验程序(图略)6 操作步骤6.1 样品处理称取25g固体检样;称取25mL液体检样,加入225mL灭菌生理盐水,研成匀浆制成混悬液。
6.2 一般培养将上述混悬液吸取5mL,接种于50mL葡萄糖肉浸液肉汤;或直接划线接种于血平板,如检样污染严重,可同时按上述量接种匹克氏肉汤,经36±1℃培养24h,接种血平板,置36±1℃培养24h,挑起乙型溶血圆形突起的细小菌落,在血平板上分纯,然后观察溶血情况及革兰氏染色,并进行链激酶试验及杆菌肽敏感试验。
6.3 形态与染色本菌呈球形或卵圆形,直径0.5~1μm,链状排列,链长短不一,短者4~8个细胞组成,长者20~30个,链的长短常与细菌的种类及生长环境有关;液体培养中易呈长链;在固体培养基中常呈短链,不形成芽孢,无鞭毛,不能运动。
细菌检验原始记录表(表格模板、doc格式)

TSB
BP
血凝
沙门氏菌(+,-/25g)
DHL
BS
TSI
CU
生化
血清
斜面
底层
产气
H2S
I
LD
VP
KCN
AFO
备注:
检验人:复核人:
你喜欢“细节或者小节,往往最能体现一个人的品格”。所以,你性格开朗、活泼可爱,用乐观感染着周围的同学;你尊敬师长,关心集体,学习自觉,尽量做到让家长老师宽心。各科成绩不太拔尖,但平衡。如此可爱的学生,老师希望你能坚定信心,有迎难而上的勇气,争取学习成绩有大的突破。
在教材中要呈现很多细腻的生活场面和真实案例。然而教材中的范例只是一种提示,它并不是唯一的或最好的。因此,老师要通过这些提示去整体把握教材,既可以利用这些范例丰富学生的认知和情感体验,又可以根据自己的教学需要进行隔离的取舍。或适当加以拓展!虽然是《思品与社会》检验时间
检验依据
SN0168-92 SN0169-92
SN0172-92 SN0170-92
检验项目
检验步骤
稀释度
检验结果
0.1
0.01
0.001
0.0001
0.00001
菌落总数(pes/g)
平板琼脂
大肠菌群(mpn/g)
LST
BGLB
大肠杆菌(mpn/g)
EC
EMB
I
(公共场所)溶血性链球菌测定原始记录表
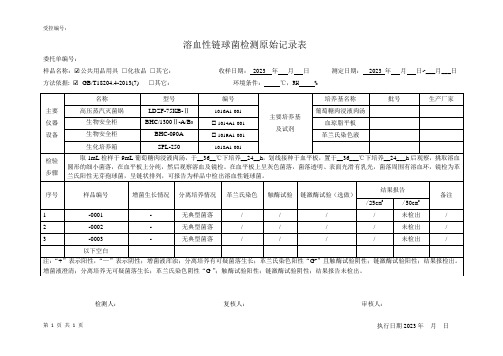
取 1mL 检样于 9mL 葡萄糖肉浸液肉汤,于__36__℃下培养__24__h,划线接种于血平板,置于__36___℃下培养__24___h 后观察,挑取溶血 圆形的细小菌落,在血平板上分纯,然后观察溶血及镜检。在血平板上呈灰色菌落,菌落透明、表面光滑有乳光,菌落周围有溶血环,镜检为革
兰氏阳性无芽孢球菌,呈链状排列,可报告为样品中检出溶血性链球菌。
检测人:
第1页共1页
复核人:
审核人: 执行日期 2023 年 月 日
序号
样品编号
增菌生长情况
分离培养情况
革兰氏染色
触酶试验 链激酶试验(选做)
结果报告
/25cm2
/50cm2备注1-0001-无典型菌落
/
/
/
/
未检出
/
2
-0002
-
无典型菌落
/
/
/
/
未检出
/
3
-0003
-
无典型菌落
/
/
/
/
未检出
/
以下空白
注:“+”表示阳性,“—”表示阴性;增菌液浑浊;分离培养有可疑菌落生长;革兰氏染色阳性“G+”且触酶试验阴性;链激酶试验阳性;结果报检出。 增菌液澄清;分离培养无可疑菌落生长;革兰氏染色阴性“G-”;触酶试验阳性;链激酶试验阴性;结果报告未检出。
型号
编号
培养基名称
批号
生产厂家
高压蒸汽灭菌锅 生物安全柜 生物安全柜
LDZF-75KB-Ⅱ BHC/1300Ⅱ-A/B3
BHC-090A
1016A1-001 1014A1-001 1019A1-001
主要培养基 及试剂
β型溶血性链球菌的测定

一、编制目的为规范本单位β型溶血性链球菌的检测编制本作业指导书。
二、适用范围本指导书适用于食品中β型溶血性链球菌的测定。
三、编制依据GB/T 4789.11-2014《食品安全国家标准食品微生物学检验β型溶血性链球菌检验》四、设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:a)恒温培养箱:36℃±1℃;b)冰箱:2℃~5℃;c)厌氧培养装置;d)天平:感量0.1g;e)均质器与配套均质袋;f)显微镜:10×~100×;g)无菌吸管:1ml(具0.01ml刻度)、10ml(具0.1ml刻度)或微量移液器及吸头h) 三角烧瓶;i)无菌培养皿:直径90mm;j)pH计或pH比色管或精密pH试纸;k)水浴装置:36℃±1℃;l)微生物生化鉴定系统。
五、培养基和试剂5.1.改良胰蛋白胨大豆肉汤5.2 哥伦比亚CNA血琼脂5.3 哥伦比亚血琼脂5.4 革兰氏染色液5.5 胰蛋白胨大豆肉汤5.6 草酸钾血浆5.7 0.25%氯化钙(CaCl2)溶液5.8 3%过氧化氢(H2O2)溶液5.9生化鉴定试剂盒或生化鉴定卡六、检验程序溶血性链球菌检验程序见图1图1溶血性链球菌检验程序七、操作步骤7.1样品处理及增菌以无菌操作取样25g(ml),加入装有灭菌225mlmTSB的均质杯,用旋转刀片式均质器以8000r/min~10000 r/min均质;或加入装有225ml mTSB的均质袋中,用拍击式均质器连续均质1min~2min,液体样品振荡混匀即可。
于36℃±1℃,厌氧培养18h~24h。
7.2 分离将增菌液划线接种于哥伦比亚CNA血琼脂,36℃±1℃,厌氧培养18h~24h,观察菌落形态。
溶血性链球在哥伦比亚CNA血琼脂平板上的典型菌落形态为直径约2mm~3mm,灰白色、半透明、光滑、表面凸起、圆形、边缘整齐,并产生β型溶血。
7.3 鉴定7.3.1分纯培养挑取5个(如小于5个则全选)可疑菌落分别接种哥伦比亚血琼脂平板和TSB增菌液,36℃±1℃,培养18h~24h。
鹤山地区孕晚期B族溶血性链球菌检测结果分析

t值
0292
6813
10571
1281
P值
0771
0000
0000
020和椎体外系
不良反应发生率高于对照组,差异有统计学意义(P<005); 两组在治疗中胃肠道不良反应发生率一致。见表 3。
表 3 两组患者不良反应比较[例(%)]
组别 例数 体质量增加
较好的治疗作用。精神分裂症表现为阳性和阴性症状[4],两 组患者在治疗后第 8周的 PANSS评分比较无差异也说明两种 药物治疗首发精神分裂症效果基本一致,但在治疗后第 2、第 4周观察组患者 PANSS评分明显高于对照组,说明奥氮平的 起效时间短于利培酮起效时间。 本次研究显示,应用奥氮平治疗的患者可有效提高患者 个人及社会功能评分,说明奥氮平患者治疗首发精神分裂症 效果在改善患者个人及社会功能评分上优于利培酮。本次研 究显示,两种药物胃肠道不良反应发生率一致,应用奥氮平治 疗的观察组患者椎体外系不良反应较少,但体质量增加的不 良反应率高于应用利培酮治疗的对照组。这可能与药物不良 反应与药物特定受体作用有关[5],奥氮平可抵消多巴胺受体 2阻断引起的椎体外系不良反应,但因奥氮平作用于多种系统 会引起患者体重增加。在临床用药中应根据患者睡眠、体质 量、睡眠等选择 合 适 的 药 物,过 度 兴 奋、偏 瘦、服 药 较 差、严 重 失眠患者可给予奥氮平加以治疗,而睡眠较多、身体肥胖的患 者可给予利培酮进行治疗。 综上所述,对于首发精神分裂症患者奥氮平和利培酮均 有较好的临床治疗效果,奥氮平的起效时间短,但是不良反应 相对较多,可根据患者自身情况选择合适药物进行治疗。
[关键词] 孕晚期;B族溶血性链球菌;检出率 ;耐药性
B族溶血性链球菌(GBS),又称无乳链球菌,是一种革兰 阳性细菌,主要 定 植 在 阴 道、胃 肠 道、尿 道 等 部 位。 分 娩 时 经
