钠钙硅玻璃化学分析方法
玻璃测试方法标准文摘

船用舷窗和矩形窗钢化安全玻璃非破坏性强度试验冲压法GB 3385-821 对象和使用范围本标准为执行ISO1095的舷窗玻璃和ISO3254的矩形窗玻璃规定了钢化安全玻璃非破坏性强度试验方法。
2 引用标准ISO 48硫化橡胶硬度测定法〔硬度为30~85IRHD〕ISO 1095 船用舷窗钢化安全玻璃ISO 3254 船用矩形窗钢化安全玻璃3 试验装置试验装置如图1所示的适当型式:a、A型:用于公称尺寸等于和大于250mm的舷窗玻璃和各种尺寸的矩形窗玻璃。
b、B型:用于公称尺寸200mm的舷窗玻璃。
建筑玻璃可见光透射比、太阳光直接透射比、太阳能总透射比、紫外线透射比及有关窗玻璃参数的测定GB/T 2680-94本标准参照采用国际标准ISO 9050-1990? 建筑玻璃——可见光透射比、太阳光直接透射比、太阳能总透射比、紫外线透射比及有关窗玻璃参数的测定?1 主题内容与适用范围本标准规定了建筑玻璃可见光透射〔反射〕比、太阳光直接透射〔反射、吸收〕比、太阳能总透射比、紫外线透射〔反射〕比、半球辐射率和遮蔽系数的测定条件和计算公式。
2 测定条件2.1 试样2.1.1 一般建筑玻璃和单层窗玻璃构件的试样,均采用同材质玻璃的切片。
钠钙硅硼玻璃化分析方法GB/T 1549-94Methods of chemical analysis of Sada-lime-alumina and borosilicate glass1 主题内容与适用范围本标准规定了钠钙硅铝硼玻璃的化学分析方法。
本标准适用于钠钙硅铝硼玻璃如中碱玻璃、无碱玻璃及类似组成玻璃的化学分析。
2 引用标准GB 1347 钠钙硅玻璃化学分析方法3 一般规定3.1 对同一测定对象,有些规定了不同的测定方法,可根据实际情况任选一种。
有争议时,以I法为仲裁法。
3.2 化学分析用的天平应准确至0.0001g;天平与砝码应定期进行检定。
“ 恒重〞系指连续两次称重之差不大于0.0002g。
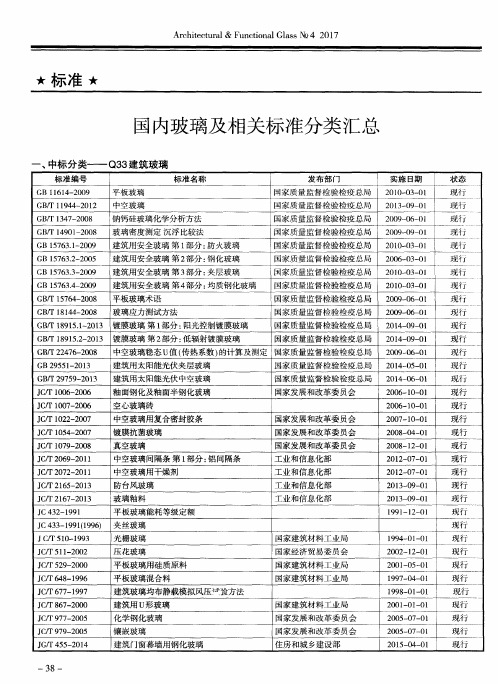
国内玻璃及相关标准分类汇总
现行 现行
G B / T 2 2 4 7 6 - 2 0 0 8
G B 2 9 5 5 1 - 2 0 1 3 G B / T 2 9 7 5 9 — 2 O 1 3 J C / T 1 0 0 6 — 2 0 0 6 J C 厂 r 1 O 0 7 — 2 0 0 6 J C / T 1 0 2 2 — 2 0 0 7 J C , 1 r 1 0 5 4 — 2 0 0 7 J C / T 1 0 7 9 — 2 0 0 8 J C / T 2 0 6 9 — 2 0 1 1 J C 厂 I 1 2 0 7 2 — 2 0 1 1 J C 厂 I ’ 2 1 6 5 — 2 0 1 3
G B 1 1 6 l 4 — 2 0 0 9
G B , r 1 1 9 4 4 — 2 0 1 2 G B 厂 1 1 3 4 7 — 2 0 0 8 G B / T 1 4 9 0 1 - 2 0 0 8
中空玻璃 钠钙 硅玻 璃化学分析方法 玻璃 密度测定 沉浮 比较法
Hale Waihona Puke 国家质量监督检验检疫 总局 2 0 l 3 — 0 9 — 0 1 国家质量监督检验检疫 总局 2 0 0 9 — 0 6 - 0 1 国家质量监督检验检疫 总局 2 0 0 9 — 0 9 一 O l
现 行 现行 现行
G B l 5 7 6 3 . 1 - 2 0 0 9 G B 1 5 7 6 3 . 2 — 2 0 0 5
现 行 现行
现行 现行
G B / T 1 5 7 6 4 — 2 0 0 8
C B / T 1 8 1 4 4 — 2 0 0 8
平板玻璃术语
玻璃应力测试方法
国家质量 监督检验 检疫 总局 2 0 0 9 — 0 6 — 0 1
工业分析思考题1-7章

5. 称取空气干燥基煤试样1.000 g,测定挥发份时,失去质量为0.2824 g,已知此空气干燥基煤试样中的水分为2.50 %,灰分为9.00 %,收到基水分为8.10 %,分别求收到基、空气干燥基、干基和干燥无灰基的挥发份及固定碳含量。
6. 什么是艾士卡试剂?在煤中硫的测定中,各组分的作用如何?
8、高锰酸钾氧化还原滴定锰时,铬、砷、锑干扰测定的原因是什么?用过氧化钠熔融法分解样品为什么能够分离铬、砷?
9、酸溶解硫化物矿石时,直接用硝酸热溶解和依次用盐酸、硝酸-高氯酸热溶解会得到什么不同的结果?
10、铬铁矿:为什么用过氧化钠熔解-水浸法可以较快地分解铬矿石,而用磷酸、硫酸等直接加热溶解则较慢?是何原因?
21、写出七种矿石主成分测定中的预处理反应和滴定反应,并指明终点指示方法。写出定量测定的计量关系。
第5章 思考题
1. 煤主要由哪些组份构成?各组份的作用如何?
2. 煤的分析有哪几类分析方法?煤的工业分析一般测定那些项目?
3. 煤中的水分以什么形态存在?应任何测定?
4. 称取空气干燥基煤试祥1.2000 g,测定挥发份时失去质量0.1420 g,测定灰份时残渣的质量0.1125 g,如已知空气干燥基水分为4%,求煤样的挥发份、灰份和固定碳的百分含量?
6、在燃烧法测定硫时,为什么不能用过量的碘标准溶液来吸收SO2,然后再用硫代硫酸钠标准溶液来返滴定剩余碘测定硫?为什么不能用过量氢氧化钾吸收SO2,反应完毕后再用加碘和酸化,硫代硫酸钠滴定的方法来测定硫?
各样品EDS分析元素

各样品EDS分析元素电子能谱分析(EDS)是一种常用的材料表征技术,可用于分析各种样品中的化学元素。
通过使用EDS,可以确定材料的成分、含量、分布以及化学环境。
下面将介绍一些常见样品的EDS分析元素。
1.金属材料:金属样品中常见的元素包括铁、铜、铝、锡、锌、钛等。
其中,铁是许多金属材料中的主要组成元素,而其他元素的含量通常较低。
通过EDS 分析,可以确定金属样品中各元素的含量和分布。
2.陶瓷材料:陶瓷样品中通常包含氧、硅、铝、钾、钙等元素。
其中,氧是陶瓷材料中最主要的元素,而硅是常见的陶瓷材料中的主要组成元素之一、通过EDS分析,可以确定陶瓷样品中各元素的含量和分布,从而帮助研究人员了解陶瓷材料的结构和特性。
3.生物材料:生物材料包括骨骼组织、牙齿、细胞等。
这些样品中的主要元素包括碳、氧、钙、磷、钠、镁等。
通过EDS分析,可以确定生物材料中各元素的含量和分布,有助于研究人员了解生物材料的组成以及与其功能相关的各元素之间的相互作用。
4.矿物石材:矿物石材包括大理石、花岗岩、石英等。
这些样品中的元素组成复杂多样,常见的有氧、硅、钙、镁、铝等。
通过EDS分析,可以确定矿物石材中各元素的含量和分布,从而帮助研究人员了解矿物石材的成分和地质特征。
5.玻璃材料:玻璃材料通常由氧、硅、钠、铝等元素组成。
其中,硅是玻璃材料中的主要组成元素,而其他元素的含量较低。
通过EDS分析,可以确定玻璃材料中各元素的含量和分布,从而帮助研究人员了解玻璃材料的成分和制备过程。
需要注意的是,EDS分析的结果受到许多因素的影响,包括样品的制备质量、仪器的性能以及分析条件的选择等。
为了获得准确可靠的结果,需要仔细选择样品制备方法、合适的EDS分析参数,并进行充分的仪器校准和质量控制。
总之,通过EDS分析,可以确定各种样品中的化学元素,从而为材料表征和研究提供有力支持。
不同样品中的元素组成及其分布情况各不相同,对于特定的样品和研究对象,可以选择合适的EDS分析方法和技术方案,以达到理想的研究目的。
测定煤灰中常量灰分元素的几种分析法

赵冰等
[3]
论述了采用电感耦合等离子体发
剂镧或锶将待测元素从与干扰元素的结合中释放
射光谱法对煤灰中硅、铝、钙、镁、钾、铁、磷、钛、钠
出来ꎻ消除物理干扰的办法是在标准溶液中加入
9 种常量元素进行测量ꎮ 采用的标液法与标灰法
的检出限范围分别为 0. 000 3 ~ 0. 014 1 mg / L、
0. 000 6 ~ 0. 011 3 mg / Lꎬ两种方法的检出限差异
测定方法 X 荧光光谱法» 、GB / T 4634—1996 « 煤灰中钾、钠、铁、钙、镁、锰的测定方法 ( 原子吸收分光光度
法) » ꎬ对大量测定煤灰灰成分的文献实验方法进行比较ꎮ 介绍了近年来常用的 4 种分析煤灰常规灰成分的方
法:常规国标的化学分析方法、X 荧光光谱法( 融片法和压片法) 、原子吸收光谱法和电感耦合等离子发射光谱
等多种元素ꎻ采用原子吸收光谱仪测试氧化钾、氧
化钠、三氧化二铁、氧化钙、氧化镁等物质ꎻ采用常
规国标化学分析法测试煤灰中各元素ꎮ 采用 X
磷、锰、钡 12 种煤灰灰分ꎮ 煤灰熔融制成样片ꎬ并
准样品给定值推算出的结果计算出样品测试回收
率在 96. 7% ~ 120. 0% ꎬ 满 足 检 测 量 的 需 求ꎻ 同
测试煤灰灰分含量的方法有:采用电感耦合
物形式报出结果ꎮ 宋义等 [1] 论述了采用熔融制
等离子发射光谱法测试煤砂中铁、钙、钠、镁、铝、
片法测试煤灰中硅、铝、铁、钙、镁、硫、钛、钾、钠、
测试煤灰中的硅、铝、铁、钙、镁、硫、钛、钾、钠、磷
利用建立的标准曲线进行测量ꎬ 由测试结果与标
钾、钛、硅、硫、磷等多种元素ꎻ采用 X 射线光谱仪
法ꎮ 剖析各种方法的优缺点以及应用过程中的问题ꎬ从而根据自身情况选择相应的方法ꎮ
第26届国际眼科光学和光学仪器标准会年会在德国柏林召开

从表4滴定结果来看, 在煮沸前加入掩蔽剂对实验结果影响较大, 会导致滴定结果偏低, 与标准样品中
A 1 0 , 含量 1 . 2 7 % ̄ H 差甚 远 ; 煮沸 后加 掩蔽 剂 , 滴 定 结果 比较 准确 , 与标 准样 品 值 A 1 O 含量 1 . 2 7 %接 近 。故 为 提高 滴定 准确 度 , 以煮 沸冷 却后 加掩 蔽 到 最佳状 态 , 分别 在 测 定 A 1 0 。 含 量 过 程 中不 同阶 段加 人 K F , 通过 观 察滴 定
结 果及 终点 颜 色变化 来确 定何 时加掩蔽 剂 才能 发挥 最大 的效 果 。
表 4是 根据 A 1 0, 滴定 过 程 中不 同阶段 加 K F滴 定结 果 , 从 而 寻找加 入 K F的最佳 时机 。
I S O F D I S 8 9 8 0 — 3和 I S O F D I S 1 4 8 8 9等 多项 国际标 准进 行 了热烈 的讨论 , 并 提 出了许 多修改 意见 。
1 O月 1 8日, I s O / T c 1 7 2 / s c 7召 开全体 代 表会 议 , 经会 议代 表 团表 决 , 一致 同意 第 2 7届 国 际眼科 光学 和 光 学仪 器标 准会 年会 于 2 0 1 5年 4月 或 5月在 中 国上海举 行 。 ( 仲 新)
参 考 文献 :
[ 1 ] G B / T 1 3 4 7 — 2 0 0 8 , 钠钙硅玻璃化学分析方法 [ s ] .
[ 2 ] 方 道腴 , 蔡祖 泉. 电光 源 工 艺 [ M] . 上海 : 复旦大学出版社 , 1 9 8 8 [ 3 ] G B 6 6 8 2 — 9 2 , 分析实验室用水规格和试验方法 [ s ] .
玻璃制备实验报告

华南师范大学实验报告学生姓名何嘉棋梁涌滨学号20122400078 20122400015专业材料化学年级、班级2012级课程名称无机非金属材料实验实验项目玻璃的制备实验类型验证设计综合实验时间2013 年12 月13日实验指导老师罗穗莲实验评分一.【实验目的】学习实验室条件下制备玻璃材料的基本训练学习玻璃的基本组成和配制二.【实验原理】绿色钠钙硅玻璃配方查资料得,钠钙硅玻璃化学组成范围如下表所示,由书上的钠钙硅玻璃的三元相图,SiO2 Na2O CaO65.8% 14.7% 8.5%,来提高玻璃的化学稳定性、热稳定性、机械强度、硬度和折射率。
加入MgO,范围为3.5%以下,是网络外体氧化物,可以使玻璃的硬化上单变慢,改善玻璃成形性能。
加入BaO,范围为0.5~1.0%,增加玻璃的折射率、密度、光泽和化学稳定性。
加入少量的Fe2O3作为脱色剂,加入少量的Cr2O3作为着色剂。
加完以下的原料之后为: Z=4R=(65.9*2+7.7*3+14.8+8.5+1.8+0.5+0.6*3+0.1*)/65.9=2.64X+Y=Z,X+Y/2=R,算去X 为1.28,Y 为2.72≈3,四面体三个是桥氧。
玻璃应该能连接成三维网络,应该保持较高的强度。
三.【实验药品与仪器】药品:二氧化硅 碳酸钙 碳酸钠 碱式碳酸镁 氧化铝 碳酸钡 氧化铁 碎玻璃仪器:坩埚四.【实验步骤】1、计算个组分原料使用配比。
2、将二氧化硅,碳酸钙,碳酸钠,碱式碳酸镁,氧化铝,碳酸钡,氧化铁,碎玻璃按照配比混合,研磨均匀。
五.【实验现象与分析】实验现象:玻璃内部产生较多裂纹,玻璃颜色为绿色,制备玻璃易碎。
结果分析: 名称SiO2 Al2O3 Na2O CaO MgO BaO Fe2O3 Cr2O3 比例(%)65.9 7.7 14.8 8.5 1.8 0.5 0.6 0.11、玻璃内部裂纹较多,证明在烧制过程中出现了较多的玻璃缺陷部分。
中国古代玻璃的起源

中国古代玻璃的起源——中国最早的古代玻璃研究作者:张婕转载日期:2011年06月22日访问次数:771干福熹①②* 承焕生① 李青会②(① 复旦大学, 上海200433; ② 中国科学院上海光学精密机械研究所, 上海 201800)摘要:研究了西汉(公元前200 年)以前不同地区的最早的中国古代玻璃. 古玻璃样品出土于新疆维吾尔自治区、湖北省、湖南省、四川省、云南省、广东省和贵州省等地. 用质子激发X 光荧光技术、能量分散X 光荧光技术和电感耦合等离子发射光谱等方法测定了玻璃的化学成分. 这些古玻璃样品的化学成分属于以下玻璃系统: Na2O(K2O)-CaO-SiO2(K2O:Na2O<1), K2O(Na2O)-CaO-SiO2(K2O:Na2O>1), K2O-SiO2 和BaO-PbO-SiO2. 从考古和历史学观点讨论了这些最早的中国古代玻璃的起源, 指出早期中国古代玻璃的制备技术是与中国的古代原始瓷和青铜冶炼技术相关. 分析了中外古代玻璃制造技术的关系.关键词:中国古代玻璃起源化学成分分析中国古代玻璃的科技考古始于20 世纪30 年代, 开创性的研究工作首先由Beck和Seligman等人[1,2]进行的. 对几十种主要从汉代至唐代的中国古代玻璃收藏样品的分析后, 认为这些古玻璃是在中国制造的, 以含氧化钡和氧化铅为这些玻璃的主要成分特征, 但是玻璃的制造技术来自西方[1,2]. 自20 世纪70 年代提出了中国古代玻璃“自创说”[3], 即中国最早的古代玻璃制造技术起源于中国. 这引起了我们这一领域的研究工作者的讨论. 近半个世纪以来, 在中国考古的发掘中出现了不少玻璃物品. 从20 世纪80 年代由于考古文物界与玻璃技术界的合作, 已积累了大量的玻璃分析数据, 但是大部分古玻璃制品属于汉朝和汉以后的(晚于公元前200 年), 对汉代以前的出土玻璃样品分析较少. 为了讨论中国古代玻璃的起源, 应该重点注意对汉代以前的古玻璃的研究. 本文提出了中国最早的古玻璃的化学成分的分析结果, 并讨论了这些玻璃的起源.1 古玻璃样品情况本文研究的古玻璃样品出土于新疆拜城县克孜尔、塔城铁厂沟以及哈密、和田(新疆省考古研究所提供); 湖北省江陵九店和随县(湖北省考古研究所提供); 四川青川、理县(四川省文物考古研究所提供); 贵州郝章(贵州省博物馆提供); 广东肇庆(广东省文物考古研究所提供); 云南江川(云南省博物馆提供); 内蒙古呼盟(内蒙古省文物考古研究所提供). 大部分玻璃物品为单色玻璃珠, 关于玻璃样品情况如表 1(表序 1~3), 古玻璃样品年代皆属西汉以前(公元前200年以前). 为了说明古代玻璃的传播, 也分析了一些中国边缘地区出土于公元前200 年以后的玻璃样品, 如表1(表序4).在烧制原始陶瓷时, 当炉温过高, 瓷釉会熔化后流下来形成釉滴, 俗称釉豆, 它已是透明的玻璃态物质, 可能是最早的中国古玻璃. 釉滴的样品来自出土于广东博罗(由广东省文物考古所提供), 样品情况见表1(表序5).表1 出土古玻璃样品情况2 实验方法实验中大部分样品的化学成分无损分析采用质子激发X光荧光技术(PIXE), 在复旦大学现代物理研究所加速器实验室进行. 实验采用外束 PIXE技术, 测量中样品置于大气中. NEC9SDH-2 串列加速器提供3.0 MeV的准直质子束, 真空与大气之间以7.5 μm的Kapton膜相隔, 实际到达样品的质子能量为 2.8 MeV. Ortec Si(Li)探测器(在5.9 MeV能量下, 峰值宽度为165 eV)放置在与质子束90°位置, 以探测样品发射的 X射线. 用GuPIX-96 程序可以从PIXE谱测得样品中元素序数大于12(Z≥12)的各元素的组成. 为了要测得玻璃中Na的含量, 部分样品在测量中用氦气包围, 以防止大气吸收损耗. 详细的实验过程见文献[4].少量样品也采用能量分散X 光荧光技术(EDXRF), 在中国科学院硅酸盐研究所进行, 用EDAX Eeagle Ⅲ设备, 与PIXE 结果作对比.用电感耦合等离子发射光谱法(ICP-AES)进行破碎样品的化学分析, 在中国科学院上海光学精密机械研究所进行. 用已知化学成分的光学玻璃ZF-1(高铅硅酸盐玻璃), BaF2(钡铅硅酸盐玻璃)和窗玻璃(钠钙硅酸盐玻璃)作为标样. 有些古玻璃样品同时用上述两种方法PIXE 或 EDXRF 与ICP-AES 对比.3 实验结果所研究的古玻璃的化学成分的分析结果见表2, 这些西汉以前中国最早古玻璃的化学成分可分3 大类: (ⅰ) 含碱钙硅酸盐玻璃(R2O- CaO-SiO2, 其中R2O 为 K2O 和 Na2O), 由于氧化钠和氧化钾含量不同, 可按氧化物重量比(K2O:Na2O)分成两种: 第一种为 K2O:Na2O <1; 第二种为K2O:Na2O>1; (ⅱ) 铅钡硅酸盐玻璃(BaO-PbO-SiO2); (ⅲ) 钾硅酸盐玻璃(K2O-SiO2).表2 出土玻璃的化学成分从表2 可以看到, 新疆与中原和西南各省的古玻璃的化学成分有很大不同, 它只有一类: 含碱钙硅酸盐玻璃, 并且K2O:Na2O<1, 只属于(ⅰ)类中的第一种. 中原和西南各省的古玻璃化学成分, 上述3 类玻璃皆有.广东博罗出土的原始瓷的釉滴的化学成分见表 2(表序 5), 它属于高钙釉滴, 其中K2O: Na2O>1.4 结果讨论从以上实验可以看到, 中国中原地区(黄河和长江流域)与西北地区(古称西域)出土最早的古玻璃的化学成分是不同的, 由此可以估计到, 它们的起源也有区别, 现分别讨论如下.4.1 中原地区中国最早的古玻璃的成分演变及其起源中国的古代青铜冶炼和炼丹技术起源于商代(公元前16 世纪~公元前11 世纪), 而原始瓷也出现于这个时期. 这时原始瓷的烧成温度一般已达到1100℃~1200 , ℃ 已有熔炼用的耐火坩埚. 中国原始瓷釉常应用植物灰作助熔剂, 因为植物草木灰的成分相差较大, 有高钙釉和低钙釉两类. 表3(表序1)列举了江西的原始瓷釉的化学成分, 它属于低钙釉. 表3(表序2)给出了广东博罗出土的原始瓷釉的化学成分, 它属于高钙釉 [5]. 从表3 中可以看到, 不论是高钙或低钙釉, 其中K2O的含量高于Na2O的含量, 这是应用植物草木灰作助熔剂的特征.表3 原始瓷釉的化学成分到西周和东周早期(春秋)炉温可以更高一些, 原始瓷在烧成时温度过高而流下来形成的透明釉滴, 已属玻璃态物质. 从我们测定的广东博罗釉滴的化学成分可知, 见表2(表序5), 它的化学成分特征也是K2O 含量大于Na2O 的含量. 釉滴可能是中国最早的古玻璃, 因为在当时十分稀少而名贵, 用作贵族的首饰和剑饰的镶嵌物.中国中原地区最早的真正的玻璃物品产生于东周早期(春秋时期), 出土的玻璃物品不多, 目前看来只有3 例: 河南固始侯古堆一号墓(吴国太子夫差的妻子之墓, 公元前504 年)的蜻蜓眼式玻璃珠[6]; 河南辉县南部战国早期墓中的吴王夫差(公元前495 年~公元前473 年)剑格上的蓝色玻璃[7]; 湖北江陵望山一号楚墓的越王勾践(公元前496 年~公元前464 年)剑格上的蓝色玻璃[8]. 湖北随县曾侯乙墓(~公元前400 年)的料珠, 它还不是全部玻璃态的, 属玻砂(frit)[9]. 由于出土时实验条件的限制, 未作仔细和完整的分析研究, 并且用不同方法测定的玻璃的化学成分也不同, 见表4, 但皆属含碱钙硅酸盐玻璃(R2O-CaO-SiO2), 由于分子比K2O:Na2O的不同分为两类.最近我们对上述古玻璃在可能的条件下再做进一步的研究. 越王勾践的剑格上的镶嵌玻璃在20 世纪80 年代初在主要对剑身作PIXE分析时也作了分析, 最近我们找了它的PIXE谱图[12], 见图1(a), 它属于钾钙硅酸盐玻璃. 我们用PIXE方法和 EDXRF方法分析了在同地(湖北江陵望山)出土的时代稍后(公元前450 年~公元前400 年)的楚墓玻璃珠(HB-3), 其化学成分见表2(表序 5), 它属于含K2O很高的含碱钙硅酸盐玻璃. 图1(b)表示了该玻璃样品的PIXE谱图. 可以看到图1(a)与(b)是十分相似的, 可以确定越王勾践的剑饰玻璃, 也是同类的玻璃系统. 这种玻璃的化学成分是在古埃及和古巴比伦玻璃中所未见的. 对比湖北江陵九店的玻璃(HB-3)与江西低钙原始瓷釉的化学成分, 见表2(表序2)与3(表序1), 可以看到它们之间的化学成分十分接近. 这说明中国中原最早的古玻璃制备技术可能从原始瓷釉技术演变而来, 产地都在长江流域. 原始瓷的瓷釉是用釉浆涂敷于陶器表面, 它不需要容器. 从制备瓷釉到制备玻璃, 在工艺上的最大变化为熔炼玻璃要有容器——耐火的坩埚, 但这在起源于商代(公元前16 世纪~公元前11 世纪)的青铜冶炼和炼丹的基础上已有条件.图1 古玻璃的PIXE 谱图(a) 湖北江陵望山出土越王勾践的剑饰上玻璃;(b) 湖北江陵望山楚墓出土玻璃珠碎片(HB-3)为了提高玻璃的透明度和降低玻璃的熔化温度, 中国古人用不同的途径在改进助熔剂上作努力. 铅丹(氧化铅)和硝石(硝酸钾)在春秋时期人们已熟悉它们, 作为药材, 而它们有助熔剂的作用, 因此战国时期, 铅钡硅酸盐玻璃和钾硅酸盐玻璃在长江流域首先发展.中国冶炼青铜中使用铅的技术起源很早, 铅能降低熔化温度并增加流动性. 早期的青铜为铜-锡-铅的合金, 所以在中国商、周时期制备青铜时已有应用铅矿的经验. 在长江流域地区, 如湖南、安徽和江西等地富产铅矿, 如方铅矿(PbS)和钡矿如重晶石(BaSO4), 人们用它们来作为玻璃的助熔剂是可以理解的. 中国铅钡硅酸盐玻璃的出土地点往往和铅矿的分布地点相一致, 在长江流域. 安徽亳州出土的半透明眼珠, 属春秋末战国初(公元前6 世纪~公元前5 世纪). 这是目前发现最早的铅钡硅酸盐玻璃品, 玻璃成分见表4(表序2). 湖南长沙资兴出土了东周的琉璃璧, 其化学成分也为铅钡硅酸盐玻璃系统, 有 100 多座墓中出土具有中国特征的玻璃璧、珠、印、剑管等200 多件, 可见当时已较普遍应用[16]. 在战国中、晚期, 铅钡硅酸盐玻璃制品已在中国的南方和西南地区发现, 如表2(表序3).中国古代铅钡硅酸盐玻璃主要采用模压的工艺, 这也是从青铜的制造中引用过来的, 至汉代已能制造大尺寸的平板玻璃, 如西汉早期广州南越王墓中已发现9.5 cm×4.5 cm×0.3 cm的平板玻璃[17], 陕西汉茂陵出土的直径为23.4 cm, 厚1.8 cm, 重达 1.9 kg的玻璃璧[18], 山东即墨出土的铅钡硅酸盐玻璃厚板, 尺寸达32.5 cm ×14.8 cm ×3.5 cm, 重量达5.25 kg[19]. 铅钡硅酸盐玻璃在中国战国至汉代之际, 在全国有很大的流传和扩展, 从南方的广东和广西, 西南的四川和贵州, 西北传至青海和甘肃, 东北至辽宁, 见图2.图2 战国至汉代我国古代铅钡硅酸盐玻璃和钾硅酸盐玻璃的出土地点示意图●示铅钡硅酸盐玻璃; +示钾硅酸盐玻璃中国古人在改进玻璃的助熔剂的另一途径为在早期含碱钙硅酸盐玻璃中增加K2O 的含量. 用硝石代替草木灰作助熔剂, 可以增加K2O的含量. 中国古人使用硝石很早, 作为药物, 在西汉时期已有史料记载. 由于硝石的熔点低(330℃), 因此也很早应用于古代炼丹术[20].20 世纪80 年代在对广西出土的古玻璃的成分分析中发现这些玻璃中Al2O3, CaO 和Na2O的含量皆很低(<3%), 而K2O 含量很高(>10%), 是比较典型的钾硅酸盐玻璃[15]. 这些古玻璃大都出土于汉代的古墓中. 目前已发现最早的钾硅酸盐玻璃珠出土于战国的古墓中, 如表2(表序2)和4(表序2). 湖北江陵和湖南长沙楚墓中, 钾硅酸盐玻璃与铅钡硅酸盐珠同时作为墓葬品[3]. 由此可见, 钾硅酸盐玻璃与铅钡硅酸盐玻璃几乎同时制作于长江流域. 至西汉前期, 钾硅酸盐玻璃也出土于西南, 见表2(表序3). 土壤的表面层有钾硝石生成, 特别在气候温暖的地方, 在雨季后进入炎热的天气时, 土壤表面有钾硝石生成. 所以广东和广西出土了汉代的钾硅酸盐玻璃, 成为中国古代钾硅酸盐玻璃的主要产地.钾硅酸盐玻璃在东南亚及印度也有出土, 见表4(表序3), 但数量不多. 如上所述, 中国春秋时期已有K2O 含量很高的硅酸盐玻璃, 时间早于印度出土的钾硅酸盐玻璃. 中国最早的钾硅酸盐玻璃产生于战国, 西汉时期已有压铸的器皿出现, 时间与东南亚和印度的古玻璃近似, 但是中国的出土数量超过国外很多. 广西合浦和贵县是海上丝绸之路的出海口, 在西汉前与国外已有文化和贸易的交往是无疑的, 有古代玻璃制造技术从外传入而在当地生产的可能性. 但是, 中国南方古代玻璃制造技术主要从中原扩展而来的, 用本地较丰富的玻璃助熔剂硝石来制备钾硅酸盐玻璃. 在广东和广西已有战国、西汉期间铅钡硅酸盐玻璃出土, 见表1(表序3), 这些玻璃也可能在南方制作, 有些古玻璃制造工艺已十分精致, 如广州西汉南越王墓的平板玻璃(铅钡硅酸盐玻璃). 因此钾硅酸盐玻璃在中国南方属于从中原的玻璃制造技术扩展而来, 并自己开发和制造.表5 一批新疆古玻璃的化学成分4.2 西域地区中国最早的古玻璃的成分特征及其起源我国新疆地处中亚(古代为西域地区), 是我国中原与西亚来往的要地. 新疆出土的古代玻璃都具有中外交往的特色. 新疆拜城和塔城出土的都是早期的玻璃珠, 这批玻璃珠均为单色无镶嵌的. 西方在公元前16 世纪~公元前13 世纪已有单色珠, 公元前13 世纪出现彩色珠, 在公元前 10 世纪~公元前6 世纪已流行镶嵌珠. 新疆拜城地区出土的这批玻璃珠都是单色珠, 图案式型也比较简单. 出土的早期玻璃珠中尚未发现当时流行的镶嵌玻璃珠.从表 2(表序 1)可知, 新疆地区这批早期玻璃珠的化学成分与西亚的古玻璃非常接近, 但玻璃中含有较多气泡, 其技术水平相比之下比较差. 这正说明当时从西方主要带来了玻璃制造技术, 而不是玻璃制品. 因为对技术的吸收和创造要有一个过程, 当时借鉴了西亚的玻璃制造技术, 采用当地的矿物, 如滑石、辉石、蛇纹石以及草木灰等原料制备出当地早期的玻璃珠. 同一地区的另一批玻璃曾用扫描电子显微镜能谱分析法 (SEM-EDM)分析[24], 结果见表5, 其K2O:Na2O比值接近于1, 与西亚玻璃成分不同, 更说明玻璃是本地制备的. 在新疆拜城和塔城出土的有些玻璃中同时含有较高的 PbO和Sb2O3, 见表2(表序1)中样品 XJ-2A和XJ-2B 和表5 中91BKKM-2 和91BKKM -26 是同时期西亚和中亚古玻璃中未发现的, 这与当地原料的特点和炼铜技术有关. 所以, 玻璃是用本地材料制造的[25].新疆拜城出土的玻璃珠, 其年代为公元前1100 年~公元前500 年(西周至春秋), 在西亚为第二亚述帝国(公元前1100 年~公元前700 年)晚期和中亚波斯帝国(公元前550 年~公元前529年)的前期, 这时古代的欧亚游牧民族已经东迁. 欧亚大陆草原地形开阔、平坦, 游牧民族的来去倏忽、迁徙无常, 对古代人们的往来起了很大的作用. 在新石器时代后期(公元前4000 年) 为印欧语系人, 其中雅利安人(Ariya)于公元前3000 年进入中东地区, 并于公元前2000 年从伊朗地区进入印度次大陆[26]. 也有人认为新疆塔里木盆地的居民在语言上属于印欧语系, 因此推断人种就是雅利安族人.从西亚的玻璃制造技术的扩展, 我们还可能看到更细微一些的情况. 在印欧人进入中东和西亚之际, 其中一派为胡里安人 (Hurrian), 在西亚于公元前2000 多年前就知道青铜、铁器和玻璃的制造. 于公元前14~15 世纪西亚米坦尼王朝(Mitanni)崩溃后移至中亚伊朗北部乌拉尔图(Urartu), 公元前7 世纪当亚述人(Assyria)侵入后, 移至目前阿尔美尼亚地区(Armenia), 其中的一派称为斯基泰人(Scythian), 来到中国新疆[27]. 波斯化的斯基泰人, 古波斯和印度文献称之为“萨迦人”, 古希腊罗马作家称之为“西叙亚人”(Sere), 汉文史籍称之为塞人. 活动的范围在迄今新疆伊犁地区、中亚北部七河地区、阿尔太地区及蒙古草原等. 塞族游牧民扮演了中外文化传播的东西陆路交通开拓者的角色.从上面的情况分析可知, 在新疆出土的公元前10 世纪~公元前8 世纪之际的钠钾钙硅酸盐玻璃珠属从西亚传入玻璃制造技术, 塞族古人在当地制作. 所以, 一般认为中国的丝绸的外传为最早的中外文化与技术交流的代表, 而玻璃技术的传入也可能成为最早的中外文化和技术交流的见证.如上所述, 中国中原地区的古玻璃制造要晚于新疆地区近400~500 年. 西周到战国时期古玻璃有可能通过原始的丝绸之路传人中原, 如同新疆的和田玉传入中原一样. 但由于路途的艰苦, 传入的玻璃品(主要为玻璃珠)是很少的, 如表4(表序1), 属战国早期的河南固始侯古堆蜻蜓眼玻璃珠和表2(表序2)所示的湖北随县曾侯乙墓的玻璃珠(HB-6)的化学成分很接近新疆克孜尔的玻璃成分.中外玻璃文化和技术的交流主要还从张骞凿空通西域以后, 主要的发展是在公元1 世纪~公元5 世纪, 当时世界古典文明时代上出现四大帝国, 即东方的东汉帝国、西欧和西亚的罗马(Roman)帝国、中亚的波斯(Persia, 中国汉朝称安息)帝国和南亚的贵霜(Kushan)帝国, 皆处于强盛时期, 丝绸之路贯穿于这四个帝国而畅通无阻, 促进了中外的交往和交流. 从西域(新疆地区)大月氏人带来了西方玻璃制品和技术, 而中原有特色的制造于汉、晋时期(公元200 年~公元300 年)的铅钡硅酸盐的单色珠和多色镶嵌玻璃珠也流传至新疆的哈密和和田, 玻璃 (XJ-42)的化学成分见表2(表序4). 该镶嵌玻璃珠出土于新疆和田阿克斯皮里古城, 为黑色基体, 眼部为绿色玻璃镶嵌在白色烧结体中, 制作得比较精致, 已体现出当时玻璃制造技术的进步.5 结论从对中国最早的古代玻璃的化学成分分析的结果可以看到, 我国古代玻璃技术的发展具有它自己的明显特色. 中国中原地区最早的古玻璃制造是从原始瓷的瓷釉制作演变过来, 用草木灰作助熔剂, 始于春秋和战国早期, 玻璃成分属含碱钙硅酸盐玻璃系统, 其中K2O 含量大于Na2O 为其主要特征, 而区别于古巴比伦和古埃及的玻璃成分. 随着制备玻璃的助熔剂的改进, 在战国中、晚期, 采用了在古代青铜制备技术和炼丹术中使用的 PbO, 发展了成分特殊的铅钡硅酸盐玻璃; 另一方面采用硝石作助熔剂而形成了钾硅酸盐玻璃. 这两类玻璃发展至汉代, 已传至我国境内南方和北方地区, 外传至朝鲜半岛、日本、东南亚和中亚地区.新疆拜城地区克孜尔古墓的玻璃是我国境内出土最早的玻璃, 玻璃的主要成分和西亚古玻璃成分相似, 但含有地方矿产特征的氧化物, 如 PbO 和Sb2O3 等. 玻璃珠的质地和艺术结构低于当时的古巴比伦和古埃及的水平, 可能是通过欧亚草原游牧部落, 如胡里安人和斯基泰人传入玻璃制作技术, 而塞族人在当地制作. 极少量的玻璃珠通过原始的丝绸之路传入中原, 主要的中外古代玻璃技术和文化的交流在汉通西域之后.参考文献1 Beck H C, Seligman C G. Barium in ancientglass. Nature, 1934, 133(6): 982—9832 Seligman C G, Ritchie P D, Beck H C. Early Chinese glass from Pre-Han to Tang’s times. Nature, 1936, 138: 721—7243 干福熹, 黄振发, 肖炳荣. 我国古代玻璃的起源问题. 硅酸盐学报, 1978, 6(1-2): 99—1044 李青会, 张斌, 承焕生, 等. 质子激发X 荧光技术在中国古玻璃分析中的应用. 硅酸盐学报, 2003, 31: 39—435 罗宏杰, 李家治, 高力明. 原始瓷化学组成及显微结构研究. 硅酸盐学报, 1996,24(1): 114—1186 河南省文物研究所, 三门峡市文物工作队. 淅川下寺春秋楚墓. 北京: 文物出版社, 19917 崔墨材. 河南辉县发现吴王夫差铜剑. 中原文物特刊, 19818 陈振裕. 望山一号墓的年代与墓主. 中国考古学会第一次年会论文集. 北京: 文物出版社, 19789 湖北省博物馆. 曾侯乙墓. 北京: 文物出版社, 1989. 65810 张福康, 程朱海, 张志刚. 中国古琉璃的研究. 硅酸盐学报, 1983, 11(1): 70—7111 后德俊. 谈我国古代玻璃的几个问题. 见: 干福熹, 编, 中国古代玻璃研究—1984 年北京国际玻璃学术讨论会论文集. 北京: 中国建筑工业出版社, 1988. 6012 Chen J X, Li H K, Ren C G, et al. PIXE Research with an external beam. Nucl Instrum Methods, 1980, 168: 437—440[DOI]13 史美光, 何欧里, 吴宗道, 等. 一批中国古代玻璃的研究. 见: 干福熹, 编. 中国古玻璃研究——1984 年北京国际玻璃讨论会论文集. 北京: 中国建筑工业出版社, 1988. 5—914 Shi M G, He D L, Zhou F Z. Chemical composition of ancient glasses unearthed in China. In: Proceedings of 15th InternationalCongress on Glass. Leningrad: Nauka, 1989. 7—1215 史美光, 何欧里, 周福征. 一批中国汉墓出土钾玻璃的研究. 硅酸盐学报, 1986,14(3): 307—31316 周世荣. 湖南出土琉璃器的主要特点及其重要意义. 考古, 1988, (6): 547—55517 广州市文物管理委员会. 广州汉墓. 北京: 文物出版社, 198218 王志杰, 朱捷元. 汉茂陵及其陪葬塚附近新发现的重要文物. 文物, 1976, (7): 51—5619 Shi M G, Zhou F Z. Investigation on ancient flat glass unearthed from Chian. Proceedings of 16th International Congress onGlass. Bol Soc Esp Cerm Vid, 1992, 7: 161—16620 孟乃昌. 汉唐硝石名实考辨. 自然科学史研究, 1983, 2(2): 97—11121 Lal B B. Examination of some ancient Indian glass specimens. Acient India, 1952, 8: 17—2722 Ngnyen T K Y(阮长奇). Ko Thuy Tinh co D Viet Nam(越南古玻璃). Henei(河内), 199823 Brill R H, Fang D M, Lange D E. Chemical analysis of some Asianglass. Proceedings of 17th International Congress onGlass. Beijing: Chinese Ceramic Society, 1995. 6: 463—46824 潜伟, 张平, 李前懋. 新疆克孜尔水库墓地出土玻璃珠的分析与研究. 见: 万辅彬, 巴莫尔, 编. 2000 年西昌第五届中国少数民族科技史国际研讨会论文集. 南宁: 广西民族出版社, 2001. 138—14525 干福熹, 李青会, 顾冬红, 等. 新疆拜城和塔城出土的早期玻璃珠的研究. 硅酸盐学报, 2003, 31: 663—66826 Stavrianos L S. A Global History. 4th ed. New Jersey: Pretice-HallInc, 1988. 58—6627 Engle A. Glass making in China. Read Glass Hist, 1976, 6-7: 1—54。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
钠钙硅玻璃化学分析方法1 主题内容与适用范围本标准规定了钠、钙、硅玻璃的化学分析方法。
本标准适用于钠、钙、硅玻璃,如建筑用平板玻璃或类似组成的玻璃化学分析。
2 分析方法2.1 标准中对同一组分并列的测定方法,可根据实际情况任选一种。
在有争议时,同一组分并列的测定方法以1法为准。
2.1.2 化学分析所用的天平应精确至0.0001克。
天平与砝码应定期进检定。
称取试样时应精确至0.0002克。
2.1.3 化学分析所用的滴定管、容量瓶、移液管应进行校正。
2.1.4 分析试样应于105~110℃烘箱中烘干1小时,在干燥器中冷却至室温后称量。
2.1.5 化学分析所用的水应为蒸馏水或去离子水;所用试剂应为分析纯或优级纯;用于标定的试剂除另有说明外应为基准试剂,标准溶液应定期标定。
在进行分析时,应作空白试验。
2.2 试样的制备试样经清选后粉碎,避免引进杂质,通过孔径为0.08毫米筛,贮存于带磨口塞的磨口瓶中备用。
2.3 烧失量的测定称取约1克试样于已恒重的铂坩埚或瓷坩埚中,放入高温炉内,从低温升起,在550℃灼烧1小时。
在干燥器中冷却至室温,称量。
反复灼烧,直至恒重。
G-G1X1=-------×100 (1)式中:G—灼烧前试样重量,克;G1—灼烧后试样重量,克。
2.4 二氧化硅的测定2.4.1 重量法-分光光度法2.4.1.1 试剂与仪器a 无水碳酸负。
b 盐酸(比重1.19,+1,5+95,1M)。
c 硫酸(1+4)。
d 40%氢氟酸。
e 氢氧化钠溶液[10%(m/ν)]:称取10克氢氧化钠于塑料杯中,加1000毫升水溶解,贮存于塑料瓶中。
f 氟化钾溶液[2%(m/ν)]:称取2克氟化钾于塑料杯中,加100毫升水溶解,贮存于塑料瓶中。
g 硼酸溶液[2%(m/ν)]。
h 对硝基酚指示剂[0.5%(m/ν)]:溶于乙醇中。
i 95%乙醇。
j 钼酸铵[(NH4)6Mo7O24 4H2O]:称取8克钼酸铵溶于100毫升水中,过滤,贮存于塑料瓶中。
h 抗坏血酸溶液[2%(m/ν)]:使用时配制。
i 二氧化硅标准溶液:准确称取0.1000克预先经1000℃灼烧1小时高纯石英(纯度为99.99%以上)于铂坩埚中,加2克无水碳酸钠,混匀。
先低温加热,逐渐升高温度到1000℃,得到透明熔体,继续熔融3~5分钟。
冷却,用热水浸取熔块于300毫升的塑为杯中,加入150毫升沸水,搅拌使期溶解(此时溶液应澄清)。
冷却,移入1升容量瓶中,用水稀释至杯线,摇匀立即转移到塑料瓶贮存。
此溶液每毫升含0.1毫克二氧化硅。
m 分光光度计。
2.4.1.2 二氧化硅比色标准曲线的绘制于一组100毫升容量中,加5毫升1M盐酸及20毫升水,摇匀,取0,1.0,2.0,3.0,4.0,5.0,6.0,7.0,8毫升二氧化硅标准溶液,加8毫升钼酸铵溶液,摇匀,于20~30℃放置15分钟,15毫升盐酸(1+1),用水稀释至90毫升左可。
加5毫升坏血酸溶液用水稀释至标线,摇匀。
1小时后,于分光光度计上,以试剂空白作参比,选用5毫米比色皿,在波长700纳米处测定溶液的吸光度。
按测得吸光度与比色溶液浓度的关系绘制标准曲线。
2.4.1.3 分析步骤称取约0.5克试样于铂坩埚中,加1.5克无水碳酸钠,与试样混匀,再取0.5克无水碳酸钠铺表面,盖上坩埚盖,先低温加热,逐渐升高温度至1000℃,熔融至透明状态,继续熔融15分钟。
用坩埚钳夹持坩埚,小心旋转,使熔融物均匀地附在坩埚内壁。
冷却,用热水浸取熔块入铂蒸发皿(或瓷蒸发皿)中。
盖上表面皿,加10毫升盐酸(1+1)溶解熔块,用少量盐酸(1+1)及热水洗净坩埚,洗液并入蒸发皿内,将皿置于水浴上蒸发至无盐酸味,冷却。
加5毫升盐酸(比重1.19),放置约5分钟,加50毫升热水,搅拌使盐类溶解。
用中速定量滤纸倾泻过滤,滤液用250毫升容量瓶承接,以热盐酸(5+95)洗涤皿壁及沉淀8~10次,热水洗~5次。
在沉淀上加4滴硫酸(1+4),将滤纸和沉淀移入铂坩埚中,放在电炉上低温烘干,升高温度使滤纸充分灰化。
于1100℃灼烧1小时,在干燥器中冷却至室温,称量。
反复灼烧,直到至恒重。
将沉淀用水润湿,加4滴硫酸(1+4)及5~7毫升氢氟酸,于低温电炉上蒸发至干,重复处理一交次。
逐渐升高温度驱尽三氧化硫白烟,将残渣于1100℃灼烧15分钟,在干燥器中冷却至室温,称量。
反复灼烧直至恒重。
将上面的滤液用水稀释至标线,摇匀。
吸取25毫长滤液于100毫升塑料杯中,加5毫升氟化钾溶液,摇匀。
放置10分钟后,加5毫升硼酸溶液,中1滴对硝基酚指示剂,滴加氢氧化钠溶液至溶液变黄色,加5毫升1M盐酸,移入100毫升容量瓶中。
加8毫升乙醇,以下分析步骤同标准曲线的绘制,测定吸光度。
从标准曲线上查得二氧化硅的含量(C)。
二氧化硅的百分含量(X2)按式(2)计算:G1-G2 C ×10X2=(--------+----------)×100 (2)G G×100式中:G1—灼烧后未经氢氟酸处理的沉淀及坩埚重量,克;G2—经氢氟酸处理后灼烧的残渣及坩埚重量,克;G—试样重量,克;C—在标准曲线上查得所分取滤液中二氧化硅的含量,毫克。
2.4.2 容量法(氟硅酸钾法)2.4.2.1 试剂a 硝酸(比重1.42)。
b 盐酸(1+1)。
c 氢氧化钾。
d 95%乙醇。
e 氯化钾。
f 氟化钾溶液[5%(m/ν)]。
g 氯化钾溶液[5%(m/ν)]:称取5克氯化钾,溶于50毫升水中,加50毫升乙醇,摇匀。
h 氯化钾乙醇溶液[15%(m/ν)]:称取15克氟化钾放在塑料杯中,加80毫升水和20毫升硝酸使其溶解,加氯化钾至饱和,放置过夜,过滤到塑料瓶中。
i 酚酞指示剂[1%(m/ν)]:溶于乙醇中。
j 0.15M氢氧化钠标准溶液:称取30克氢氧化钠溶于5升经煮沸过的冷水中,贮存于装有钠石灰干燥管的塑料瓶中,充分摇匀。
氢氧化钠标准溶液的标定:称取约0.7克苯二甲酸钾于300毫升烧杯中,加放150毫升经煮沸、 冷却、中和过的水,搅拌使其溶解。
加15滴酚酞指示剂,用氢氧化钠标准溶液滴定至微红色。
氢氧化钠标准溶液对二氧化硅的滴定度按式(3)计算:m×60.08×1000GSO2=---------------- (3)ν ×816.80式中:Yso2—氢氧化钠标准溶液对二氧化硅的滴定度,毫克/毫升;m—称取苯二甲酸氢钾重量,克;ν— 滴定时消耗氢氧化钠标准溶液的体积,毫升;60.08—二氧化硅的分子量;816.08—苯二甲酸氢钾的分子量。
2.4.2.2 分析步骤称取约0.1克试样于镍坩埚中,加2克左右氢氧化钾,先低温熔融,经常摇支坩埚。
然后,在600~650℃继续熔融15~20分钟。
旋转坩埚,使熔融物均匀地附着在坩埚内壁。
冷却,用热水浸取熔融物于300毫升塑料杯中。
盖上表面皿,一次加入15毫升硝酸,再用少量盐酸(1+1)及水洗净坩埚,洗液并于塑料杯中,控制试液体积在60毫升左右。
冷却至室温,在搅拌下加入氯入钾至过饱和(过饱和量控制在0.5~1克),缓慢加入10毫升氟化钾溶液,用塑料棒搅拌,放置7~10分钟。
用塑料漏斗或涂蜡玻璃漏斗以快速定性滤纸过滤,用氯化钾溶液洗涤塑料杯2~3次,再洗涤滤纸一次。
将滤纸和沉淀放回原塑料杯中,沿杯壁加入10毫升氯化钾乙醇溶液及1毫升酚酞指示剂。
用0.15M氢氧化钠标准溶液中和未洗净的残余酸,仔细搅拌滤纸,并擦洗杯壁,直至试液呈现微红色不消失。
加入200~250毫升中和过的沸水,立即以0.15M氢氧化钠标准溶液滴定至微红色。
二氧化硅的百分含量(X2)按式(4)计算:Tso2×νX=------------×100 (4)G ×1000式中: Tso2—氢氧化钠标准溶液对二氧化硅的滴定度,毫克/毫升;ν—滴定时消耗氢氧化钠标准溶液的体积,毫升;G—试样重量,克。
2.5 三氧化二铝的测定2.5.1 试剂a 40%氢氟酸。
b 硫酸(1+1)。
c 盐酸(1+1)。
d 氨水(1+1)。
e 36%乙酸。
f 氢氧化钾溶液[20%(m/ν)]:贮存于塑料瓶中。
g 六次甲基四胺溶液。
h 二甲酚橙指示剂[0.2%(m/ν)]。
i 0.01M乙二胺四乙酸二钠(EDTA)标准溶液:称取3.7克EDTA于烧杯中,加入约200毫升水,加热溶解,用水稀释至1升;j 0.01M乙酸锌标准溶液:称取2.1克乙酸锌于烧杯中,加入少量水及2毫升乙酸溶液,用水稀释至1升。
k 氧化钙标准溶液:准确称取l.7848克预先经105~110℃烘干2小时的碳酸钙溶于20毫升盐酸(1+1)中,加热微沸,以驱尽二氧化碳。
冷却,移入1升容量瓶中,用水稀释至标线,摇匀。
此溶液每毫升含1毫克氧化钙。
i 钙指示剂[2-羟基(2)羟基-4-磺酸-1重氮萘)-萘酸]:将1克钙指示剂与50克硫酸钾混合,在玛瑙乳钵中研磨混匀,贮存于磨口棕色瓶中。
EDTA标准溶液的标定:吸取10毫升氧化钙标准溶液于300毫升烧杯中,加约150毫升水,滴加氢氧化钾溶液调节PH值近似为12后,再加2毫升氢氧化钾溶液于。
加入适量的钙指示剂,用0.01MEDTA标准溶液滴定至由酒红色变为亮蓝色。
EDTA标准溶液对三氧化二铝、氧化钙、氧化镁的滴定度按式(5)、(6)、(7)计算:m 101.96TAl2O3=------------×-------- (5)ν×56.08 2mTCaO=--- (6)νmTMgO=------------×40.30 (7)ν×56.08式中:TAl2O3—EDTA标准溶液对三氧化二铝的滴定度,毫克/毫升;TCa—EDTA标准溶液对氧化钙的滴定度,毫克/毫升;TMgO—EDTA标准溶液对氧化镁的滴定度,毫克/毫升;m—取氧化钙的量,毫克;ν—标定时消耗EDTA标准溶液的体积,毫升;101.96—三氧化二铝的分子量;56.08—氧化钙的分子量;40.03—氧化镁的分子量。
乙酸锌标准溶液与EDTA标准溶液体积比的测定:取10毫升0.01MEDTA标准溶液于300毫升烧杯中,加约150毫升水,再加5毫升六次甲基四胺溶液(此时溶液PH应为5.5~5.8)和3~4滴二甲酚橙指示剂,用0.01M乙酸锌标准溶液滴定至溶液由黄色变为红色。
乙酸锌标准溶液体积比按式(8)计算:10K=----- (8)ν式中:K—每毫升乙酸锌标准溶液相当于EDTA标准溶液的毫升数;ν—滴定时消耗乙酸锌标准溶液的体积,毫升。
2.5.2 分析步骤称取约0.5克试样于铂皿中,用少量水润湿,加1毫升硫酸(1+1)和7~10毫升氢氟酸,于低温电炉上蒸发至冒三氧化硫白烟。
