微波常压法合成正丁醚
正丁醚的制备
反应装置
蒸馏纯化装置
步骤: 反应
按图装置仪器。在250mL三颈园底烧瓶中, 加入31mL正丁醇和约5mL浓 硫酸, 摇动使混合均匀, 并加入几粒沸石。在分水器中装(V-3)mL水, 然后将 烧瓶在石棉网上用小火加热, 使瓶内液体沸腾, 开始回馏, 在分水器中可以发 现液面增加, 这是由于反应生成的水以及未反应的正丁醇,经冷凝管聚集在分 水器内, 由于比重的不同, 水在下层, 而比重较水轻的正丁醇浮于水面而流回 到反应瓶中, 继续加热到瓶内温度升高到134~135℃(约需1h)。待分水器已
全部被水充满时, 表示反应已基本完成。
纯化 反应物冷却后, 把反应物连同分水器中的水一起到入内盛50mL水的分液 漏斗中,充分振摇, 静止后, 分出产物正丁醚, 用两份15 mL50%硫酸萃取洗涤 两次, 再用15 mL水洗涤两次, 然后用无水氯化钙(1~2g)干燥。 干燥后的产 物仔细地注入50mL蒸馏烧瓶中, 蒸馏收集139~144℃的馏份。
正丁醚的制备
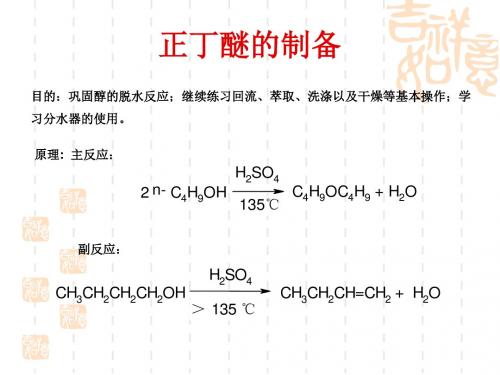
目的:巩固醇的脱水反应;继续练习回流、萃取、洗涤以及干燥等基本操作;学 习分水器的使用。 原理: 主反应:
2 n- C4H9OH
H2SO4 135℃ C4H9OC4H9 + H2O
副反应:
H2SO4 CH3CH2CH2CH2OH > 135 ℃ CH3CH2CH=CH2 + H2O
装置:
注意事项:
ቤተ መጻሕፍቲ ባይዱ
1)加热回流时加热速度不能过快,反应后期可适当提高加热功率,但反 应温度不能过高,防止副反应和积炭; 2)用硫酸洗涤时应注意硫酸的加入速度; 3)蒸馏时防止蒸干。 问题: 1) 如何严格控制反应温度?怎样得知反应比较完全了? 2) 各步洗涤的目的是什么?
正丁醚的合成

正丁醚的合成
一、目的和要求
掌握由正丁醇分子间脱水制备正丁醚的原理 和实验方法。 掌握分水装置的安装和操作。 掌握控制反应温度的实验技能。 掌握较高沸点液态有机物的蒸馏操作技能。 巩固萃取和蒸馏的基本操作。
二、实验原理
主反应:
2 CH3CH2CH2CH2OH
H2SO4 ~135 C
o
CH3CH2CH2CH2OCH2CH2CH2CH3 + H2O
注意事项
1. 投料时须充分摇动,否则硫酸局部过浓,加热后易使 反 应溶液变黑。
2. 反应开始回流时,因为有恒沸物的存在,温度不可能马 上达到 135℃。但随着水被蒸出,温度逐渐升高,最后达 到 135℃以上,即应停止加热。如果温度升得太高,反应 溶液会炭化变黑,并有大量副产物丁烯生成。
思考题
1. 使用分水器的目的是什么? 2. 制备正丁醚时,试计算在本实验中理论上应分出 多少体积的水? 3. 反应物冷却后,为什么要倒入水中?精制时,各 步洗涤的目的何在?
1. 仪器 三口烧瓶(100ml), 球形冷凝管, 分水器等。 2. 试剂 正丁醇,浓H2SO4, 50%硫酸,无水CaCl2。
四、分水装置
分水器
五、实验步骤
100mL干燥三口瓶
7 mL正丁醇 1 mL浓硫酸 1-2粒沸石
* 图3.3-1 *分水器检漏 *分水器装满水,再放出1mL
振摇,混合均匀
装分水装置
加热至微沸,回流分水 至分水器基本被水充满
停止加热 冷却后倾入含50 mL
水的分液漏斗中
分液,弃下层
粗正丁醚
(有机层)
1. 2×5 mL 50% H2SO4洗涤 2. 10 mL水洗涤
无水CaCl2干燥
正丁醚的制备5页word文档

实验教案课题(项目)名称:正丁醚的制备计划学时: 6 实验类型: 1.演示性□ 2.验证性□ 3.综合性√ 4.设计性□ 5.其它□授课日期: 年月日第周星期第节正丁醚的制备一、目的要求1.掌握醇分子间脱水制醚的反应原理和实验方法。
2.学习分水器的实验操作。
3.巩固分液漏斗的实验操作。
二、基本原理反应式主反应:副反应:物理常数:四、实验步骤在50 mL两颈瓶中加入5.2 mL 正丁醇,0.8 mL 浓硫酸,两粒沸石,摇动混合均匀,安好装置。
分水器内加水至支管后放去0.5 mL水即分水器内有( V—0.5 ) mL水。
开始小火加热,保持瓶内液体微沸,开始回流,温度控制在134~135 ℃,待分水器已全部被水充满时表示反应已基本完成(约需1小时),停止加热。
反应物冷却后,把混合物连同分水器里的水一起倒入内盛7 mL水的分液漏斗中,充分振摇。
静止后,分出产物粗制正丁醚,用50 % H2SO4洗涤两次(3 mL ×2),再用5 mL水洗涤一次。
分出有机层。
用无水氯化钙干燥产品。
将干燥后的粗产品倒入圆底烧瓶中蒸馏(注意不要把氯化钙倒入瓶中!),收集139~142 ℃的馏分。
称量产品,计算产率,测定折光率及红外光谱。
五、实验装置六、注意事项1. 加料时,正丁醇和浓硫酸如不充分摇动混匀,硫酸局部过浓,加热后易使反应溶液变黑。
2. 按反应式计算,生成水的量约为0.8 g左右,但是实际分出水的体积要略大于理论计算量,因为有单分子脱水的副产物生成。
3. 本实验利用恒沸混合物蒸馏方法,采用分水器将反应生成的水层上面的有机层不断流回到反应瓶中,而将生成的水除去。
在反应液中,正丁醚和水形成恒沸物,沸点为94.1 ℃,含水。
正丁醚的制备

正丁醚的制备一、目的要求1.掌握醇分子间脱水制醚的反应原理和实验方法。
2.学习分水器的实验操作。
3.巩固分液漏斗的实验操作。
二、基本原理反应式主反应:副反应:物理常数:四、实验步骤在50 mL两颈瓶中加入5.2 mL 正丁醇,0.8 mL 浓硫酸,两粒沸石,摇动混合均匀,安好装置。
分水器内加水至支管后放去0.5 mL水即分水器内有( V—0.5 ) mL水。
开始小火加热,保持瓶内液体微沸,开始回流,温度控制在134~135 ℃,待分水器已全部被水充满时表示反应已基本完成(约需1小时),停止加热。
反应物冷却后,把混合物连同分水器里的水一起倒入内盛7 mL水的分液漏斗中,充分振摇。
静止后,分出产物粗制正丁醚,用50 % H2SO4洗涤两次(3 mL ×2),再用5 mL水洗涤一次。
分出有机层。
用无水氯化钙干燥产品。
将干燥后的粗产品倒入圆底烧瓶中蒸馏(注意不要把氯化钙倒入瓶中!),收集139~142 ℃的馏分。
称量产品,计算产率,测定折光率及红外光谱。
五、实验装置六、注意事项1. 加料时,正丁醇和浓硫酸如不充分摇动混匀,硫酸局部过浓,加热后易使反应溶液变黑。
2. 按反应式计算,生成水的量约为0.8 g左右,但是实际分出水的体积要略大于理论计算量,因为有单分子脱水的副产物生成。
3. 本实验利用恒沸混合物蒸馏方法,采用分水器将反应生成的水层上面的有机层不断流回到反应瓶中,而将生成的水除去。
在反应液中,正丁醚和水形成恒沸物,沸点为94.1 ℃,含水33.4 %。
正丁醇和水形成恒沸物,沸点为93 ℃,含水45.5 %。
正丁醚和正丁醇形成二元恒沸物,沸点为117.6 ℃,含正丁醇82.5 %。
此外正丁醚还能和正丁醇、水形成三元恒沸物,沸点为90.6 ℃,含正丁醇34.6 %,含水29.9 %。
这些含水的恒沸物冷凝后,在分水器中分层。
上层主要是正丁醇和正丁醚,下层主要是水。
利用分水器可以使分水器上层的有机物流回反应器中。
正丁醚的制备.

正丁醚的制备一.实验目的 1.学习和掌握正丁醚的制备原理和方法2.掌握分液漏斗的使用,带分水器的回流操作二.反应式三.实验试剂 正丁醇 31ml ,浓硫酸 5ml ,50% H 2SO 4 / H 2O四.实验步骤配料(加一粒沸石)安装反应装置分水器加水小火加热沸腾,回流停火,冷却改为蒸馏装置 补加一粒沸石 蒸 馏15ml 50% H SO / H O 洗两次,除正丁醇(H 2O,正丁醇,正丁醚)有机层 有机层15ml H 2O 洗两次,除H 2SO 4 有机层1-1.5g CaCl 2干燥除水 粗产物蒸 馏收集139-143℃馏分产品(称重上交,计算产率)五.实验注意事项1.加料时摇荡烧瓶使浓硫酸与正丁醇混合均匀2.了解分水器的原理和使用范围,正确使用分水器3.回流反应时,用小火加热,不可用分层火焰4.改为蒸馏装置时,要充分冷却,再加1~2粒沸石,防止暴沸5.在后处理洗涤过程中,要清楚有机层和水层及各步洗涤的目的6.用无水CaCl 2 干燥时,所用锥形瓶要干燥无水7.H 2SO 4分清98%浓硫酸和50%硫酸讲解部分:1.实验反应的关键是控制反应温度(强调火焰的调节,反应瓶底离石棉网0.5-1cm 的距离,避免温度太高)2.配料时,先加正丁醇,再缓加浓H 2SO 4 ,并晃动烧瓶,同时用冷水浴冷却;否则温度上升太高,浓H 2SO 4 会将正丁醇氧化。
2 CH 3CH 2CH 2CH 2OH( CH 3CH 2CH 2CH 2 )2 O H 2O +24主反应:副反应: CH 3CH 2CH 2CH 2OH CH 3CH 2CH = CH 2 H 2O H 2SO 4 , >135 ℃+反应仪器装置的安装要点(第一次合成实验则讲)3.分水器①安装装好反应瓶,调好高度后,装分水器,首先向分水器中加水到离支管处2-3mm ,再试一下分水器是否能顺利的放水、并不漏水。
②介绍分水器的原理和使用方法,特别是放水的具体操作,控制流出速度。
正丁醚制备实验报告doc

正丁醚制备实验报告篇一:正丁醚实验报告XX 年 12 月 7 日姓名系年级组别同组者科目有机化学实验题目制备正丁醚仪器编号【实验目的】1. 掌握分子间脱水制醚的反应原理和实验方法。
2. 学习使用分水器,进一步训练和熟练掌握回流、加热和萃取等基本操作。
【实验原理】利用醇钠与卤代烃反应合成醚,这种合成方法的反应机理是烷氧负离子对卤代烷或硫酸酯的亲核取代反应。
醇分子间脱水生成醚是制备简单醚的常用方法。
用硫酸作为催化剂,在不同的温度下正丁醇和硫酸作用生成的产物会有不同,主要是正丁醚或丁烯,因此反应需严格控制温度。
浓H2SO4主反应浓H2SO4副反应【主要仪器及实验装置图】主要仪器如表1所示。
表1主要仪器主要实验装置图如图1所示。
图1.分水装置制备正丁醚【主要试剂及产物的理化参数】主要试剂及产物的物化性质如表2所示。
表2要物料及产物的理化参数【主要试剂用量及其计算】主要试剂试剂用量及其计算如表3所示。
表3要试剂试剂用量及其计算【实验流程】【实验记录】【产率】?%?m1?m2?100%m1 49?36.2??100%?58.2%49【讨论】若不缓慢倒入浓硫酸,将会导致部分原料碳化,影响产品质量与产率。
且温度应控制得当,以免产生较多的副产物。
【思考题】1.如何得知反应已经比较完全?答:分水器全部被水充满时,可认为反应比较完全。
2.反应物冷却后为什么要倒入50ml水中?各步的洗涤目的何在?答:反应物倒入50ml水中以除去正丁醇。
在5%NaOH溶液中以除去副产品丁烯,加水除NaOH,加饱和CaCl2除去水与醇。
3.能否用本实验方法由乙醇和2-丁醇制备乙基仲丁基醚?你认为用什么方法比较好?答:不能,因为会发生重排反应,使副产物增多。
可使用威廉孙制醚法。
篇二:正丁醚的制备有机化学实验报告实验七正丁醚的制备实验日期:XX年11月14日一、实验目的:1、掌握醇分子间脱水制备醚的反应原理和实验方法。
2、学习使用分水器的实验操作。
正丁醚的制备

实验十五、正丁醚的制备一、实验目的1.掌握低级伯醇脱水制备醚的方法。
2.熟悉分水器的安装和使用方法。
二、实验原理低级伯醇在酸性脱水剂催化下,共热生成单醚。
主反应:CH3CH2CH2CH2OH H SO(CH3CH2CH2CH2)2O+H2O副反应:CH3CH2CH2CH2OH H SOCH3CH2CH2CH2+H2O三、实验仪器及试剂仪器:250 mL四口瓶分水器球形冷凝管分液漏斗温度计蒸馏装置试剂:正丁醇浓硫酸5%的氢氧化钠溶液饱和氯化钙溶液无水氯化钙四、实验操作反应装置如下图所示。
正丁醚的制备在250 mL的四口瓶中加入31 mL正丁醇,再加入5 mL浓硫酸,充分摇匀后加入2~3粒沸石。
将反应装置在电热套上加热至微沸,进行反应。
反应进行中,水层不断增加,反应温度逐渐上升。
如果水层超过分水器的支管,可打开分水器下面的旋钮,分出一部分水。
当反应达到134~136℃时(约1.5 h),可停止加热(若继续加热,则反应液变黑并有较多副产物烯的生成),然后将反应物冷却至室温。
将馏出液倒入盛有50 mL水的分液漏斗中,充分振荡,静置,分出水层。
粗产物依次用25 mL水、50 mL 5%的NaOH、15 mL水和15 mL饱和氯化钙溶液洗涤,最后用无水氯化钙干燥。
干燥好的产物进行蒸馏,收集140~144℃馏分。
纯正丁醚为无色液体,沸点142.2℃,d420=0.773,n D20=1.399。
五、实验记录1.所加试剂的量2.所得产物的量六、思考与讨论1.计算本实验反应中应生成水的量。
2.如何得知反应已经完全?3.反应物冷却后为什么倒入50 mL的水中?各步洗涤的目的何在?七、注意事项1.分水器中先预加入一定体积的水。
2.制备正丁醚的适宜温度是130~140℃,但开始回流时,这个温度很难达到,因为正丁醚与水形成共沸物(b.p.=94.1℃,含水33.4%)。
另外,正丁醚与水和正丁醇形成三元共沸物(b.p.=90.6℃,含水29.9%正丁醇34.6%),正丁醇也可与水形成共沸物(b.p.=93℃,含水44.5%)故应在100~115℃之间反应0.5 h之后才可达到130℃以上。
固体超强酸固定床催化正丁醇制备丁醚研究

固体超强酸固定床催化正丁醇制备丁醚研究正丁醚,又名二丁醚,是一种性能良好的有机溶剂,其蒸汽压低,且基本不溶于水,对有机化合物的溶解能力强,所以它是较乙醚更为良好的萃取剂,可作为有机合成中的惰性介质及溶剂。
同时作为液态醚类,在提高柴油十六烷值(CN)的同时,也可促进柴油完全燃烧,降低尾气烟度,是一类较理想的柴油机含氧燃料。
微波技术以其特有的优点受到各国化学工作者的关注。
与常规加热法相比,微波辐射促进合成方法具有显著的节能、提高反应速率、缩短反应时间、减少污染且能实现一些常规方法难以实现的反应等优点。
由美国CEM公司研制的Discover微波精确有机合成系统,是世界上唯一无需机械转动的单模微波有机合成系统,也是唯一的通过内置系统软件控制所有条件和系统参数的微波合成系统,在专业微波合成反应方面已经显示了它的优越性。
Discover采用专利环形腔设计,单模微波,自动变频输出,普通的微波辐射更集中,使反应更快速。
正丁醚,又名二丁醚,是一种性能良好的有机溶剂,对许多有机化合物都有很强的溶解力。
正丁醚同水的分离性好,在贮存时生成过氧化物毒性和危险性少,是安全性很高的溶剂。
正丁醚是对称醚,在酸催化下醇分子间失水是制备对称醚的传统制备方法。
制备正丁醚的实验方法都是采用一次把正丁醇和浓硫酸原料加进反应瓶,混合均匀后加热回流,将生成的水分出,温度控制在135℃以下,产率都在32%~36%左右。
曾有人研究认为正丁醚产率受分水量影响,随着分出水量的增加产率提高可达50%。
采用正丁醚的传统制备方法时有机物易碳化,副产物多,且产品难分离提纯,催化剂不可重复使用,污染较大,有待进一步改进,将催化剂改为固体超强酸可有效解决这些问题。
本文采用固体超强酸做催化剂,对超强酸催化制备正丁醚的工艺条件进行了研究。
一、实验部分1.仪器与试剂。
正丁醇(CP 天津市天大化工实验厂)管式固定床反应系统(北京卫星制造厂)HPGC/6890/MS5973气-质联用仪,美国;色谱条件:弹性石英毛细管柱、载气He、气化室280℃、接口温度280℃、柱温80℃、以15℃/min升温至150℃,再以20℃/min升温至240℃;质谱条件:电离源EI、电子能量70ev、离子源温度230℃、质量范围30-500v、电压1.40kv。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
微 波 输 出 功 率 的增 大 而 增加 , 40 ~4 0 微 波 功 率 最 适 宜 . 率 过 大 时 , 应 一 开 始 以 0W 8W 功 反 就 迅 速 生 成 大 量水 , 放 出大 量 气 体 , 丁 醚 的 产 量 很 低 . 是 由 于 发 生 了 正 丁 醇 分 子 内 并 正 这 脱 水 生 成 丁烯 的 副 反 应 微 波 方 法 和 常 规 方 法对 照 实 验 的结 果 见 表 3 .
微 波 常 压 法 合 成 正 丁 醚
范 平 ‘ 崔 瑾 葛 春 华 , , 高 晓 玮 杨 春 常 ,
( 1辽 宁大 学 化 学科 学 与工 程学 院 . 宁 沈 阳 103 辽 10 6 2辽 宁省 标 准样 品开 发 中心 , 宁 沈 阳 10 o ) 辽 1o 6
摘
要 : 用微 波 常压 法 用 正 丁醇在 浓 硫 酸作 用 下 的 脱 水 反 应 合成 了 正 丁醚 反 应 时 采 利
1 实 验部 分
L A型微 波消化 炉 , 照文 献 进行改造 , 参 在炉 的左上方开 -4, ; 贝折光 仪 ; ' 阿 孔 岛
津 48型红外光谱 仪 , 膜法 ;12 0 液 10 型气相色谱仪 . 所用试 剂均为市售 分析纯或 化学 纯 .
按 照 合 成 方 法 考 察 了微 波 条 件 对 正 丁 醇 脱 水 反 应 的影 响 , 果 见 表 1 表 2 结 和
表 1 微 波辐 射 时 间的影 响 。
表2 微 波 输 出 功 率 的 影 响
2 0 3 0 0 40 6 4 2 40 8 50 2 8 4 l 64 5 7 77
从表 3的实验结果 可知 , 利用 微 波常压法 合成 正 丁醚 , 不仅 可大 大缩 短 反应 时 间 , 而
且 也 可使 正 丁 醚 的 产 量 有 所 提 高 [参 考 文 献 ]
1 金 钦汉 微 渡化 学 [ . ] M] 北京 : 科学 出版社 .99 19 . 2 Mig.D M P Mi al . 】 t e a. hm.o v J ,9 12 ( ) ] ne , c e B ∞ R,t 1C e Sc s h P D ] 19 .O 1 3 G d eR,n t F Wetw yK。t T  ̄ hdo et[ ] 18 ,7 3 :7 : ey S fl . .a a e it s c a eraLt J .9 62 ( ) 29 4 B g ms D R, igsM P J( C e t[] 19 ,6 2 ) 66 a h , M no , hn J ,9 15 (5 ,98. t
莲 曹 1 ・ 沈 人从 有 化 方 的 学 科 工 翥 蟊 ,3 ’ 辽 阳 事 机 学 面 教 和 研 作 平’ 女 宁 1 - 0 -
维普资讯
第 1 期
范
平 , : 波 常压 法合 成 正 丁醚 等 微
6 3
2 结 果 与讨 论
微 浊 辐 射 时 问 , 1 1 1 2 2 2 】 mn 0 5 7 0 2 5
正 丁 醴 / g 32 54 64 77 66 49
微 波 功率/ W 正 丁 醚 把 檄 杖 辐 射 2 『n 0I I I
*微 被 功 率 . 0 I " O f
间 只需 2 i, 应速 度 至少 是 常规 反应 的 6 0m n 反 倍 关键 词 : 渡 辐射 ; 擞 脱水 ; 丁醚 . 正
中图分 类 号 :6 3 4 3 0 2 2 文 献 标识 码 : A
近年来 利用微 波 加热促 进有机 反应 的报道 越来 越 多 , 涉及 到酯化 、 缩台 、 加成 和重 环 排等多种 反应 , 波辐射能 加速 化学反应 已为多个 实验 所证 实” J在 已研 究 的这些 反 应 微 。. 中 O 烷基化多 利用碱性条件下 的亲核取代 反应 , 利用 醇脱 水 反应 者较少 . 此 , 们 . 而 为 我 对 S W- L A型微波 消化炉进行 了小 改动 , 在微 波常压条件 下 , 用普 通的 回馏 和分水 装置 . 使 以正丁醇 为原料在浓 硫酸 的催 化作用 下脱水合成 了正丁醚 , 反应 时间只需 2 i 0 mn而在 常 规加热条 件下完成 相同 的反应 至少 约需 1 f . 2 nn 0 i
维普资讯
辽 宁 大 学学 报
自然科 学版 第2 9卷 第 1 崩 20 年 02
J t q L O LAO NG U VE S T OU f A F I NI Ni R I Y
Nawa c,cs目 m t '2S hne
.
2 H0 1 2 9 .  ̄O2
由 实 验 结 果 可 知 , 丁 醇 的脱 水 反 应 对 正
表 3
微 波方 法 和常 规 方 法 的对照
微 波 辐射 时 间 很 敏 感 , 辐 射 2 i , 当 0 rn时 正 a 丁 醚 最 高 产 量 可 达 7 7 . 波 辐 射 时 间 过 .g 微 长时 , 发 生碳 化 , 量 反 而 下 降 正 丁 醇 的 易 产 脱 水 反 应 受 微 波输 出功 率 的 影 响 也 很 大 , 随
12 合 成 方 法
在 10r 0 1 l L圆底 烧瓶 中依 次加人 3 1正 丁醇 , . 1 浓 s lr l L 4 5r l L o 和两小 粒沸石 , 摇匀 将 圆底烧 瓶置于微 波炉 内的玻璃平 台上 , 空气冷凝管 穿过微 波炉顶 的小 孔与其 相连 . 用 空 气冷凝管 的上 口接分水 器 , 再接水 冷凝管 . 用 40W 微 波辐 射 2 i. 使 0 0 mn 待反应 物 冷至 室 温, 先用 1 1饱 和 N C 洗一次 , 5r l L a1 再分别用 l 1饱 和 C C 洗两次 , 5r l L aI  ̄ 用无水 c c a b干燥 过 夜后 , 减压 ( 水泵 ) 蒸馏 收集 17 1 ℃的馏分 . 0 一I0 所得 化台 物 为无 色透 明液体 , 139 ( 献值 : .9 2 ; c1 : 3 ( — — ) .96 文 139 ) m(n ) l O Co C . O
