第1节 元素周期表(带详细解析)_
第一节元素周期表

【解析】选C。本题考查对元素周期表的认识,第1周期只有两
种元素,故A项错。2号元素位于元素周期表中的最后一列,故B
项错。10号元素为稀有气体元素,其下面必为18号稀有气体元
素,故D项错。
类型 二
元素周期表的应用 )
【典例】(2013·聊城高一检测)下列说法正确的是( A.原子序数之差为2的两种元素不可能位于同一主族 B.D-核外有36个电子,则元素D位于第4周期第ⅦA族
二、现行元素周期表的编排原则
周期表 中的顺序给元素编号。 1.原子序数:按照元素在_______ 2.原子序数与原子结构之间的关系: 核电荷数 质子数 核外电子数 。 原子序数=_________=_______=___________
电子层数 原子序数
最外层电子数
电子层数
三、元素周期表的结构 1.周期(横行): 7 个横行,即有__ 7 个周期。 (1)数目:元素周期表有__
C.位于同一主族相邻的甲乙两种元素,甲的原子序数为x,则乙 的原子序数可能为x+4
D.位于同一周期的甲乙两种元素,甲位于ⅠA族,原子序数为x,
乙位于ⅢA族,则乙原子序数可能为x+19
【解题指南】解答本题要注意以下3点: (1)第1~7周期分别含有2、8、8、18、18、32、32种元素,同 一主族两种元素的原子序数的差值为上列数值或连续几个数值 之和。 (2)不同周期ⅠA族与ⅢA族之间相隔的元素数量不一定相同。
(3)简单阴离子的核外电子与同周期的稀有气体相同。
【解析】选B。氢和锂两种元素的原子序数之差为2,却同位于 第ⅠA族,A错误;简单阴离子的核外电子与同周期的稀有气体相 同,D-核外有36个电子,即与第4周期的0族元素Kr处于同一周期, 且D比Kr少一个电子,即在第ⅦA族,B正确;甲乙同主族,根据元
元素周期表(带详细解析)
第一章物质结构元素周期律第一节元素周期表重难点一元素周期表1.构成原子(离子)的微粒间关系(1)原子序数=核电荷数=核内质子数=核外电子数(原子中)。
(2)离子电荷数=质子数-核外电子数。
(3)质量数(A)=质子数(Z)+中子数(N)。
(4)质子数(Z)=阳离子的核外电子数+阳离子的电荷数。
(5)质子数(Z)=阴离子的核外电子数-阴离子的电荷数。
2.元素周期表的结构(3)过渡元素元素周期表中从ⅢB到ⅡB共10个纵行,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为金属元素,统称为过渡元素。
特别提醒族序数为Ⅱ、Ⅲ的地方是主族和副族的分界线,第一次分界时主族在副族的前面,第二次分界时副族在主族的前面。
“第一次”指ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ依次排列。
“第二次”指ⅠB ⅡB ⅢA ⅣA ⅤA ⅥA ⅦA 0依次排列。
重难点二 零族定位法确定元素的位置 1.2.比大小定周期比较该元素的原子序数与0族元素的原子序数大小,找出与其相邻近的两种0族元素,那么该元素就和序数大的0族元素处于同一周期。
3.求差值定族数(1)若某元素原子序数比相应的0族元素多1或2,则该元素应处在该0族元素所在周期的下一个周期的ⅠA 族或ⅡA 族。
(2)若比相应的0族元素少1~5时,则应处在同周期的ⅢA ~ⅦA 族。
(3)若差其他数,则由相应差值找出相应的族。
重难点三 元素的性质与原子结构 1.碱金属单质的相似性和递变性 (1)相似性①与O 2反应生成相应的氧化物,如Li 2O 、Na 2O 等。
②与Cl 2反应生成RCl ,如NaCl 、KCl 等。
③与H 2O 反应,能置换出H 2O 中的氢,反应通式为2R +2H 2O===2ROH +H 2↑。
④与非氧化性酸反应,生成H 2,反应通式为2R +2H +===2R ++H 2↑。
(R 表示碱金属元素)(2)递变性从Li 到Cs ,随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子核对核外电子的吸引能力逐渐减弱,失电子能力逐渐增强,金属性逐渐增强。
化学元素周期表讲解

化学元素周期表讲解化学元素周期表是现代化学的基础工具之一,它将元素按照一定的规律排列,展示了元素的化学性质和特征。
下面对元素周期表进行详细的讲解。
第一周期:氢(H)、氦(He)第一周期只包含两个元素,分别是氢和氦。
氢是宇宙中最丰富的元素,它在化学反应中常作为还原剂或燃料使用。
氦是非金属元素,常用于氦气球和液体燃料。
第二周期:锂(Li)、铍(Be)、硼(B)、碳(C)、氮(N)、氧(O)、氟(F)、氖(Ne)第二周期包含的元素较多,包括锂、铍、硼、碳、氮、氧、氟和氖。
锂、铍和硼是典型金属元素,碳是非金属元素,氮是气体元素,而氧、氟和氖是负电性很高的元素。
第三周期:钠(Na)、镁(Mg)、铝(Al)、硅(Si)、磷(P)、硫(S)、氯(Cl)、氩(Ar)第三周期的元素包括钠、镁、铝、硅、磷、硫、氯和氩。
钠是典型金属元素,镁和铝也是金属,硅是非金属元素,而磷、硫、氯和氩各具特殊的化学性质。
第四周期:钾(K)、钙(Ca)、钛(Ti)、铬(Cr)、锰(Mn)、铁(Fe)、镍(Ni)、铜(Cu)第四周期的元素包括钾、钙、钛、铬、锰、铁、镍和铜。
这些元素的物理和化学性质各异,广泛应用于许多领域,如钢铁制造、电池工业等。
第五周期:锌(Zn)、镓(Ga)、锗(Ge)、砷(As)、硒(Se)、溴(Br)、氪(Kr)第五周期包括锌、镓、锗、砷、硒、溴和氪。
其中锌是重要的金属元素,镓、锗、砷和硒是非金属元素,溴是液体元素,氪是惰性气体元素。
第六周期:铷(Rb)、锶(Sr)、钇(Y)、锆(Zr)、铌(Nb)、钼(Mo)、锝(Tc)、钌(Ru)第六周期的元素包括铷、锶、钇、锆、铌、钼、锝和钌。
这些元素具有重要的催化剂、电子器件和合金材料的应用。
第七周期:钯(Pd)、银(Ag)、镉(Cd)、铟(In)、锡(Sn)、锑(Sb)、碲(Te)、碘(I)、氙(Xe)第七周期的元素包括钯、银、镉、铟、锡、锑、碲、碘和氙。
这些元素在化学反应中发挥重要的作用,也广泛应用于光电子器件、催化剂等领域。
化学元素周期表详解

起源简介现代化学的元素周期律是1869年的德米特里·伊万诺维奇·门捷列夫首创的。
1913年英国科学家莫色勒利用阴极射线撞击金属产生X射线,发现原子序数越大,X射线的频率就越高,因此他认为原子核的正电荷决定了元素的化学性质,并把元素依照核内正电荷(即质子数或原子序数)排列,经过多年修订后才成为当代的周期表。
常见的元素周期表为长式元素周期表。
在长式元素周期表中,元素是以元素的原子序数排列,最小的排行最先。
表中一横行称为一个周期,一纵列称为一个族,最后有两个系。
除长式元素周期表外,常见的还有短式元素周期表,螺旋元素周期表,三角元素周期表等。
道尔顿提出科学原子论后,随着各种元素的相对原子质量的数据日益精确和原子价(化合价)概念的提出,就使元素相对原子质量与性质(包括化合价)之间的联系显露出来。
德国化学家德贝莱纳就提出了“三元素组”观点。
他把当时已知的54种元素中的15种,分成5组,每组的三种元素性质相似,而且中间元素的相对原子质量等于较轻和较重的两个元素相对原子质量之和的一半。
例如钙、锶、钡,性质相似,锶的相对原子质量大约是钙和钡的相对原子质量之和的一半。
法国矿物学家尚古多提出了一个“螺旋图”的分类方法。
他将已知的62种元素按相对原子质量的大小顺序,标记在绕着圆柱体上升的螺旋线上,这样某些性质相近的元素恰好出现在同一母线上。
这种排列方法很有趣,但要达到井然有序的程度还有困难。
另外尚古多的文字也比较暧昧,不易理解,虽然是煞费苦心的大作,但长期未能让人理解。
英国化学家纽兰兹把当时已知的元素按相对原子质量大小的顺序进行排列,发现无论从哪一个元素算起,每到第八个元素就和第一一个元素的性质相近。
这很像音乐上的八度音循环,因此,他干脆把元素的这种周期性叫做“八音律”,并据此画出了标示元素关系的“八音律”表。
显然,纽兰兹已经下意识地摸到了“真理女神"的裙角,差点就揭示元素周期律了。
不过,条件限制了他做进一步的探索,因为当时相对原子质量的测定值有错误,而且他也没有考虑到还有尚未发现的元素,只是机械地按当时的相对原子质量大小将元素排列起来,所以他没能揭示出元素之间的内在规律。
第一节元素周期表(共40张PPT)
第ⅦA 族
与水缓慢反应
(2)原子结构特点 Cl2+H2O=HCl+HClO
静置后,液体分为两层。
通一过个以 12上C相质比量较同×,1点/思12考:钠和钾最的外性质层有 7个电子
静置后,液体分为两层。
和递变性。 (氧化性:Cl2 >I2)
核电荷数依次增多
不同点: 电子层数依次增多 上层无色,下层分别呈橙红色、紫红色
第一章 物质结构、元素周期律
第一节 元素周期表 一、元素周期表的结构
原子序数:依原子核电荷数由小到大的顺序给元素编号,这种
编号叫原子序数。
原子序数=核电荷数=质子数=核外电子数 (一)元素周期表的编排原则
1、横行: 把电子层数相同的各种元素按原子序数递增顺序
从左到右排列。
2、纵行: 把最外层电子数相同的各种元素按电子层数递增顺序 从上而下排成。
性逐渐增强,非金属性逐渐减弱。
2. 元素性质与原子结构有有密切的关系,主要与原子
核外的排布,特别是最外层电子数有关。原子结构
相似的一族元素,它们在化学性质上表现出相似性 和递变性。
1、砹(At)原子序数85,与F、Cl、Br、I同族,推测砹或
砹的化合物不可能具有的性质是( B)
A、砹易溶于某些有机溶剂 B、砹能与水剧烈反应
应越来越
,剧生烈成的氧化物越来越
。
最高复价杂氧化物对应水化物的碱性越来越 。
强
讨论1:Li与K 应如何保存? Li封存于固体石蜡中, 少量K保存于煤油中。
讨论2:碱金属与盐酸: 2R+2H+= 2R++H2 ↑ 讨论3:碱金属与盐溶液: 先与水反应
讨论4:Li+、Na+、K+、Rb+、Cs+也具有强还原性吗? 没有。 有较弱的氧化性。 氧化性: Li+ > Na+ > K+ > Rb+ > Cs+
(完整版)元素周期表详解

(完整版)元素周期表详解元素周期表中元素及其化合物的递变性规律1 原子半径(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
注意:原子半径在VIB族及此后各副族元素中出现反常现象。
从钛至锆,其原子半径合乎规律地增加,这主要是增加电子层数造成的。
然而从锆至铪,尽管也增加了一个电子层,但半径反而减小了,这是与它们对应的前一族元素是钇至镧,原子半径也合乎规律地增加(电子层数增加)。
然而从镧至铪中间却经历了镧系的十四个元素,由于电子层数没有改变,随着有效核电荷数略有增加,原子半径依次收缩,这种现象称为“镧系收缩”。
镧系收缩的结果抵消了从锆至铪由于电子层数增加到来的原子半径应当增加的影响,出现了铪的原子半径反而比锆小的“反常”现象。
2元素变化规律(1)除第一周期外,其余每个周期都是以金属元素开始逐渐过渡到非金属元素,最后一稀有气体元素结束。
(2)每一族的元素的化学性质相似3元素化合价(1)除第1周期外,同周期从左到右,元素最高正价由碱金属+1递增到+7,非金属元素负价由碳族-4递增到-1(氟无正价,氧无+6价,除外);(2)同一主族的元素的最高正价、负价均相同(3) 所有单质都显零价4单质的熔点(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增5元素的金属性与非金属性(1)同一周期的元素电子层数相同。
因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增;(2)同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。
6最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价氧化物的水化物的酸性越强。
《第一节 元素周期表》PPT课件
2 、根据金属单质与水或者与酸反 应置换出氢的难易程度判断。 3、可以根据最高价氧化物对应的 水化物碱性的强弱判断。
我们要的最终结果是?
碱金属元素的原子的最外层都是1个电 子,性质相似,都是强还原剂 随着核电荷数的增加,碱金属元素原子 的电子层数逐渐 增多 ,原子半径逐 渐 增大,原子核对最外层电子的引力逐 渐 减弱 。失去最外层电子的能力逐渐-增强 ----,金属性(还原性)逐渐--------- 更剧烈, 轻微的 生成H2 生成H2 爆炸, 生成H2
遇水立 遇水立 即燃烧,即燃烧, 爆炸 爆炸
碱金属与水反应的通式:
2R + 2H2O
C)最高价氧化物对应的水化物都是强碱 最高价氧化物 对应的水化物的碱性?
LiOH < NaOH < KOH< RbOH< CsOH
D)元素都具有强的金属性 单质都具有强的还原性 何谓金属性? 金属性是指元素的原子失去
主族序数 = ? = ?= ?
过渡元素:
元素周期表中从
______ ⅢB 到______ ⅡB 共10个纵行,包括了 第Ⅷ族和全部副族元素,共60多种元
素,全部为金属元素,统称为过渡元
素。
注 意
注意:金属与非金属的分界线
注意:纵行的排列顺序
注意:同周期的第IIA与第IIIA元 素的原子序数的差值
锂 碱 金 属 元 素
Li
Na K
3
11 19
+3
2
1
1
1
1
2
3 4
0.152
钠
钾 铷 铯
+11
2
8
1
0.186
0.227
+19
人教版高中化学必修二课件第一章第一节第1课时元素周期表
提示:短周期元素中族序数与周期数相同的有三种元素:
氢、铍、铝。若族序数(或周期数)为1,则为氢;若族序数(或 周期数)为2,则为铍;若族序数(或周期数)为3,则为铝。
2.主族序数=最高正价数,这一关系有例外吗?请举例。
提示:这个关系对除O、F两种元素以外的任何主族元素都
是成立的,因为O、F无最高正价。
二、元素在元素周期表中位置的确定方法 1.以0族为基准给元素定位 稀有气体元素 周期数 He 一 Ne 二 Ar 三 Kr 四 Xe 五 Rn 六
原子序数
2
10
18
36
54
86
(1)确定纵行数(族序数)。 元素的纵行数=原子序数-相近且小的稀有气体原子序
数,所得纵行数与族序数的对应关系如下表。
纵行数 1 2 13 14 15 16 17 18
族序数
纵行数
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
3 4 5 6 7 8、9、10 Ⅷ族
0族
11 12
族序数 ⅢB ⅣB ⅤB ⅥB ⅦB
ⅠB ⅡB
(2)确定周期数。 元素的周期数=原子序数相近且小的稀有气体的周期数
+1。
例如:判断原子序数为41的元素在元素周期表中的位置。 分析:41与36接近,有41-36=5,该元素处于第五周期ⅤB 族。使用此法若为第六、七周期ⅢB族(含镧系、锕系元素)后 的元素需再减14定位。 2.根据每周期元素的种类给元素定位 周期序数 一 二 三 四 五 六 七
6.X、Y、Z是短周期三种元素,它们在周 期表中的位置如右图所示,试回答:
(1)X元素单质的化学式是________。
(2)Z元素的原子结构示意图为________。
(3)Y在元素周期表中的位置是
化学元素周期表解读
化学元素周期表解读化学元素周期表(简称元素周期表)是化学中一个重要的工具,用于系统地组织和展示所有已知化学元素的信息。
它按照元素的原子序数递增的顺序,将元素分组并排列在一张表中。
该表提供了各个元素的原子序数、原子量、元素符号等基本信息,为科学家们研究元素和化合物的性质以及开展化学实验提供了便利。
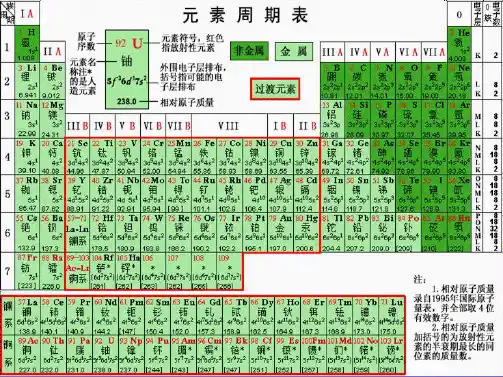
1. 元素周期表的组织结构元素周期表按照元素的电子排布和化学性质,将元素划分为若干个周期和若干个族。
周期指的是元素的原子核外电子壳层数。
我们通常所说的第一周期、第二周期等,就是指元素原子的最外层电子壳层数。
族是指具有相似化学性质的元素群。
元素周期表中共有7个周期和18个族,分别从第1周期到第7周期,从1族到18族。
元素周期表的主体部分由四个区域组成:主族元素区、过渡金属元素区、稀土元素区和超铀元素区。
主族元素区包含1族至2族和13族至18族,通常包括非金属、金属和半金属元素。
过渡金属元素区是3至12族,包含过渡金属元素和内过渡金属元素。
稀土元素区是位于主表之下的一行14个元素,它们被分组放置在一个矩形区域内。
超铀元素区则包含所有人工合成的放射性元素。
2. 周期表的基本信息元素周期表的每个格子代表一个元素,格子中常包含元素符号、原子序数和原子量等信息。
元素符号是化学元素的缩写,如氢气的符号是H,氧气的符号是O。
原子序数是指元素原子核内所包含的质子数量,也是元素在周期表中的编号。
原子量则是指一个元素的相对原子质量,它的数值等于元素原子质量数的平均值。
元素周期表中的元素还可以按照一些特定的属性进行分类。
例如,我们可以将元素分为金属、非金属和半金属三类。
金属元素通常具有良好的导电性和热导性,而非金属元素通常不具备这些性质。
半金属元素则介于金属和非金属之间,具有部分金属和部分非金属的特性。
3. 元素周期表的应用元素周期表为科学家们研究元素和化合物的性质提供了基础和便利。
通过元素周期表,科学家们可以推断出一个元素的一些性质。
元素周期表(含详解)
元素周期律、元素周期表基础热身1.关于元素周期表的说法正确的是()A.元素周期表有8个主族B.ⅠA族的元素全部是金属元素C.元素周期表有7个周期D.短周期是指第一、二周期2.石墨烯是仅由一层碳原子构成的新型材料,具有超强的导电性。
下列元素与碳元素处于同一主族的是() A.He B.O C.Si D.P3.第ⅠA族元素具有相似的化学性质,是由于它们的原子具有相同的()A.原子半径B.电子层数C.核外电子数D.最外层电子数4.下列气态氢化物最稳定的是()A.HCl B.HBr C.HF D.HI5.下列说法不正确...的是()A.钾的金属性比钠强B.溴的非金属性比氯强C.ⅦA族中原子半径最小的是氟D.第三周期中,除稀有气体元素外原子半径最大的是钠能力提升6.[2012·黄冈高三联考] 图K15-1为周期表中短周期的一部分,若a原子最外层电子数比次外层电子数少3个,下说法中不正确...的是()图K15-1A.原子半径大小顺序是c>b>d>a B.d的氢化物比a的氢化物稳定C.a和d的原子结合可以形成带3个负电荷的阴离子D.a、b、c最高价氧化物对应水化物的酸性强弱关系是c>b>a7.(双选)短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14。
X与Z同主族,Y 与W同主族,且X的原子半径小于Y。
下列叙述正确的是()A.原子半径:Y<Z<W B.Z在化合物中呈+1价C.Y与W可形成离子化合物D.Z的单质能与X的氧化物反应8.短周期主族元素A、B、C、D,原子序数依次增大。
A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。
下列叙述正确的是() A.原子半径:A<B<C<D B.非金属性:A>CC.最高价氧化物对应水化物的酸性:D<C D.单质B常温下能溶于浓硝酸9.[2012·杭州第一次质检] W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章 物质结构 元素周期律第一节元素周期表重难点一 元素周期表1.构成原子(离子)的微粒间关系(1)原子序数=核电荷数=核内质子数=核外电子数(原子中)。
(2)离子电荷数=质子数-核外电子数。
(3)质量数(A)=质子数(Z)+中子数(N)。
(4)质子数(Z)=阳离子的核外电子数+阳离子的电荷数。
(5)质子数(Z)=阴离子的核外电子数-阴离子的电荷数。
2.元素周期表的结构 (1)周期 周期 短周期长周期一 二 三 四 五 六 七 对应行数 1 2 3 4 5 6 7 所含元素种类 28818183232 (排满时) 元素原子序数起止号(若排满) 1~2 3~10 11~18 19~36 37~54 55~8687-118每周期0族元素原子序数 2 10 18 36 54 86(2)族 族 主族(A) 副族(B) Ⅷ 0 族数 771 1列序号 1213 14 15 16 17 3 4 5 6 7 11 12 8 9 10 18族序号ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡBⅧ(3)过渡元素元素周期表中从ⅢB 到ⅡB 共10个纵行,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为金属元素,统称为过渡元素。
特别提醒 族序数为Ⅱ、Ⅲ的地方是主族和副族的分界线,第一次分界时主族在副族的前面,第二次分界时副族在主族的前面。
“第一次”指ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ依次排列。
“第二次”指ⅠB ⅡB ⅢA ⅣA ⅤA ⅥA ⅦA 0依次排列。
重难点二 零族定位法确定元素的位置 1.明确各周期零族元素的原子序数周期 一 二 三 四 五 六 七 原子序数210183654861182.比大小定周期比较该元素的原子序数与0族元素的原子序数大小,找出与其相邻近的两种0族元素,那么该元素就和序数大的0族元素处于同一周期。
3.求差值定族数(1)若某元素原子序数比相应的0族元素多1或2,则该元素应处在该0族元素所在周期的下一个周期的ⅠA 族或ⅡA 族。
(2)若比相应的0族元素少1~5时,则应处在同周期的ⅢA ~ⅦA 族。
(3)若差其他数,则由相应差值找出相应的族。
重难点三 元素的性质与原子结构 1.碱金属单质的相似性和递变性 (1)相似性①与O 2反应生成相应的氧化物,如Li 2O 、Na 2O 等。
②与Cl 2反应生成RCl ,如NaCl 、KCl 等。
③与H 2O 反应,能置换出H 2O 中的氢,反应通式为2R +2H 2O===2ROH +H 2↑。
④与非氧化性酸反应,生成H 2,反应通式为2R +2H +===2R ++H 2↑。
(R 表示碱金属元素) (2)递变性从Li 到Cs ,随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子核对核外电子的吸引能力逐渐减弱,失电子能力逐渐增强,金属性逐渐增强。
表现为:①与O 2的反应越来越剧烈,产物更加复杂,如Li 与O 2反应只能生成Li 2O ,Na 与O 2反应还可以生成Na 2O 2,而K 与O 2反应能够生成KO 2等。
②与H 2O 的反应越来越剧烈,如K 与H 2O 反应可能会发生轻微爆炸,Rb 与Cs 遇水发生剧烈爆炸。
③对应离子的氧化性依次减弱,即氧化性:Li +>Na +>K +>Rb +>Cs +。
④最高价氧化物对应水化物的碱性逐渐增强,CsOH 的碱性最强。
特别提醒 (1)碱金属单质性质的相似性和递变性是其原子结构的相似性和递变性的必然结果。
(2)因Na 、K 等很活泼的金属易与H 2O 反应,故不能从溶液中置换出不活泼的金属。
2.卤素单质的相似性、递变性和特性 (1)相似性①与H 2反应生成相应的氢化物:X 2+H 2===2HX 。
②与活泼金属(Na 等)反应生成相应的金属卤化物:2Na +X 2=====点燃2NaX 。
③与H2O反应:X2+H2O===HX+HXO(X指Cl、Br、I)2F2+2H2O===4HF+O2(2)递变性①从上到下,卤素单质的氧化性逐渐减弱,阴离子的还原性逐渐增强,即氧化性:F2>Cl2>Br2>I2,还原性:I->Br->Cl->F-。
②随着原子序数递增,与H2反应越来越难,氢化物的稳定性逐渐减弱,还原性逐渐增强,其水溶液的酸性逐渐增强,HCl、HBr、HI的熔、沸点依次升高。
③卤素单质与变价金属(如Fe)反应时,与F2、Cl2、Br2生成高价(如FeBr3),而与I2只能生成低价(FeI2)。
(3)卤素单质的特殊性质①氟元素无正价,无含氧酸。
②Cl2易液化。
③Br2是在常温下唯一的一种液态非金属单质。
④碘为紫黑色固体,易升华,淀粉遇I2变蓝色。
特别提醒F与Cl、Br、I的性质在某些方面差别较大:(1)卤素单质与水的反应;(2)F-的还原性极弱;(3)氢氟酸为弱酸,而盐酸、氢溴酸、氢碘酸为强酸;(4)F无正价、无含氧酸,而Cl、Br、I有最高正价和含氧酸。
3.同主族元素性质递变规律由碱金属元素和卤素的性质来看,元素的化学性质,主要由原子的最外层电子数决定,其次是电子层数。
原子结构相似的元素,它们的化学性质表现出相似性和递变性。
同主族从上至下,元素及其典型化合物性质递变规律,如下表所示:物质类别性质递变规律元素元素金属性逐渐增强元素非金属性逐渐减弱单质氧化性逐渐减弱还原性逐渐增强非金属元素氢化物气态稳定性逐渐减弱水溶液酸性逐渐增强还原性逐渐增强最高价氧化物对应水化物碱性逐渐增强酸性逐渐减弱归纳总结由碱金属元素、卤素推导出的同主族元素金属性、非金属性变化规律适合其他所有同主族元素,这里必须强调的是金属性增强是指同主族的金属元素之间的金属性相比,自上而下金属性增强;非金属性减弱是指同主族的非金属之间,非金属性随原子序数的增大逐渐减弱。
如第ⅣA 族中,非金属性C>Si,金属性Ge<Sn<Pb。
4.元素金属性和非金属性强弱的比较(1)金属性强弱的比较比较金属性的强弱,其实质是看元素原子失去电子的能力,越易失电子,金属性越强。
①从元素原子结构判断a.当最外层电子数相同时,电子层数越多,原子半径越大,越易失电子,金属性越强。
b.当电子层数相同时,核电荷数越多越难失电子,金属性越弱(以后学)。
②从元素单质及其化合物的相关性质判断a.金属单质与水或酸反应越剧烈,元素金属性越强。
b.最高价氧化物对应水化物的碱性越强,元素金属性越强。
③根据金属活动性顺序表判断一般来说排在前面的金属元素其金属性比排在后面的强。
④离子的氧化性强弱判断离子的氧化性越强,则对应金属元素的金属性越弱。
特别提醒金属性强弱的比较,关键是比较原子失去电子的难易,而不是失去电子的多少。
如Na失去一个电子,而Mg失去两个电子,但Na的金属性比Mg强。
(2)非金属性强弱的比较比较元素非金属性的强弱,其实质是看元素原子得到电子的难易程度,越易得电子,非金属性越强。
①从元素原子结构判断a.当电子层数相同时,核电荷数越多,非金属性越强;b.当最外层电子数相同时,核电荷数越多,非金属性越弱。
②从元素单质及其化合物的相关性质判断a.单质越易跟H2化合,生成的氢化物也就越稳定,氢化物的还原性也就越弱,其非金属性也就越强。
b.最高价氧化物对应水化物的酸性越强,其非金属性越强。
如H2SO4的酸性强于H3PO4,说明S的非金属性比P强。
c.非金属单质间的置换反应,例如:Cl2+2KI===2KCl+I2,说明氯的非金属性比碘强。
d.元素的原子对应阴离子的还原性越强,元素的非金属性就越弱。
如S2-的还原性比Cl-强,说明Cl的非金属性比S强。
特别提醒(1)金属性和非金属性讨论的对象是元素,具体表现为该元素的单质或特定化合物的性质。
(2)氧化性和还原性讨论的对象是具体物质或某物质中的特定粒子,具体表现在该物质中某元素得失电子的能力。
重难点四核素1.元素、核素、同位素之间的区别和联系(1)元素、核素、同位素的比较元素核素同位素概念具有相同核电荷数的同类原子的总称具有一定数目的质子和一定数目的中子的一种原子质子数相同而中子数不同的同一种元素的不同原子互称为同位素范围宏观概念,指同类原子,既可是游离态又可是化合态微观概念,指某种原子微观概念,指某种元素的几种原子之间的关系特点 只与质子数有关,与中子数、核外电子数无关不同的核素间质子数、中子数、电子数可能有相同处,也可能均不同 同位素间质子数相同,化学性质相同,质量数不同,物理性质不同实例16 8O 、18 8O 、16 8O 2-都属氧元素11H 、21H 、31H 、4019K 、4020Ca不同核素11H 、21H 、31H为氢的同位素(2)元素、核素、同位素之间的关系图2.元素的相对原子质量(1)元素的相对原子质量就是按照该元素各种同位素原子所占的一定百分比算出的平均值。
(2)元素的相对原子质量的计算设某元素有多种不同的核素,A 、B 、C ……表示各核素的相对原子质量,a%、b%、c%……为各核素的原子数目百分数,则元素的相对原子质量计算式为Mr =A·a%+B·b%+C·c%+……例如,氯元素有3517Cl 和3717Cl 两种天然、稳定的同位素,3517Cl 的原子数目百分数为75.77%,3717Cl的原子数目百分数为24.23%;3517Cl 的相对原子质量为34.969,3717Cl 的相对原子质量为36.966。
则氯元素的相对原子质量为: 34.969×75.77%+36.966×24.23%=35.453。
题型1 元素周期表的结构例1 若把周期表原先的主、副族号取消,由左到右按原顺序编为18列。
如碱金属为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是( )A .第3列元素种类最多,第14列元素的化合物种类最多B .第10列元素全部是金属元素C .第18列元素单质全部是气体D .只有第2列元素的原子最外层有2个电子解析 第3列元素中包括镧系和锕系元素,各有15种元素,所以种类最多,第14列元素中包括碳元素,碳元素可形成有机物,故化合物的种类最多,A 正确;第10列为过渡金属,故B 正确;第18列元素为稀有气体元素,单质全部为气体,故C 正确;D 项中除第2列元素的原子最外层有2个电子外,其他如He 、部分过渡金属元素最外层也是2个电子。
答案 D对每一族中各原子的最外层电子数不熟悉,忽略He 最外层也是两个电子。
题型2 元素位置的确定例22007年3月21日,我国公布了111号元素Rg的中文名称。
该元素名称及所在周期是() A.钅仑第七周期B.镭第七周期C.铼第六周期D.氡第六周期解析经推算第七周期的稀有气体元素的原子序数为118,所以111号元素位于第七周期,故C项和D项是错误的;又知镭为第ⅡA族元素,排除B项,所以A项正确。
