烷烃同分异构的种类
烷烃的同系列及同分异构现象

CH3CH2CH2CH
CHCH 56
2CH2CH2CH2CH2CH3 7 8 9 10 11
CH3CH2CH2CHCHCH 3 1 2 3 4 CH3
1 确定主链:有两根等长的长链。两根长链均有两个侧链。侧链位次
均为4,5。侧链的碳原子数均为3,7。
黑字长链4位无侧分支,5位有侧分支。绿字长链4,5位
侧链均有侧 分支。侧分支少优先。
2 编 号:黑字编号,取代基位置4,5。蓝字编号取代基位置7,8。取黑字编号。
3 命 名: 中文命名 4-丙基-5-(1-异丙基丁基)十一烷
英文命名 5-(1-isopropylbutyl)-4-propylundecane
20
第三节 烷烃的构型及分子模型
一、碳原子的四面体概念及分子模型 构型:
由于C的四个sp3轨道的几何构型为正四面体,轨道对称夹角为 109028`,这就决定的烷烃分子中碳原子的排列不是直线形的。 甲烷的正四面体构型可用契性透视式表示:
实线表示处在纸平面上的价键,虚契性线表示处在纸面的价键, 实契性线表示处在纸面前的价键。
23
有机化学中的同分异构现象
碳架异构体
位置异构体
或 CH3(CH2)4CH3
6
有机化合物构造式的表达方式 :
蛛网式
H HH HH HC C C C C H
HH HHH
结构简式
H3C CH CH2 CH2 CH3 CH3
CH3CHCH2CH2CH2CH3 CH3
键线式
OH
7
碳、氢原子的级
CH3
CH3
1oH 2oH 3oH
H3C C CH2 CH CH3 1oC 2oC 3oC 4oC
烷烃同分异构体:碳原子数为10以内的所有烷烃(共150种)

碳原子数为10以内的所有烷烃同分异体(共150种)1种)一、CH4同分异构体(共1、甲烷二、C同分异构体(共1种)2H61、乙烷同分异构体(共1种)三、C3H81、丙烷四、C同分异构体(共2种)4H101、丁烷2、2—甲基丙烷五、C同分异构体(共3种)5H121、戊烷2、2—甲基丁烷3、2 , 2—二甲基丙烷六、C同分异构体(共5种)6H141、己烷2、2—甲基戊烷3、3—甲基戊烷4、2 , 2—二甲基丁烷5、2 , 3—二甲基丁烷同分异构体(共9种)七、C7H161、庚烷2、2—甲基己烷3、3—甲基己烷4、3—乙基戊烷5、2 , 2—二甲基戊烷6、2 , 3—二甲基戊烷7、2 , 4—二甲基戊烷8、3 , 3—二甲基戊烷9、2 , 2 , 3—三甲基丁烷同分异构体(共18种)八、C8H181、辛烷2、2—甲基庚烷3、3—甲基庚烷4、4—甲基庚烷5、3—乙基己烷6、2 , 2—二甲基己烷7、2 , 3—二甲基己烷8、2 , 4—二甲基己烷9、2 , 5—二甲基己烷10、3 , 3—二甲基己烷11、3 , 4—二甲基己烷12、2—甲基—3—乙基戊烷13、3—甲基—3—乙基戊烷14、2 , 2 , 3—三甲基戊烷15、2 , 2 , 4—三甲基戊烷16、2 , 3 , 3—三甲基戊烷17、2 , 3 , 4—三甲基戊烷18、2 , 2 , 3 , 3—四甲基丁烷九、C同分异构体(共35种)9H201、壬烷2、2—甲基辛烷3、3—甲基辛烷4、4—甲基辛烷5、3—乙基庚烷6、4—乙基庚烷7、2 , 2—二甲基庚烷8、2 , 3—二甲基庚烷9、2 , 4—二甲基庚烷10、2 , 5—二甲基庚烷11、2 , 6—二甲基庚烷12、3 , 3—二甲基庚烷13、3 , 4—二甲基庚烷14、3 , 5—二甲基庚烷15、4 , 4—二甲基庚烷16、2—甲基—3—乙基己烷17、2—甲基—4—乙基己烷18、3—甲基—3—乙基己烷19、3—甲基—4—乙基己烷20、2 , 2 , 3—三甲基己烷21、2 , 2 , 4—三甲基己烷22、2 , 2 , 5—三甲基己烷23、2 , 3 , 3—三甲基己烷24、2 , 3 , 4—三甲基己烷25、2 , 3 , 5—三甲基己烷27、3 , 3 , 4—三甲基己烷28、3 , 3—二乙基戊烷29、2 , 2—二甲基—3—乙基戊烷30、2 , 3—二甲基—3—乙基戊烷31、2 , 4—二甲基—3—乙基戊烷32、2 , 2 , 3 , 3—四甲基戊烷33、2 , 2 , 3 , 4—四甲基戊烷34、2 , 2 , 4 , 4—四甲基戊烷35、2 , 3 , 3 , 4—四甲基戊烷同分异构体(共75种)十、C10H221、癸烷2、2—甲基壬烷3、3—甲基壬烷4、4—甲基壬烷5、5—甲基壬烷6、3—乙基辛烷7、4—乙基辛烷8、2 , 2—二甲基辛烷9、2 , 3—二甲基辛烷10、2 , 4—二甲基辛烷11、2 , 5—二甲基辛烷12、2 , 6—二甲基辛烷13、2 , 7—二甲基辛烷14、3 , 3—二甲基辛烷15、3 , 4—二甲基辛烷16、3 , 5—二甲基辛烷17、3 , 6—二甲基辛烷18、4 , 4—二甲基辛烷19、4 , 5—二甲基辛烷20、4—正丙基庚烷21、4—异丙基庚烷22、2—甲基—3—乙基庚烷23、3—甲基—3—乙基庚烷24、4—甲基—3—乙基庚烷25、2—甲基—4—乙基庚烷26、3—甲基—4—乙基庚烷27、4—甲基—4—乙基庚烷28、2—甲基—5—乙基庚烷29、3—甲基—5—乙基庚烷30、2 , 2 , 3—三甲基庚烷31、2 , 2 , 4—三甲基庚烷32、2 , 2 , 5—三甲基庚烷34、2 , 3 , 3—三甲基庚烷35、2 , 3 , 4—三甲基庚烷36、2 , 3 , 5—三甲基庚烷37、2 , 3 , 6—三甲基庚烷38、2 , 4 , 4—三甲基庚烷39、2 , 4 , 5—三甲基庚烷40、2 , 4 , 6—三甲基庚烷41、2 , 5 , 5—三甲基庚烷42、3 , 3 , 4—三甲基庚烷43、3 , 3 , 5—三甲基庚烷44、3 , 4 , 4—三甲基庚烷45、3 , 4 , 5—三甲基庚烷46、2—甲基—3—异丙基己烷47、3 , 3—二乙基己烷48、3 , 4—二乙基己烷49、2 , 2—二甲基—3—乙基己烷50、2 , 3—二甲基—3—乙基己烷51、2 , 4—二甲基—3—乙基己烷52、2 , 5—二甲基—3—乙基己烷53、3 , 4—二甲基—3—乙基己烷54、2 , 2—二甲基—4—乙基己烷55、2 , 3—二甲基—4—乙基己烷56、2 , 4—二甲基—4—乙基己烷57、3 , 3—二甲基—4—乙基己烷58、2 , 2 , 3 , 3—四甲基己烷59、2 , 2 , 3 , 4—四甲基己烷60、2 , 2 , 3 , 5—四甲基己烷61、2 , 2 , 4 , 4—四甲基己烷62、2 , 2 , 4 , 5—四甲基己烷63、2 , 2 , 5 , 5—四甲基己烷64、2 , 3 , 3 , 4—四甲基己烷65、2 , 3 , 3 , 5—四甲基己烷66、2 , 3 , 4 , 4—四甲基己烷67、2 , 3 , 4 , 5—四甲基己烷68、3 , 3 , 4 , 4—四甲基己烷69、2 , 4—二甲基—3—异丙基戊烷70、2—甲基—3 , 3—二乙基戊烷71、2 , 2 , 3—三甲基—3—乙基戊烷72、2 , 2 , 4—三甲基—3—乙基戊烷73、2 , 3 , 4—三甲基—3—乙基戊烷74、2 , 2 , 3 , 3 , 4—五甲基戊烷75、2 , 2 , 3 , 4 , 4—五甲基戊烷。
烷烃

⑷若有几个等长碳链时,要选含有最多 取代基的碳链作主链。 ⑸若在主链的两端等距离处有取代基且 多于两个时,要使第三个取代基的位次 较小,依此类推。
第三节 烷烃的化学性质
一、稳定性 二、卤代反应及反应机制 反应机理就是研究反应是如何发生、如何 发展、如何结束的。 烷烃卤代反应的反应机理是游离基链锁反 应(free radical chain reaction)。
⑵主链编号:从靠近取代基的一端, 用阿拉伯数字依次为主链编号。
⑶取代基处理:将取代基的编号和名称放在 母体前面,中间用半字线连接。 相同的取代基合并,取代基数目用中文小写 数字表示,取代基的位次需一一标出,中间 用逗号隔开。 不同的取代基在母体前面的排列依据基团的 “次序规则”进行比较后按“较优基团后列 出”原则列出。
本章要点:
1.烷烃的结构特点:
碳原子都是SP3杂化,所有的键都是σ键, σ键的特点。
2.碳原子的种类:
伯、仲、叔、季(1°级、2°级、3°级、4°级)碳原子。
3.烷烃的同分异构现象:
碳链异构和构象异构;构象异构的概念、定义、乙烷的两种典型构象、丁烷 的四种典型构象的Newman投影式、稳定性比较。
第二节 烷烃的命名法
一、普通命名法
正、异、新; 伯、仲、叔、季碳原子。 举例说明。
二、系统命名法
常见的基团名称: RCH3CH3CH2甲基 methyl 乙基 ethyl
烷基 Alkyl
正丙基 propyl
CH3CH2CH2-
(CH3)2CH异丙基 isopropyl
烷烃同分异构体的书写

烷烃同分异构体的书写
烷烃是一类仅由碳和氢组成的有机化合物,分子结构为直链或环状的碳骨架。
同分异构体是指具有相同分子式但结构不同的化合物。
书写烷烃同分异构体时,可以通过改变碳骨架的连接方式或分子的空间排列来产生不同的结构。
以下是一些常见的烷烃同分异构体的示例:
1. 丁烷(分子式:C4H10)的同分异构体:
-正丁烷:
CH3-CH2-CH2-CH3
- 2-甲基丙烷:
CH3-CH(CH3)-CH3
2. 戊烷(分子式:C5H12)的同分异构体:
-正戊烷:
CH3-CH2-CH2-CH2-CH3
- 2-甲基丁烷:
CH3-CH(CH3)-CH2-CH3
- 2,2-二甲基丙烷:
CH3-C(CH3)2-CH3
3. 己烷(分子式:C6H14)的同分异构体:
-正己烷:
CH3-CH2-CH2-CH2-CH2-CH3
- 2-甲基戊烷:
CH3-CH(CH3)-CH2-CH2-CH3
- 3-甲基戊烷:
CH3-CH2-CH(CH3)-CH2-CH3
这只是一小部分烷烃同分异构体的示例,实际上,随着碳原子数量的增加,同分异构体的数量将呈指数级增长。
通过在碳骨架上引入支链或环状结构,可以生成更多不同的同分异构体。
【新教材】烷烃的同分异构体书写及取代物的种类

【新教材】烷烃的同分异构体书写及取代物的种类【学习目标】1、掌握同分异构体的概念,会辨析“四同”2、会用“减碳法”正确书写常见烷烃的同分异构体,掌握烷烃取代物的找法 【主干知识梳理】一、同分异构体、同分异构现象 正丁烷和异丁烷物理性质的比较1(1)同分异构现象:化合物具有相同的分子式,但具有不同的结构的现象 (2)同分异构体:具有同分异构现象的化合物互称为同分异构体 (3)同分异构体特点①分子式相同,即:化学组成和相对分子质量相同 ②可以是同类物质,也可以是不同类物质 ③结构不同,性质可能相似也可能不同 ④同分异构体之间的转化是化学变化 【微点拨】①同分异构体要求分子式相同,但结构不同,二者缺一不可;分子式相同,则相对分子质量相等,但相对分子质量相等的物质,分子式不一定相同,如:CO 和C 2H 4②结构不同意味着同分异构体不一定是同类物质,如:CH 3CH 2CH===CH 2和③同分异构体的结构一定不同,因此它们的物理性质存在差异;如果同分异构体的结构相似,属于同类物质,则它们的化学性质相似;如果同分异构体是不同类别的物质,则它们的化学性质不同④烷烃中,甲烷、乙烷、丙烷不存在同分异构体,其他烷烃均存在同分异构体,且同分异构体的数目随碳原子数的增加而增多,如:丁烷有2种同分异构体、己烷有5种同分异构体、癸烷有75种同分异构体。
同分异构现象是有机物种类繁多的原因之一 2、化学“四同”的比较对象原子单质有机化合物无机化合物、有机化合物性质化学性质几乎完全相同,物理性质略有差异化学性质相似,物理性质差异较大化学性质相似,熔沸点、密度规律性变化化学性质相似或不同,物理性质有差异【对点训练1】1、下列叙述正确的是()A.分子式相同,各元素含量也相同的物质是同种物质B.通式相同的不同物质一定属于同系物C.分子式相同的不同物质一定是同分异构体D.相对分子质量相同的不同物质一定是同分异构体二、烷烃同分异构体的书写方法——“减碳法” (烷烃只存在碳链异构,以C6H14为例)书写的步骤碳架式注意①将分子中所有碳原子连成直链作为主链C—C—C—C—C—C (a)②从主链一端取下一个碳原子作为支链(即甲基),依次连在主链对称轴一侧的各个碳原子上,此时碳骨架有两种(b)(c)甲基不能连在①位和⑤位碳原子上,否则与原直链时相同;对于(b)中②位和④位碳原子等效,只能用一个,否则重复③从主链上取下两个碳原子作为一个支链(即乙基)或两个支链(即两个甲基)依次连在主链对称轴一侧的各个碳原子上,此时碳骨架结构有两种(d)(e)②位或③位碳原子上不能连乙基,否则主链上会有5个碳原子,则与(b)中结构重复(1)两注意:①选择碳原子数最多的碳链为主链;②找出对称轴(2)四句话:主链由长到短,支链由整到散,位置由心到边,排列对、邻到间(3)取代基不能连在末端,否则与原直链时相同(4)从母链上取上的碳原子数,不得多于母链所剩余的碳原子数【当堂训练】烷烃(C n H2n+2,只可能存在碳链异构)n=1n=2n=3n=4n=51、分子式为C7H16的烷烃中,在结构式中含有3个甲基的同分异构体数目是( )A.2个 B.3个 C.4个 D.5个2、分子式为C8H18,每个分子中含有4个甲基的烃的结构可能是( )A.5种 B.6种 C.7种 D. 8种三、烷烃烃基的找法、一卤代烃的找法和多卤代烃的找法1、烷烃烃基的找法2(1)同一个碳原子上连接的氢原子等效如:甲烷(CH4)分子中4个氢原子是等效的(2)同一个碳原子上所连接的甲基上的氢原子等效如:新戊烷()分子中四个甲基等效,各甲基上的氢原子完全等效,也就是说新戊烷分子中的12个H 原子是等效的(3)分子中处于对称位置上的氢原子是等效的如:分子中的18个氢原子是等效的3、烷烃一氯代物和多氯代物的找法(1)一元取代物的找法:烃分子中有多少中结构不同的氢原子,其一元取代物就有多少种同分异构体①根据烷基的种类确定一元取代物种类如:丁基(—C4H9)的结构有4种,戊基(—C5H11)的结构有8种,则C4H9Cl有4种,C5H11Cl有8种②等效氢法:有几种等效氢原子就有几种一元取代物1、某烃的一种同分异构只能生成1种一氯代物,该烃的分子式可以是( )A.C3H8 B.C4H10 C.C5H12 D.C6H142、某烃的一卤代物有四种不同沸点的产物,则烃可能是( )A.甲烷 B.C3H8 C.C4H10 D.2-甲基丙烷3、(多选)C6H14的各种同分异构体中,所含甲基数和它的一氯代物的数目与下列相符的是( )A.2个甲基,4种一氯代物 B.3个甲基,4种一氯代物C.3个甲基,5种一氯代物 D.4个甲基,4种一氯代物4、含碳原子个数为10或小于10的烷烃中,其一卤代烷烃不存在同分异构体的烷烃共有( )A.2种B.3种C.4种D.5种(2)多元取代物种类——分次定位法如:C3H8的二氯代物,先找一氯代物,再利用等效氢法,再用氯原子取代一氯代物上的氢原子①二氯代物的找法:先找一氯代物,再用氯原子取代一氯代物上的氢原子CH2Cl2C2H4Cl2C3H6Cl2C4H8Cl21、某烃的相对分子质量为86,其结构中含有1个—CH2—和4个—CH3,则该烃的二氯代物有()A.5种 B.6种 C.7种 D.8种2、C4H10的二氯取代产物异构体数目为( )A.7种 B.8种 C.9种 D.10种②三氯代物的找法:先找二氯代物,再用氯原子取代二氯代物上的氢原子CHCl3C2H3Cl3C3H5Cl34如:乙烷分子中共有6个H原子,若有一个H原子被Cl原子取代所得一氯乙烷只有一种结构,那么五氯乙烷有多少种?假设把五氯乙烷分子中的Cl原子转换为H原子,而H原子转换为Cl原子,其情况跟一氯乙烷完全相同,故五氯乙烷也有一种结构。
烷烃

一.定义,通式和同系列定义:由碳和氢两种元素组成的饱和烃称为烷烃.通式: CnH2n+2同系列: 相邻的两种烷烃分子组成相差一个碳原子和两个氢原子,像这样结构相似,而在组成上相差一个或几个CH2的一系列化合物称为同系列.二.同分异构体甲烷,乙烷和丙烷没有同分异构体,从丁烷开始产生同分异构体.碳链异构体:因为碳原子的连接顺序不同而产生的同分异构体.随着分子中碳原子数目的增加,碳链异构体的数目迅速增多.三.烷烃的结构碳原子的最外层上有4个电子,电子排布为1S22S22P2,碳原子通过SP3杂化形成四个完全相同的SP3杂化轨道,所谓杂化就是由若干个不同类型的原子轨道混合起来,重新组合成数目相等的.能量相同的新轨道的过程.由1个S轨道与3个P轨道通过杂化后形成的4个能量相等的新轨道叫做SP3杂化轨道,这种杂化方式叫做SP3杂化.在形成甲烷分子时,4个氢原子的S轨道分别沿着碳原子的SP3杂化轨道的对称轴靠近,当它们之间的吸引力与斥力达到平衡时,形成了4个等同的碳氢σ键.实验证明甲烷分子是正四面体型的.4个氢原子占据正四面体的四个顶点,碳原子核处在正四面体的中心,四个碳氢键的键长完全相等,所有键角均为109.5.σ 键的特点:(1)重叠程度大,不容易断裂,性质不活泼.(2)能围绕其对称轴进行自由旋转.四.烷烃的命名碳原子的类型:伯碳原子:(一级)跟另外一个碳原子相连接的碳原子.仲碳原子:(二级)跟另外二个碳原子相连接的碳原子.叔碳原子:(三级)跟另外三个碳原子相连接的碳原子.季碳原子:(四级)跟另外四个碳原子相连接的碳原子.普通命名法其基本原则是:(1)含有10个或10个以下碳原子的直链烷烃,用天干顺序甲,乙,丙,丁,戊,已,庚,辛,壬,癸10个字分别表示碳原子的数目,后面加烷字.例如: CH3CH2CH2CH3 命名为正丁烷.(2)含有10个以上碳原子的直链烷烃,用小写中文数字表示碳原子的数目.如CH3(CH2)10CH3命名为正十二烷.(3)对于含有支链的烷烃,则必须在某烷前面加上一个汉字来区别.在链端第2位碳原子上连有1个甲基时,称为异某烷,在链端第二位碳原子上连有2个甲基时,称为新某烷.如: 正戊烷异戊烷新戊烷系统命名法系统命名法是我国根据1892年曰内瓦国际化学会议首次拟定的系统命名原则.国际纯粹与应用化学联合会(简称IUPAC法)几次修改补充后的命名原则,结合我国文字特点而制定的命名方法,又称曰内瓦命名法或国际命名法.烷基:烷烃分子去掉一个氢原子后余下的部分.其通式为CnH2n+1-,常用R-表示.常见的烷基有:甲基CH3— (Me)乙基CH3CH2— (Et)正丙基CH3CH2CH2— (n-Pr)异丙基(CH3)2CH— (iso-Pr)正丁基CH3CH2CH2CH2— (n-Bu)异丁基(CH3)2CHCH2— (iso-Bu)仲丁基(sec-Bu)叔丁基(CH3)3C— (ter-Bu)在系统命名法中,对于无支链的烷烃,省去正字.对于结构复杂的烷烃,则按以下步骤命名:选择分子中最长的碳链作为主链,若有几条等长碳链时,选择支链较多的一条为主链.根据主链所含碳原子的数目定为某烷,再将支链作为取代基.此处的取代基都是烷基.从距支链较近的一端开始,给主链上的碳原子编号.若主链上有2个或者个以上的取代基时,则主链的编号顺序应使支链位次尽可能低.将支链的位次及名称加在主链名称之前.若主链上连有多个相同的支链时,用小写中文数字表示支链的个数,再在前面用阿拉伯数字表示各个支链的位次,每个位次之间用逗号隔开,最后一个阿拉伯数字与汉字之间用半字线隔开.若主链上连有不同的几个支链时,则按由小到大的顺序将每个支链的位次和名称加在主链名称之前.如果支链上还有取代基时,则必须从与主链相连接的碳原子开始,给支链上的碳原子编号.然后补充支链上烷基的位次.名称及数目.五.物理性质1.状态:在常温常压下,1至4个碳原子的直链烷烃是气体,5至16个碳原子的是液体,17个以上的是固体.2.沸点:直链烷烃的沸点随分子量的增加而有规律地升高.而低级烷烃的沸点相差较大,随着碳原子的增加,沸点升高的幅度逐渐变小.沸点的高低取决于分子间作用力的大小.烷烃是非极性分子,分子间的作用力(即范德华力)主要是色散力,这种力是很微弱的.色散力与分子中原子数目及分子的大小成正比,这是由于分子量大的分子运动需要的能量也大.多一个亚甲基时,原子数目和分子体积都增大了,色散力也增大,沸点即随之升高.色散力是一种近程力,它只有在近距离内才能有效地发挥作用,随着分子间距离的增大而迅速减弱.带着支链的烷烃分子,由于支链的阻碍,分子间不能像直链烷烃那样紧密地靠在一起,分子间距离增大了,分子间的色散力减弱,所以支链烷烃的沸点比直链烷烃要低.支链越多,沸点越低.3.熔点:直链烷烃的熔点,其本上也是随分子量的增加而逐渐升高.但偶数碳原子的烷烃熔点增高的幅度比奇数碳原子的要大一些.形成一条锯齿形的曲线.烷烃的熔点也主要是由分子间的色散力所决定的.固体分子的排列很有秩序,分子排列紧密,色散力强.固体分子间的色散力,不仅取决于分子中原子的数目和大小,而且也取决于它们在晶体中的排列状况.X-光结构分析证明:固体直链烷烃的晶体中,碳链为锯齿形的,由奇数碳原子组成的锯齿状链中,两端的甲基处在一边,由偶数碳原子组成的锯齿状链中,两端的甲基处在相反的位置.即偶数碳原子的烷烃有较大的对称性,因而使偶数碳原子链比奇数碳原子更为紧密,链间的作用力增大,所以偶数碳原子的直链烷烃的熔点要高一些.4.溶解度:烷烃是非极性分子,又不具备形成氢键的结构条件,所以不溶于水,而易溶于非极性的或弱极性的有机溶剂中.5.密度:烷烃是在所有有机化合物中密度最小的一类化合物.无论是液体还是固体,烷烃的密度均比水小.随着分子量的增大,烷烃的密度也逐渐增大.六.化学性质烷烃是非极性分子,分子中的碳碳键或碳氢键是非极性或弱极性的σ键,因此在常温下烷烃是不活泼的,它们与强酸.强碱.强氧化剂.强还原剂及活泼金属都不发生反应.氧化反应:烷烃很容易燃烧,燃烧时发出光并放出大量的热,生成CO2和H2O.CH4 + 2O2 CO2 + 2H2O + 热量在控制条件时,烷烃可以部分氧化,生成烃的含氧衍生物.例如石蜡(含20—40个碳原子的高级烷烃的混合物)在特定条件下氧化得到高级脂肪酸.RCH2CH2R + O2 RCOOH + RCOOH2,裂化:烷烃在隔绝空气的条件下加强热,分子中的碳碳键或碳氢键发生断裂,生成较小的分子,这种反应叫做热裂化.如:CH3CH2CH2CH3 CH4 + CH2=CHCH3CH3CH3 + CH2=CH2CH2=CHCH2CH3 + H2取代反应:卤代反应是烷烃分子中的氢原子被卤素原子取代.将甲烷与氯气混合,在漫射光或适当加热的条件下,甲烷分子中的氢原子能逐个被氯原子取代,得到多种氯代甲烷和氯化氢的混合物.CH4 +Cl2 CH3Cl + HClCH3Cl + Cl2 CH2Cl2 + HClCH2Cl2 + Cl2 CHCl3 + HClCHCl3 + Cl2 CCl4 + HCl卤素反应的活性次序为:F2 >Cl2 > Br2 > I2对于同一烷烃,不同级别的氢原子被取代的难易程度也不是相同的.大量的实验证明叔氢原子最容易被取代,伯氢原子最难被取代.卤代反应机理:实验证明,甲烷的卤代反应机理为游离基链反应,这种反应的特点是反应过程中形成一个活泼的原子或游离基.其反应过程如下:(1)链引发: 在光照或加热至250—400度时,氯分子吸收光能而发生共价键的均裂,产生两个氯原子游离基,使反应引发.Cl2 2Cl(2)链增长:氯原子游离基能量高,反应性能活泼.当它与体系中浓度很高的甲烷分子碰撞时,从甲烷分子中夺取一个氢原子,结果生成了氯化氢分子和一个新的游离基——甲基游离基.Cl + CH4 HCl + CH3甲基游离基与体系中的氯分子碰撞,生成一氯甲烷和氯原子游离基.CH3 + Cl2 CH3Cl + Cl反应一步又一步地传递下去,所以称为链反应.CH3Cl + Cl CH2Cl + HCl3CH2Cl + Cl2 CH2Cl2 + Cl(3)链终止: 随着反应的进行,甲烷迅速消耗,游离基的浓度不断增加,游离基与游离基之间发生碰撞结合生成分子的机会就会增加. Cl + Cl Cl2CH3 + CH3 CH3CH3CH3 + Cl CH3Cl七.重要的烷烃。
烷烃同分异构
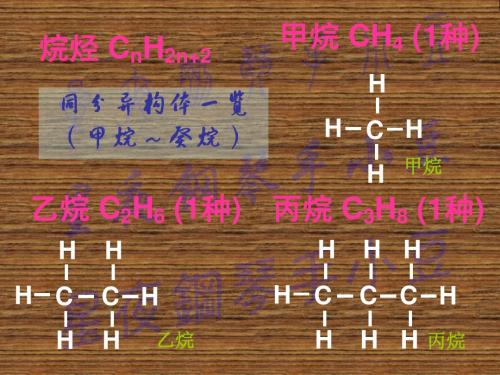
2-甲基辛烷 3-甲基辛烷
C C C C C C C C
C
4-甲基辛烷
C
C C C C C C C
C C C C C C C C C C
2,2-二甲基庚烷
2,3-二甲基庚烷
C
C
2,4-二甲基庚烷
C C C C C C C C C
C C C C C C C
2,5-二甲基庚烷
C
C
2,6-二甲基庚烷
C C C C C C C C
CH3 CH3
2,2-二甲基丁烷
CH3
3-甲基戊烷
CH3 C CH2 CH3 CH3 CH CH CH3 CH3 CH3
2,3-二甲基丁烷
庚烷 C7H16 (9种)
CH3 CH2 CH2 CH2 CH2 CH2 CH3 庚烷 CH3 CH CH2 CH2 CH2 CH3 CH3
CH3 CH2 CH CH2 CH2 CH3 CH3
按照主链碳数逐渐减少,取代基由简到繁,取代位次由小到 大的顺序排列的,并标有CCS系统命名(含有异丙基的除 外)。 星夜钢琴手小豆
2008年8月14日
3-甲基庚烷
CH3 CH2 CH2 CH CH2 CH2 CH3 CH3
4-甲基庚烷
CH3 CH3 C CH2 CH2 CH3 CH2 CH3
2,2-二甲基己烷
CH3 CH CH CH2 CH2 CH3 CH3 CH3 CH3 CH CH2 CH
2,3-二甲基己烷
CH2 CH3
2,4-二甲基己烷
CH3 CH3 CH3 CH CH2 CH2 CH CH3
2,5-二甲基-3-乙基己烷
3,3-二甲基-4-乙基己烷
C C C C C C C C
烷烃的同分异构体数目规律

烷烃的同分异构体数目规律哎呀,今天咱们来聊聊烷烃的同分异构体,听起来是不是有点高深?别担心,我保证让你听得津津有味,保证没有干巴巴的公式。
烷烃就是碳和氢的结合体,简单的说就是那些像石油、天然气里的小家伙。
想象一下,你在油炸小吃的时候,油滋滋作响,那种感觉就像烷烃在化学反应中欢快地跳舞。
烷烃有很多种,特别是它们的同分异构体,哇,真是让人眼花缭乱。
你知道吗,同分异构体就像是同一支乐队的不同乐器,各有各的特点。
就拿丁烷来说,丁烷其实有两种不同的结构,第一种是直链的,咱们叫它“正丁烷”,第二种则是分支的,叫做“异丁烷”。
这就像你在不同的场合听到的同一首歌,不同的演绎风格会给你带来截然不同的感受。
听起来有趣吧?想象一下,正丁烷在舞台上展现出自己高大上的身材,而异丁烷则是一个活泼的小家伙,在旁边灵活地跳跃。
说到同分异构体的数目,有一个规律,那就是随着碳链的增加,异构体的数量也跟着水涨船高。
比如,五个碳的戊烷有三种异构体,六个碳的己烷更是多达五种。
你有没有发现,越往上走,这种规律就越明显,真是让人感叹大自然的鬼斧神工,仿佛是上天在给我们每个烷烃都量身定做了一套独特的“服装”。
每个异构体都有自己的性格和用途,简直就像人们一样,各有各的长处。
不过,你知道的,这些同分异构体可不只是好看而已,实际应用也相当广泛。
像正丁烷,常常用作燃料,供我们烹饪美味的佳肴。
反观异丁烷,它则被广泛应用于制冷剂和喷雾剂中,想象一下,正是这些小分子在默默为我们的生活提供便利。
它们之间的竞争就像是生活中的小故事,充满了各种酸甜苦辣,有时候还会让人哭笑不得。
在这里,咱们还得提一下命名规则,尤其是国际化学命名法,它就像是给这些小家伙们起了名字的“父母”。
名字起得可好玩了,简直能让人忍不住笑出声。
比如,六个碳的六种异构体,它们的名字就像是一场嘉年华,各种排列组合,让人看得眼花缭乱。
不过,一旦你掌握了这个规律,认出它们的名字可就容易多了。
真是让人感叹,化学的魅力就在于此,咱们平时接触的每一件事情都和它们息息相关。
