Fisher投影式与锯架式的互相转化
构象间的转换
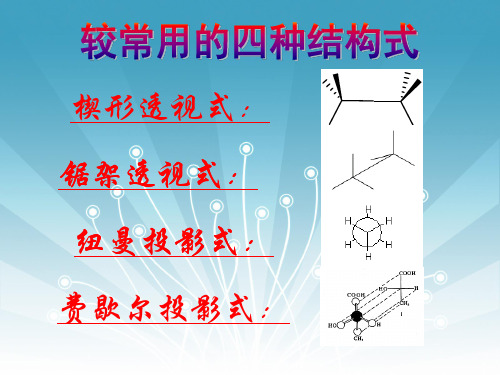
单键可以自由旋转,分子中的原子或基团 围绕单键旋转时,可以产生不同空间排布方 式,即产生不同的构象,再根据构象进行各 种结构式的转换。
H
1 CHO 2
H OH
1CHO 2
OH
H H
OH OH
3 2 4 CH2OH OHC 1
H 3
OH
=
3 H HOCH2 4 OH
4 CH2OH
眼睛由此从下向上看
由楔形式写费歇尔投影式
[1] 东北师大等五院校合编.《有机化学》(第三版) 北京:高等教育出版社,1993 [2] 邢其毅等.《基础有机化学》(第二版) 北京:高等教育出版社,1992 [3] 王积涛等.《有机化学》(第二版) 天津: 南开大学出版社,2003 [4] 邢其毅主编.《基础有机化学示范教学》 北京:北京大学出版社,1983 [5] 叶秀林.《立体化学》 北京:高等教育出版社,1982
2
OH
=
3 H OH HOCH2 4 (2)
OH CHO 1
4 CH2OH (1)
H 2
4 HOCH2 (3)
1 CHO
OH
1800 HO
2 H
3
OH
CHO 1
H
3
OH
HOCH2 4 (4) 重叠式构象
HOCH2 4 (5) 交叉式构象
1 CHO 1 CHO H HO 2 3 H 4 CH2OH 4 CH2OH (1) (2) OH H 3 HO OH 2 H
4 CH2OH ⑴
4 CH2OH ⑵
把分子立体模型放在眼前,从C-C单键的延长线上 观察,用圆心表示前面的碳原子,用圆表示后面的 0 碳原子,分别从圆心和圆上引出三条互为120 的射线 作为价键,用以连接碳原子上的三个原子或基团。
费歇尔投影式

书写注意
费歇尔投影式严格表示了各个原子或基团空间与平面的关系,所以使用时应注意以下事项。同时,也可以逆 用这些规则来判别不规范的费歇尔投影式之间,是同一种构型还是对应异构体,下面就用氟氯溴碘化碳(假想物) 举例子。
(1)某一个化合物的费歇尔投影式只能在纸平面上平移,投影式不能离开纸平面翻转180°,否则一对对映体 的投影式便能相互重叠。
投影式
四面体型分子投影式被投影至平面上变成费歇尔投影式为了方便书写和比较,特别是对于含有多个手性碳原 子的糖化物和氨基酸等有机分子,德国化学家费歇尔(Fischer E)于1891年,首次提出一种用二维图象和平面式 子表示三维分子立体结构的重要方法——费歇尔投影式。 右图即为四面体型分子投影式被投影至平面上变成费 歇尔投影式。
投影规则
乳酸的费歇尔投影式
为了作出统一的分子构型表达式,费歇尔曾制定了三条投影规则 :
(1)将碳链放在垂直线上或竖起来,把氧化态较高的碳原子或命名时编号最小(主链中第一号)的碳原子C1 放在最上端。
(2)投影时假定手性碳原子放在纸平面上,与垂直线(vertical line)相连的原子或基团(垂直方向的键 /竖键) 表示伸向纸面后方,即远离读者;与水平线(horizonal line)相连的原子或基团(水平方向的键 /横键)表示伸向 纸面前方,即伸向读者。 “横前竖后”规则是费歇尔式最基本的硬性规定。
哈沃式中己醛糖的吡喃环用一个垂直于纸平面的六角向着读者细线的含氧桥环边表示离开读者。
定义内容
投影规则
概念辨析
书写注意
概念辨析
有机物的同分异构现象可分成两大类:构造异构和立体异构。其中,立体异构又包括顺反异构、对映异构和 构象异构三种情况。而费歇尔投影式主要用于对映异构的书写,对映异构体是分子式相同,构造式相同,但构型 不同,互为镜象但不能重合的立体异构体。 从构象上分析,费歇尔式都是不稳定的重叠式构象,因此,在进行 构象分析时不用费歇尔式。
化学第三章立体化学

C=Y
CY (Y) (C)
Y为C、O、N等常见原子,是几重键就相当于连几 个相同的原子。
H (C) CH CH2 相当于 C C H
(C) H
H(C) H(C)
相当于 (C)
H
( C)
(C)
H
H (C)
(C) (C) C CH 相当于 C C H
(C) (C)
(N) (C) C N 相当于 C N
H
H
CC C6H5
CH3 CC
H
H
(顺,顺)
H CC
C6H5
H H
CC
H
CH3
(顺,反)
H
C C6H5
H
CH3
CC
C
H
H
(反,反)
H
H
H
CC
CC
C6H5
H
CH3
(反,顺)
H
CH2CH3 CH3CH2
CH(CH3)2
CC
CC
CH3
CH2CH2CH3 CH3
CH2CH2CH3
(三) Z , E - 命名法
H5 4 H
CC
CH3
3 2H CC 1
H
COOH
(2E,4Z) – 2,4- 己二烯酸
(四)顺反异构体的性质(一般规律的比较)
顺、反-丁烯二酸的物理性质
异构体
熔点/℃ 密度
溶解度( 25℃) /(g/100g·H2
O)
顺-丁烯二酸 130
1.590
78.8
反-丁烯二酸 287
1.625
0.7
1.构造式(结构式)相同(分子的结构相同,构型不同)
2. 比较各种取代原子或原子团的排列顺序时,先比 较直接相连的第一个原子的原子序数。如果是相同 原子,那就再比较第二个、第三个……原子的原子 序数。 C(CH3)3 > CH(CH3)2 > CH2CH3 > CH3
第5章习题及参考答案

第5章习题及参考答案解释下列名词:(1)旋光性 (2)手性 (3)对映体 (4)非对映体 (5)内消旋体 (6)外消旋体 解:(1)使偏振光的振动平面发生旋转的性质。
(2)物质的分子和它的镜像不能重合的特征。
(3)分子式,构造式相同,构型不同互呈镜像对映关系的立体异构现象称为对映异构。
(4)不为实物和镜像关系的异构体。
(5)分子中存在一个对称面,分子的上半部和下半部互为实物和镜像,这两部分的旋光能力相同,但旋光方向相反,从而使旋光性在分子内被相互抵消,因此不具有旋光性的化合物。
(6)由等量的一对对映体组成的物质。
、现有某旋光性物质mL 的溶液一份: (1)将一部分该溶液放在5cm 长的盛液管中,测得旋光度为+°,试计算该物质的比旋光度。
(2)若将该溶液放在10cm 长的盛液管中测定。
你观察到的旋光度应是多少 解:(1) +100°;(2) +5°判断下列化合物中有无手性碳原子,并用“*”标出手性碳原子。
解:&下列叙述是否正确,为什么(1)具有R 构型的化合物一定是右旋(+)的。
(1)(3)(4)(2)CH 3CH 2CH 2CHCH 2OHCH 3CH 3CH 2CH 2CH 2CHCH 2ClCH 3BrCH 2CHCH 2FCH 2Cl(1)(3)(4)(2)CH 3CH 2CH 2CHCH 2OH CH 3CH 3CH 2CH 2CH 2CHCH 2ClCH 3BrCH 2CHCH 2FCH 2Cl***(2)有旋光性的分子一定含有手性原子。
(3)含有手性原子的分子一定具有旋光性。
(4)一个分子从R 构型转化到另一个分子的S 构型一定进行了构型翻转。
(5)对映体除旋光方向相反外,其物理性质和化学性质完全相同。
解: 均不正确。
)下列化合物中哪些具有旋光性解:化合物B 、C 、D 具有旋光性。
用R/S 标记下列分子的构型。
(1) (2):(3) (4)解:(A) R ,(B) R ,(C) R ,(D) R判断下列化合物之间的关系,哪些是同一化合物,哪些是对映体,哪些是非对映体(1).和OCH 3CH 3(3)(1)(6)(5)(2)OH 3HC 2H 5ClCH 3CH 2Cl 3C 2H 5CH 2OH H 3CHO H 32H COOH Cl CH 3ClHCOOHCH 3A.B. C. E. -F.A. C. D.B.(2)和 (3)和.解: (1) 同一化合物,(2) 对映体,(3 )非对映体下列化合物的构型式中,哪些是对映体哪些是内消旋体哪些是相同的 (1)A. B. (2)A. B.(3) A B|解:(1) A 、B 为内消旋体。
第5章习题与参考答案
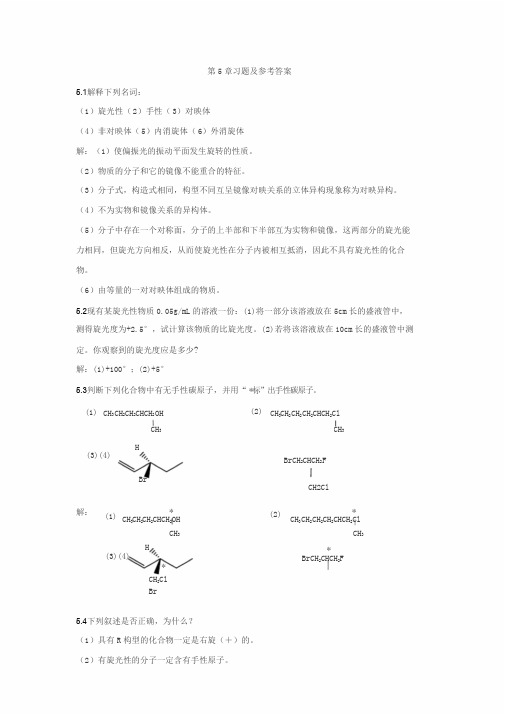
第5章习题及参考答案5.1解释下列名词:(1)旋光性(2)手性(3)对映体(4)非对映体(5)内消旋体(6)外消旋体解:(1)使偏振光的振动平面发生旋转的性质。
(2)物质的分子和它的镜像不能重合的特征。
(3)分子式,构造式相同,构型不同互呈镜像对映关系的立体异构现象称为对映异构。
(4)不为实物和镜像关系的异构体。
(5)分子中存在一个对称面,分子的上半部和下半部互为实物和镜像,这两部分的旋光能力相同,但旋光方向相反,从而使旋光性在分子内被相互抵消,因此不具有旋光性的化合物。
(6)由等量的一对对映体组成的物质。
5.2现有某旋光性物质0.05g/mL的溶液一份:(1)将一部分该溶液放在5cm长的盛液管中,测得旋光度为+2.5°,试计算该物质的比旋光度。
(2)若将该溶液放在10cm长的盛液管中测定。
你观察到的旋光度应是多少?解:(1)+100°;(2)+5°5.3判断下列化合物中有无手性碳原子,并用“*标”出手性碳原子。
(1) C H3CH2CH2CHCH2OH (2) C H3CH2CH2CH2CHCH2ClCH3CH3 H(3)(4)BrCH2CHCH2FBrCH2Cl解:(1) *CH3CH2CH2CHCH2OH (2) *CH3CH2CH2CH2CHCH2ClCH3CH3H (3)(4)** BrCH2CHCH2FCH2ClBr5.4下列叙述是否正确,为什么?(1)具有R构型的化合物一定是右旋(+)的。
(2)有旋光性的分子一定含有手性原子。
(3)含有手性原子的分子一定具有旋光性。
(4)一个分子从R构型转化到另一个分子的S构型一定进行了构型翻转。
(5)对映体除旋光方向相反外,其物理性质和化学性质完全相同。
解:均不正确。
5.5下列化合物中哪些具有旋光性?OHOHA.B.C.OH (1)(2)(3)OCH3OHCH3D.E.F.O(6) (4)(5)O HHH3CH 解:化合物B、C、D具有旋光性。
有机化学B习题课-期中

类似:烯烃及芳香烃的α-卤代
12
化学性质
烯烃马氏:Cl2,HCl,H2SO4(会水解成醇), Br2+H2O,Br2+NaCl/H2O
炔烃马氏:Cl2(FeCl3),HCl(HgCl2,加热),H2O (H2SO4/HgSO4, 会烯醇异构)
烯烃,炔烃反马氏: HBr自由基加成;B2H6+H2O2/OH-/H2O 加成速率:双键上电子云密度越大,即给电子基越多 越易加成 13
有机化学习题课
1
考试题型
一、回答问题(28%) 命名、构型构象、对映体、自由基稳定性、 反应速率及反应活性、熔沸点、定位效应 二、写出反应的主产物(23%) (必要时请注明立体化学问题) 三、推测结构、鉴别(10%) 四、机理题 (15%) 五、合成题(24%)
2
命名
(3Z,5E)-2-甲基-3,5-辛二烯 编号位置使双键尽可能小
10
化学性质
烷烃的卤化反应
反应条件:光照、高温或催化剂
反应机理:自由基
反应活性:叔氢 〉仲氢 〉伯氢 卤原子的选择性:I>Br>Cl>F
CH3CHCH3 + Br2 CH3 hv 127 (CH3)2CHCH2Br + (CH3)3CBr <1% >99%
11
V(1 H):V(2 H) : V(3 H) =1:82:1600
强
中
NR2 OR R
NHR
NH2
OH
NHCOR C6H5
OCOR X
20
弱
苯环的定位基团
第二类定位基(间位定位基)(钝化) 中
强
NR3 CHO
NO2 COR
大学有机化学第八章立体化学(对映异构)

3. 楔型式转化为 Fischer 投影式
方法:将纸面上竖直向上的基团和伸向纸面后方的 基团写在 Fischer 投影式的竖线上,上下关系不变;
其余两个基团写在横线上,左右关系不变。
COOH C OH
H3C
COOH
H H 3C
OH
H
COOH C OH
HO
COOH C
H H 3C
H CH3
COOH
COOH COOH
COOH H HO C CH 3
H OH CH3 CH3 OH H
COOH C H3C H OH
-
(2) 二者的关系:互为镜像(实物与镜像关系,或者 说左、右手关系)。二者无论如何也不能完全重叠。
与镜像不能重叠的分子,称为手性分子
对映异构体
分子的构造相同,但构型不同;形成实物与镜象、相 似而不能重合的两种分子,称为对映异构体(对映体) 对映体:成对存在,旋光能力相同,但旋光方向相反 二者能量相同(分子中任何两原子的距离相同)
H Cl H H Cl
Cl H H Cl Cl H H Cl
360° /4
Cl H
Cl
相同
S4
判断分子是否手性的依据:
※ 凡具有对称面、对称中心的分子,都是非手性分子。 ※ 有无对称轴,对分子是否有手性无决定作用。 一般:※ 当分子中只有一个C* ,分子一定有手性。 ※ 当分子中有多个手性中心时,要借助对称因素。无对称 面,又无对称中心的分子,必是手性分子。
实验事实:
CH3 CH COOH
OH α 羟基丙酸 ( 乳酸 ) 来 源 旋光性 。 + 3.82 。 3.82 。 0
从肌肉中得到的肌肉乳酸 葡萄糖发酵得到的乳酸 酸牛奶中得到的乳酸
旋光异构BEI

含n个不同手性碳原子的化合物,可能有的旋光
异构体的数目有2n个,外消旋体的数目2n-1对。
非对映异构体
不呈物体与镜象关系的异构体叫做非对映异构体。分 子中有两个以上手性中心时,就有非对映异构现象。
非对映异构体的特征: 1.物理性质不同(熔点、沸点、溶解度等)。 2.比旋光度不同。 3.旋光方向可能相同也可能不同。 4.化学性质相似,但反应速度有差异。
转,构型不变。 5.任意两个基团调换偶数次,构型不变。 6.任意两个基团调换奇数次,构型改变。
8
快速判断Fischer投影式构型的方法
1. 当最小基团位于竖线时,其余三个基团由大→中 →小为顺时针方向,则投影式的构型为R,反之为S。 2. 当最小基团位于横线时,其余三个基团由大→中→ 小为顺时针方向,则投影式的构型为S,反之为R。
素而具有手性。 29
30
二、 丙二烯型化合物
当C1和C3各连有不同基团时,也有旋光异构体。
实例:a=苯基,b=萘基,1935年拆分。 Vont Hoff(荷兰)Bel(法) (1901年诺贝尔奖)
31
如2,3-戊二烯就已分离出对映异构体。
CH 3
CH 3 CH 3
CH 3
CC C
CC C
H
H H
COOH
COOH COOH
COOH
I
II
III
IV
(2R,3S) (2S,3R) (2R,3R) (2S,3S)
这四种异构体中 (III)和(IV) 是对映体;(I)和(II)是同一 种物质(分子中有一个对称面)称为内消旋体。
酒石酸只有三种异构体,右旋体,左旋体和内消旋体。
内消旋体与外消旋体的异同
H
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Fisher投影式
锯架式
然后按照单键的可旋转性旋转到自己想要的构型进行分析
接点碳1和碳2的锯架式 (两根红线代表条一根化学键,即 Fisher投影式中的红线代表的化学键)
→
CH3 C C2H5
CH3
→
锯架式完整图,旋转可得任意构象图
可以根据自己的需要转到合适的角度,判断其构型,也可转 到合适的角度来书写Newsman式. 以上是接点碳数为2的情况,进而可以扩展到接点碳数至无 穷.
第三章习题
3-6 标明下列分子中手性碳原子的构型,并指出他们之间的关 系。 典型问题: 1.概念混淆:构型表示与构型标记 1. 2.Fisher投影式与锯架式的互相转换 3.手性碳原子R,S构型的判别
1. 构型表示与构型标记 构型的表示:球棒式,立式透视式,费歇尔投影式。 构型的标记: (1). D-L构型标记法; (2).R-S构型标记法。 注意题目要求:标明构型。 回顾知识点
2. Fisher投影式与锯架式的互相转换 本人做这类题的方法:逐个接点碳法(百试百爽的方法) 首先看一下Fisher投影式的定义:在Fisher投影式中, 横线连接的两个原子或原子团是伸向观察者的,伸 向纸面前方;竖线连接的两个原子或原子团是背离观 察者,伸向纸面后方。 例: CO2 OH CO2H
总结: 1. Fisher投影式与锯架式的互相转换是互通的,也可 以用这种方法来有锯架式向Fisher投影式转换。 2. 无论Fisher投影式有多复杂,其跟锯架式的转换 都是按照以下的形式转换的,只要熟练了,就可以 按照以下的形式直接看着Fisher投影式直接写出, 而无需经过中间步骤.
按照箭头方向如下形式依次书写:
H
HO
CH3
H
→
HO
C CH3
立体透视式
H
→
C CO2H
CH3 锯架式
Fisher投影式
以上例子是接点碳数为一个的情况,下面看接点碳两个的情况: 以3-6(1)为例:
Cl
接 碳 点 1
H
→
Cl
C
H C
CH3 H OH C2H5
Fisher投 式 影
接 碳 点 2
H
CH3
Cl CH3
}
CH3 H C C 2H 5
