挥发性脂肪酸的测定——5种方法
VFA的测定方法

VFA的测定方法一、药品:1、10%NaOH溶液2、NaOH标准溶液,0.1000mol/l3、10%磷酸溶液(或15%硫酸)4、酚酞指示剂二、步骤:1、于蒸馏瓶中放入100ml废水水样(其VFA不超过1800mg/l),加入几滴酚酞。
2、加入10%NaOH溶液使水样呈碱性,并使NaOH微过量。
开始蒸馏至蒸馏瓶中剩余液体为50-60ml为止。
3、冷却,加蒸馏水至蒸馏瓶中液体100ml左右。
用10ml10%磷酸溶液酸化,在接收瓶中(或烧杯)放入10-20ml蒸馏水,并使接收瓶与蒸馏瓶上的冷凝管连接,导入管应浸入接收瓶液面以下,蒸馏至瓶中液体为15-20ml为止,待蒸馏瓶冷却后加入50ml蒸馏水再次蒸馏至15-20ml为止(这次蒸馏结果差别不大时可以不做)。
4、用NaOH标准溶液滴定馏出液至淡粉色不消失为止。
三、计算:VFA(mg/l)=式中:VNaOH—滴定时消耗的NaOH标准溶液(ml)C¬—NaOH标准溶液的浓度(mol/l)Vs—废水水样的体积(ml)挥发性脂肪酸(VFA)的测定挥发性脂肪酸(VFA)是厌氧消化过程的重要中间产物,甲烷菌主要利用VFA形成甲烷,只有少部分甲烷由CO2和H2生成。
但CO2和H2的生成也经过高分子有机物形成VFA的中间过程。
由此看来,形成甲烷的过程离不开VFA 的形成,但是VFA在厌氧反应器中的积累能反映出甲烷菌的不活跃状态或反应器操作条件的恶化,较高的VFA(例如乙酸)浓度对甲烷菌有抑制作用。
因此在反应器运行中,出水VFA用作重要的控制指标。
在VFA测定中,常进行VFA总量测定,其单位以mmol/l或换算为按乙酸计,以单位mg/l表示,对VFA中各种低级脂肪酸(乙酸、丙酸等)的分别定量分析也是重要的,有时常需要知道以COD表示的VFA的量(即VFA以单位mgCOD/l)表示,此时也需要知道VFA中各种有机酸的含量,因此它们换算为COD的换算系数是不同的。
挥发性脂肪酸的测定——5种方法
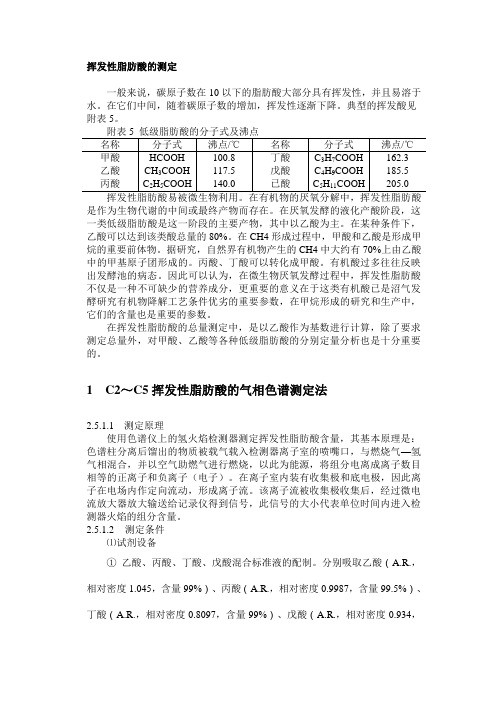
挥发性脂肪酸的测定一般来说,碳原子数在10以下的脂肪酸大部分具有挥发性,并且易溶于水。
在它们中间,随着碳原子数的增加,挥发性逐渐下降。
典型的挥发酸见附表5。
是作为生物代谢的中间或最终产物而存在。
在厌氧发酵的液化产酸阶段,这一类低级脂肪酸是这一阶段的主要产物,其中以乙酸为主。
在某种条件下,乙酸可以达到该类酸总量的80%。
在CH4形成过程中,甲酸和乙酸是形成甲烷的重要前体物。
据研究,自然界有机物产生的CH4中大约有70%上由乙酸中的甲基原子团形成的。
丙酸、丁酸可以转化成甲酸。
有机酸过多往往反映出发酵池的病态。
因此可以认为,在微生物厌氧发酵过程中,挥发性脂肪酸不仅是一种不可缺少的营养成分,更重要的意义在于这类有机酸已是沼气发酵研究有机物降解工艺条件优劣的重要参数,在甲烷形成的研究和生产中,它们的含量也是重要的参数。
在挥发性脂肪酸的总量测定中,是以乙酸作为基数进行计算,除了要求测定总量外,对甲酸、乙酸等各种低级脂肪酸的分别定量分析也是十分重要的。
1 C2~C5挥发性脂肪酸的气相色谱测定法2.5.1.1 测定原理使用色谱仪上的氢火焰检测器测定挥发性脂肪酸含量,其基本原理是:色谱柱分离后馏出的物质被载气载入检测器离子室的喷嘴口,与燃烧气—氢气相混合,并以空气助燃气进行燃烧,以此为能源,将组分电离成离子数目相等的正离子和负离子(电子)。
在离子室内装有收集极和底电极,因此离子在电场内作定向流动,形成离子流。
该离子流被收集极收集后,经过微电流放大器放大输送给记录仪得到信号,此信号的大小代表单位时间内进入检测器火焰的组分含量。
2.5.1.2测定条件⑴试剂设备①乙酸、丙酸、丁酸、戊酸混合标准液的配制。
分别吸取乙酸(A.R.,相对密度1.045,含量99%)、丙酸(A.R.,相对密度0.9987,含量99.5%)、丁酸(A.R.,相对密度0.8097,含量99%)、戊酸(A.R.,相对密度0.934,含量100%)各25μL 于50mL 容量瓶中,再加入2.5mL 甲酸(A.R.,相对密度1.22,含量88%),最后用蒸馏水定容。
挥发性脂肪酸VFA测定步骤与方法

挥发性脂肪酸的测定一、GC(Gas chromatograph)工作条件仪器:GC-14B型气相色谱仪(日本岛津公司)毛细柱:NUKOLTM Capillary Column ( Supelco );Column No.34292-07B30m×0.32mm×0.25μm film thickness气相色谱仪参数:色谱柱采用毛细吸管柱,柱温130℃,汽化温度180℃,采用氢离子火焰检测器,检测温度180℃,载气为氮气,压力为60 KPa,氢气压力为50 KPa,氧气压力50 KPa,灵敏度(档)为101,衰减 3.0二、样品制备1.试剂制备(1)配制25%w/v 的偏磷酸溶液,将25g偏磷酸溶在100mL双蒸水中(2)巴豆酸的配制,在100ml的偏磷酸溶液中加入0.6464g的巴豆酸,定容到100mL。
(可先用80 ml双蒸水,加热溶解偏磷酸,然后定容至100 ml)(3)标准样品,准确称取色谱标准级乙酸0.9100 g、丙酸0.3700 g、丁酸0.1765 g、异丁酸0.1765g、戊酸和异戊酸分别为0.1985g,分别溶于双蒸水中,再各自定容至100 mL。
2.样品制备(1) 发酵液取(或过滤瘤胃液)VFA测定1ml样品到离心管中,再加入0.2 ml的偏磷酸巴豆酸混合溶液,-20℃冰箱保存过夜,解冻后12000rpm离心5min,取上清液保存,测定前再12000rpm离心5min(或少许通过0.22μm针式滤器,滤液直接进样用 1.0微升微量进样器瞬时注入色谱仪,进样量为0.2-1.0μL。
(2) 食糜及粪样VFA测定取1g置于离心管中,加入5-10倍的双蒸水,混合均匀。
取1mL上清夜,加偏磷酸巴豆酸0.2mL/mL。
其它步骤同上。
3.保留时间的确定与样品处理相同,在 1 ml标准样品中加入0.2mL偏磷酸与巴豆酸的混合样,上样测出乙酸、丙酸、丁酸、异丁酸、戊酸和异戊酸的保留时间。
实验7污泥中挥发性脂肪酸的测定

实验三污泥中挥发性脂肪酸的测定一、实验目的挥发性脂肪酸(VFA)包括甲酸、乙酸、丙酸、丁酸、戊酸、己酸及它们的异构体,在VFA测定中,其单位常换算为按乙酸计,以mg/L表示。
常用的测定方法有滴定法和气相色谱分析法。
通过本实验将掌握滴定法测定污泥中VFA的方法。
二、实验原理VFA的含量是污染性质的一项重要指标,如新鲜污泥中的脂肪酸含量为10~30mg/L。
消化正常的污泥,其中脂肪酸的含量只有1~5mg/L。
VFA在酸性条件下,经加热蒸馏随水蒸汽逸出,用水蒸汽吸收并用NaOH滴定。
三、实验仪器及试剂1、实验仪器(1)圆底烧瓶;(2)玻璃导管;(3)锥形瓶;(4)电炉。
2、实验试剂(1)磷酸或硫酸;(2)酚酞指示剂;(3)蒸馏水;(4)0.1mol/L的NaOH。
四、实验步骤1、样品的制备移取50mL污泥离心上清液于500mL圆底烧瓶中,加50mL蒸馏水,再加2mL 磷酸或2mL硫酸。
接好玻璃导管,将橡胶塞塞严。
导管一头接烧瓶口,另一头接冷凝管,冷凝管下面导管插入盛有25mL蒸馏水作为吸收液的250mL锥形瓶中。
2、样品的标定加热蒸馏至烧瓶刻度的20mL左右,停止加热使其冷却。
再加入50mL蒸馏水继续蒸馏至烧瓶刻度的25mL 左右。
取下锥形瓶,在电炉上加热至沸,趁热加10滴酚酞指示剂,用0.1mol/L 的NaOH 滴定,记录用量。
挥发性脂肪酸测定实验记录如表3-3所示。
表3-3 挥发性脂肪酸测定实验记录表 序号 氢氧化钠溶液浓度/(1-∙L mol ) 滴定消耗氢氧化钠体积/mL水样体积/mL 挥发性脂肪酸含量/(1-∙L mg ) 1233、数据处理挥发性脂肪酸含量L (mg/L)=100021⨯V cV (3-7) 式中 c ——氢氧化钠溶液浓度,mol/L ;V 1——滴定消耗氢氧化钠体积,mLV 2——水样体积,mL 。
五、讨论(1)在污泥的两相厌氧消化中,如何有效控制挥发性脂肪酸?(2)自行了解气相色谱法测定VFA 的方法,有条件可以进行操作。
挥发性脂肪酸和乳酸的测定方法研究_林秋萍

0.4
丁酸
0.269
0.283
0.277
0.272
0.290
0.261
0.275
1.1
3 小结 本实验采用低温的水做溶剂, 目的是尽量避免
样 品 提 取 过 程 中 VFA 的 挥 发 , 水 做 溶 剂 使 样 品 提 取 比 较 完 全 。程 序 升 温 测 定 , 各 组 分 分 离 效 果 较 好 , 分 析 时 间 短 , 精 密 度 、精 确 度 较 高 , 适 用 大 批 量 样 品 的测定。
色谱 柱 : 2m×3mm 内 装 5%聚 二 乙 二 醇 丁 二 酸 酯
林秋萍, 河南省农业科学院科学实验中心, 副研究员, 450002, 河南省郑州市农业路 1 号。
李瑾、冯书惠、王会锋、王铁良, 单位及通讯地址同第一作者。 收稿日期: 2006- 05- 08
( DEGS) +1%磷酸的不锈钢柱。 仪器条件: 柱温 110℃ 2℃/min 120℃, 进样器、检测
1 对号入座。要正确按不同畜禽种类和不同生长、发育阶段选用不同比例的预混料品种 , 能量饲料添加要准确, 搅拌 要均匀。
2 更换预混料要循序渐进。突然更换预混料畜禽不适应, 影响采食和生长。使用中应逐渐增加新料用量, 减少旧料用 量, 大约一周时间过渡到完全使用新预混料。
3 要按推荐配方配合饲料。有很多养殖户使用预混料常常凭自己的经验, 随便改变推荐配方, 造成各项营养指标不能 满足畜禽各期的生长需要。
挥发性脂肪酸测定

四、挥发性脂肪酸的比色测定法:测定原理:含挥发性脂肪酸的样液,在加热的条件下,与酸性乙二醇作用生成酯,此酯与羧胺反应,形成氧肟酸。
在高铁试剂存在下,氧肟酸转化为高铁氧肟酸的棕红色络合物,其颜色的深浅在一个较大的范围内与反应初始物——挥发性脂肪酸的含量成正比,故可用比色法测定。
⑴试剂①1:1硫酸:浓硫酸(相对密度1.84,C.P.)加到同体积蒸馏水中稀释配制。
②4.5mol/L的氢氧化钠:称取180g氢氧化钠(C.P.)溶于水中,冷后以蒸馏水稀释至1L。
③10%硫酸羟胺溶液:称取硫酸羟胺(C.P.)10.0g,溶于100mL蒸馏水中。
④酸性氯化铁试剂:将20.0g分析纯FeCl3·6H2O溶于500mL水中,准确加入20.0mL浓硫酸,并以蒸馏水稀释至1L。
(配置好后应该静置过夜,除去沉淀)⑤乙二醇:分析纯⑵测定步骤①乙酸标准液的配制。
精确称取乙酸(分析纯,相对密度1.045,含量99.0%)1.010g,以蒸馏水稀释至100mL,此溶液含乙酸10mg/mL。
②乙酸标准曲线绘制:准确吸取10 mg/mL乙酸标准溶液1mL、5mL、10mL、15mL、20mL、25mL、30mL,分别置于100ml容量瓶内,以蒸馏水定容至刻度,摇匀,即得100、500、1000、1500、2000、2500、3000mg/L的乙酸标准系列液。
吸取0.5mL乙酸标准液置于比色管中,同时吸取0.5ml蒸馏水作空白管,每管中准确加入1.5ml乙二醇和0.2ml稀硫酸,充分混合,于沸水浴中加热3min,应避免试管与加热器壁直接接触。
然后立即将试管置于冷水中冷却。
加入0.5mL硫酸羟胺和2ml 4.5mol/L的氢氧化钠,并混匀,放置1min。
然后各个管中加入10mL 酸性氯化铁试剂,用蒸馏水定容到25mL,并充分摇匀,静置5min,用分光光度计以500nm波长测定光密度,以纵坐标表示浓度值,横坐标表示光密度值绘制标准曲线。
挥发酸的测定方法-磷酸法

挥发性脂肪酸(VFA)的测定挥发性脂肪酸是厌氧硝化过程的中间产物,甲烷菌主要利用VFA 形成甲烷, 只有少部分甲烷由CO 2和H 2生成。
VFA 在厌氧反应器中的积累能反映出甲烷菌 的不活跃状态或反应器操作条件的恶化,较高的VFA 浓度对甲烷菌有抑制作用。
VFA 包括甲酸、乙酸、丙酸、丁酸、戊酸、己酸及它们的异构体,在运转 良好的反应器中,乙酸比例较高,反应器不好时,甲酸、丙酸浓度升高。
在VFA 测定中,其单位常换算为按乙酸计,以 mg/L 表示。
常用的测定方法有:滴定法和气相色谱分析法滴定法测VFA :1、 原理将废水酸化后,从中蒸馏出挥发性脂肪酸,再以酚酞为指示剂用氢氧化钠滴 定馏出液。
废水中的氨态氮先在碱性条件下蒸馏出。
2、 仪器:50ml 碱式滴定管、锥形瓶、带磨口的具支蒸馏烧瓶(500ml )、 与烧瓶配套的蛇形冷凝管、橡胶导管、电炉试剂:(1) 10%氢氧化钠:10g 氢氧化钠溶于水,稀至100ml 。
(2) 10%磷酸溶液:取70ml 浓磷酸稀释至1L 。
(3) 酚酞指示剂:称取0.5g 酚酞溶于50ml 95%的乙醇中,用水稀释至100ml 。
(4) 氢氧化钠标准溶液(0.1000mol/L):称取60g 氢氧化钠溶于50ml 水中,转 入聚乙烯瓶中静置24h ,吸取上层清夜约7.5ml 置于1000ml 容量瓶中,稀释至标 线。
标定:称取在105-110C 干燥过的基准试剂(邻)苯二甲酸氢钾约0.5g (称准 至0.0001g),置于250ml 锥形瓶中,加无二氧化碳水100ml 使之溶解,加入4滴 酚酞指示剂,用待标定的氢氧化钠标液滴定至浅红色为终点, 同时,用无二氧化 碳水做空白滴定。
m-苯二甲酸氢钾的质量(g);计算:氢氧化钠标液浓度(mol / L)= m 1000 y - V o 204.23V o —滴定空白时消耗氢氧化钠标液的量(ml)V,—滴定苯二甲酸氢钾时消耗氢氧化钠的量(ml);204.23—苯二甲酸氢钾的摩尔质量(g/L)3、实验步骤(1) 于蒸馏烧瓶中加入100ml待测水样,几粒玻璃珠,加入几滴酚酞指示剂,然后加入10%氢氧化钠溶液使使水样呈碱性(溶液出现红色),并使氢氧化钠略过量。
挥发性脂肪酸VFA测定步骤与方法

挥发性脂肪酸的测定一、GC ( Gas chromatograph )工作条件仪器:GC-14B型气相色谱仪(日本岛津公司)毛细柱:NUKOLTM Capillary Column ( Supelco ) ;ColumnNO.34292-07B30m X 0.32mm X 0.25 阿film thickness气相色谱仪参数:色谱柱采用毛细吸管柱,柱温130 C,汽化温度180 C,采用氢离子火焰检测器,检测温度180 C,载气为氮气,压力为60 KPa,氢气压力为50 KPa,氧气压力50 KPa,灵敏度(档) 为101,衰减3.0二、样品制备1 .试剂制备(1)配制25%w/v 的偏磷酸溶液,将25g偏磷酸溶在100mL双蒸水中(2)巴豆酸的配制,在100ml的偏磷酸溶液中加入0.6464g的巴豆酸,定容到100mL。
(可先用80 ml双蒸水,加热溶解偏磷酸,然后定容至100 ml )(3 )标准样品,准确称取色谱标准级乙酸0.9100 g、丙酸0.3700 g、丁酸0.1765g、异丁酸0.1765g、戊酸和异戊酸分别为0.1985g,分别溶于双蒸水中,再各自定容至100 mL。
2. 样品制备(1)发酵液取(或过滤瘤胃液)VFA测定1ml样品到离心管中,再加入0.2 ml的偏磷酸巴豆酸混合溶液,-20 C冰箱保存过夜,解冻后12000rpm 离心5min,取上清液保存,测定前再12000rpm 离心5mi n(或少许通过0.22 ^m针式滤器,滤液直接进样用1.0微升微量进样器瞬时注入色谱仪,进样量为0.2 — 1.0 ^L。
⑵食糜及粪样VFA测定取1g置于离心管中,加入5 —10倍的双蒸水,混合均匀。
取1mL上清夜,加偏磷酸巴豆酸0.2mL/mL 。
其它步骤同上。
3. 保留时间的确定与样品处理相同,在1 ml标准样品中加入0.2mL偏磷酸与巴豆酸的混合样,上样测出乙酸、丙酸、丁酸、异丁酸、戊酸和异戊酸的保留时间。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
5 VFA的滴定法分析
(1)原理
本法原理是将废水以磷酸酸化后,从中蒸发出挥发性脂肪酸,再以酚酞为指示剂用NaOH溶液滴定馏出液。
废水中的氨态氮可能对测定形成干扰,因此应当首先在碱性条件下蒸发出氨态氮,如果要同时测定氨态氮,以硼酸溶液吸收后滴定之。
因此此法可用于氨态氮和VFA的联合测定。
(2)药品
①10%NaOH溶液
②NaOH标准溶液,0.1000mol/l
③10%磷酸溶液,取70ml密度1.7mg/cm3的磷酸用水稀释至1L。
④酚酞指示剂,1%的乙酸溶液。
(3)测定步骤
于蒸馏瓶中放入50—200ml待测废水,其VFA含量不超过30mmol。
如水样体积不足100ml,可以蒸馏水稀释至100ml。
放入几滴酚酞指示剂。
加入10%NaOH溶液,使溶解呈碱性,并使NaOH略过量。
开始蒸馏,至蒸馏瓶中剩余的液体为50—60ml为止。
用蒸馏水将蒸馏瓶剩余液体稀释至原来的体积,用10ml10%的磷酸酸化,在接受瓶中放入10ml蒸馏水并使接受瓶与蒸馏瓶上的冷凝管连接,导入管应浸入接受瓶的液面以下。
蒸馏至瓶中液体为15—20ml为止。
待蒸馏瓶冷却后,加入50ml蒸馏水再次蒸馏,至剩余10—20ml液体为止。
为了除去二氧化碳、硫化氢、二氧化硫等干扰物,可向馏出液中通入高纯氮气10—15min,然后加入10滴酚酞,用NaOH标准溶液滴定至淡粉色不消失为止。
(4)计算
挥发性脂肪酸含量计算如下:
VFA=V (NaOH)*C*1000/Vs (mmol/L)
式中:V(NaOH)-----滴定消耗的NaOH标准溶液的体积,ml;
c ------ 滴定消耗的NaOH标准溶液的准确浓度,mol/L;
挥发性脂肪酸(VFA)的测定
挥发性脂肪酸是厌氧硝化过程的中间产物,甲烷菌主要利用VFA形成甲
烷,只有少部分甲烷由CO
2和H
2
生成。
VFA在厌氧反应器中的积累能反映出甲
烷菌的不活跃状态或反应器操作条件的恶化,较高的VFA浓度对甲烷菌有抑制作用。
VFA包括甲酸、乙酸、丙酸、丁酸、戊酸、己酸及它们的异构体,在运转良好的反应器中,乙酸比例较高,反应器不好时,甲酸、丙酸浓度升高。
在VFA测定中,其单位常换算为按乙酸计,以mg/L表示。
常用的测定方法有:滴定法和气相色谱分析法
一、滴定法测VFA:
1、原理
将废水酸化后,从中蒸馏出挥发性脂肪酸,再以酚酞为指示剂用氢氧化钠滴定馏出液。
废水中的氨态氮先在碱性条件下蒸馏出。
2、仪器:50ml碱式滴定管、锥形瓶、带磨口的具支蒸馏烧瓶(500ml)、与烧瓶配套的蛇形冷凝管、橡胶导管、电炉
试剂:
(1)10%氢氧化钠:10g氢氧化钠溶于水,稀至100ml。
(2)10%磷酸溶液:取70ml浓磷酸稀释至1L。
(3)酚酞指示剂:称取0.5g酚酞溶于50ml 95%的乙醇中,用水稀释至
100ml。
(4)氢氧化钠标准溶液(0.1000mol/L):称取60g氢氧化钠溶于50ml水中,转入聚乙烯瓶中静置24h,吸取上层清夜约7.5ml置于1000ml容量瓶中,稀释至标线。
称取在105-110℃干燥过的基准试剂(邻)苯二甲酸氢钾约0.5g(称准至0.0001g),置于250ml锥形瓶中,加无二氧化碳水100ml使之溶解,加入4
滴酚酞指示剂,用待标定的氢氧化钠标液滴定至浅红色为终点,同时,用无二氧化碳水做空白滴定。
氢氧化钠标准溶液浓度(mol/L)=M×1000/[(V1-V0) ×204.23]
式中:
m—称取苯二甲酸氢钾的质量(g);
V0—滴定空白时所耗氧氧化钠标准溶液体积(ml);
V1—滴定苯二甲酸氢钾时所耗氢氧化钠标准溶液的体积(ml);
204.23—苯二甲酸氢钾的摩尔质量(g/mol)。
3、测定步骤:
(1)于蒸馏烧瓶中加入100ml待测水样,几粒玻璃珠,加入几滴酚酞指示剂,然后加入10%氢氧化钠溶液使使水样呈碱性(溶液出现红色),并使氢氧化钠略过量。
(2)打开冷凝水,开始蒸馏,蒸馏至瓶中液体为50~60ml,(如果测定氨氮,则可用50ml硼酸吸收馏出液。
如果不,可倒掉。
)
(3)加入约40~50ml蒸馏水,加入10ml10%磷酸酸化,在接受瓶中加入10ml蒸馏水,将冷凝管插入液面下,蒸馏至瓶中液体为15~20ml。
待冷却后,加入50ml蒸馏水继续蒸馏,至瓶中剩余液体10~20ml止。
(4)向馏出液中加入10滴酚酞指示剂,用氢氧化钠标液滴定至氮淡粉红色不消失止,记录用量。
计算:挥发酸(VFA)(mg/l)= (V3-V4)×N×60×103/V5
式中:
V3—滴定样品时所消耗的NaOH毫升数;
V4—滴定空白时所耗的NaOH毫升数;
V5—取样量(ml);
N—NaOH溶液的浓度(mol/L);
60—乙酸的分子量。
注意事项:
(1)蒸馏前打开冷凝水;
(2)冷却时,把接受瓶移开,以免倒吸;
及分析日期等。
