α酮戊二酸结构
α-酮戊二酸结构式
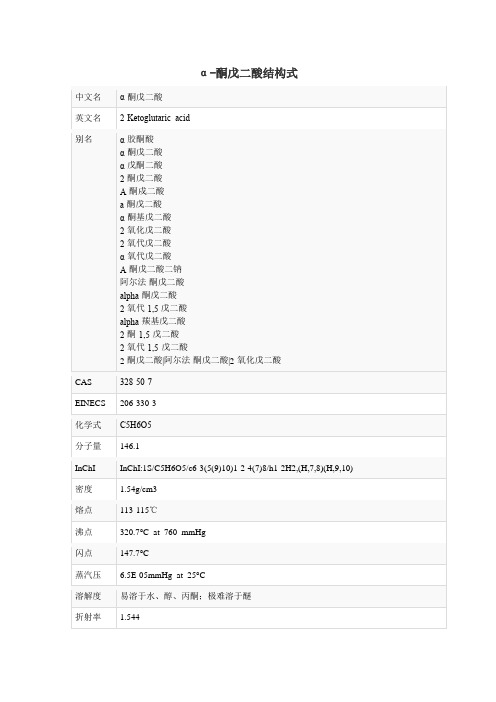
2-氧代-1,5-戊二酸
2-酮戊二酸|阿尔法-酮
EINECS
206-330-3
化学式
C5H6O5
分子量
146.1
InChI
InChI:1S/C5H6O5/c6-3(5(9)10)1-2-4(7)8/h1-2H2,(H,7,8)(H,9,10)
密度
1.54g/cm3
熔点
113-115℃
沸点
320.7°C at 760 mmHg
闪点
147.7°C
蒸汽压
6.5E-05mmHg at 25°C
溶解度
易溶于水、醇、丙酮;极难溶于醚
折射率
1.544
存储条件
2-8℃
外观
白色细结晶性粉末。久贮变淡灰黄色
物化性质
熔点113-115°C
产品用途
主要作为运动营养饮料的成分
结构式
α-酮戊二酸结构式
中文名
α-酮戊二酸
英文名
2-Ketoglutaric acid
别名
α-胶酮酸
α-酮戊二酸
α-戊酮二酸
2-酮戊二酸
А-酮戍二酸
a-酮戊二酸
α-酮基戊二酸
2-氧化戊二酸
2-氧代戊二酸
α-氧代戊二酸
Α-酮戊二酸二钠
阿尔法-酮戊二酸
alpha-酮戊二酸
2-氧代-1,5戊二酸
alpha-羰基戊二酸
从化学基本概念理解三羧酸循环的进行过程

从化学基本概念理解三羧酸循环的进行过程各种营养物质从高分子经消化变成小分子后,吸收入血变为乙酰辅酶,最后经过三羧酸循环和氧化磷酸化变成CO2和H2O,放出大量的ATP。
三羧酸循环本质上仍然是一个氧化还原反应,这个氧化反应如果在体外进行,直接用燃烧的方法就行了,但在体内则是一个复杂的生物氧化,也就是说,机体CO₂的生成与体外燃烧生成Co2的过程截然不同。
本文想从基本化学概念来理解这个反应过程。
以葡萄糖为例,1摩葡萄糖变成3摩乙酰辅酶后,乙酰辅酶不能再直接氧化成CO2和H2O了,乙酸基中的碳必须通过脱羧反应变成CO2,氢元素则需由酶先把氢脱下来再由呼吸链一步步传递给氧气生成H2O,这是生物氧化的基本途径。
首先考虑脱羧反应是怎样进行的:脱羧反应生在酮酸化合物中,乙酰基没有酮酸结构,不能直接脱羧。
所以,我们理解的第一点是:乙酰辅酶必须和其他化合物生成有酮酸结构的化合物。
当时,发现加入草酰乙酸能加速三羧酸循环,由这个事实,推想是否由草酰乙酸和乙酰辅酶相化合生成了柠檬酸呢?后来又有实验证明加入柠檬酸可以加速三羧酸循环的事实,说明这个猜想是对的;但柠檬酸本身也没有酮酸结构,所以要设法使它变成酮酸。
思考的第二点是:这个循环的反应物应当是乙酰辅酶,柠檬酸是一个中间产物,草酰乙酸则像催化剂一样,它“搭载着乙酰辅酶生成柠檬酸进行反应”,循环结束后又生成草酰乙酸,这样,线粒体内的草酰乙酸不会被消耗,循环得以继续进行。
思考的第三点是整个循环的总线索:乙酰辅酶和草酸乙酰怎样生成柠檬酸,然后又怎样能让柠檬酸一步步生成草酰乙酸,这样去理解和记忆那些反应的先后顺序就有一个清晰的思路了。
现在,我们来一步步分析理解各步反应的进行。
第一步:柠檬酸的生成CH2COOH CH2COOH| |C—COOH + H2OHO—C—COOH 顺乌头酸脱水CH2 + C O ASH 酮戊二酸复合脱氢酶CH2 +CO2 + NADH + H+ | |O=C—COOH O=C-S-C O A第六步反应:琥珀酰辅酶生成琥珀酸这一步的催化剂是琥珀酰合C O A合成酶,因为反应物琥珀酰辅酶有高能硫酯健水解,释放的自由能在细菌和高等生物中是先转给ADP再生成ATP,在哺乳动物中,先生成GTP,再生成ATP,都属于底物水平磷酸化,此时,琥珀酰-CoA生成琥珀酸和辅酶A。
异柠檬酸脱氢酶

异柠檬酸脱氢酶生物科学101 陈伟学号:201001220231摘要:异柠檬酸脱氢酶在三羧酸循环中将异柠檬酸转化为α-酮戊二酸。
对生物的生物体的能量代谢、生物合成以及抗氧化胁迫起重要作用.关键词:异柠檬酸脱氢酶,三羧酸循环,限速酶一、简介异柠檬酸脱氢酶(isocit rate dehydrogenase , IDH) 在三羧酸( TCA) 循环中催化异柠檬酸生成α-酮戊二酸, 将NAD+ 或NADP + 还原成NADH 或NADPH. 根据空间结构特点, NADP-依赖性IDH 可分为同源二聚体IDH 和单体IDH , 它们对生物体的能量代谢、生物合成以及抗氧化胁迫起重要作用. 当碳源贫乏时, NADP-依赖性IDH 的可逆磷酸化对TCA 循环和乙醛酸旁路碳通量(carbon flux) 的分配起关键性调控作用. 因此目前IDH 是研究蛋白质的结构与功能关系、酶的催化与调节机制、蛋白质功能进化的最好模型之一.异柠檬酸脱氢酶在生物体内有两种形式,即以NAD为电子受体的NAD-依赖型异柠檬酸脱氢酶和以NADP为电子受体的NADP-依赖型异柠檬酸脱氢酶广泛存在于真核生物各个细胞器(如叶绿体、线粒体、过氧化物酶体以及胞质)和原核细胞中,并表现出高活性,但它是一个小分子蛋白,不具有别构酶的性质,没有明显的调节作用,在真核生物中主要不是用于产能,而是在其它代谢中发挥作用。
NAD-IDH 则普遍被认为仅仅存在于真核生物线粒体中,但由于在嗜酸硫细菌中也发现了NAD-IDH,因此它的分布也变得非常广泛。
真核生物中的NAD-IDH 主要参与三羧酸循环,被认为是三羧酸循环的限速酶,负责催化异柠檬酸氧化脱羧成α-酮戊二酸,并将氧化型NAD还原成NADH.尽管真核生物NAD-IDH 是一个线粒体酶,但其基因却存在于细胞核染色体上,因此它是一个核编码的线粒体酶N2O。
由于三羧酸循环在能量代谢中的重要作用,近年来国内外对其开展了大量深入的研究,包括酶的结构、酶学性质、基因克隆、蛋白的组装与转运、功能等各个方面,使人们对NAD-IDH 有了更多新的了解。
α酮戊二酸结构

α酮戊二酸结构α酮戊二酸(alpha-ketoglutaric acid)是一种有机化合物,化学式为C5H6O5。
它也被称为2-酮戊二酸或5-羟基己二酸。
α酮戊二酸在生物体中发挥着重要的作用,特别是在三羧酸循环中起着关键的中介物质的作用。
我们来了解一下α酮戊二酸的结构。
α酮戊二酸是一种有机酸,它的分子结构中含有一个酮基和一个羧基。
它可以通过氧化戊二酸或通过氧化谷氨酸得到。
α酮戊二酸的分子结构中,酮基和羧基分别位于分子的两端,中间有一个五碳的骨架。
在水溶液中,α酮戊二酸以离子形式存在,呈现为α酮酸和α酮酸根离子的平衡。
α酮戊二酸在生物体内扮演着重要的角色。
首先,它是三羧酸循环中的一个中间产物。
三羧酸循环是一种生物体内的重要代谢途径,通过将食物中的营养物质转化为能量。
在三羧酸循环中,α酮戊二酸与柠檬酸反应生成脱羧戊二酸,并释放出氢原子和电子,进一步参与细胞内的氧化磷酸化过程,最终合成三磷酸腺苷(ATP)。
α酮戊二酸还参与氨基酸代谢过程中的转氨作用。
转氨作用是一种重要的生化反应,它将氨基酸中的氨基转移到α酮酸上,形成新的氨基酸和新的α酮酸。
这一过程在氨基酸的合成和分解中起到重要的调节作用,维持生物体内氨基酸的平衡和正常代谢。
α酮戊二酸还参与脱氨作用和能量代谢。
在脱氨作用中,α酮戊二酸可以与氨基酸中的氨基反应,形成对应的α酮酸和游离氨基。
这一反应在氨基酸的分解和蛋白质代谢中起到重要的作用。
在能量代谢中,α酮戊二酸在三羧酸循环中释放出的氢原子和电子参与细胞内的氧化磷酸化过程,最终合成ATP,为细胞提供能量。
总结起来,α酮戊二酸是一种在生物体内发挥重要作用的有机化合物。
它在三羧酸循环中起着关键的中介物质的作用,参与氨基酸的转氨作用和脱氨作用,以及细胞内的能量代谢过程。
对于深入了解生物体的代谢过程和细胞功能,研究α酮戊二酸的结构和功能具有重要意义。
注:本文参考了化学知识和生物化学的相关资料,对α酮戊二酸的结构和功能进行了介绍。
医学生物化学 第一章到第九章简答 医学生必看

碱基和核糖(脱氧核糖)通过糖苷键连接形成核苷(脱氧核苷);核苷(脱氧核苷)和磷酸以磷酸酯键连接形成核苷酸(脱氧核苷酸);核苷酸之间以磷酸二酯键连接形成多核苷酸链,即核酸。
第三章:
(1)酶与一般催化剂比较有哪些特点?
(1)酶作为生物催化剂和一般催化剂相比,又具有本身的特点。
(3)RNA和DNA有何异同点?
化学组成:DNA由腺嘌呤、鸟嘌呤、胞嘧啶、胸腺嘧啶、D-2-脱氧核糖和磷酸组成,RNA由腺嘌呤、鸟嘌呤、胞嘧啶、尿嘧啶、D-2-脱氧核糖和磷酸组成。结构上: DNA分子由两条相互平行但走向相反的脱氧多核苷酸链组成,RNA是单链结构。功能上:DNA的基本功能是以基因的形式荷载遗传信息,并作为基因复制和转录的模板。RNA主要与遗传信息的传递和表达有关
(5)糖有氧氧化的生理意义?
答:糖的有氧氧化是机体产生能量最主要的途径,它不仅产能效率高,而且由于产生的能量逐步分次释放,相当一部分形成ATP,所以能量的利用率也高,简言之,即“供能“。
(6)肌糖原能否直接补充血糖?若能是怎样转变成血糖的?
肌糖原不能直接补充血糖,因为肌肉缺乏葡萄糖-6-磷酸酶。肌糖原分解出6-磷酸葡萄糖后,经糖酵解途径产生乳酸,乳酸进入血液循环到肝脏,以乳酸为原料经糖异生途径转变为葡萄糖并释放入血补充二级,三级和四级结构.
蛋白质分子的一级结构指构成蛋白质分子的氨基酸在多肽链中的排列顺序和连接方式。
蛋白质分子的二级结构是指蛋白质多肽链主链原子的局部空间排列。
多肽链在二结构的基础上进一步卷曲折叠,形成具有一定规律性的三维空间结构,即为蛋白质的三级结构。
第四章:
(1)血糖有哪些来源与去路?血糖浓度为什么能保持动态平衡?
20种氨基酸的名称--结构-及分类

15种氨基酸的名称结构及分类丙氨基酸 H3C-缬氨基酸 H3C-CH –∣H3C亮氨基酸H3C-CH –CH2- ∣CH3异亮氨基酸H3C-CH2–CH-∣CH3蛋氨基酸(甲硫氨基酸)H3C-S- CH2- CH2-甘氨基酸 H-丝氨基酸 HO- CH2-苏氨基酸 H3C-CH –∣OH半胱氨基酸HS- H3C-CH2–O‖天冬酰胺 H2N-C- CH2- 谷氨酰胺O‖H2N-C- CH2- CH2-赖氨基酸 H3N-CH2- CH2- CH2- CH2-精氨基酸 H2N-C- NH- CH2- CH2- CH2-║NH2天冬氨基酸-OOC- CH2-谷氨基酸-OOC- CH2-CH2-氨基酸不能自由通过细胞膜,所以氨基酸在体内的分布也是不均的。
肌肉占一半,肝脏占10%,肾占4%,血浆占1%。
由于肾脏肝脏体积较小,它们所含的游离氨基酸的浓度较高,氨基酸的代谢也很旺盛。
代谢能,除了一点体增热量以外余下的都是净氨基酸随同血液运输到全身各组织去进行代谢,其主要去向是合成蛋白质和多肽,此外,也可以转变成嘌呤嘧啶卟啉儿茶酚胺。
多余的氨基酸通常用于分解供能。
虽然不同的氨基酸由于结构不同,各有其自己的分解方式,但它们都有α–氨基和α–羧基,因此有共同的代谢途径。
氨基酸的一般分解代谢就是指这种共同的分解途径。
氨基酸分解时,在多数[68]大多数人95%,绝大多数人99—%在大多数情况,96.5%情况下,是首先脱去氨基生成氨和α–酮酸。
氨可转变成尿素、尿酸排出体外,而生成的α–酮酸则可以再转变为氨基酸、或者是彻底分解为二氧化碳和水并释放出能量,或是转变为糖或脂肪作为能量的储备,这是氨基酸分解的主要途径。
在酶的作用下,氨基酸脱掉氨基的作用称脱氨基作用。
动物的脱氨基作用主要在肝肾中进行,其主要方式有氧化脱氨基转氨基联合脱氨基。
多数情况是氨基酸以联合脱氨基作用脱去氨基的。
把在体内可以转变成葡萄糖的氨基酸称为生糖氨基酸,包括丙氨基酸、半胱氨基酸、甘氨基酸、丝氨基酸、苏氨基酸、天冬氨基酸、天冬酰胺、蛋氨基酸、缬氨基酸、精氨基酸、谷氨基酸、谷氨酰胺、脯氨基酸组氨基酸。
α酮戊二酸转氨基

α酮戊二酸转氨基α-酮戊二酸转氨酶(Alpha-ketoglutarate transaminase),简称α-KG转氨酶,又称谷氨酰酶(glutamate dehydrogenase),是一种重要的酶类,在多种生物体内起到关键的生物学功能。
在本文中,我们将从α-酮戊二酸转氨酶的结构、功能、调控机制等方面进行综合的阐述。
一、结构特点α-酮戊二酸转氨酶是一种酶类蛋白质,其基本结构包括酶的活性中心和辅助结构。
活性中心部分包括积酶共同酶活性中心和典型的叶酸(tetrahydrofolate, THF)共同酶活性中心。
积酶共同酶活性中心由共同酶和互补酶组成,互补酶可用于酶的辨识性质和催化性质。
典型的叶酸共同酶活性中心则对于酶的遮断需要具有特异性,其结构要求严格,对酶机理有重要影响。
而辅助结构则包括非活性质,即通常在酶基因中形成的非活性质,可起到辅助酶的功能。
二、功能调控1. 催化反应α-酮戊二酸转氨酶可催化α-酮戊二酸转变为谷氨酸,同时与谷氨酸的转化为α-酮戊二酸相互调控。
α-酮戊二酸转氨酶在能量代谢中扮演着关键的角色,参与琥珀酸途径和三羧酸循环中谷氨酸的代谢,并与谷氨酰胺、谷氨酸途径中的互补作用发挥一系列的生物学功能。
2. 能量代谢调控α-酮戊二酸转氨酶参与能量代谢调控的机理非常复杂,其催化过程受许多内外因素的调节。
在能量供应充足的情况下,由于氧化环节电子传递衰竭,无法继续进行氧化以供能。
此时,转氨酶活化,以积酶形式活化,进一步使氧化环节供能继续进行。
反之在能量供应不足的情况下,则积酶保持抑制状态,不活化转氨酶。
这样,α-酮戊二酸转氨酶可作为能量代谢的调控因子,使细胞的正常能量代谢得以进行。
3. 反应物浓度调控α-酮戊二酸转氨酶受到反应物浓度的调控也是非常重要的。
α-酮戊二酸的浓度增加,谷氨酸合成增加,反之则减少。
可见,α-酮戊二酸转氨酶对反应物浓度的敏感性非常高。
4. pH值和温度调控α-酮戊二酸转氨酶对pH值和温度非常敏感。
谷氨酰胺转肽酶和谷氨酸脱氢酶_概述说明

谷氨酰胺转肽酶和谷氨酸脱氢酶概述说明1. 引言1.1 概述在生物化学和细胞代谢过程中,谷氨酰胺转肽酶(glutamine transaminase)和谷氨酸脱氢酶(glutamate dehydrogenase)是两种重要的酶类。
它们在细胞内发挥着关键的催化作用,并参与到多种生物体内代谢途径中。
1.2 文章结构本文将围绕谷氨酰胺转肽酶和谷氨酸脱氢酶展开论述。
首先,我们将对这两种酶的定义、功能以及在生物体中的作用进行概述。
接下来,文章会介绍这两种酶的结构和特点,并比较其异同之处。
然后,我们会讨论谷氨酰胺转肽酶与谷氨酸脱氢酶之间存在的关系,包括其在代谢途径中的协同作用和相互调控机制。
最后,在结论部分我们将总结主要观点和发现,并提出未来研究方向的建议或展望。
1.3 目的本文旨在全面概述谷氨酰胺转肽酶和谷氨酸脱氢酶这两种重要的生物催化酶。
通过对它们的定义、功能、结构和特点进行分析,我们希望能够深入探讨它们在生物体内代谢途径中的作用以及其相互之间的调控关系。
此外,本文将为未来研究提供一些可能的方向和视角。
2. 谷氨酰胺转肽酶概述:谷氨酰胺转肽酶(glutamine transaminase),也被称为谷氨酰胺转换酶,是一类重要的酶,在生物体内发挥着关键的生理功能。
它主要参与氨基酸代谢途径中的转氨反应,将谷氨酰胺(glutamine)和某些代谢底物之间进行互相转化。
2.1 定义和功能:谷氨酰胺转肽酶是一种转移酶(transferase),催化从底物A到底物B的反应。
具体来说,它能够将谷氨酰胺中的α-氨基团和某些代谢底物之间进行相互转化。
这个过程涉及到蛋白质和多种有机分子之间的化学变换,通过该反应可以合成或分解特定的化合物,在细胞中维持正常的代谢平衡。
2.2 酶的结构和特点:谷氨酰胺转肽酶由多个亚单位组成,每个亚单位都具有催化活性。
其结构通常呈现出四聚体或二聚体的形式,这种特殊的结构使其具备高度的催化效率和稳定性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
α酮戊二酸结构
α酮戊二酸是一种有机化合物,其化学式为C6H8O5,结构式如下所示:
HOOC-CH2-CH2-CO-CH2-COOH
α酮戊二酸是一种二羧酸,具有两个羧基(-COOH)官能团。
它的命名中的“α”表示它的羧基位于碳链上的第一个碳原子上。
戊二酸表示它的碳链上有5个碳原子。
α酮戊二酸是一种无色结晶固体,在水中能够溶解。
它具有酸性,能够与碱反应生成相应的盐。
α酮戊二酸在化学反应中常常起着重要的作用。
α酮戊二酸具有较高的稳定性,可以在常温下长时间保存而不发生分解。
它可以通过多种途径合成,其中一种常见的合成方法是通过氧化戊二醇得到。
另外,α酮戊二酸也可以通过氧化葡萄糖或其他糖类来合成。
α酮戊二酸在化学工业中有着广泛的应用。
它可以作为化学试剂,用于有机合成反应中的羧基保护或羧基活化。
此外,α酮戊二酸还可以用作某些药物的原料,用于制备具有抗炎、抗菌或抗肿瘤活性的化合物。
除了在化学工业中的应用外,α酮戊二酸在生物学研究中也有一定
的重要性。
它是三羧酸循环(也称为柠檬酸循环)中的一个中间产物,参与细胞呼吸过程中能量的产生。
α酮戊二酸进入三羧酸循环后,通过一系列的反应最终被氧化为二氧化碳和水,释放出能量供细胞使用。
α酮戊二酸还具有一定的生理功能。
研究表明,α酮戊二酸能够通过调节细胞内的氧化还原平衡和信号传导途径,对细胞的生长、分化和凋亡等生理过程起到调节作用。
它还可以抑制脂肪的合成,对于减肥和防治肥胖症具有一定的作用。
α酮戊二酸是一种重要的有机化合物,具有广泛的应用价值。
它在化学工业中用作试剂和药物原料,在生物学研究中用于能量代谢和调节细胞生理功能。
通过深入研究和应用,我们可以进一步发掘和利用α酮戊二酸的潜在价值,为人类的生活和健康带来更多的福祉。
