11统计热力学初步
统计热力学初步(1)
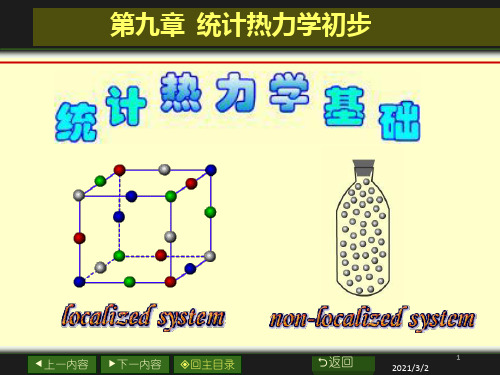
f总 3n f平 3
例:单原子分子 n 1
双原子分子 n 2
f转振 3n 3
fr 0 fv 0
fr 2 fv 1
线型多原子分子 n n fr 2 fv 3n 5
非线型多原子分子 n n fr 3 fv 3n 6
CO2 (3,2,4)、NH 3 (3,3,6) CH4(3,3,9)
t r v e n
平动 转动 振动 电子 核子 通常,原子核总是处于基态,电子在温度不高时一般也处 于基态,这两种能量在统计研究中可以不加考虑,主要考虑 分子的平动、转动和振动。
上一内容 下一内容 回主目录
返回
10
2021/3/2
9.1粒子各运动形式的能级及能级简并度
(2)分子运动自由度数 f :描述分子的空间位置和形 状所需的独立坐标的数目。
统计热力学是联系微观结构与宏观性质的桥梁
基本观点:宏观量是相应微观量的统计平均值。
上一内容 下一内容 回主目录
返回
4
2021/3/2
引言
3、几个基本概念:
粒子(子):分子、原子、离子。
系统的分类
独立子: U nii
(1) 按粒子间有无相互作用 相依子: U nii U p
独立子系统(Assembly of independent particles):粒子 之间的相互作用可以忽略。
第九章 统计热力学初步
上一内容 下一内容 回主目录
返回
1
2021/3/2
引言
1、何谓统计热力学?
研究热现象 宏观理论(经典热力学) 平衡态理论
的理论
微观理论(统计物理学) (统计热力学)
非平衡态理论
涨落理论
2、统计热力学与经典热力学的关系
统计热力学基础

9.1 粒子各种运形式的能级及能级的简并度
三维平动子的能级
在统计力学中,将在空间作三维平动的粒子称为
“三维平动子”。平动子具有的“平动能”(t)是量
b 子t化的8hm2
nx2 a2
n
2 y
b2
nz2 c2
平动量子数 nx、ny、nz的值只能取正整数(1,
2,3, ),一组(nx、ny、nz)就规定了三
在统计热力学中,把构成宏观物质体系的各种不同
子 的微观粒子,统称为:“ ”
Introduction
统计体系的分类
根据体系中的每个粒子是否可以分辨,可将统计体统 分为“定域子体系”和“离域子体系”,或者分别 “定位体系”和“非定位体系” 定域子体系 体系中每个粒子是可以分辨的,可以设
想,把体系中每个粒子分别编号而不会 混淆 例如晶体体系
h 6.6261034 J s
9.1 粒子各种运形式的能级及能级的简并度
三维平动子的能级
t
h2 8m
nx2 a2
ny2 b2
nz2 c2
微观粒子的每一个量子状态都有一个特定的能量值, 但是,不同的量子状态的能量值可能是相等的,也就 是说,一个能级可以对应的不同的量子状态,某一个 能级所对应的量子状态数,称为这个能级的简并度
9.1 粒子各种运形式的能级及能级的简并度
微观粒子的不同运动形式
平动、转动和振动是分子的整体运动的三种形式,而原 子内部电子的运动(e)和原子核运动(n)两种运动形式则 是分子内部更深层粒子的运动形式
随着人们对物质结构层次认识的深入,知识了原子内部 还有其他的运动形式,例如“夸克”和“层子”的运动 形式等,但是对于系统在宏观过程中发生的一般物理化 学变化,涉及不到这些运动形式,因此,这里,我们主 要考虑上述5种运动形式
第六章统计热力学初步

S =klntmax
=1.3810-23ln[2exp(6.021023 )]JK-1 =5.76JK-1
3.玻耳兹曼分布 在温度高于0K的通常情况下,任一微观粒子都有从 基态激发的倾向,它们在众多能级间形成许多不同方式 的分布。玻耳兹曼分布为其中的最概然分布方式: (6.3) 其中ni是分配于i能级的粒子数,i是i能级的能量 值,gi是i能级的简并度,所谓简并度就是具有相同能 量的量子状态数,N是系统中微观粒子总数,k是玻耳兹 曼常数,T是热力学温度,ei / kT 称为玻耳兹曼因子。 令 (6.4) / kT
第六章 统计热力学初步
经典热力学依据经验定律,通过逻辑推理导出了 平衡系统的宏观性质及其变化规律的,它不涉及 粒子的微观性质。 但是宏观物体的任何性质总是微观粒子运动的宏 观反映 。 统计热力学的任务就是从物质的微观结构来了解 物质宏观性质的本质 。 在物理化学中,应用统计力学方法研究平衡系统 的热力学性质,称为统计热力学。
统计热力学初步PPT课件

第九章 统计热力学初步
Statistical Thermodynamics
学习要求:
明确统计热力学的基本假设,理解最概然分布与平衡 分布及摘取最大项原理 掌握 Boltzmann 分布律及其各物理量的意义与适用条 件;理解粒子配分函数、体系配分函数的意义与表达 式,配分函数的析因子性质。 理解不同独立子体系的配分函数,q 及Θ与热力学函 数间的关系。 重点掌握平动能与平动配分函数,转动能与转动配分 函数,振动能与振动配分函数的计算。 理解系统的热容、熵及其他热力学函数与配分函数的 关系。
能 级 : 1 , 2, , i
一 种 分 配 方 式 :N 1 , N 2, , N i
W DCN N1CN N 2N1 N 1!(N N !N 1)!N 2!((N N N N 1 1 )! N 2)!
N! N!
N1!N2 !
Ni !
(能级Ⅰ、Ⅱ)
i
各能级的简并度是g1,g2, …,能级的 分布数是n1,n2,…,由于同一能级的粒 子可处于不同量子态,则
定域子系统和离域子系统
独立子系统和相依(倚)子系统
按粒子间相互作用情况不同,可分为: 独立子系统( system of independent particles)
——粒子之间除弹性碰撞之外,无其它相互作用 (理想气体)。 相依(倚)子系统( system of interacting particles)
3.一维谐振子
v(1 2)h 0,1,2,
ν——粒子的振动频率,与结构有关,数值 可由光谱数据获得。 υ——振动量子数 υ= 0,1,2,
gV , 1
一维谐振子
4.电子和原子核
电子运动及核运动的能级差一般都很大,一 般的温度变化难以产生能级的跃迁或激发,所以 本章只讨论最简单的情况,即一般认为系统中各 粒子的这两种运动处于基态。
11统计热力学

ε0 /kT
q
0
q e
0
ε0 /kT
q
q e
0
ε0 /kT
q
说明: 1、选择不同的能量零点对配分函数的值有影响
但对玻耳兹曼分布的能级分布数无影响
三、统计系统的分类 1、按粒子的运动情况不同 •离域子系统(全同粒子系统):
粒子处于混乱,无固定位置,无法彼此分辨
如气体、液体
•定域子系统(可辨粒子系统):
粒子有固定平衡位置,可加编号区分,如固体
2、按粒子间的相互作用情况不同 •独立子系统:
粒子间相互作用可忽略,如理想气体
•相依子系统:
粒子间相互作用不能忽略 如真实气体、液体等
gi e εi /kT 配分函数(总有效容量)
i
gie -i / kT 称为能级 i 的有效容量
ε j /kT
3、任意两能级i、k上 粒子数之比:
ni gi e εk /kT nk gk e
εi /kT
二、玻耳兹曼分布式的推导
定域子系统:
g WD N! i ni !
M N-M 0 10 … … 4 6 5 5 6 4 … … 10 0
WD 1 210 252 210 1 … … PD 9.8 10-4 … 0.20508 0.24609 0.20508 … 9.8 10-4 M N-M 0 20 … … 9 11 10 10 11 9 … … 20 0
WD 1 1 … 167960 184756 167960 … PD 9.5 10-7 … 0.16018 0.17620 0.16018 … 9.5 10-7
ni i
g WD N! i ni !
ni i
11热力学基础
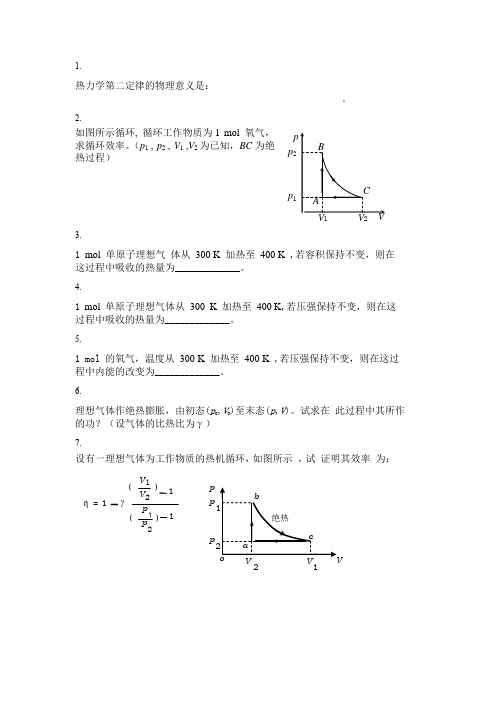
热力学第二定律的物理意义是:_____________________________________________________________。
2.如图所示循环, 循环工作物质为1 mol 氧气,求循环效率。
(p 1 , p 2 , V 1 ,V 2为已知,BC 为绝 热过程)p 221p 13.1 mol 单原子理想气 体从 300 K 加热至 400 K ,若容积保持不变,则在这过程中吸收的热量为_____________。
4.1 mol 单原子理想气体从 300 K 加热至 400 K ,若压强保持不变,则在这过程中吸收的热量为_____________。
5.1 mol 的氧气,温度从 300 K 加热至 400 K ,若压强保持不变,则在这过程中内能的改变为_____________。
6.理想气体作绝热膨胀,由初态(p 0,V 0)至末态(p ,V )。
试求在 此过程中其所作的功?(设气体的比热比为γ)7.设有一理想气体为工作物质的热机循环,如图所示 ,试 证明其效率 为:p 1 1p 2V 1V 2 ( ) 1γ η = 1 ( )p1 2pp一定量的理想气体,从a 状态(2p 1,V 1)经历如图所示的直线过程到b 状态(p 1,2V 1),则ab 过程中系统作功A =___________,内能改变 Δ E =___________。
p 1p2p 119.一 mol 双原子理想气体完成如图所示的1→2→3→4→1 循环过程.求 : (1)气体对外作的净功A ; (2)气体吸收的热量Q 1 ; (3)循环效率-3m 3)p 1=12p 2=10.一 定量的理想气体完成如图所示的1→2→3→4→1 循环过程,其中1→2和3→4是等压过程,2→3和4→1 为 绝热过程,已知2状态的温度为T 2,3状态的温度为T 3,求 : 循环效率。
11.1 mol 双原子理想气体完成如图所示的a →b →c →a 循环过程,其中a →b 为等温过程。
第十一章 热力学基础

3
m i E= RT M 2
i=3
m PV = RT M
的过程中内能的变化: 由a—b—c—d的过程中内能的变化: 的过程中内能的变化
m i i ∆E = Ed − Ea = R(Td − Ta ) = ( PdVd − PaVa ) M 2 2 3 5 −3 5 −3 = (1.013 × 10 × 3 × 10 − 3 × 1.013 ×10 × 1× 10 ) = 0 2
Mi E(T) = RT µ2
5 5 o o E = R(T2 −T ) = ×8.31×(127 c − 27 c) 1 2 2 = 2077.5(J )
如图: 如图:温度都由 T1— T2 状态发生了相同的变化。 状态发生了相同的变化。
等效 传热——作功
加热
搅拌作功
三、热量 热与功的等效性 热量:系统与外界之间由于存在温度差而传递的能量。 热量:系统与外界之间由于存在温度差而传递的能量。 (在没有作功的传热过程中它是系统内能变化的量度) 在没有作功的传热过程中它是系统内能变化的量度) Q = ∆E = E2 - E1
d (QP ) = dW = PdV
理想气体物态方程
m PV = RT M
m dV ⇒ dW = PdV = RT M V V2 m V2 dV m = QT = WT = ∫ RT RT ln V1 M V M V1
又因
PV1 = PV 1 2
P m 1 ⇒ QT = WT = RT ln M P2
内能的变化只与始末温度有关,与过程无关. 内能的变化只与始末温度有关,与过程无关.
m i i E (T ) = RT = PV M 2 2
第六章 统计热力学初步教案

3 ⎛ ∂ ln T ⎞ 3 ⎛ ∂ ln Qt ⎞ = NkT 2 i ⎜ Ut = NkT 2 ⎜ ⎟ = NkT ⎟ 2 ⎝ ∂T ⎠V , N 2 ⎝ ∂T ⎠V , N
3 ⎛ ∂U t ⎞ C V ,t = ⎜ = Nk ⎟ 2 ⎝ ∂ T ⎠V , N
S t = k ln
QtN U t 3 + = Nk ln Qt − k ln N !+ Nk 2 N! T Qt 5 = Nk ln + Nk N 2
(6.28)式称为沙克尔(Sackur)—特鲁德(Tetrode)方程。
(2) 转动配分函数
∞ ⎛ J ( J +1) Θr ⎞ T Qr = ∫ ( 2J +1) exp⎜ − ⎟ dJ = 0 T Θ r ⎝ ⎠ 2 8π IkT = 2 h
上式适用于异核双原子分子, 也适用于非对称的线型多原子分子, 但对于同核双原子分子或 对称的线型多原子分子,由于分子对称性的缘故,
第六章
统计热力学初步
§ 6.1
(1)统计热力学的研究对象和方法
引言
从分析微观粒子的运动形态入手,用统计平均的方法确立微观粒子的运动与物质宏观 性质之间的联系,这在物理学科中称为统计力学。统计力学已发展成为一门独立的学科,它 是沟通宏观学科和微观学科的桥梁。 在物理化学中, 应用统计力学方法研究平衡系统的热力 学性质,称为统计热力学。将统计热力学原理应用于结构比较简单的系统,如低压气体,原 子晶体等,其计算结果与实验测量值能很好地吻合。 (2) 统计系统的分类 按照粒子是否可以分辨(即区别),可分为定域子系统(或称定位系统,可别粒子系统)和 离域子系统(或称非定位系统、等同粒子系统)。按照粒子之间有无相互作用,又可分为独立 粒子系统和非独立粒子系统。低压气体,当作独立粒子系统处理,这正是本章所要讨论的主 要对象。 (3) 统计热力学的基本假定 统计热力学认为: “对于宏观处于一定平衡状态的系统而言,任何一个可能出现的微观 ............................. 状态都具有相同的数学概率 ” 。也就是说,在众多的可能出现的微观状态中,任何一个都没 ............ 有明显理由比其它微观状态更可能出现, 这称为等概率假定 。 等概率假定 是统计热力学的基 ..... ..... 本假定。 系统的总微观状态数就等于各种分布的微观状态数之和。即
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
分子能级能量标度零点有两种选择方法:
①2选020/取5/13能量的绝对零点为起点,而确定基态能量为某2一1
数值0,则分子配分函数:
Q
g ei / kT i
g e0 / kT 0
g1e1 / kT
g2e2 / kT
②规定基态能量0= 0——相对零点。则分子配分函数Q0:
Q0
g ei / kT i
衡物系:
两者结合可研究物系中
热力学是一种宏观的理论
大量粒子运动的宏观和
统计热力学则是一种微观的理论 微观两个方面,彼此联
系,互为补充。
经典统计法——Boltzmann统计,适用于
统计热力学有
量子统计法
粒子间无作用的体系。 Bose-Einstein统计 针对粒子间
存在相互作
Fermi-Dirac统计 用的体系
k
方法总数为:n!
mi!
i 1
2. N个可辩粒子在k个能级上某一种分布的微观状态数
将N个可辩粒子分配在k个能级上,分布如下:
能级
1 2 3 …… k
某一种分布形式 n1 n2 n3 …… nk
分布必须符合两个条件: ∑ni = N ; ∑ni i = U
此种分布的微观状态数为: t j N! ni!
g0
g1e1 / kT
g2e2 / kT
式中:i = i – 0,表示 能级相对于基态的能量值。
两种能量标度零点的关系为: Q Q0e0 / kT
∵能量标度零点的选择不同,∴求得的分子配分函数值也
不同。但这种不同对于玻尔兹曼分布定律没有影响,即:
ni
N Q
g ei / kT i
N Q0
g ei / kT i
I RD2
分子的折合质量
m1 m2
m1 m2
(3) 一维谐振子
作一维简谐运动的粒子即一维谐振子。双原子分子中
原子沿化学键方向的振动、原子晶体中各原子在点阵点附 近的202振0/5/1动3 可近似为一维简谐运动,其能级公式为: 7
振
1 h
2
式中: ——振动量子数; ——谐振子的振动频率。
4. 简并度:量子力学把某能级 i 所能拥有的量子状态数称 作该能
级的简并度,以gi表示。简并度也称退化度或统计权重。 5. 能级分布与状态分布
(1) 能级分布: N、U、V确定的平衡体系中,各能级的能 量值也确定,
分别用0、1、2……i……表示。能级分布说明了平衡体 系中N个粒子如何分布于各个能级上。
2020/5/13
8
(2) 状态分布 状态分布是说明N、U、V确定的体系中,粒子如何分
i
g ni i
ni!
4. 离域子体系某一种分布的微观状态数
将N个不可分辨的粒子分配于k个能级上,使各能级i
上的粒子数为ni ,而每个能级又有gi个简并度,其分布的
微观状态数为:
tj
2020/5/13
i
(ni gi 1)! ni!(gi 1)!
12
对于实际体系的能级分布,在T不是很低的情况下,总有
玻尔兹曼定理将系统的宏观性质(S)与微观性质()联系起
来。对于N、U、V均为一定的系统来说, 应为系统的
总微观状态数即应为各种分布的微观状态数之和: =∑tj 但是统计热力学认为,当系统中粒子数N足够大时,在各
种分布中,微观状态数最多的最可几分布就可以代表系统
的平衡分布。所以玻尔兹曼定理 式可近似改写为:
其能级公式为:
平
h2 8m
x a
2 2
y2 b2
z2 c2
式中:h=6.62610–34J·s,为Plank常数。
2020/5/13
6
(2) 刚性转子
双原子分子可近似为原子间距RD保持不变的刚性转子。
量子理论得出刚性转子的能级公式为:
转
J J
1
h
8
2 2
I
式中:J——转动量子数;I——转子的转动惯量:
i
3. 能级有简并度时某一种分布的微观状态数
将2020N/5/1个3 可辩粒子分配在各个能级i 上,而每个能级又11有
gi 个简并度,则分布如下:
能级
1, 2, 3,……,k
某一种分布
n1, n2, n3, ……, nk
各能级的简并度
g微观状态数为: t j N!
现的几率应有所不同。当体系中粒子处于任一分布D,分
布方式的微态数为WD,所以分布D出现的几率PD为:
WD P D2020/5/13
在指定N、U、V条件下微态数最大的分布— 14
—最可几分布。
统计热力学将WD称为分布D的热力学几率,就称为N、 U、V条件下体系总的热力学几率。
2. 最可几分布与平衡分布
误差越小。当N足够大时,其相对误差可以忽略不计。
§4 玻尔兹曼分布
(1) 所研究系统的特性
运用Maxwell—Boltzmann统计法研究的系统应具有下
列特性:
1. 宏2020观/5/13状态确定的密闭系统
16
2. 独立子系统 (2) 玻尔兹曼定理
U = ∑ni i S = k ln
k = 1.3810-23J·K-1
g ei /kT i
g ei /kT i
—— 表示 i 能级的有效状态数;
giei /kT——表示所有能级的有效状态数之和,简称
“状态和”——分子配分函数的物理意义。
由玻尔兹曼分布定律可证明下列关系:
ni nj
g ei / kT i
g e j / kT j
与玻尔兹曼分布定律同称为 玻尔兹曼公式
(2) 能量标度零点的选择
相依子体系,如: 真实气体。
独立子体系的内能 U N j N—体系中粒子数;
j 1
j—第j个粒子的运动能
N
相依子体系的内能U j U P ,Up—粒子相互作用
2020/5/13
j 1
的总位能。4
(2) 离域子体系与定域子体系 ①离域子体系:粒子处于混乱的运动状态,
它们没有固定的位置,各粒子无法彼此分
式中:ni —分配于i 能级的粒子数;i — i能级的能量值;
gi — i能级的简并度;N — 系统中微观粒子总数;
k — 玻尔兹曼常数;T — 热力学温度。
ei / kT — 玻尔兹曼因子
玻尔兹曼分布定律指出了微观粒子在各能级间的平衡分布
的方式,应用十分广泛。大量事实已经证明,无论是定域
子系统还是离域子系统,它们的能量分布都遵守玻尔兹曼
2020/5/13
第十一章 统计热力学初步
主讲:刘建
材料与化学工程系
1
统计热力学初步
§1 基本概念
§2 粒子体系的分布及其微观状态数
§3 最可几分布与平衡分布
§4 玻尔兹曼分布
§5 分子配分函数
§6 分子配分函数的求算及应用
§7 理想气体反应的平衡常数
2020/5/13
2
统计热力学初步
统计热力学与热力学的研究对象都是含有大量粒子的平
能量最低的能级——基态;其余能级——激发态。
当温度在0K时,系统内所有微观粒子均处于基态。而
T>0K 时,任一微观粒子都有从基态激发的倾向,这就
引起它们在众多能级间形成许多不同方式的分布。玻尔兹
2020/5/13
18
曼指出,其中最可几的分布方式为:
ni
N
gi ei / kT
玻尔兹曼分布定律
gi ei / kT
ni << gi , 于是上式简化为:t j
i
g ni i
ni!
5. 体系的总微观状态数
对一平衡的宏观体系来说,可以有多种分布。例如:
能级 某一种分布 另一种分布 第三种分布
……
1 2 ……k n1 n2 ……nk n’1 n’2……n’k n”1 n”2……n”k
……
简并度 g1, g2……gk
在体系处于平衡态情况下,最可几分布的数学几率实
际是随着粒子数增大而减小的。尽管体系在N、U、V确
定的平衡情况下,粒子的分布方式仍然千变万化,但几乎
没有超出紧靠最可几分布的一个极小的范围,或者说所出
现的分布几乎就可以用最可几分布来代表。∴N、U、V
确定的体系达平衡时,粒子的分布方式几乎将不随时间而
变化,这种分布就称为平衡分布。显然,平衡分布即最可
辩。又称等同粒子体系。如:气体; 按照体系中粒
②定域子体系:粒子的运动是定域化的, 子运动的情况
粒子可以互相区分。又称可辩粒子体系。
如:晶体。
2. 粒子的运动形式——粒子有多种运动形式,如:
分子的质心在空间的平动——分子的外部运动 粒子的动能
等于各独立
分子绕质心的轴的转动
分子的内部运动
运动形式所 具有的能量
2020/5/13
15
几分布所能代表的那些分布。
3. 斯特林公式
任一宏观体系中都含有大量的粒子,求算体系的微观状
态数时,常需要求 N!或 ni! 的值,而其中N或ni往往是很 大的数。这时我们就需要一近似公式——斯特林(Stirling)
公式:lnN!≈NlnN – N 式中N越大,运用该式的相对
分布定律。令:Q 2020/5/13
g ei /kT i
称为分子配分函数,将Q 代入玻尔兹曼分布定律19 :
ni
N Q
giei / kT
玻尔兹曼分布定律指出了微观粒子能量分布中最可几的
分布方式,那么这种最可几分布的微观状态数是多少呢?
当系统中粒子数足够多(1023)时,对于定域子系统,一种分
然202而0/5/1对3 某些热力学量的数值却会有一定的影响。 22
