工业如何制镁详细流程
工业如何制镁详细流程

海水中镁的含量是L,仅次于氯和钠,总储藏量预计有2×1015t 。
在陆地上,镁的矿物主假如菱镁矿(主要成分是 MgCO3)。
煅烧菱镁矿能够获取氧化镁,再加工成镁。
用这类方法制得的氧化镁,纯度不高,还要耗费大批的能源,并且污染环境。
假如能从海水中提取镁,不单能够获取高纯度的镁,并且能耗低、没有污染。
所以海水提镁在本世纪 40 年月创始以来,发展极快。
当前生界上生产的镁已有 60%取自海水中。
那么,镁是如何的一种金属呢?如何从海水中提取镁?从海水中提镁的化学原理和方法对我们有什么启迪呢?镁和海水提镁镁和镁的化合物镁是现有最轻的构造金属。
它在制取高强度的轻合金中有重要的地位。
比如,一种含镁 80%(还含有铝、铜、锡、锰、钛等元素)的合金,密度只有cm3,不足钢铁的1/4 ,却有钢铁的强度,是制造汽车、飞机、火箭的重要资料。
镁原子简单失掉最外层的两个电子,变为镁离子(Mg2+)。
所以,镁的复原性较强,能够用作冶炼一些金属的复原剂。
比如,四氯化钛就是用镁来复原成钛的。
镁在空气里点燃,放出大批的热,产生刺眼的白光。
利用这个性质,镁能够用来制造照明弹等。
氧化镁是白色粉末,味苦,俗称苦土。
土壤里含有少许氧化镁,所以它有苦味。
氧化镁是离子化合物,熔点高达 2800℃,在高温下仍十分稳固,所以是优秀的耐火资料。
上海宝山钢铁厂所用的耐火资料,要求氧化镁的纯度在 98%以上。
氧化镁在制造水泥、纸浆、医药、精华石油和橡胶工业中也有很多用途。
镁盐的种类好多,有的很有适用价值。
比如,运动员用来擦手的白色粉末,就是有很强吸湿能力的碳酸镁。
硫酸镁是泻盐,能够医治便秘和驱除蛔虫。
海水提镁海水是含有多种离子的混淆溶液,此中阳离子有钠离子、钾离子和镁离子等。
海水提镁,就是要把镁离子跟其余阳离子分别开来。
利用离子反响生成难溶物质,能够使某些离子从溶液中析出。
那么,能不可以向海水中加入一种离子,使镁离子变为积淀析出,而其余的阳离子仍留在海水中呢?【实验 3-1】氯化镁、氯化钠跟碱溶液的反响在两支试管里分别加入 3mL氯化镁溶液和氯化钠溶液。
金属镁的生产工艺

金属镁的生产工艺金属镁是一种重要的金属材料,在航空航天、汽车制造、电子技术等领域具有广泛的应用。
生产金属镁的主要工艺包括镁矿开采、矿石矿砂分离、提取、精炼和铸造等几个步骤。
以下为你详细介绍金属镁的生产工艺。
首先是镁矿开采。
金属镁主要来源于镁矿石,常见的镁矿石有菱镁矿、硬岩膏岩、海水镁盐等。
镁矿的开采主要通过露天开采和井下开采两种方式进行。
露天开采是将镁矿石露天暴露后进行采掘。
首先,通过爆破将矿石区域表层的岩石炸碎,然后使用巨型挖掘机将碎石矿石装入运输车辆中。
井下开采则是通过挖掘竖井或水平巷道的方式,将镁矿石从地下开采出来。
接下来是矿石矿砂分离。
这一步是将开采得到的镁矿石和杂质矿石进行分离,通常采用磁选法、浮选法和重选法等方法。
其中,磁选法适用于具有吸磁性的物质(如矿石中的铁矿物),可通过磁选机进行分离;浮选法适用于具有浸润性差的物质(如矿石中的硅酸盐),通过气泡将目标矿物上浮,达到分离的目的;而重选法适用于具有密度差异的矿石,将矿石放入重选机中,利用重力分离矿石。
之后是提取和精炼。
提取过程中,将分离出的镁矿砂加入高温的电炉中,进行煅烧。
在高温下,镁矿砂中的镁氧化物会发生还原反应,得到金属镁。
精炼过程中,将得到的金属镁经过熔炼、电解和脱氧等处理,去除杂质,提高镁的纯度。
最后是铸造。
通过精炼后的金属镁可以进行铸造,根据需要进行不同形状的铸件制造。
常见的铸造方法有砂模铸造、压力铸造和精密铸造等。
其中,砂模铸造是将金属镁熔融后倒入砂模中,待凝固后取出成型;压力铸造则是将熔融的金属镁注入压力铸造机中,通过高压快速充模,使金属镁凝固成型;而精密铸造则是通过模具和真空或气体压力控制,将金属镁精确地注入模具中,得到高精度的铸件。
综上所述,金属镁的生产工艺包括镁矿开采、矿石矿砂分离、提取、精炼和铸造等多个步骤。
这些工艺的顺序和特定的操作方法都对金属镁的生产质量和效率有重要影响,因此需要科学合理地进行控制和操作。
镁的工艺流程

镁的工艺流程
《镁的工艺流程》
镁是一种重要的金属材料,广泛应用于航空航天、汽车制造、电子产品等领域。
其生产工艺流程经过多次改进和优化,具有高效、环保、节能的特点。
首先,镁的生产需要从常见的镁原料矿石开始。
常见的原料包括轻质镁矿、菱镁矿、角闪石等。
这些矿石经过选矿、破碎、浸出等工艺步骤,将其中的镁提取出来。
在这一步骤中,需要借助化学反应和机械装备,对矿石进行处理,以获得高纯度的镁。
接下来,提取出的镁会进行熔炼和电解精炼。
镁在高温条件下熔化后,将其转移到电解槽中进行电解。
这一步骤需要借助电能进行,可以高效地将镁从杂质中分离出来。
在精炼过程中,可以对镁进行进一步的纯化和净化,以满足不同工业领域对镁产品质量的要求。
最后,经过精炼的镁会被进一步加工成各种规格和形态的产品。
例如,可以将镁合金用于汽车制造,将镁粉末用于火箭发动机制造等。
在这一步骤中,需要运用各种加工设备和工艺技术,以确保镁产品的质量和性能。
总的来说,镁的生产工艺流程包括提取原料、熔炼精炼、加工制造等多个环节,需要借助化学、物理和机械等多种技术手段。
随着工业技术的发展,镁的生产工艺将不断得到改进和优化,以满足不断增长的市场需求。
镁冶炼过程

过程
将菱镁矿与碳混合,在高 温下进行还原反应,生成 镁和一氧化碳。
优缺点
该方法成本较低,但会产 生大量的一氧化碳排放, 对环境有一定影响。
熔盐电解法
原理
利用电解熔融的氯化镁, 将镁离子还原成镁。
过程
将氯化镁熔融后进行电解 ,在阴极上得到镁和氯气 。
优缺点
该方法得到的镁纯度高, 但能耗较大,且需要处理 氯气。
镁冶炼过程
目录
• 镁冶炼概述 • 镁矿石的开采与选矿 • 镁矿石的预处理 • 镁的冶炼方法 • 镁冶炼的环境影响与治理 • 镁冶炼的发展趋势与展望
01
镁冶炼概述
镁的性质和用途
镁的性质
镁是一种轻质、有延展性的银白 色金属,具有较高的热导率和电 导率。
镁的用途
镁在航空、汽车、电子、通讯、 军事等领域广泛应用,作为结构 材料和功能性材料。
破碎
将大块原矿破碎成小块,以便 于后续的筛分和磨碎。
磨碎
将筛分后的矿石进行磨碎,使 矿石颗粒变得更细,便于浮选 和磁选。
磁选
对于某些具有磁性的矿物,通 过磁场将其与非磁性矿物分离 。
选矿设备与技术
筛分设备
振动筛、圆筒筛等 。
浮选设备
浮选机、搅拌桶等 。
破碎设备
颚式破碎机、圆锥 破碎机等。
磨碎设备
球磨机、棒磨机等 。
生物法
利用微生物或酶等生物手段将氧化镁还原成 镁。
优缺点
这些方法各有优缺点,适用范围也不同,需 要根据实际情况选择合适的冶炼方法。
05
镁冶炼的环境影响与治理
镁冶炼的环境影响
大气污染
镁冶炼过程中会产生大量的烟尘 和废气,其中包含二氧化硫、氮 氧化物、颗粒物等污染物,对大
化工生产中的镁、铝冶炼流程分析
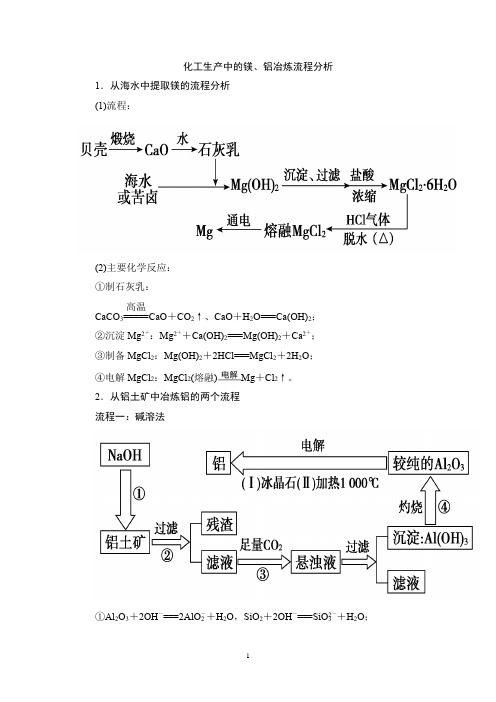
化工生产中的镁、铝冶炼流程分析1.从海水中提取镁的流程分析(1)流程:(2)主要化学反应:①制石灰乳:CaCO 3=====高温CaO +CO 2↑、CaO +H 2O===Ca(OH)2;②沉淀Mg 2+:Mg 2++Ca(OH)2===Mg(OH)2+Ca 2+;③制备MgCl 2:Mg(OH)2+2HCl===MgCl 2+2H 2O ;④电解MgCl 2:MgCl 2(熔融)Mg +Cl 2↑。
2.从铝土矿中冶炼铝的两个流程流程一:碱溶法①Al 2O 3+2OH -===2AlO -2+H 2O ,SiO 2+2OH -===SiO 2-3+H 2O ;③AlO-2+CO2+2H2O===Al(OH)3↓+HCO-3,SiO2-3+2CO2+2H2O===H2SiO3↓+2HCO-3。
(2)步骤③中不用盐酸(或H2SO4)酸化的理由是因为AlO-2与酸反应生成的Al(OH)3具有两性,可溶于强酸,不易控制酸的量;CO2廉价而且生成的副产物NaHCO3用途广泛,经济效益好。
(3)步骤④中得到较纯的Al2O3,可能含有SiO2杂质,在电解时它不会影响铝的纯度的原因:由于SiO2的熔点很高,在加热到1 000 ℃左右时不会熔化,因而不影响铝的纯度。
流程二:酸溶法讨论回答下列问题:(1)写出①、②中可能发生反应的离子方程式。
①Al2O3+6H+===2Al3++3H2O,Fe2O3+6H+===2Fe3++3H2O;②Al3++4OH-===AlO-2+2H2O,Fe3++3OH-===Fe(OH)3↓。
(2)步骤②中不用氨水沉淀Fe3+的原因:Al(OH)3只能溶于强碱,不能溶于氨水,用氨水不能将Fe(OH)3和Al(OH)3分离。
练一练1.目前世界上60%的镁是从海水中提取的。
已知海水提取镁的主要步骤如下:(1)关于加入试剂①作沉淀剂,有以下几种不同方法,请完成下列问题。
) ;(二) ;(三) ;(四) 。
镁冶炼的关键步骤

物理提取方法通常适用于从矿石中提取镁,而 化学提取方法适用于从含镁化合物中提取镁。
钙热还原法和硅热还原法是常用的化学提取方法 ,适用于从氧化物或氯化物中提取镁。
03
镁的精炼
镁的电解精炼
01
电解精炼原理
通过电解熔融的镁盐,将杂质从 镁中分离出来,得到高纯度的镁 。
对镁合金进行适当的热处理,以提高其力学性能 和稳定性。
镁合金的应用领域
汽车工业
用于制造汽车零部件,如发动机 罩、车门、座椅框架等,以减轻 重量并提高燃油经济性。
航空航天领域
用于制造飞机和航天器的零部件 ,如机身、机翼、起落架等,以 减轻重量并提高性能。
电子产品领域
用于制造手机、笔记本电脑等电 子产品的外壳、支架等部件,以 提高产品的外观和质感。
05
镁冶炼的节能与环保
节能技术
回收余热
利用高温烟气余热进行发电或供热,提高能源利 用效率。
高效燃烧技术
采用高效燃烧器、优化燃烧工艺,降低燃料消耗 。
回收副产
利用镁冶炼过程中产生的副产品,如氯化镁、氧 化镁等,进行回收再利用。
环保措施
废气处理
01
安装废气处理设施,对排放的废气进行脱硫、除尘等处理,减
电解槽设计
02
03
电解工艺参数
电解槽采用优质材料制成,具有 良好的耐腐蚀性和绝缘性,确保 电解过程稳定进行。
控制电解ห้องสมุดไป่ตู้度、电流密度和电解 时间等工艺参数,以获得高品质 的镁。
镁的化学精炼
化学精炼原理
利用化学反应将杂质从镁中分离出来,常用的化学 精炼方法有钙热还原法和真空蒸馏法。
一工业如何制镁详细流程
一工业如何制镁详细流程海水中镁的含量是1.29g/L,仅次于氯和钠,总蕴藏量估计有2×1015t。
在陆地上,镁的矿物主要是菱镁矿(主要成分是MgCO3)。
煅烧菱镁矿可以得到氧化镁,再加工成镁。
用这种方法制得的氧化镁,纯度不高,还要消耗大量的能源,并且污染环境。
如果能从海水中提取镁,不仅可以得到高纯度的镁,而且能耗低、没有污染。
所以海水提镁在本世纪40年代开创以来,发展极快。
目前世界上生产的镁已有60%取自海水中。
那么,镁是怎样的一种金属呢?怎样从海水中提取镁?从海水中提镁的化学原理和方法对我们有什么启示呢?镁和海水提镁镁和镁的化合物镁是现有最轻的结构金属。
它在制取高强度的轻合金中有重要的地位。
例如,一种含镁80%(还含有铝、铜、锡、锰、钛等元素)的合金,密度只有1.8g/cm3,不足钢铁的1/4,却有钢铁的强度,是制造汽车、飞机、火箭的重要材料。
镁原子容易失去最外层的两个电子,变成镁离子(Mg2+)。
因此,镁的还原性较强,可以用作冶炼一些金属的还原剂。
例如,四氯化钛就是用镁来还原成钛的。
镁在空气里点燃,放出大量的热,产生耀眼的白光。
利用这个性质,镁可以用来制造照明弹等。
氧化镁是白色粉末,味苦,俗称苦土。
土壤里含有少量氧化镁,因此它有苦味。
氧化镁是离子化合物,熔点高达2800℃,在高温下仍十分稳定,因此是优良的耐火材料。
上海宝山钢铁厂所用的耐火材料,要求氧化镁的纯度在98%以上。
氧化镁在制造水泥、纸浆、医药、精炼石油和橡胶工业中也有许多用途。
镁盐的种类很多,有的很有实用价值。
例如,运动员用来擦手的白色粉末,就是有很强吸湿能力的碳酸镁。
硫酸镁是泻盐,可以医治便秘和驱除蛔虫。
海水提镁海水是含有多种离子的混合溶液,其中阳离子有钠离子、钾离子和镁离子等。
海水提镁,就是要把镁离子跟其他阳离子分离开来。
利用离子反应生成难溶物质,可以使某些离子从溶液中析出。
那么,能不能向海水中加入一种离子,使镁离子变成沉淀析出,而其他的阳离子仍留在海水中呢?【实验3-1】氯化镁、氯化钠跟碱溶液的反应在两支试管里分别加入3mL氯化镁溶液和氯化钠溶液。
工业制镁的化学方程式三个
工业制镁的化学方程式三个1.引言1.1 概述工业制镁是指通过化学反应从原料中提取出纯度较高的镁金属的过程。
镁是一种轻金属,具有较低的密度和较高的强度,具有广泛的应用领域,如航空航天、汽车制造、电子设备等。
由于其特殊的化学性质和广泛的用途,工业制镁的研究和开发一直备受关注。
工业制镁的化学方程式是指在制备过程中所涉及到的化学反应式。
通过不同的方法和原料,可以得到不同的化学方程式。
这些方程式描述了原料与反应剂之间的化学变化,以及生成镁金属的过程。
在本文中,将介绍工业制镁的三个主要化学方程式。
这些方程式涉及到不同的工艺和反应条件,通过配比和控制,可以获得所需的镁金属产品。
掌握这些方程式对于理解工业制镁的过程和优化生产具有重要意义。
通过本文的概述部分,读者将对工业制镁的概念有一个初步的了解,了解到工业制镁的化学方程式是理解和研究这一领域的基础。
在后续的章节中,我们将详细介绍工业制镁的三个化学方程式,并探讨其在生产中的应用和研究意义。
同时,我们还将总结本文的主要内容,并探讨进一步研究的方向和可能性。
通过阅读本文,读者将能够更深入地了解工业制镁的化学方程式及其在实际应用中的重要性。
文章结构部分的内容应包括对整篇文章的分章节、分段落的组织和安排的说明。
在这篇长文中,按照目录所示,共有引言、正文和结论三个部分。
其中,正文部分又包括了工业制镁化学方程式一、二、三三个小节。
为了使文章具有良好的逻辑结构和阅读流畅性,可以按照以下结构来组织文章:1. 引言1.1 概述在引言部分首先对工业制镁的重要性进行简要介绍,概述工业制镁的应用范围和意义。
1.2 文章结构(本小节)描述整篇文章的结构安排,包括各个章节的标题和次序,以及每个章节的内容概览。
1.3 目的突出本文的撰写目的,即阐述工业制镁的化学方程式三个,给读者明确预期。
2. 正文2.1 工业制镁的化学方程式一在本小节中,详细介绍工业制镁的第一个化学方程式,包括具体反应物和生成物的化学式,反应过程和条件等。
工业制镁的方法
工业制镁的方法一、前言镁是一种重要的金属元素,它具有轻质、高强度、耐腐蚀等特性,因此被广泛应用于航空、汽车、电子等领域。
工业制镁是指将天然镁矿石或海水中的镁盐提取出来,并经过一系列的工艺流程加工成为纯度较高的金属镁。
本文将介绍几种常见的工业制镁方法。
二、熔盐电解法熔盐电解法是目前最常用的工业制镁方法之一。
该方法适用于海水和地下水中含有较高浓度的氯化镁和硫酸镁的情况。
具体步骤如下:1. 将氯化钠和氯化钾混合在一起,加入到反应釜中,并加热至500℃左右,使其形成液态状态。
2. 将氯化铝和氟化铝混合在一起,加入到反应釜中,并搅拌均匀。
3. 将氧化铝粉末加入到反应釜中,并搅拌均匀。
4. 在反应釜中通入氢气,使其与上述物质发生反应生成镁气。
5. 将镁气通过管道输送到另一个反应釜中,其中放置有液态铅和氯化钠,使其与铅发生反应生成金属镁。
6. 将金属镁从反应釜中取出,并经过一系列的加工流程,得到纯度较高的工业制镁。
三、热还原法热还原法也是一种常见的工业制镁方法。
该方法适用于天然镁矿石含量较高的情况。
具体步骤如下:1. 将天然镁矿石粉末加入到反应釜中,并加入适量的碳粉末。
2. 在反应釜中通入氮气,使其与上述物质形成惰性气氛。
3. 加热反应釜至高温状态,使其发生还原反应生成金属镁。
4. 将金属镁从反应釜中取出,并经过一系列的加工流程,得到纯度较高的工业制镁。
四、水解法水解法是一种比较新颖的工业制镁方法。
该方法适用于含有较高浓度硫酸盐和硝酸盐的地下水和尾水。
具体步骤如下:1. 将含有硫酸盐和硝酸盐的水样加入到反应釜中,并加入适量的氢氧化钠。
2. 加热反应釜至高温状态,使其发生水解反应生成氢氧化镁。
3. 将氢氧化镁从反应釜中取出,并经过一系列的加工流程,得到纯度较高的工业制镁。
五、结语以上三种工业制镁方法是目前比较常见的几种方法。
不同的方法适用于不同情况下的镁矿石或海水。
在实际生产中,还需要根据具体情况选择合适的工艺流程进行加工。
镁的提炼方法
镁的提炼方法一、引言镁是一种银白色的轻质金属,具有较高的热导率和电导率,广泛应用于航空航天、汽车、电子和通信等领域。
随着科技和工业的发展,对镁的需求量不断增加,因此研究和开发高效的镁提炼方法对于保障镁资源的供应和推动相关产业的发展具有重要意义。
二、镁的资源分布与开采镁资源主要分布在地壳中,以菱镁矿(MgCO3)和白云石(MgO·CaO·2SiO2)等形式存在。
开采镁矿的方法主要包括露天开采和地下开采,具体采用哪种方法取决于矿山的规模、地形和矿体分布等因素。
开采出的矿石经过破碎、磨细和浮选等加工工序,可以获得高品位的镁化合物,如菱镁矿、轻烧氧化镁等。
三、镁的提炼方法从菱镁矿中提取镁的方法主要包括以下步骤:1.矿石的破碎和磨细:将菱镁矿破碎成小块,然后磨细成粉状,以便进行下一步的化学反应。
2.酸浸:将磨细的矿石与硫酸反应,生成硫酸镁(MgSO4)和二氧化碳气体。
这一步是提取镁的关键步骤之一,因为硫酸镁在水中的溶解度较高,便于后续的分离和提纯。
3.脱水:将硫酸镁溶液在高温下加热,去除其中的水分,得到无水硫酸镁。
这一步是为了使硫酸镁结晶析出,便于分离和纯化。
4.电解:将无水硫酸镁溶解在熔融盐中,然后通电进行电解还原,得到金属镁。
这一步是提取镁的最后一步,也是最关键的一步,因为金属镁的化学性质非常活泼,易于与氧气发生反应。
从白云石中提取镁的方法与从菱镁矿中提取镁的方法类似,也是通过酸浸、脱水、电解等步骤提取金属镁。
不同之处在于白云石需要经过高温煅烧,以使其中的氧化钙和二氧化硅与氧化镁分离,便于后续的化学反应和分离提纯。
除了从矿物中提取镁的方法外,还有一些其他方法可用于制备金属镁。
例如,通过氢还原法将氧化镁或氯化镁还原成金属镁;通过硅热还原法将氧化镁或氯化镁与硅铁反应,生成硅酸镁和金属镁;以及通过电解熔融氯化镁的方法制备金属镁。
这些方法虽然在实际生产中的应用相对较少,但在某些特殊情况下仍具有一定的应用价值。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
海水中镁的含量是L,仅次于氯和钠,总蕴藏量估计有2X1015t
在陆地上,镁的矿物主要是菱镁矿(主要成分是MgC03。
煅烧菱镁矿可以得
到氧化镁,再加工成镁。
用这种方法制得的氧化镁,纯度不高,还要消耗大量的能源,并且污染环境。
如果能从海水中提取镁,不仅可以得到高纯度的镁,而且能耗低、没有污染。
所以海水提镁在本世纪40年代开创以来,发展极快。
目前世界上生产的镁已有60%取自海水中。
那么,镁是怎样的一种金属呢?怎样从海水中提取镁?从海水中提镁的化学原理和方法对我们有什么启示呢?
镁和口海水提镁
镁和镁的化合物镁是现有最轻的结构金属。
它在制取高强度的轻合金中有重要的地位。
例如,一种含镁80%(还含有铝、铜、锡、锰、钛等元素)的合金,密度只有cm3不足钢铁的1/4,却有钢铁的强度,是制造汽车、飞机、火箭的重要材料。
镁原子容易失去最外层的两个电子,变成镁离子(Mg2+。
因此,镁的还原性较强,可以用作冶炼一些金属的还原剂。
例如,四氯化钛就是用镁来还原成钛的。
镁在空气里点燃,放出大量的热,产生耀眼的白光。
利用这个性质,镁可以用来制造照明弹等。
氧化镁是白色粉末,味苦,俗称苦土。
土壤里含有少量氧化镁,因此它有苦味。
氧化镁是离子化合物,熔点高达2800r,在高温下仍十分稳定,因此是优良的耐火材料。
上海宝山钢铁厂所用的耐火材料,要求氧化镁的纯度在98%以上。
氧
化镁在制造水泥、纸浆、医药、精炼石油和橡胶工业中也有许多用途。
镁盐的种类很多,有的很有实用价值。
例如,运动员用来擦手的白色粉末,就是有很强吸湿能力的碳酸镁。
硫酸镁是泻盐,可以医治便秘和驱除蛔虫。
海水提镁海水是含有多种离子的混合溶液,其中阳离子有钠离子、钾离子和镁离子等。
海水提镁,就是要把镁离子跟其他阳离子分离开来。
利用离子反应生成
难溶物质,可以使某些离子从溶液中析出。
那么,能不能向海水中加入一种离子,使镁离子变成沉淀析出,而其他的阳离子仍留在海水中呢?
【实验3- 1】氯化镁、氯化钠跟碱溶液的反应
在两支试管里分别加入3mL氯化镁溶液和氯化钠溶液。
再分别加入1mL氢氧化钠溶液,观察发生的现象。
用澄清石灰水代替氢氧化钠溶液,重复做上述实验。
由实验知道,在氯化钠溶液中加入氢氧化钠溶液或石灰水,都不发生明显的变化。
而在氯化镁溶液中加入氢氧化钠溶液或石灰水,都生成白色沉淀,这种沉淀是氢
氧化镁。
反应的化学方程式是
MgCI2+ 2NaOH=Mg(OH)2+2NaCI
MgCI2+ Ca(OH)2=Mg(OH)2 +CaCI2
氯化钠和氯化镁都是电解质,它们的溶液中分别有钠离子和镁离子,这跟在海水中存在的形式一样。
因此,向海水中加入碱溶液,镁离子也能转变成氢氧化镁,从而跟其他阳离子分离。
海水提镁用的碱是廉价的石灰乳,它是利用海滩大量沉积的贝壳资源(主要成分是CaCO3,经煅烧成生石灰再溶于水制成的。
用海水提镁时,先把海水抽入特大的池中,倒入石灰乳,便生成氢氧化镁的悬浊液。
待沉淀沉降后取出沉淀,经洗涤后得到纯度很高的氢氧化镁。
它没有多大用途,必须使它变成有用的氧化镁和金属镁。
氢氧化镁不稳定,受热后分解成氧化镁和水。
Mg(OH)2MgO+H2O
要使+2价的镁离子得到电子而还原成单质镁,是比较困难的。
如果用类似炼铁的方法冶炼镁,需要很高的温度。
例如在2000C下用焦炭还原氧化镁,才能制得单质镁。
这样得到的镁常含有较多的杂质。
MgOb CM+ COT
因此,工业上常用电解法使镁离子在阴极得到电子,还原成单质镁。
用电解的方法冶炼镁,先要获得含有镁离子的熔融液。
在镁的化合物中,典型的离子化合物有氧化镁和氯化镁。
氧化镁的熔点太高(2800C),而氯化镁的熔点要低得多 (714C)。
所以人们选择氯化镁作为电解制取镁的原料。
用盐酸溶解氢氧化镁(或氧化镁),再使溶液浓缩,就得到氯化镁
Mg(OH)牡2HCI=MgCI2+ 2H2O
境下进行
1从海水中提取镁的流程:
L租盐水重结品•精盐
贝売邀豊臨0—石灰乳
有关反应的化学方程式:
MgCl2+ Ca(OH 2^= Mg (OH 2 J + CaCL
Mg( OH 2+ 2HCI MgC2 + 21^0
MgCl2 • 6H2O ' MgCl2 + 6H0f
MgCl2(融熔)一口Mg+ CI2T
2 •镁的化学性质(使用镁时一定要用砂纸将表面氧化膜除去)
(1)与非金属反应
Mg+ Cl2 虽逖 MgCb; 2Mg+ O兰地2MgO 3Mg+ N兰地MgNb; 2Mg+ CO 匚「2MgOF C;
(2)与酸反应:M叶2HCI^=MgCl2+ H4
(3)与水反应:M叶2HO '' Mg(OH)2 + H4(注意:镁只与热水反应,不与冷水反应)
3、镁的用途:镁铝合金用于制造火箭,飞机;镁燃烧发出耀眼白光,常用来制造信号弹及焰火;氧化镁熔。
