澄清度检查法
澄清度检查标准操作规程

德信诚培训网
更多免费资料下载请进: 好好学习社区 澄清度检查标准操作规程
1 目的与适用范围
本规程规定了本公司检品澄清度的检查方法和操作要求。
适用于本公司检品澄清度检查。
2 职责
质量保证部负责本规程的实施。
3 内容
3.1引用标准:《中华人民共和国药典》(2010年版 二部附录)
3.2 试剂与溶液
3.2.1 试剂
3.2.1.1乌洛托品(AR 级)
3.2.1.2 硫酸肼(AR 级)
3.2.2 溶液
3.2.2.1 10%乌洛托品溶液
3.3 仪器与用具
3.3.1 水浴锅
3.3.2 恒温干燥箱
3.3.3 紫外分光光度计
3.4 操作步骤
3.4.1 本法系在室温条件下,将用水稀释至一定浓度的供试品溶液与等量的浊。
3.2.112.11澄清度检查法

(2)操作方法:
④比浊:
在室温条件下,将用水稀释至一定浓度的 供试品溶液与等量的浊度标准液分别置于 配对的比浊用玻璃管中,在浊度标准液制 备5min后,在暗室内垂直同置伞棚灯下照 度为1000lx从水平方向观察比较。
(2)操作方法:
⑤结果判定:
如果供试品溶液的浑浊程度低于规定几号 的浊度标准液判为符合规定,否则判为不 符合规定。
③浊度标准液的制备 ④比浊
⑤结果判定
目视法
(2)检查方法及步骤:
①浊度标准贮备液的制备:
加水溶解
必要时可在40℃ 水沐中温热溶解
放置4-6小时
10%乌洛托品溶液
加水至刻度摇匀
硫酸肼 1.00g
10ml 10ml
25℃避光静置24小时
目视法
(2)检查方法及步骤:
②浊度标准贮原液的制备:
加水至刻度摇匀
15ml
1000池中照紫外可见 分光光度法在550纳米的波长处测 定其吸光度应在0.12-0.15范围内。
(2)检查方法及步骤:
③浊度标准液的制备:
目视法
级号
0.5
原液(ml) 2.5
1 234
5.0 10.0 30.0 50.0
水(ml)
97.5 95.0 90.0 70.0 50.0
(3)注意事项:
目视法
3
温度对制备浊度标准贮备液的浑浊程度影响明显,故规定 两液混合后的反应温度保持在25℃正负一度。温度过低反 应不能进行,温度过高也可使浑浊度降低。
4
制备浊度标准贮备液原液和标准液均应用澄清的水。用于 配制供试品溶液的水为注射用水或新沸放冷的澄清水。
浊度仪法
浊度仪法仅适用于无色供试品溶液,且溶液不能有气泡。 通过浊度仪测定的供试品溶液的浊度值和浊度标准液的 浊度值进行比较,判断供试品是否合格。
澄清度检查法

澄清度检查法1 简述本法是检査药品溶液的浑浊程度,即浊度。
药品溶液中如存在细微颗粒,当直射光通过溶液时,可引致光散射和光吸收的现象,致使溶液微显浑浊;所以澄清度可在一定程度上反映药. 247 .品的质量和生产工艺水平。
澄清度检查法(《中国药典》2 0 1 0年版二部附录IX B )是用规定级号的浊度标准溶液与供试品溶液比较,以判定药品溶液的澄清度或其浑浊程度。
2 仪器与用具2 . 1 比浊用玻璃管内径15.1 6 m m,平底,具塞,以无色、透明、中性硬质玻璃制成,要求供试品管与标准管的内径、标线刻度(距管底为4 0 m m )—致。
2 . 2 伞棚灯用可见异物检查法标准操作规范中第一法灯检法项下的检查装置,照度为1000 lx。
3 试药与试液3 . 1 浊度标准贮备液的制备称取于105°C干燥至恒重的硫酸肼l.OOg置1 0 0 m l量瓶中,加水适量使溶解,必要时可在40°C的水浴中温热溶解,并用水稀释至刻度,摇勻,放置4 .6h;取此溶液与等容量的1 0 %乌洛托品溶液混合,摇匀,于25°C避光静置24h,即得。
本液置冷处避光保存,可在两个月内使用,用前摇勻。
3 . 2 浊度标准原液的制备取浊度标准贮备液15. Ornl,置1000ml量瓶中,加水稀释至刻度,摇匀,取适量、置l c m吸收池中,照紫外-可见分光光度法(《中国药典》2 0 1 0年版二部附录W A )在5 5 0 n m的波长处测定,其吸光度应在0.1 2 ~ 0 . 1 5范围内。
本液应在4 8 h内使用,用前摇匀。
3 . 3 浊度标准液的制备取浊度标准原液与水,按下表配制,即得。
本液应临用新制,用前摇勻。
级号0. 5 .1 2 3 4浊度标准原液(ml) 2.5 5. 0 10. 0 30. 0 50.0水(ml) 97. 5 95. 0 90. 0 70. 0 50. 04 操作方法4. 1 除另有规定外,将一定浓度的供试品溶液与该品种项下规定的浊度标准液,分别置于配对的比浊用玻璃管中,液面高度为4 0 m m,在浊度标准液制备5 m i n后,于暗室内垂直同置于伞棚灯下,照度为1000 lx,从水平方向观察比较,用以检查溶液的澄清度或其浑浊程度。
2020版《中国药典》溶液澄清度与颜色检验操作规程

2020版《中国药典》溶液澄清度与颜⾊检验操作规程⼀、⽬的:制订详尽的⼯作程序,规范检验操作,保证检验数据的准确性。
⼆、范围:本标准适⽤于样品溶液澄清度与颜⾊的检查。
三、职责:1、检验员:严格按操作规程操作,认真、及时、准确地填写检验记录;2、化验室负责⼈:监督检查检验员执⾏本操作规程。
四、内容:1、溶液颜⾊检查法:1.1定义:本法系将药物溶液的颜⾊与规定的标准⽐⾊液⽐较,或在规定的波长处测定其吸光度。
品种项下规定的“⽆⾊”系指供试品的颜⾊相同于⽔或所⽤溶剂,“⼏乎⽆⾊”系指供试品溶液的颜⾊不深于相应⾊调0.5号标准⽐⾊液。
1.2仪器:纳⽒⽐⾊管(25ml),全⾃动⾊差计1.3第⼀法除另有规定外,取各品种项下规定量的供试品,加⽔溶解,置于25ml的纳⽒⽐⾊管中,加⽔稀释⾄10ml。
另取规定⾊调和⾊号的标准⽐⾊液10ml,置于另⼀25ml纳⽒⽐⾊管中,两管同置⽩⾊背景上,⾃上向下透视;或同置⽩⾊背景前,平视观察,供试品管呈现的颜⾊与对照管⽐较,不得更深。
如供试品管呈现的颜⾊与对照管的颜⾊深浅⾮常接近或⾊调不完全⼀致,使⽬视观察⽆法辨别两者的深浅时,应改⽤第三法(⾊差计法)测定,并将其测定结果作为判定依据。
1.3.1⽐⾊⽤重铬酸钾溶液:精密称取在120℃⼲燥⾄恒重的基准重铬酸钾0.4000g,置500ml量瓶中,加适量⽔溶解并稀释⾄刻度,摇匀,即得。
每lml溶液含0.800mg的K2Cr207。
1.3.2⽐⾊⽤硫酸铜溶液:取硫酸铜约32.5g,加适量的盐酸溶液(1→40)使溶解成500ml;精密量取10ml,置碘量瓶中,加⽔50ml、醋酸4ml与碘化钾2g,⽤硫代硫酸钠滴定液(0.1mol/L)滴定,⾄近终点时,加淀粉指⽰液2ml,继续滴定⾄蓝⾊消失。
每lml硫代硫酸钠滴定液(0.1mol/L)相当于24.97mg的CuS04·5H20。
根据上述测定结果,在剩余的原溶液中加适量的盐酸溶液(1→40),使每lml溶液中含62.4mg的CuS04·5H20,即得。
药品溶液澄清度检查法

药品溶液澄清度检查法一目的:制定溶液澄清度检查法,规范溶液澄清度的测定的操作。
二适用范围:适用于溶液澄清度的测定。
三责任者:品控部。
四正文1 简述澄清度是检查药品溶液的浑浊程度,即浊度。
药品溶液中如存在细微颗粒,当直射光通过溶液时,可引致光散射和光吸收的现象,致使溶液微显浑浊;所以澄清度可在一定程度上反映药品的质量和生产工艺水平。
澄清度检查法(中国兽药典2005年版一部附录83页)是用规定级号的浊度标准溶液与供试品溶液比较,以判定药品溶液的澄清度或其浑浊程度。
2 仪器与用具2.1 比浊用玻璃管内径15~16mm,平底,具塞,以无色硬质中性玻璃制成,要求供试品管与标准管的内径、标线刻度(距管底为40mm)一致。
2.2 伞棚灯用澄明度检查装置(见注射剂标准操作规程中的澄明度检查法项下),照度为1000lx。
3 试药与试液3.1 硫酸肼和乌洛托品均应符合中国兽药典规定。
3.2 浊度标准贮备液的制备称取于105℃干燥至恒重的硫酸肼1.00g,置100ml量瓶中,加水适量使溶解,必要时可在40℃的水浴中温热溶解,并用水稀释至刻度,摇匀,放置4~6小时;取此溶液与等量的10%乌洛托品溶液混合,摇匀,于25℃避光静置24小时,即得。
本液置冷处避光保存,可在两个月内使用,用前摇匀。
3.3 浊度标准原液的制备取浊度标准贮备液15.0ml,置1000ml量瓶中,加水稀释至刻度,摇匀,取适量,置1cm吸收池中,照分光光度法(《按紫外分光光度法》执行),在550nm的波长处测定,其吸收度应在0.12~0.15范围内。
本液应在48小时内使用,用前摇匀。
3.4 浊度标准液的制备取浊度标准液与原液与水,按下表配制,即得。
本液应临用时制备,使用前充分摇匀。
4 操作方法4.1 除另有规定外,将一定浓度的供试品溶液与该药品项下规定的浊度标准液,分别置于配对的比浊用玻璃管中,液面高度为40mm,在浊度标准液制备5分钟后,同置黑色背景上,在漫射光下从比色管上方向下观察,比较,或置于伞棚灯下,照度为1000lx,从水平方向观察比较,用以检查溶液的澄清度或其浑浊程度。
溶液澄清度中国药典与欧洲药典
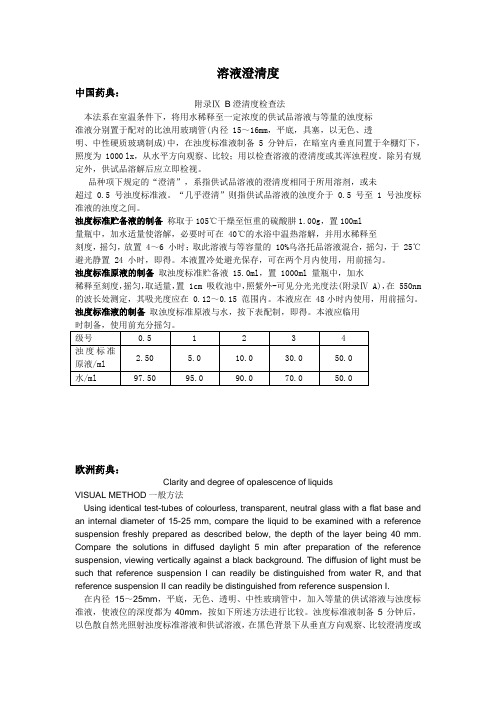
溶液澄清度中国药典:附录ⅨB澄清度检查法本法系在室温条件下,将用水稀释至一定浓度的供试品溶液与等量的浊度标准液分别置于配对的比浊用玻璃管(内径 15~16mm,平底,具塞,以无色、透明、中性硬质玻璃制成)中,在浊度标准液制备 5 分钟后,在暗室内垂直同置于伞棚灯下,照度为 1000 lx,从水平方向观察、比较;用以检查溶液的澄清度或其浑浊程度。
除另有规定外,供试品溶解后应立即检视。
品种项下规定的“澄清”,系指供试品溶液的澄清度相同于所用溶剂,或未超过 0.5 号浊度标准液。
“几乎澄清”则指供试品溶液的浊度介于 0.5 号至 1 号浊度标准液的浊度之间。
浊度标准贮备液的制备称取于105℃干燥至恒重的硫酸肼1.00g,置100ml量瓶中,加水适量使溶解,必要时可在 40℃的水浴中温热溶解,并用水稀释至刻度,摇匀,放置 4~6 小时;取此溶液与等容量的 10%乌洛托品溶液混合,摇匀,于 25℃避光静置 24 小时,即得。
本液置冷处避光保存,可在两个月内使用,用前摇匀。
浊度标准原液的制备取浊度标准贮备液 15.0ml,置 1000ml 量瓶中,加水稀释至刻度,摇匀,取适量,置 1cm 吸收池中,照紫外-可见分光光度法(附录Ⅳ A),在 550nm 的波长处测定,其吸光度应在 0.12~0.15 范围内。
本液应在 48小时内使用,用前摇匀。
浊度标准液的制备取浊度标准原液与水,按下表配制,即得。
本液应临用时制备,使用前充分摇匀。
欧洲药典:Clarity and degree of opalescence of liquidsVISUAL METHOD一般方法Using identical test-tubes of colourless, transparent, neutral glass with a flat base and an internal diameter of 15-25 mm, compare the liquid to be examined with a reference suspension freshly prepared as described below, the depth of the layer being 40 mm. Compare the solutions in diffused daylight 5 min after preparation of the reference suspension, viewing vertically against a black background. The diffusion of light must be such that reference suspension I can readily be distinguished from water R, and that reference suspension II can readily be distinguished from reference suspension I.在内径15~25mm,平底,无色、透明、中性玻璃管中,加入等量的供试溶液与浊度标准液,使液位的深度都为40mm,按如下所述方法进行比较。
《中国药典》四部通则澄清度检查法中可能存在问题的探讨
在溶液澄清度检查中,经常会遇到这样的问题:不同实 验室间或同一实验室在不同实验日间,同一批次样品与按规 定随行配制的浊度标准液相比较时,会得出截然相反的检查 结论。特别是使用仪器法时,此类问题更为明显。
本文旨在找出上述问题的根源所在,并尝试给出适宜的 解决方案。文献报道,采用标准化的操作,通过与浊度标准溶 液进行比对的方式,利用浊度仪进行准确测量,可最大程度 上避免实验偏差[10-15]。因此,本研究采用统一的作业指导书对 全部实验过程进行标准化的操作,利用实验室间比对的方 式,探讨 ChP 四部通则澄清度检查法中可能存在的问题。
托品)共计 6 个来源单位,见表 1。上述试剂均为分析纯。 1.4 方法
澄清度检查法
澄清度检查法操作规程1 目的建立澄清度检查法操作规程,使其规范化、合理化。
2 范围适用于澄清度检查法的检验操作。
3 职责3.1 质量控制部检验人员对具体操作负责;3.2 质量保证部负责监督本规程的执行。
4 定义4.1 澄清:指供试品溶液的澄清度与所用溶剂相同,或不超过0.5号浊度标准液的浊度。
4.2 几乎澄清:指供试品溶液的浊度介于0.5号至1号浊度标准液的浊度之间。
5 内容5.1 概述与原理澄清度检查法系将药品溶液与规定的浊度标准液相比较,用以检查溶液的澄清程度,是利用药物与杂质在特定溶剂中溶解性能的差异而设计的检查项目,主要用于原料药与注射剂的质量控制。
浊度是一种光学效应,是光线与溶液中的悬浮颗粒相互作用的结果,它表征光线透过水层时受到障碍的程度。
5.2 仪器与用具5.2.1 比浊用玻璃管:内径15~16mm,平底,具塞,以无色、透明、中性硬质玻璃制成,要求供试品管与标准管的内径、标线刻度(距管底为40mm) 一致。
5.2.2 伞棚灯用可见异物检查法标准操作规范中第一法灯检法项下的检查装置,照度为1000 Lx。
5.3 试药与试液5.3.1 浊度标准贮备液的制备:称取于105℃干燥至恒重的硫酸肼1.00g置l00ml 量瓶中,加水适量使溶解,必要时可在40℃的水浴中温热溶解,并用水稀释至刻度,摇匀,放置4~6小时;取此溶液与等容量的10%乌洛托品溶液混合,摇匀,于25℃避光静置24小时,即得。
该溶液置冷处避光保存,在两个月内使用,用前摇匀。
5.3.2 浊度标准原液的制备:取浊度标准贮备液15.0ml,置l000ml量瓶中,加水稀释至刻度,摇匀,取适量,置lcm吸收池中,照紫外一可见分光光度法(SOP-QC-00-001-00)在550nm的波长处测定,其吸光度应在0.12~0.l5范围内。
本液应在48h内使用,用前摇匀。
5.3.3 浊度标准液的制备:取浊度标准原液与水,按下表配制,即得。
本液应临5.4 操作方法5.4.1 除另有规定外,将一定浓度的供试品溶液与该品种项下规定的浊度标准液,分别置于配对的比浊用玻璃管中,液面高度为40mm,在浊度标准液制备5min 后,于暗室内垂直同置于伞棚灯下,照度为1000 lx,从水平方向观察比较,用以检查溶液的澄清度或其浑浊程度。
EP欧洲药典和CP中国药典关于澄清度和溶解度的异同
出自20斤不是肉
1、澄清度检查法 Clarity and Degree of Opalescence
• CP2020 中国药典2020 P124 • EP 9.8 2.2.1
出自20斤不是肉
澄清度——标准
CP
• 品种项下规定的“澄清”,系指供试品溶液的 澄清度与所用溶剂相同,或不超过0.5号浊 度标准液的浊度。“几乎澄清”,系指供试品 溶液的浊度介于0.5号至1号浊度标准液的浊 度之间。
标准液应临用时制备,使用前充分摇匀。
2.2.1.-1. Mix and shake before use.
出自20斤不是肉
2、溶解度 Solubility
• CP 2020 凡例第十五项性状 • EP 9.8 General notices-CHARACTERS
出自20斤不是肉
溶解度
CP
•
•溶 解 度 是 一 种 物 理 性 质 。 各 品 种 项 下 选 用 的 部 分 溶 剂 及 其 在 该 溶 剂中的溶解性能,可供精制或制备溶液时参考;对在特定溶剂中的溶 • 解性能需作质量控制时,在该品种检查项下另作具体规定。相关名 词术语如下:
不同之处:CP的目视法没提到做系统适应性,但是仪器法有做。
出自20斤不是肉
澄清度——浊度标准储备液 Primary opalescent suspension
CP
EP
• Hydrazine sulfate solution:
• 称取于105℃干燥至恒重的硫酸肼1.00g, 置100ml量瓶中,加水适量使溶解,必要时 可在40℃的水浴中温热溶解,并用水稀释至 刻度,摇匀,放置4-6小时;取此溶液与等
EP欧洲药典和CP中国药典关 于澄清度和溶解度的异同
澄清度检查操作规程
范围:原辅料、成品职员:检验室对本规程的实施负责正文:1.原理——澄清度是检查药品溶液的浑浊程度,即浊度。
药品溶液中如存在细微颗粒,当直射光通过溶液时,可引致光散射和光吸收的现象,致使溶液微显浑浊;所以澄清度可在一定程度上反映药品的质量和生产工艺水平。
澄清度检查法是用规定级号的浊度标准溶液与供试品溶液比较,以判定药品溶液的澄清度或浑浊程度。
2.仪器与用具2.1比浊用玻璃管内径15~16mm,平底,具塞,以无色硬质中性玻璃制成,要求供试品管与标准管的内径、标线刻度(距管底为40mm)一致。
2.2伞棚灯用澄明度检查装置,照度为1000Lx。
3.试药与试渡3.1硫酸肼和乌洛托品(分析纯)3.2浊度标准贮备液的制备称取硫酸肼1.00g置100ml量瓶中,加水适量使溶解,必要时可在40℃的水浴中温热溶解,并用水稀释至刻度,摇匀,放置4~6小时;取此溶液与等容量的10%乌洛托品溶液混合,摇匀,于25℃避光静置24小时,即得。
本液置冷处避光保存,可在两个月内使用,用前摇匀。
3.3浊度标准原液的制备取浊度标准贮备液15.0ml,置1000ml量瓶中,加水稀释至刻度摇匀,取适量、置1cm吸收池中,照分光光度法在550nm的波长处测定,其吸收度应在0.12~0.15范围内。
本液应在48小时内使用,用前摇匀。
3.3.1执行《紫外分光光度法标准操作规程》3.3.1执行《紫外分光光度计标准操作规程》3.4 浊度标准原液的的制备取浊度标准原液与水,按下表配制,即得。
本液应4.1除另有规定外,将一定浓度的供试品溶液与该品种项下规定的浊度标准液,分别置于配对的比浊用玻璃管中,液面高度为40mm,在浊度标准液制备5分钟后,同置黑色背景上,在漫射光下从比色管上方向下观察,比较,或置于伞棚下,照度为1000lx,从水平方向观察比较,用以检查溶液的澄清度或其浑浊程度。
4.2在进行比较时,如供试品溶液管的浊度接近标准管时,应将比浊管交换位置后再行观察。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附录Ⅸ B 澄清度检查法
本法系在室温条件下,将用水稀释至一定浓度的供试品溶液与等量的浊度标
准液分别置于配对的比浊用玻璃管(内径15~16mm,平底,具塞,以无色、透
明、中性硬质玻璃制成)中,在浊度标准液制备 5 分钟后,在暗室内垂直同置于
伞棚灯下,照度为1000 lx,从水平方向观察、比较;用以检查溶液的澄清度或
其浑浊程度。
除另有规定外,供试品溶解后应立即检视。
品种项下规定的“澄清”,系指供试品溶液的澄清度相同于所用溶剂,或未
超过0.5 号浊度标准液。
“几乎澄清”则指供试品溶液的浊度介于0.5 号至 1 号
浊度标准液的浊度之间。
浊度标准贮备液的制备称取于105℃干燥至恒重的硫酸肼1.00g,置100ml
量瓶中,加水适量使溶解,必要时可在40℃的水浴中温热溶解,并用水稀释至
刻度,摇匀,放置4~6 小时;取此溶液与等容量的10%乌洛托品溶液混合,摇
匀,于25℃避光静置24 小时,即得。
本液置冷处避光保存,可在两个月内使用,用前摇匀。
浊度标准原液的制备取浊度标准贮备液15.0ml,置1000ml 量瓶中,加水
稀释至刻度,摇匀,取适量,置1cm 吸收池中,照紫外-可见分光光度法(附录ⅣA),在550nm 的波长处测定,其吸光度应在0.12~0.15 范围内。
本液应在48
小时内使用,用前摇匀。
浊度标准液的制备取浊度标准原液与水,按下表配制,即得。
本液应临用
时制备,使用前充分摇匀。
