双液系沸点组成图
实验二 双液系沸点-成分图的绘制
双液系沸点-成分图的绘制一、实验目的1、用冷凝回流法测定不同浓度的环己烷-乙醇体系的沸点;2、正确使用阿贝折射仪;3、绘制沸点-成分图,确定体系的最低恒沸点和相应的组成。
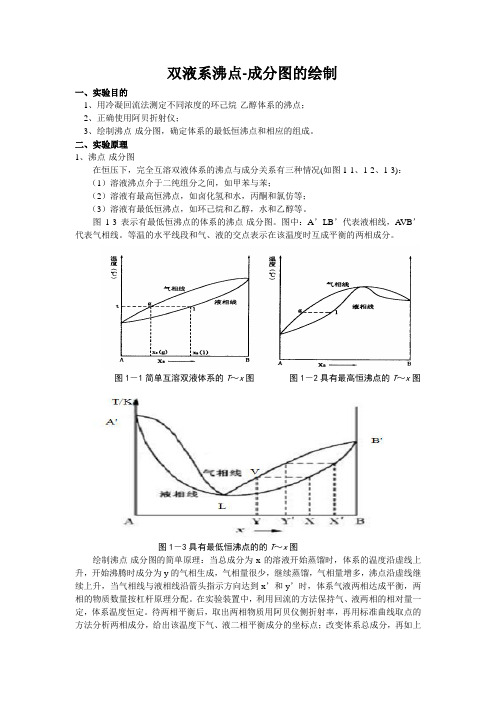
二、实验原理1、沸点-成分图在恒压下,完全互溶双液体系的沸点与成分关系有三种情况(如图1-1、1-2、1-3):(1)溶液沸点介于二纯组分之间,如甲苯与苯;(2)溶液有最高恒沸点,如卤化氢和水,丙酮和氯仿等;(3)溶液有最低恒沸点,如环己烷和乙醇,水和乙醇等。
图1-3表示有最低恒沸点的体系的沸点-成分图。
图中:A’LB’代表液相线,A VB’代表气相线。
等温的水平线段和气、液的交点表示在该温度时互成平衡的两相成分。
图1-1简单互溶双液体系的T~x图图1-2具有最高恒沸点的T~x图图1-3具有最低恒沸点的的T~x图绘制沸点-成分图的简单原理:当总成分为x的溶液开始蒸馏时,体系的温度沿虚线上升,开始沸腾时成分为y的气相生成,气相量很少,继续蒸馏,气相量增多,沸点沿虚线继续上升,当气相线与液相线沿箭头指示方向达到x’和y’时,体系气液两相达成平衡,两相的物质数量按杠杆原理分配。
在实验装置中,利用回流的方法保持气、液两相的相对量一定,体系温度恒定。
待两相平衡后,取出两相物质用阿贝仪侧折射率,再用标准曲线取点的方法分析两相成分,给出该温度下气、液二相平衡成分的坐标点;改变体系总成分,再如上法找出另一对坐标点。
将所有气相点和液相点连成气相线和液相线,即得T-x平衡图。
2、阿贝仪的使用阿贝仪利用了折射和全反射全反射原理设计而成。
将样品滴在棱镜上,旋转棱镜使目镜能看到半明半暗现象。
旋转补偿棱镜消除色散,在转动棱镜使明暗界线正好与目镜中的十字线交点重合,从标尺上直接读取折射率。
三、实验仪器及药品1、仪器恒沸点仪阿贝尔折射仪(WZS-I 940168)蒸馏瓶电阻丝变压器水银温度计(50~100℃,分度值0.1℃)恒温水浴装置5mL、20mL移液管滴瓶万分之一天平2、药品乙醇环己烷图1-4 恒沸点仪四、实验内容1、沸点和两相成分的测定1)洗净、烘干蒸馏瓶,加20mL乙醇使温度升高并沸腾,每隔30s记一次数据;2)待温度稳定3min后,记最终温度及大气压;3)断电,用两只滴管取支管口处气相冷凝液及蒸馏瓶中液体,用阿贝折射仪测折射率,气相冷凝液测1次,液相测2次;4)蒸馏瓶中依次加2mL、2mL、3mL、4mL、5mL环己烷,按上述方法测沸点及气液两相折射率;5)回收母液,少量环己烷洗蒸馏瓶3~4次,注入20mL环己烷,测纯沸点及气液两相折射率;6)再向蒸馏瓶中依次加0.5mL、0.5mL、0.5mL、2mL、5mL、5mL乙醇,分别测沸点及气、液两相折射率。
异丙醇-环己烷双液系相图

渤海大学学生实验报告课程名称:任课教师:实验室名称:物理化学实验室(二)房间号实验时间: 2013 年月日学院化学化工与食品安全学院专业班级姓名学号同组人实验项目异丙醇-环己烷双液系相图组别实验成绩一、实验目的1、了解物理化学实验中常用的物理方法-光学方法的基本原理2、绘制异丙醇-环己烷双液系的沸点-组成图,确定其沸点组成及衡沸温度3、进一步理解分馏原理4、掌握阿贝折射计的原理及使用方法二、实验原理在常温下两种液态以任意比例相互溶解所组成的体系称之为完全互溶双液系。
在恒定压力下,表示溶液沸点与组成关系的图称之为沸点-组成图。
本实验利用回流及分析的方法来绘制相图。
取不同组成的溶液在沸点仪中回流,测定其沸点及其气液组成。
沸点数据可由温度计获得,气-液相组成可通过测其折射率,然后由组成-折射率曲线中最后确定。
三、仪器与试剂沸点测定仪阿贝折射仪吸液管调压变压器温度计移液管(1ml 10ml 25ml) 异丙醇环己烷四、实验装置渤海大学实验报告用纸(第页共页)五、实验步骤1.已知浓度溶液折射率的测定取异丙醇和环己烷以及环己烷摩尔分数分别为0.2、0.4、0.6、0.8四种组成的溶液在25℃下,逐次用阿贝折射计测定其折射率,绘制组成-折射率的关系曲线;2,溶液沸点及气液组成的测定(1)取25ml异丙醇于沸点测定仪之蒸馏瓶内,连好路线,打开回流冷却水,接通电源加热至沸腾。
待温度恒定后,记下温度将调压变压器调至零处,停止加热充分冷却后取样,用阿贝折射计分别测定气相和液相冷凝液的折射率,按上述步骤分别测各液体的沸点及气相冷凝液和液相折射率;(2)将蒸馏瓶内的溶液倒入回馏瓶中,并用环己烷清洗蒸馏瓶,然后取25ml环己烷于蒸馏瓶内,按(1)的操作步骤进行,以后分别加入异丙醇0.2ml,0.3ml,0.5ml,1ml,4ml,5ml,测定其沸点及气相冷凝液和液相折射率。
六、数据记录和处理大气压:大气压:101.56kpa; 压力校正因素:溶液沸点与大气压有关沸点校正:△t=t/10 *(101.325-p)/101.325 tb=t+△t编号项目1 2 3 4 5 6 7 8t0c 66.4 64.6 63.9 64.1 64.3 64.6 65.7 71.6气相ny1 1.4029 1.4027 1.4012 1.4005 1.3995 1.3988 1.3962 1.38422 1.4027 1.4028 1.4010 1.4007 1.3994 1.3987 1.3964 1.3843平均 1.4028 1.4027.5 1.4011 1.4006 1.39945 1.39875 1.3963 1.38425xg41.4 42.2 45.0 45.8 47.9 49.6 61.4 69.0液相nx1 1.4212 1.4191 1.4119 1.4106 1.3891 1.3831 1.3751 1.36372 1.4211 1.4190 1.4120 1.4108 1.3890 1.3832 1.3750 1.3635平均 1.42115 1.41905 1.41195 1.4007 1.38905 1.38315 1.37505 1.3636xl5.8 10.0 25.0 46.1 63.8 70.4 80.0 94.8 △t -0.0154 -0.0150 -0.0148 -0.0149 -0.0149 -0.0150 -0.0152 -0.0166tb66.3846 64.585 63.8852 64.0851 64.2851 64.585 65.6848 71.5834恒沸温度校正前63.95 后63.94 恒沸组成xg = xl=45.7渤海大学实验报告用纸(第页共页)七结果讨论与分析1.产生误差的原因:a.温度计的水银球应一半在液体中,一半在气相中,以确保气液达平衡,否则将影响实验结果。
4.3完全互溶双液系统讲解

T x1
x2
x3 x4
A
xB
B
一、理想的完全互溶的双液系统
T-p-x图
T
液 pA*
TA*
液
A
xB
pB* 气
气 气
TB* B
一、理想的完全互溶的双液系统
T-p-x图
二、杠杆规则
T g
TB*
DC E
l TA*
B
x1
xA x2
A
xA
物系点:系统物质的总组成点(不管相的存在状态)
二、杠杆规则
假设某压力下液态混合物沸腾时气液平衡的物系点为C点,那 么有: n总 nA nB nl ng
三、非理想的完全互溶双液系统
1. 正负偏差不大的体系
气液相图与理想液态混合物气液相图基本类似
p
p
T
A
xB
(a) p-x图
BA
xB
BA
xB
B
(b) p-x-y图
(c) T-x-y图
三、非理想的完全互溶双液系统
2. 正偏差很大的体系 有最高点
p-液相组成线
p
p
p-气相组成线
A
xB
B
(a) p-x图
A
xB
B
(b) p-x-y图
pA、pB偏离拉乌尔定律都很大,p-x图上形成最高点。
三、非理想的完全互溶双液系统
2. 正偏差很大的体系
g
T lg lg
(c) T-x-y图
l
l
A
x1
B
xB
在p-x图上有最高点,在T-x图上就有最低点,称最低恒沸点。 最低恒沸点对应的组成称最低恒沸组成。在此组成下蒸馏双 液系:yA = xA , yB= xB,A与B达不到分离目的,类似蒸馏 具有恒定沸点的纯物质,所以此点上混合物称恒沸混合物。
双液系相图的绘制

对量一定,则体系的温度也随之而定。
三、仪器与试剂
❖ 沸点仪
(一套);
❖ 调压变压器
(一台);
❖ 阿贝折光仪
(一台);
❖ 超级恒温槽
(一套);
❖ 1/10温度计(50—100℃) (一支);
❖ 1/10温度计(0—50℃) (一支);
❖ 小烧杯
(一个);
❖ 小试管(5mL带软木塞) (若干);
❖ 吸管
(2支);
❖ 红外线干燥箱
(1台);
❖ 擦镜纸
❖ 乙酸乙酯(AR);
❖ 无水乙醇(AR);
❖ 不同比例的乙醇—乙酸乙酯混合液;
❖ 丙酮(C.P);
❖ 无水酒精(AR)
❖ 重蒸水
四、实验步骤
❖ 1.乙醇-乙酸乙酯液的折光率组成工作曲线 的测绘
《仪器分析原理》D.A.斯科格等著,上海科技出版社 P.299(1980)
《物理化学实验》,北京大学化学系,北京大学出版社 P.28(1981)
参考文献
《物理化学实验指导书》,吴子生,严忠主编,东北大 学出版社,1995
《物理化学实验》,复旦大学等编,人民教育出版社 (1979)
E.W.Washburn International Critical tabbies of Namerical Data Physics Chemistry and Technology Lr P320(1928).
一、 实验目的
❖ 1.用回流冷凝法测定沸点时气相与液相的组 成,绘制双液系相图。并找出恒沸点混合物 的组成 及恒沸点的温度。
❖ 2. 掌握测定双组分液体的沸点及正常沸点的 测定方法.
物理化学实验报告讲义完全互溶双液系沸点-组成图的测定

图 3-11 完全互溶双液系的沸点-组成图
仪器和药品
实验原理
室温下两种液体混合后,按其相互溶解情况,可形成完全互溶、部分互溶和完全不 互溶三种类型的混合物。完全互溶的双液系,因两种组分具有不同的挥发性,故在一定 外压下混合物沸腾时,平衡共存的气、液两相的组成通常不同。同时,混合物的沸点也 会随着平衡组成的不同而发生变化。因此,在恒压下将溶液蒸馏,测定其相平衡温度(沸 点)和相平衡组成(气相组成,液相组成),描述这种关系的图,称为恒压下的沸点-组成 图。获得此类相图的方法称为蒸馏法。
仪器:平衡蒸馏仪一套(见图 3-12);阿贝折光仪(附带超级恒温水浴);调压器; 数字式温度计;取样管;洗耳球;移液管,漏斗。
药品:环己烷(A·R);无水乙醇(A·R)。
实验步骤
1.配制具有不同组成的环己烷-乙醇溶液 22 mL。打开连接在阿贝折光仪上的超级恒 温水浴,恒温于 250.1 oC。
2.向干燥蒸馏瓶中加入 22 mL 无水乙醇,盖好磨口塞,通冷却水。打开加热器电源 开关,缓慢调节调压器的输出电压至 20 V 左右,加热蒸馏瓶,待蒸馏瓶内的液体稳定沸 腾 3~5 min 后,记录沸点及大气压,切断电源。
作曲线上查得的各试样组成记入表 3-3。
表 3-3 二组分气-液平衡相图原始数据记录表
试剂加入量 V/mL 环己烷 无水乙醇
沸点/℃
气相冷凝液
折光率
y 环己烷
平衡液相
二组分溶液沸点—组成图的绘制

学号:21成绩:基础物理化学实验报告实验名称:二组分溶液沸点—组成图的绘制应用化学二班级3 组号实验人姓名:xx同组人姓名:xx指导老师:周崇松实验日期:2013.9湘南学院化学与生命科学系一.实验目的1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。
2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。
3.掌握阿贝折射仪的使用方法。
二.实验原理在一定的外压下,纯液体的沸点是恒定的,但对于完全互溶双液系,沸点不仅与外压有关,而且还与其组成有关,并且在沸点时,平衡的气-液两相组成往往不同。
根据相律:F=C-P+2,一个气液共存的二组分体系,其自由度为2,只需再任意确定一个变量,其自由度就减为1,整个体系的存在状态就可以用二维图来描述。
本实验中采用在一定压力下,作出体系的温度T 和组分x 的关系图,即T-x 图。
完全互溶体系的T-x 图可分为三类:①液体与Raoult 定律的偏差不大,在T-x 图上,溶液的沸点介于两种纯液体的沸点之间(图1.a ),如苯-甲苯系统;②由于两组分的相互作用,溶液与Raoult 定律有较大的负偏差,在T-x 图上存在最高沸点(图1.c ),如卤化氢-水系统;③ 溶液与Raoult 定律有较大的正偏差,在T-x 图上存在最低沸点(图1.b ),如乙醇-水系统。
②和③类溶液,在最高或最低沸点时的气-液两相组成相同,这些点称为恒沸点,此浓度的溶液称为恒沸点混合物,相应的温度称为恒沸温度,相应的组成称为恒沸组成。
本实验所要测绘的环己烷-乙醇体系即属于第二类溶液。
对于一个组成恒定的封闭系统,当系统达到气液平衡温度时,气液两相的组成和温度恒定不变,以此便能得到该温度下的平衡气-液两相组成的一对坐标。
依次改变系统的组成就能得到一系列的平衡气-液两相组成坐标点,用光滑曲线连接即成相图。
实验所用的沸点仪结构如图2,冷凝管底部的小球用以收集冷凝下来的气相样品。
电热丝直接浸入溶液中加热可避免暴沸现象,温度计外的小玻璃罩有利于降低周围环境可能造成的温度计读数波动。
实验2 dyl双液相图
物理化学实验备课材料实验二完全互溶两组分液态混合物的气液平衡相图一、基本介绍相平衡属于物理化学的重要教学内容,其中气液平衡是最常见,同时也是讨论最多的内容之一。
理想的二组分体系在全部浓度范围内符合拉乌尔定律。
结构相似、性质相近的组分之间可以形成近似的理想体系,此时体系的沸点组成图(T -x图)如下图1a所示。
大多数情况下为非理想体系,这时在反映体系沸点与组成关系的T-x图上将出现或正或负的偏差,当这一偏差足够大时,T-x曲线上将出现极低点(对拉乌尔定律产生极大正偏差,如下图1b所示)或极高点(对拉乌尔定律产生极大负偏差,如下图1c所示)。
出现极大点的体系常见的有:乙酸异戊酯—四氯乙烷;丙酮-氯仿;水—盐酸;水—硝酸等。
出现极小点的体系常见的有:四氯化碳—乙酸乙酯;甲醇—苯;正丙醇—水;异丙醇—环己烷,乙醇—水等。
这种最高和最低沸点称为恒沸点,所对应的溶液称为恒沸混合物。
注意,恒沸混合物不是一种物质,而是一种具有特定组成的混合物。
在恒沸点是气液两相的组成一致。
恒沸混合物的组成由温度或压力中的一个所确定,即指定温度,压力及组成由体系自定,不能改变。
图1 两组分体系的等压T-x图根据相平衡原理,对二组分体系,当压力恒定时.在气液平衡两相区,体系的自由度为1。
若温度一定.则气液两相的组成也随之而定,反之亦然。
当原溶液组成一定时,根据杠杆原理,两相的相对量也一定。
反之,实验中利用回流的方法保持气液两相的相对量一定,则体系的平衡温度也随之而定。
沸点测定仪就是根据这一原理设计的。
二、实验目的1、用沸点测定仪测定常压下不同组成的正丙醇—水体系的沸点,绘制该体系的T-x图。
2、掌握沸点测定方法。
阿贝折射仪1-反光镜;2-棱镜座转轴;3-遮光板;4-温度计;5-进光棱镜座;6-色散调节手轮; 7-色散刻度图;8-目镜;9-盖板10-手轮;11-折射棱镜;12-照明刻度盘聚光镜;13-温度计座3、进一步掌握阿贝折射仪的测量原理及操作方法。
实验六 完全互溶双液体系沸点
实验六完全互溶双液体系沸点~组成图的绘制一、实验目的1.了解溶液的沸点与气液二相组成的关系;2.绘制环己烷-异丙醇溶液的沸点~组成图;3.进一步理解分馏原理;4.掌握阿贝折光仪的正确使用方法。
二、基本原理液体的沸点是液体的饱和蒸气压与外压相等时的温度。
在一定的外压下,单一组分的液体有确定的沸点值,对于一个完全互溶的双液体系,沸点不仅与外压有关,还和液体的组成有关。
在常温下,具有挥发性的A和B两种液体以任意比例相互溶解所组成的物系,在恒定压力下表示该溶液沸点与组成关系的相图称之为沸点~组成图,即T ~x图。
完全互溶双液体系在恒压下的沸点~组成图大致可分为以下三类。
图6-1简单互溶双液体系的T~x图图6-2具有最高恒沸点的T~x图图6-3具有最低恒沸点的的T~x图第Ⅰ类:溶液沸点介于两纯组分沸点之间,如苯与甲苯的混合体系,其沸点~组成图如图6-1所示。
此类溶液在恒压下蒸馏时,其气相组成和液相组成并不相同,具有较低蒸气压的液体(B)在气相中的组成X B(g)总是小于在液相中的组成X B(l),因此可以通过反复蒸馏——精馏,使互溶的二组分完全分离。
第Ⅱ类:溶液具有最高恒沸点,如卤化氢和水、丙酮与氯仿等,其沸点~组成图如图6-2所示。
第Ⅲ类:溶液具有最低恒沸点,如苯与乙醇、乙醇与水、环己烷与异丙醇、环己烷与乙醇、乙醇与1,2-二氯乙烷等,其沸点~组成图如图6-3所示。
在第Ⅱ、Ⅲ类的T ~x图中,出现极值点(极大值或极小值),在极值点处加热蒸发时,只能使气相的总量增加,气液相组成及沸点均保持不变,此点的温度称为恒沸点。
在恒沸点时,气相的组成与液相的组成相同,称为恒沸组成。
而具有此组成的混合物称为恒沸混合物。
对于Ⅱ、Ⅲ两类溶液,简单的反复蒸馏只能获得某一纯组分和恒沸混合物,而不能同时得到两种纯组分。
恒沸点和恒沸混合物的组成与外压有关,改变外压可使恒沸点和恒沸混合物的组成发生变化。
本实验环己烷与异丙醇的混合物属于第Ⅲ类溶液,具有最低恒沸点。
实验二 双液系组分的测定
实验二双液系的气—液平衡相图一、实验目的:1.绘制在标准压力下乙酸乙酯-乙醇双液系的气-液平衡相图2.学会阿贝折光仪的使用方法3.初步学会通过折光率确定二元液体组成的方法4. 掌握测定双组分液体的沸点以及正常沸点的方法二、实验原理两种液态物质混合后的双组分混合液称为双液系。
两个组分若能以任意比互溶称为完全互溶双液系。
溶液的沸点是指液体的蒸汽压与外界压力相等时的温度,在一定的外压下,纯液体的沸点有确定值;双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。
根据相律:自由度= 组分数-相数+ 2因此,气液共存的双组分体系的自由度为2。
只要确定一个变量,整个体系的存在状态可以用二维图象来描述。
例如,在一定温度下,可以画出体系的压力p和组分x的关系图(图1, 请参考实验教材),这就是相图。
在T-x相图上,还有温度、液相组成和气相组成三个变量,但是只有一个自由度。
一旦设定某个变量,则其它两个变量必有相应的确定值。
图1为完全互溶双液系的沸点-组成图。
组分分析:本实验使用数字阿贝折光仪对样品进行分析,关于数字阿贝折光仪的使用方法和折光仪的工作原理见《物理化学实验》(复旦大学)(高等教育出版社第二版)262页。
五、实验步骤1. 沸点测定:用量筒取25ml乙醇或乙酸乙酯并倒入沸点仪中,注意电热丝应完全浸没在液体中,打开冷凝水接通电源并调节电压)待溶液沸腾后,调节冷凝水流量,温度计的读数稳定后方可读取沸点,并记录环境温度计的读数,在上述过程中要不断把气相凝聚液倒回圆底烧瓶中。
投料表:计算乙醇含量:Y乙醇=2. 折光率的测定及组成的确定停止加热,用干燥的长滴管分别从支管和冷凝管的上口取样,注意一个滴管只能取一个样,不得使同一个滴管取不同的样,每取一个样要测定三次折光率。
这样就得到两个系列的溶液的折光率。
未知溶液的组成从对应的折光率-组成工作曲线查得。
将乙醇、乙酸已酯以及系列溶液的沸点和气、液两相组成列表并绘制乙醇-乙酸已酯的温度-组成相图。
6.双液系相图的绘制
化学化工学院
化学化工学院
实验6:双液系相图的绘制 数据处理
1. 将实验数据列表。 2. 绘制工作曲线,即环己烷—乙醇标准溶液的折光率与组 成的关系曲线。 3. 根据工作曲线确定各待测溶液气相和液相的平衡组成, 4. 确定最低恒沸点的温度和组成。
化学化工学院
实验6:双液系相图的绘制 思考题
1. 待测溶液的浓度是否需要精确计量?为什么? 2. 本实验不测纯环己烷、纯乙醇的沸点,而直接用标准压 力下的数据,这样会带来什么误差? 3. 如果要测纯环己烷、纯乙醇的沸点,蒸馏瓶必须洗净, 而且烘干,而测混合液沸点和组成时,蒸馏瓶则不洗也不 烘,为什么?
化学化工学院
实验6:双液系相图的绘制
测定方法
本实验选择一个具有最低恒沸点的环己烷—乙醇体系。在 100KPa下测定一系列不同组成的混合溶液的沸点及在沸点 时呈平衡的气液两相的组成,绘制T—x图,并从相图中确 定恒沸点的温度和组成。测定沸点的装置叫沸点测定仪。 这是一个带回流冷凝管的长颈圆底烧瓶。冷凝管底部有一 半球形小室,用以收集冷凝下来的气相样品。电流通过浸 入溶液中的电阻丝。这样既可减少溶液沸腾时的过热现象, 还能防止暴沸。测定时,温度计水银球要一半在液面下, 一半在气相中,以便准确测出平衡温度。
化学化工学院
实验6:双液系相图的绘制
双液系的T—x图有三种情况: (1)理想溶液的T—x图,它表示混合液的沸点介于A、B二 纯组分沸点之间。这类双液系可用分馏法从溶液中分离出 两个纯组分。 (2)有最低恒沸点体系的T—x图和有最高恒沸点体系的 T—x图。这类体系的T—x图上有一个最低和一个最高点, 在此点相互平衡的液相和气相具有相同的组成,分别叫做 最低恒沸点和最高恒沸点。对于这类的双液系,用分馏法 不能从溶液中分离出两个纯组分。
