元素 原子 分子区别和联系
原子和分子有什么区别

原子和分子有什么区别原子和分子是物质世界中最基本的概念,在化学中扮演着重要的角色。
尽管它们都是构成物质的微观粒子,但是它们之间存在着一些区别。
本文将详细探讨原子和分子之间的区别。
1. 定义和组成原子是物质的最小单位,由一个或多个质子、中子和电子组成。
所有的元素都由原子构成,其特定的原子序数决定了其在周期表中的位置。
分子是由两个或多个原子通过化学键连接而成的结构。
分子可以是由相同类型的原子组成的,也可以是由不同类型的原子组成的。
不同类型的原子组合在一起形成化合物分子,例如水分子(H2O)由两个氢原子和一个氧原子组成。
2. 结构和稳定性原子是化学反应的基础单位,具有固定的原子序数和特定的化学性质。
它们通常以球形的形式存在,由核(质子和中子)和电子云组成。
原子的质量主要集中在核内,而电子云则环绕着核。
分子具有一定的结构,原子通过共享或转移电子来形成不同类型的化学键。
分子的结构可以是线性、平面或立体的,取决于原子之间的连接方式。
分子的稳定性取决于化学键的强度和结构的稳定性。
3. 数量表示原子不能被分割或进一步细分,因此在化学计量中,通常使用摩尔来表示物质的量。
摩尔是物质的数量单位,其中一个摩尔的物质约含有6.022 × 10^23个粒子(阿伏伽德罗常数)。
分子是物质中最小的可自由存在的单位,可以单独存在,也可以作为化合物的一部分存在。
在化学方程式中,通常使用分子来表示物质的量,并使用相应的化学式表示其组成。
4. 物质状态原子可以以不同的物质状态存在,包括固体、液体和气体。
例如,在常温下,氧原子以双原子气体(O2)的形式存在。
分子的物质状态取决于组成它们的原子的物质状态。
根据分子之间的相互作用力,分子可以以固体、液体或气体的形式存在。
5. 化学性质原子的化学性质取决于其电子结构和原子序数。
不同类型的原子具有不同的化学性质和反应特性。
例如,氧原子(O)倾向于与其他元素形成氧化物。
分子的化学性质取决于组成它们的原子之间的化学键类型和强度。
分子与原子的联系与区别

分子与原子的联系与区别1. 什么是原子?1.1 原子的定义原子就像是物质的基本构件,简单说,它是构成一切东西的“小砖块”。
想象一下,一个可口的汉堡,原子就是每一块面包、每一片生菜的最小单位。
每个原子都有一个中心叫原子核,里面有质子和中子,外面则围绕着电子,像行星围绕着太阳一样。
1.2 原子的种类原子有很多种,每种都有不同的特性。
比如,氧原子和氢原子,听起来是不是像两个朋友?它们可以结合在一起,形成水,这是我们生活中最离不开的东西。
所以,原子之间的“友谊”非常重要!2. 分子是什么?2.1 分子的定义分子可以看作是由两个或多个原子组成的“小团队”。
就像是一个乐队,多个乐器齐奏出美妙的音乐。
分子的构成可以非常简单,比如氧气(O₂)是由两个氧原子组成的;也可以非常复杂,比如蛋白质,它是由成千上万的原子组成的复杂结构。
2.2 分子的种类分子也有很多种类,像我们身边的空气、食物,甚至是我们的身体,都是由分子构成的。
不同的分子可以带来不同的味道和感觉,想想你吃的冰淇淋和热辣的咖喱,都是分子在里面起作用哦。
3. 原子与分子的联系3.1 分子是由原子组成的原子和分子的关系就像是单个乐手与整个乐队之间的关系。
没有原子,就没有分子;而分子则是由多个原子组合而成的。
所以,如果你了解了原子,理解分子也就不难了。
3.2 共同构成万物这些原子和分子一起构成了我们身边的一切。
无论是石头、树木,还是人类,都是由它们组合而成的。
有时候,想象它们在宇宙中翩翩起舞,就觉得生活充满了诗意。
4. 原子与分子的区别4.1 规模大小原子是基本单位,而分子是由多个原子组成的。
因此,分子的规模往往要比单个原子大得多。
你可以想象,原子就像是沙滩上的沙粒,而分子就像是一个个装满沙子的沙堡。
4.2 性质不同原子的性质主要由它的电子构成决定,而分子的性质则取决于原子的组合方式。
比如,同样都是由氧和氢构成的水(H₂O)和过氧化氢(H₂O₂),它们的性质完全不同,一个能喝,另一个则是漂白剂!这就像两个看似相似的人,性格却天差地别。
分子、原子、离子区别

分子、原子、离子区别分子是由原子构成的微观原子是原子核和核外电子构成的. 微观离子是带电的原子,是原子得或者失去核外电子时形成的.离子是带电的原子或原子团。
微观一、、原子指化学反应中的最小微粒;元素指拥有相同核电荷数的一类原子的总称;分子是保持物体化学性质的最小微粒;质子是带电的原子二、原子:1、原子内通常存在质子、中子、电子。
其数量级大约是10^-10m。
因此,与常见物体相比,原子是一个极小的物体,即使把一亿个氧原子排成一排,其长度仍不足1cm,人们只能通过一些特殊的仪器才能间接观测到单个的原子。
2、原子内中子和质子的质量相近且远大于电子,原子核由质子与中子组成,因此原子的质量极小,且99.9%集中在原子核。
3、原子核外分布着电子,电子占据一组稳定的轨道。
当它们吸收和放出光子的时候,电子也可以在不同能级之间跃迁,此时吸收或放出光子的能量与轨道之间的能量差相等。
电子决定了一个元素的化学性质,并且对原子的磁性有着很大的影响。
三、离子:1、离子是指原子由于自身或外界的作用而失去或得到一个或几个电子使其达到最外层电子数为8个或2个(氦原子)或没有电子(四中子)的稳定结构。
这一过程称为电离。
电离过程所需或放出的能量称为电离能。
2、在化学反应中,金属元素原子失去最外层电子,非金属原子得到电子,从而使参加反应的原子或原子团带上电荷。
带电荷的原子叫做离子,带正电荷的原子叫做阳离子,带负电荷的原子叫做阴离子。
阴、阳离子由于静电作用而形成不带电性的化合物。
四、元素:元素(element)又称化学元素,指自然界中一百多种基本的金属和非金属物质,它们只由几种有共同特点的原子组成,其原子中的每一核子具有同样数量的质子,用一般的化学方法不能使之变得更为简单,并且单独地或组合地构成一切物质。
一些常见元素的例子有氢,氮和碳。
到2007年为止,总共有118种元素被发现,其中94种是存在于地球上。
拥有原子序数大于82(即铋Bi及之后的元素)都是不稳定,并会进行放射衰变。
分子和原子的联系与区别

分子和原子的联系与区别
分子和原子是化学概念中的两个重要概念,它们之间存在连接,但又有一些区别。
联系:
1. 组成关系:分子是由原子通过化学键连接而成的,一个分子通常由两个或多个原子组成。
2. 表示方式:分子和原子都有相应的化学式来表示。
分子可以用化学式或分子式(如H2O表示水分子)表示,原子则通常
用元素符号表示(如H表示氢原子)。
3. 物质存在形态:绝大多数物质是以分子的形式存在的,如水、氧气等。
原子通常以离子的形式存在,如钠离子Na+、氯离子Cl-等。
区别:
1. 组成粒子:分子是由两个或多个原子通过共享电子形成的。
原子是化学元素中的最小单位,由质子、中子和电子组成。
2. 电荷:分子中的原子在化学键中共享电子,因此不带电荷。
而原子可以带正电荷(失去电子形成阳离子)或负电荷(获得电子形成阴离子)。
3. 大小:分子通常比原子大,原子直径约为0.1纳米,而分子
的大小取决于组成其的原子数目和原子之间的化学键。
总结来说,分子是由原子通过化学键连接而成的,是物质存在的基本单位之一。
原子是最基本的物质单位,不能再分割为其他物质。
高三物理总结原子与分子物理

高三物理总结原子与分子物理原子与分子物理是高中物理课程的重要内容之一,涉及到物质的微观结构和性质。
通过对原子和分子的认识,可以更好地理解物质的性质和变化规律。
本文将对高三物理中的原子与分子物理进行总结与归纳。
一、原子的基本结构原子是构成物质的基本单位,由原子核和电子组成。
原子核由质子和中子构成,质子带正电荷,中子不带电荷。
电子带负电荷,绕原子核运动。
二、元素与原子序数元素是由具有相同质子数的原子组成的纯物质。
元素的原子序数等于原子核中的质子数。
根据元素的原子序数,元素可以按一定顺序排列,形成元素周期表。
三、同位素同位素是指质子数相同、中子数不同的原子,它们具有相同的化学特性,但物理性质有所差异。
同位素广泛应用于医学、工业和科学研究等领域。
四、分子的组成分子是由两个或多个原子通过化学键结合而成的,可以是同种元素的原子组合,也可以是不同元素的原子组合。
五、化学键的种类化学键是原子之间的连接方式,常见的化学键有共价键、离子键和金属键等。
共价键是通过电子的共享形成的,离子键是由正、负电荷之间的相互吸引形成的,金属键是金属原子的电子云共享形成的。
六、离子化合物与分子化合物离子化合物是由正、负离子通过离子键结合而成的,分子化合物是由共价键连接的分子组成的。
离子化合物通常具有高熔点和良好的导电性,而分子化合物通常具有较低的熔点和离子化合物相比较差的导电性。
七、化学方程式与化学计量化学方程式用于表示化学反应,包括反应物、生成物和反应条件等信息。
化学计量是指反应物与生成物之间的摩尔比例关系,通过化学计量可以计算物质的摩尔质量和化学计量比。
八、摩尔与摩尔质量摩尔是物质的计量单位,表示1摩尔物质包含的基本单位数量。
摩尔质量是指单位摩尔物质的质量,可以通过元素的原子质量累加得到。
九、气体的状态方程气体的状态方程可以描述气体的体积、压强和温度之间的关系。
理想气体状态方程为PV=nRT,其中P表示气体的压强,V表示气体的体积,n表示气体的摩尔数,R为气体常数,T表示气体的温度。
分子、原子、离子及元素的关系
注 事
意 项
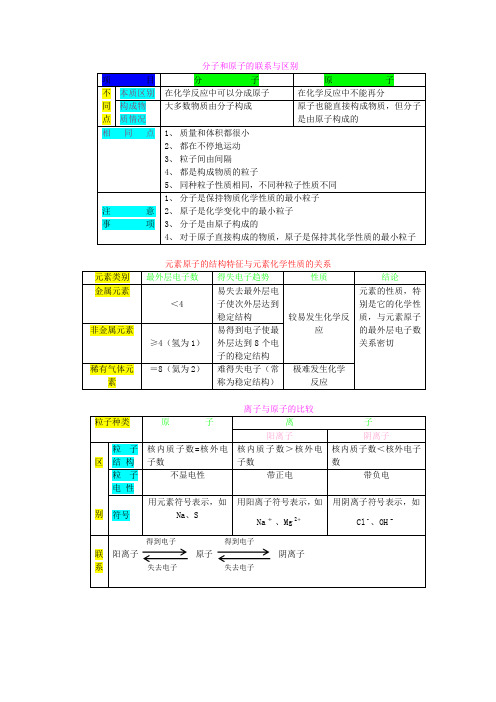
元素类别 金属元素
最外层电子数 <4
得失电子趋势 易失去最外层电 子使次外层达到 稳定结构 易得到电子使最 外层达到 8 个电 子的稳定结构 难得失电子(常 称为稳定结构)
性质
结论 元素的性质,特 别是它的化学性 质,与元素原子 的最外层电子数 关系密切
非金属元素 ≥4(氢为 1) 稀有气体元 素 =8(氦为 2)
分子和原子的联系与区别 项 不 同 点 相 目 本质区别 构成物 质情况 同 点 分 子 原 在化学反应中不能再分 原子也能直接构成物质,但分子 是由原子构成的 子 在化学反应中可以分成原子 大多数物质由分子构成
1、 质量和体积都很小 2、 都在不停地运动 3、 粒子间由间隔 4、 都是构成物质的粒子 5、 同种粒子性质相同,不同种粒子性质不同 1、 分子是保持物质化学性质的最小粒子 2、 原子是化学变化中的最小粒子 3、 分子是由原子构成的 4、 对于原子直接构成的物质,原子是保持其化学性质的最小粒子 元素原子的结构特征与元素化学性质的关系
较易发生化学反 应
极难发生化学 反应
离子与原子的比较 粒子种类 粒 子 结 构 粒 子 电 性 别 符号 原 子 离 阳离子 区 核内质子数=核外电 子数 不显电性 用元素符号表示,如 Na、S
得到电子
子 阴离子 核内质子数<核外电子 数 带负电 用阴离子符号表示,如 Cl 、OH
-
核内质子 数>核外电 子数 带正电 用阳离子符号表示, 如 Na
表示方法 微 的 运 动 粒
H 2 、He 物理变化是分子运动 的结果,如:水的蒸 发
2 、CO 3 -
离子运动的结果可能是物 理变化,也可能是化学变 化,如:NaCl 的溶解是物 理变化,NaCl 与 AgNO 3 反 应是化学变化
分子、原子、离子及元素的关系
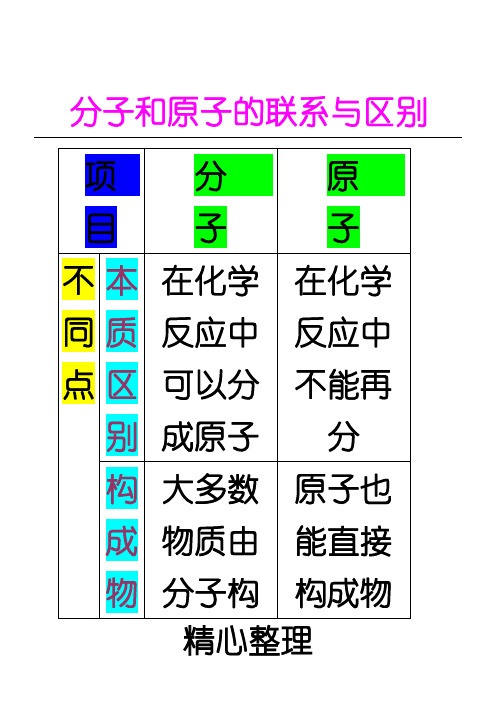
项分 目子 不 本 在化学 同 质 反应中 点 区 可以分
别 成原子 构 大多数 成 物质由
原 子 在化学 反应中 不能再 分 原子也 能直接
精心整理
物 分子构 构成物
质 成 质,但分
情
子是由
况
原子构
成的
相 1、 质量和体积都
同
很小
点 2、 都在不停地运
动
3、 粒子间由间隔
精心整理
稳定
结构
稀 =8 难得 极
有 (氦 失电 难
气为 子 发
体 2) (常 生
元
称为 化
素
稳定 学
结反
构) 应
精心整理
离子与原子的
比较
粒子 原
离
种类 子
子
阳离 阴离
子子
粒 核内 核内 核内
区 子 质子 质子 质子
结 数= 数> 数<
精心整理
构 核外 核外 核外 电子 电子 电子
别 数数 数 粒 不显 带正 带负 子 电性 电 电 电 性 用元 用阳 用阴 符 素符 离子 离子 号 号表 符号 符号
阴离子
失电子
失电子 构分 成裂
系
分
子
元素与原子的比较 精心整理
元
原
素
子
概 具有相同 化学变化
念 核电荷数 中的最小
(即核内 粒子
质子数)
的一类原
子的总称
区 只讲种 既将种
分 类,不讲 类,又讲
精心整理
个数 个数 使 用于描 用于描述 用 述物质 物质的微 范 的宏观 观构成 围 组成 举 水由氢元 每个水分 例 素和氧元 子由两个
原子、原子核、分子、离子、质子、中子、电子

原子分子离子质子电子的区别原子由原子核和在原子核和带负电的电子组成。
(原子核一般由带正电荷的质子和不带电的中子构成。
)量子是一个比拟广泛的概念~应该是指量子力学中研究的各种粒子 ,包括质子 ,中子 ,电子⋯⋯粒子也是比拟广泛的概~泛指各种微粒。
离子是带电微粒~因为量子,粒子X围太大,没法比拟。
能确定大小的最小的是电子吧~1、分子是保持物质化学性质的最小粒子〔原子、离子也能保持物质的化学性质〕。
原子是化学变化中的最小粒子。
例如:保持氯气化学性质的最小粒子是D〔氯分子〕〔 A 、Cl B 、Cl- C 、2Cl D 、 Cl2 〕。
保持CO2 化学性质的最小粒子是 CO2 分子;保持水银的化学性质的最小粒子是汞原子。
在电解水这一变化中的最小粒子是氢原子和氧原子。
原子中:核电荷数〔带正电〕=质子数 =核外电子数相对原子质量 =质子数 +中子数原子是由原子核和核外电子构成的,原子核是由质子和中子构成的,构成原子的三种粒子是:质子〔正电〕、中子〔不带电〕、电子〔带负电〕。
一切原子都有质子、中子和电子吗?〔错!一般的氢原子无中子〕。
某原子的相对原子质量=某原子的质量 /C 原子质量的1/12 。
相对原子质量的单位是“1,〞它是一个比值。
相对分子质量的单位是“1。
〞由于原子核所带电量和核外电子的电量相等,电性相反,因此整个原子不显电性〔即电中性〕。
2、①由同种元素组成的纯洁物叫单质〔由一种元素组成的物质不一定是单质,也可能是混合物,但一定不可能是化合物。
〕②由一种分子构成的物质一定是纯洁物,纯洁物不一定是由一种分子构成的。
③由不同种元素组成的纯洁物一定是化合物;由不同种元素组成的物质不一定是化合物,但化合物一定是由不同种元素组成的。
纯洁物与混合物的区别是物质的种类不同。
单质和化合物的区别是元素的种类不同。
④由两种元素组成的,其中一种是氧元素的化合物叫氧化物。
氧化物一定是含氧化合物,但含氧化合物不一定是氧化物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
元素、分子和原子的区别与联系
元素组成物质
宏观概念,只讲同类原子总称构成构成
构成微观概念,既讲
原子分子
16.粒子:如原子、离子、分子、电子、质子等,它们都是微观概念,既表示种类又可表示个数。
分子、原子、离子都是构成物质的粒子。
金属单质和稀有气体由原子直接构成;
非金属单质、非金属与非金属形成的共价化合物由分子构成,化合物中既有金属元素又有
非金属元素的离子化合物是由离子构成。
17.分子:分子是保持物质化学性质的最小粒子。
分子由原子构成,
例:1个水分子由2个氢原子和1个氧原子构成
18.原子:原子是化学变化中的最小粒子。
(注意:原子不是构成物质的最小粒子。
)
原子的的构成:原子由核外带负电的电子和带正电的原子核构成,原子核由带正电的质子
和不带电的中子构成。
在不显电性的粒子里:核电荷数=质子数=核外电子数
注意:原子不是构成物质的最小粒子。
原子只是化学变化中的最小粒子;
普通氢原子核中只有质子无中子,氢原子的原子核就是一个质子。
分子和原子的区别:在化学变化中分子可分为更小的粒子---原子,原子不能再分。
物质发生物理变化时只是分子间的间隔发生变化,而分子本身没有发生变化;发生化学变化时,
分子被破坏,分子本身发生变化。
在一切化学反应中,反应前后元素的种类、原子的种类、原子的数目和原子的质量都不变。
19.原子团:由两种或两种以上元素的原子构成,在化学反应中通常以整体参加反应的原子集团
常见的原子团:SO42- CO32- NO3- OH- MnO4- MnO42- ClO3- PO43- HCO3- NH4+
碳酸氢根(HCO3-)硫酸氢根(HSO4-)磷酸氢根(HPO42-)磷酸二氢根(H2PO4-)
注意:原子团只是化合物中的一部分,不能脱离物质单独存在,因此含原子团的物质必定有
三种或三种以上元素,二种元素组成的物质不含原子团。
原子团在化学反应中可再分为更小的粒子原子。
20.离子:带电的原子或原子团叫离子。
带正电的离子叫阳离子;带负电的离子叫阴离子。
离子里:质子数=核电荷数=电子数±带电量
离子符号的写法:离子的电荷数标在右上角,电荷的数值等于它对应的化合价
阳离子:Na+ Mg2+ Al3+、H+ NH4+、Fe2+ Fe3+ Ca2+
阴离子:O2-、OH- S2-、 F- Cl- SO4 2- CO32- NO3- MnO4- PO43- MnO42- ClO3-
21.核外电子排布的规律:核外电子按能量由低到高从里往外排,第一层最多容纳2个电子,
第二、三层最多容纳8个电子。
按顺序背诵:质子数从1~18的元素符号和名称:
氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩
22.稳定结构:最外层电子数是8(只有一层的为2)的结构。
元素的化学性质跟原子的最外层电子数关系最密切,原子的最外层电子数决定元素的化学性质:
最外层电子数小于4时,易失去最外层所有电子,成为阳离子;(通常是金属元素)
最外层电子数多于4时,易得到电子使最外层电子数变为8,成为阴离子(通常是非金属元素)
最外层电子数与化合价的关系:(元素的最高正价等于原子的最外层电子数)
最外层电子数小于4时,最外层电子数就是元素的化合价(正价);最外层电子数多于4时,最外层电子数-8=元素的化合价。
