【大题】工科物理大作业热力学
大学物理习题详解 热力学第二定律

©物理系_2012_09《大学物理AII 》作业 No.12 热力学第二定律一、判断题:(用“T ”和“F ”表示)[ T ] 1.任何可逆热机的效率均可表示为:高低T T -=1η 解:P301,根据卡诺热机的效率[ F ] 2.若要提高实际热机的效率, 可采用摩尔热容量较大的气体做为工作物质。
解:P294-295,根据热机效率的定义吸净Q A =η,显然工作物质从高温热源吸收的热量越少,对外作的功越多,其效率越高。
根据热量的定义T C MmQ ∆=,温差一定的时候,摩尔热熔C 与热量成正比。
[ F ] 3.一热力学系统经历的两个绝热过程和一个等温过程,可以构成一个循环过程 解:P308题知循环构成了一个单热源机,这违反了开尔文表述。
[ F ] 4.不可逆过程就是不能沿相反方向进行的过程。
解:P303 [ T ] 5.一定量的理想气体向真空作绝热自由膨胀,体积由1V 增至2V ,在此过程中A =0,Q =0,0=∆T ,0>∆S 。
解:P292,P313二、选择题:1.如果卡诺热机的循环曲线所包围的面积从图中的a b c d a 增大为 a b ′c ′d a ,那么循环a b c d a 与a b ′c ′d a 所作的功和热机效率变化情况是: [ D ] (A) 净功增大,效率提高(B) 净功增大,效率降低(C) 净功和效率都不变 (D) 净功增大,效率不变 解:卡诺循环的效率121T T-=η只与二热源温度有关,曲线所围面积在数值上等于净功,所以净功增大,效率不变。
2.对于循环热机,在下面节约与开拓能源的几个设想中,理论上可行的是: [ B ] (A) 改进技术,使热机的循环效率达100%(B) 利用海面与海面下的海水温差进行热机循环作功 (C) 从一个热源吸热,不断作等温膨胀,对外作功 (D) 从一个热源吸热,不断作绝热膨胀,对外作功解:根据热力学第二定律,(A)是第二类永动机,是不可能制成的;(C)是单热源机;(D)是从热源吸热怎么作绝热膨胀。
高考物理力学知识点之热力学定律真题汇编附答案精选全文完整版

可编辑修改精选全文完整版高考物理力学知识点之热力学定律真题汇编附答案一、选择题1.一定质量的理想气体,从状态M开始,经状态N、Q回到原状态M,其p-V图象如图所示,其中QM平行于横轴,NQ平行于纵轴.则()A.M→N过程气体温度不变B.N→Q过程气体对外做功C.N→Q过程气体内能减小D.Q→M过程气体放出热量2.下列说法正确的是()A.决定封闭理想气体压强大小的是,分子密集程度和分子的平均动能B.决定理想气体压强的是,分子平均动能和分子种类C.质量相同的0C︒的水和0C︒的冰具有相同的内能D.一定质量的理想气体绝热自由膨胀过程,内能一定减少3.下列过程中可能发生的是()A.将两瓶不同液体混合,然后它们又自发地各自分开B.利用其他手段,使低温物体温度更低,高温物体的温度更高C.打开一高压密闭容器,其内气体自发溢出后又自发溢进去,恢复原状D.某种物质从高温热源吸收20kJ的热量,全部转化为机械能,而没有产生其他任何影响4.下面几幅图中,有关功与内能的说法中正确的是A.图1中迅速下压活塞,棉花会燃烧起来,说明热传递可以使物体的温度升高B.图2中重物下落带动叶片转动,由于叶片向水传递热量而使水的温度升高C.图3中降落的重物使发电机发电,电流对水做功使水的温度升高D.做功和热传递都可以使物体的内能增加5.根据学过的热学中的有关知识,判断下列说法中正确的是()A.机械能可以全部转化为内能,内能也可以全部用来做功转化成机械能B.凡与热现象有关的宏观过程都具有方向性,在热传递中,热量只能从高温物体传递给低温物体,而不能从低温物体传递给高温物体C.尽管科技不断进步,热机的效率仍不能达到100%,制冷机却可以使温度降到-293 ℃D.第一类永动机违背能量守恒定律,第二类永动机不违背能量守恒定律,随着科技的进步和发展,第二类永动机可以制造出来6.关于永动机和热力学定律的讨论,下列叙述正确的是()A.第二类永动机违背能量守恒定律B.如果物体从外界吸收了热量,则物体的内能一定增加C.保持气体的质量和体积不变,当温度升高时,每秒撞击单位面积器壁的气体分子数增多D.做功和热传递都可以改变物体的内能,但从能的转化或转移的观点来看这两种改变方式没有区别7.如图所示,一定质量的理想气体密封在绝热(即与外界不发生热交换)容器中,容器内装有一可以活动的绝热活塞.今对活塞施以一竖直向下的压力F,使活塞缓慢向下移动一段距离后,气体的体积减小.若忽略活塞与容器壁间的摩擦力,则被密封的气体( )图13-2-4A.温度升高,压强增大,内能减少B.温度降低,压强增大,内能减少C.温度升高,压强增大,内能增加D.温度降低,压强减小,内能增加8.根据热力学定律和分子动理论可知,下列说法中正确的是( )A.已知阿伏加德罗常数和某物质的摩尔质量,一定可以求出该物质分子的质量B.满足能量守恒定律的宏观过程一定能自发地进行C.布朗运动就是液体分子的运动,它说明分子做永不停息的无规则运动D.当分子间距离增大时,分子间的引力和斥力同时减小,分子势能一定增大9.下列说法正确的是_________.A.布朗运动是液体分子的无规则运动B.只有外界对物体做功才能增加物体的内能C.功转变为热的实际宏观过程是可逆过程D.一定量的气体,在压强不变时,分子每秒对器壁单位面积平均碰撞次数随着温度降低而增加10.在下列叙述中,正确的是A.物体里所有分子动能的总和叫做物体的内能B.—定质量的气体,体积不变时,温度越高,气体的压强就越大C.对一定质量的气体加热,其内能一定增加D.随着分子间的距离增大分子间引力和斥力的合力一定减小11.如图所示,绝热容器中间用隔板隔开,左侧装有气体,右侧为真空.现将隔板抽掉,让左侧气体自由膨胀到右侧直至平衡,在此过程中()A.气体对外界做功,温度降低,内能减少B.气体对外界做功,温度不变,内能不变C.气体不做功,温度不变,内能不变D.气体不做功,温度不变,内能减少12.一定质量的理想气体,从状态a开始,经历ab、bc、ca三个过程回到原状态,其V-T 图像如图所示,其中图线ab的反向延长线过坐标原点O,图线bc平行于T轴,图线ca平行于V轴,则()A.ab过程中气体压强不变,气体从外界吸热B.bc过程中气体体积不变,气体不吸热也不放热C.ca过程中气体温度不变,气体从外界吸热D.整个变化过程中气体的内能先减少后增加13.下列说法正确的是()A.物体放出热量,其内能一定减小B.物体对外做功,其内能一定减小C.物体吸收热量,同时对外做功,其内能可能增加D.物体放出热量,同时对外做功,其内能可能不变14.研究表明,新冠病毒耐寒不耐热,温度在超过56℃时,30分钟就可以灭活。
《大学物理学》热力学基础练习题
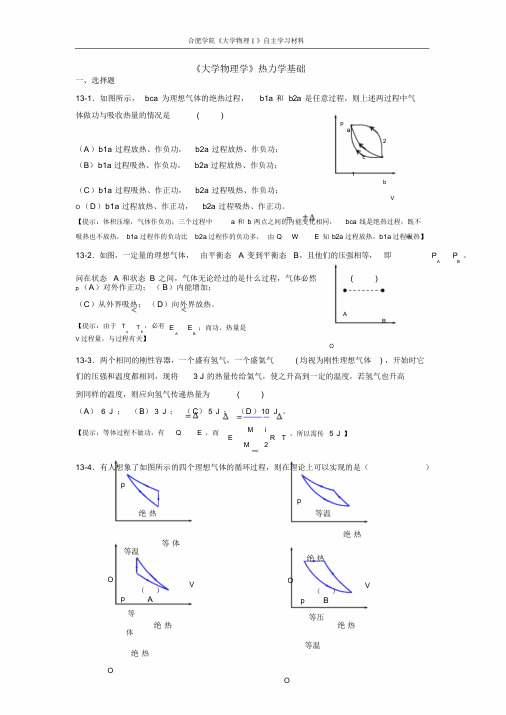
合肥学院《大学物理Ⅰ》自主学习材料《大学物理学》热力学基础一、选择题13-1.如图所示,bca 为理想气体的绝热过程,b1a 和b2a 是任意过程,则上述两过程中气体做功与吸收热量的情况是( )pa2(A)b1a 过程放热、作负功,b2a 过程放热、作负功;c(B)b1a 过程吸热、作负功,b2a 过程放热、作负功;1b(C)b1a 过程吸热、作正功,b2a 过程吸热、作负功;VO (D)b1a 过程放热、作正功,b2a 过程吸热、作正功。
【提示:体积压缩,气体作负功;三个过程中 a 和b 两点之间的内能变化相同,bca 线是绝热过程,既不吸热也不放热,b1a 过程作的负功比b2a 过程作的负功多,由Q W E 知b2a 过程放热,b1a 过程吸热】13-2.如图,一定量的理想气体,由平衡态 A 变到平衡态B,且他们的压强相等,即P P 。
A B问在状态 A 和状态 B 之间,气体无论经过的是什么过程,气体必然( )p (A)对外作正功;(B)内能增加;(C)从外界吸热;(D)向外界放热。
AB【提示:由于T T ,必有A B E E ;而功、热量是A BV 过程量,与过程有关】O13-3.两个相同的刚性容器,一个盛有氢气,一个盛氦气( 均视为刚性理想气体) ,开始时它们的压强和温度都相同,现将 3 J 的热量传给氦气,使之升高到一定的温度,若氢气也升高到同样的温度,则应向氢气传递热量为( )(A) 6 J ;(B)3 J ;(C)5 J ;(D)10 J 。
【提示:等体过程不做功,有Q E ,而M iE R TM 2mol,所以需传 5 J 】13-4.有人想象了如图所示的四个理想气体的循环过程,则在理论上可以实现的是()pp绝热等温绝热等体等温绝热Op 等()AV Op()B等压V 绝热绝热体等温绝热OOVV ()C()D【提示:(A) 绝热线应该比等温线陡,(B)和(C)两条绝热线不能相交】热力学基础-1合肥学院《大学物理Ⅰ》自主学习材料13-5.一台工作于温度分别为327℃和27℃的高温热源与低温热源之间的卡诺热机,每经历一个循环吸热2000J,则对外做功()(A)2000 J ;(B)1000 J ;(C)4000 J ;(D)500 J 。
大学物理热学部分习题

热学部分大作业选择题:1.如图,一定量的理想气体,由平衡状态A变到平衡状态B (p A= p B),则无论经过的是什么过程,系统必然对外作正功.(B) 内能增加.(A)(C) 从外界吸热.(D) 向外界放热.2.设有以下一些过程:(1) 两种不同气体在等温下互相混合.(2) 理想气体在定体下降温.(3) 液体在等温下汽化.(4) 理想气体在等温下压缩.(5) 理想气体绝热自由膨胀.在这些过程中,使系统的熵增加的过程是:(A) (1)、(2)、(3). (B) (2)、(3)、(4).(C) (3)、(4)、(5). (D) (1)、(3)、(5).3.一容器贮有某种理想气体,其分子平均自由程为0λ,若气体的热力学温度降到原来的一半,但体积不变,分子作用球半径不变,则此时平均自由程为(A) 02λ.(B)λ.(C) 2/λ.(D)λ/ 2.4.如图所示,一绝热密闭的容器,用隔板分成相等的两部分,左边盛有一定量的理想气体,压强为p0,右边为真空.今将隔板抽去,气体自由膨胀,当气体达到平衡时,气体的压强是(A) p0.(B) p0 / 2.(C)2γp0.(D) p0 / 2γ.(=γCp/C V)5.一绝热容器,用质量可忽略的绝热板分成体积相等的两部分.两边分别装入质量相等、温度相同的H2气和O2气.开始时绝热板P固定.然后释放之,板P将发生移动(绝热板与容器壁之间不漏气且摩擦可以忽略不计),在达到新的平衡位置后,若比较两边温度的高低,则结果是:(A) H2气比O2气温度高.(B) O2气比H2气温度高.(C)两边温度相等且等于原来的温度.(D) 两边温度相等但比原来的温度降低了.6.人设计一台卡诺热机(可逆的).每循环一次可从400 K的高温热源吸热1800 J,向300 K的低温热源放热800 J.同时对外作功1000 J,这样的设计是(A) 可以的,符合热力学第一定律.(B) 可以的,符合热力学第二定律.(C) 不行的,卡诺循环所作的功不能大于向低温热源放出的热量.(D) 不行的,这个热机的效率超过理论值.7. 1 mol刚性双原子分子理想气体,当温度为T时,其内能为(A)RT23.(B)kT23.(C) RT 25. (D) kT 25.(式中R 为普适气体常量,k 为玻尔兹曼常量)8. 理想气体经历如图所示的abc 平衡过程,则该系统对外作功W ,从外界吸收的热量Q 和内能的增量E ∆的正负情况如下: (A) ΔE >0,Q >0,W <0.(B) ΔE >0,Q >0,W >0. (C) ΔE >0,Q <0,W <0.(D) ΔE <0,Q<0,W <0. 9. 某理想气体状态变化时,内能随体积的变化关系如图中AB 直线所示.A →B 表示的过程是 (A) 等压过程. (B) 等体过程.(C) 等温过程. (D) 绝热过程.10. 一定量理想气体经历的循环过程用V -T 曲线表示如图.在此循环过程中,气体从外界吸热的过程是 (A) A →B . (B) B →C .(D) B →C 和B →C .T ,气体分子的质量为m .根据理想气x 方向的分量平方的平均值(A) m kT x 32=v . (B) m kT x 3312=v . (C) m kT x /32=v . (D) m kT x /2=v .12. 玻尔兹曼分布律表明:在某一温度的平衡态,(1) 分布在某一区间(坐标区间和速度区间)的分子数,与该区间粒子的能量成正比.(2) 在同样大小的各区间(坐标区间和速度区间)中,能量较大的分子数较少;能量较小的分子数较多.(3) 在大小相等的各区间(坐标区间和速度区间)中比较,分子总是处于低能态的概率大些.(4) 分布在某一坐标区间内、具有各种速度的分子总数只与坐标区间的间隔成正比,与粒子能量无关.以上四种说法中,(A) 只有(1)、(2)是正确的.(B) 只有(2)、(3)是正确的.(C) 只有(1)、(2)、(3)是正确的.(D) 全部是正确的.13. 两个完全相同的气缸内盛有同种气体,设其初始状态相同,今使它们分别作绝热压缩至相同的体积,其中气缸1内的压缩过程是非准静态过程,而气缸2内的压缩过程则是准静态过程.比较这两种情况的温度变化:(A) 气缸1和2内气体的温度变化相同.(B) 气缸1内的气体较气缸2内的气体的温度变化大.(C) 气缸1内的气体较气缸2内的气体的温度变化小.(D) 气缸1和2内的气体的温度无变化.14. 根据热力学第二定律判断下列哪种说法是正确的.(A) 热量能从高温物体传到低温物体,但不能从低温物体传到高温物体.(B) 功可以全部变为热,但热不能全部变为功.(C) 气体能够自由膨胀,但不能自动收缩.(D) 有规则运动的能量能够变为无规则运动的能量,但无规则 pO V a b c V O pOV b1 2 ac运动的能量不能变为有规则运动的能量.15. 如图,bca 为理想气体绝热过程,b 1a 和b 2a 是任意过程,则上述两过程中气体作功与吸收热量的情况是:(A) b 1a 过程放热,作负功;b 2a 过程放热,作负功.(B) b 1a 过程吸热,作负功;b 2a 过程放热,作负功.(C) b 1a 过程吸热,作正功;b 2a 过程吸热,作负功.(D) b 1a 过程放热,作正功;b 2a 过程吸热,作正功.16. 热力学第二定律表明:(A) 不可能从单一热源吸收热量使之全部变为有用的功.(B) 在一个可逆过程中,工作物质净吸热等于对外作的功.(C) 摩擦生热的过程是不可逆的.(D) 热量不可能从温度低的物体传到温度高的物体.17. 设有下列过程:(1) 用活塞缓慢地压缩绝热容器中的理想气体.(设活塞与器壁无摩擦)(2) 用缓慢地旋转的叶片使绝热容器中的水温上升.(3) 一滴墨水在水杯中缓慢弥散开.(4) 一个不受空气阻力及其它摩擦力作用的单摆的摆动.其中是可逆过程的为(A) (1)、(2)、(4).(B) (1)、(2)、(3).(C) (1)、(3)、(4).(D) (1)、(4).18. 某理想气体分别进行了如图所示的两个卡诺循环:Ⅰ(abcda )和Ⅱ(a'b'c'd'a'),且两个循环曲线所围面积相等.设循环I的效率为η,每次循环在高温热源处吸的热量为Q ,循环Ⅱ的效率为η′,每次循环在高温热源处吸的热量为Q ′,则(A) η < η′, Q < Q ′. (B) η < η′, Q > Q ′.(C) η > η′, Q < Q ′. (D) η > η′, Q > Q ′.19. 一物质系统从外界吸收一定的热量,则(A) 系统的内能一定增加.(B) 系统的内能一定减少.(C) 系统的内能一定保持不变.(D) 系统的内能可能增加,也可能减少或保持不变.20. 一定量的理想气体,从p -V 图上初态a 经历(1)或(2)过程到达末态b ,已知a 、b 两态处于同一条绝热线上(图中虚线是绝热线),则气体在(A) (1)过程中吸热,(2) 过程中放热. (B) (1)过程中放热,(2) 过程中吸热. (C) 两种过程中都吸热.(D) 两种过程中都放热.21. 气缸中有一定量的氮气(视为刚性分子理想气体),经过绝热压缩,使其压强变为原来的2倍,问气体分子的平均速率变为原来的几倍?(A) 22/5. (B) 22/7.(C) 21/5. (D) 21/7.填空题1. 已知f (v )为麦克斯韦速率分布函数,N 为总分子数,则(1) 速率v > 100 m ·s -1的分子数占总分子数的百分比的表达式为_________; V p O a b cda 'b 'c 'd 'p V(2) 速率v > 100 m ·s -1的分子数的表达式为__________________.2. 当理想气体处于平衡态时,若气体分子速率分布函数为f (v ),则分子速率处于最概然速率v p 至∞范围内的概率△N / N =________________.3. 如图,温度为T 0,2 T 0,3 T 0三条等温线与两条绝热线围成三个卡诺循环:(1) abcda ,(2) dcefd ,(3) abefa ,其效率分别为 η1____________,η2____________,η 3 ____________.4. 1 mol 的单原子分子理想气体,在1 atm 的恒定压强下,从0℃加热到100℃,则气体的内能改变了_______________J .(普适气体常量R =8.31 J ·mol -1·K -1 )5. 如图所示,一定量的理想气体经历a →b →c 过程,在此过程中气体从外界吸收热量Q ,系统内能变化∆E ,请在以下空格内填上>0或<0或= 0:Q _____________,∆E ___________. 6. 一定量理想气体,从同一状态开始使其体积由V 1膨胀到2V 1,分别经历以下三种过程:(1) 等压过程;(2) 等温过程;(3)绝热过程.其中:__________过程气体对外作功最多;____________过程气体内能增加最多;__________过程气体吸收的热量最多.7. 一热机从温度为 727℃的高温热源吸热,向温度为 527℃的低温热源放热.若热机在最大效率下工作,且每一循环吸热2000 J ,则此热机每一循环作功_________________ J .8. 在推导理想气体压强公式中,体现统计意义的两条假设是(1) ______________________________________________________;(2) ______________________________________________________.9. 有一卡诺热机,用290 g 空气为工作物质,工作在27℃的高温热源与 -73℃的低温热源之间,此热机的效率η=______________.若在等温膨胀的过程中气缸体积增大到2.718倍,则此热机每一循环所作的功为_________________.(空气的摩尔质量为29×10-3kg/mol ,普适气体常量R =8.31 11K mol J --⋅⋅)10. 从分子动理论导出的压强公式来看, 气体作用在器壁上的压强, 决定于______________________和_______________________.11. 已知一定量的理想气体经历p -T 图上所示的循环过程,图中各过程的吸热、放热情况为:(1) 过程1-2中,气体__________.(2) 过程2-3中,气体__________.(3) 过程3-1中,气体__________. 计算题 1. 容器内有11 kg 二氧化碳和2 kg 氢气(两种气体均视为刚性分子的理想气体),已知混合气体的内能是8.1×106 J .求:(1) 混合气体的温度;(2) 两种气体分子的平均动能.(二氧化碳的M mol =44×10-3 kg ·mol -1 ,玻尔兹曼常量k =1.38×10-23 J ·K -1摩尔气体常量R =8.31 J ·mol -1·K -1 )[ T =300 K ; kT252=ε=1.04×10-20 J ]2. 一定量的刚性双原子分子理想气体,开始时处于压强为 p 0 = 1.0×105 Pa ,体积为V 0 =4×10-3 m 3,温度为T 0 = 300 K 的初态,后经等压膨胀过程温度上升到T 1 = 450 K ,再经绝热过程温度降回到T 2 = 300 K ,求气体在整个过程中对外作的功.[ W =700 J . ] p O3T 02T 0T 0f a d b c e p V p T O 1 2 33. 温度为25℃、压强为1 atm 的1 mol 刚性双原子分子理想气体,经等温过程体积膨胀至原来的3倍. (普适气体常量R =8.31 1--⋅⋅K mol J 1,ln 3=1.0986)(1) 计算这个过程中气体对外所作的功.(2) 假若气体经绝热过程体积膨胀为原来的3倍,那么气体对外作的功又是多少?[W= 2.72×103 J ; W =2.20×103 J ]4. 容器内有M = 2.66 kg 氧气,已知其气体分子的平动动能总和是E K =4.14×105 J ,求:(1) 气体分子的平均平动动能;(2) 气体温度.(阿伏伽德罗常量N A =6.02×1023 /mol ,玻尔兹曼常量k =1.38×10-23 J ·K -1 )[ 211027.8-⨯=w J ;k wT 32== 400 K ] 5. 一定量的某种理想气体,开始时处于压强、体积、温度分别为p 0=1.2×106 Pa ,V 0=8.31×10-3m 3,T 0 =300 K 的初态,后经过一等体过程,温度升高到T 1 =450 K ,再经过一等温过程,压强降到p = p 0的末态.已知该理想气体的等压摩尔热容与等体摩尔热容之比C p /C V =5/3.求:(1) 该理想气体的等压摩尔热容C p 和等体摩尔热容C V .(2) 气体从始态变到末态的全过程中从外界吸收的热量.(普适气体常量R = 8.31 J·mol -1·K -1) [ R C p 25= 和 RC V 23= ; Q = △E +W =1.35×104 J .]6. 理想气体作卡诺循环,高温热源的热力学温度是低温热源的热力学温度的n 倍,求气体在一个循环中将由高温热源所得热量的多大部分交给了低温热源. [ n Q Q 112= ] 7. 一超声波源发射超声波的功率为10 W .假设它工作10 s ,并且全部波动能量都被1 mol氧气吸收而用于增加其内能,则氧气的温度升高了多少?(氧气分子视为刚性分子,普适气体常量R =8.31 J ·mol -1·K -1 )[ ∆T =4.81 K . ]8. 1 kg 某种理想气体,分子平动动能总和是1.86×106 J ,已知每个分子的质量是3.34×10-27 kg ,试求气体的温度.(玻尔兹曼常量 k =1.38×10-23 J ·K -1)[k w T 32== 300 K ] 9. 有ν 摩尔的刚性双原子分子理想气体,原来处在平衡态,当它从外界吸收热量Q 并对外作功A 后,又达到一新的平衡态.试求分子的平均平动动能增加了多少.(用ν、Q 、A和阿伏伽德罗常数N A 表示)[23=∆w k ∆T =3(Q -A ) / (5ν N A ) 式中N A 为阿伏伽德罗常数. ] 10. 容积V =1 m 3的容器内混有N 1=1.0×1025个氢气分子和N 2=4.0×1025个氧气分子,混合气体的温度为 400 K ,求:(1) 气体分子的平动动能总和.(2) 混合气体的压强. (普适气体常量R =8.31 J ·mol -1·K -1 ) 【 51014.4⨯=K E J ; p = n kT =2.76×105 Pa 】11. 以氢(视为刚性分子的理想气体)为工作物质进行卡诺循环,如果在绝热膨胀时末态的压强p 2是初态压强p 1的一半,求循环的效率.[ %18112=-=T T η ]12. 将1 kg 氦气和M kg 氢气混合,平衡后混合气体的内能是2.45×106 J ,氦分子平均动能是 6×10-21 J ,求氢气质量M . [ 51.02H =M kg ]热学部分习题解答一、选择题:1. B2. D3. B4. B5. B6. D7. C8. B9. A 10. A 11. D 12. B 13. B14. C 15. B 16. C 17. D 18. B 19. D 20. B 21. D二、填空题:1. [ (1) ⎰∞100d )(vv f (2) ⎰∞100d )(vv Nf] 2. [⎰∞p f v v v d )(]3. [33.3% ; 50% ;66.7% ]4. [1.25×103J]5. [>0; >0]6. [等压;等压;等压]7. [400J ]8. [(1) 沿空间各方向运动的分子数目相等; (2) 222zy x v v v == ] 9. [ 33.3% ; 8.31×103 J ]10. [单位体积内的分子数n ; 分子的平均平动动能 ]11. [ 吸热 ; 放热 ; 放热 ]三、计算题:1. 解:(1) RTM M i RT M M i E 2mol 221mol 1122+= RM M i M M i E/T ⎪⎪⎭⎫ ⎝⎛+=2mol 221mol 1122=300 K(2) kT 261=ε=1.24×10-20 JkT 252=ε=1.04×10-20 J2. 解:等压过程末态的体积 1001T T V V =等压过程气体对外作功)1()(01000101-=-=T T V p V V p W =200 J根据热力学第一定律,绝热过程气体对外作的功为W 2 =-△E =-νC V (T 2-T 1)这里 000RT V p =ν,R C V 25=,则 500)(25120002==--=T T T V p W J气体在整个过程中对外作的功为 W = W 1+W 2 =700 J .3. 解:(1) 等温过程气体对外作功为⎰⎰===000333ln d d V V V V RT V V RT V p W 2分=8.31×298×1.0986 J = 2.72×103 J 2分 (2) 绝热过程气体对外作功为V V V p V p W V V V V d d 00003003⎰⎰-==γγRT V p 1311131001--=--=--γγγγ2分 =2.20×103 J2分 4. 解:(1) M / M mol =N / N A∴ N =MN A / M mol21A mol 1027.8-⨯===MN E M N E w K k J3分 (2) k wT 32== 400 K2分 5. 解:(1) 由 35=V p C C 和 R C C V p =-可解得 R C p 25= 和 R C V 23= 2分(2) 该理想气体的摩尔数 ==000RT V p ν 4 mol在全过程中气体内能的改变量为 △E =ν C V (T 1-T 2)=7.48×103 J2分 全过程中气体对外作的功为 011lnp p RT W ν= 式中 p 1 ∕p 0=T 1 ∕T 0则 30111006.6ln ⨯==T T RT W ν J . 2分 全过程中气体从外界吸的热量为 Q = △E +W =1.35×104 J . 2分6. 解:理想气体卡诺循环的效率 121T T T -=η1分 ∵ 21nT T = n 11-=η1分 又据 n Q Q 11112-=-=η1分得 n Q Q 112= 2分7. 解: A = Pt = T iR v ∆21, 2分∴ ∆T = 2Pt /(v iR )=4.81 K . 3分8. 解: N = M / m =0.30×1027 个 1分==N E w K / 6.2×10-21 J 1分k wT 32== 300 K 3分 9. 解:设两个平衡态的温度差为∆T ,则Q -A =∆E =25νR ∆T =25ν N A k ∆T 3分∴23=∆w k ∆T =3(Q -A ) / (5ν N A ) 2分式中N A 为阿伏伽德罗常数. 10. 解:(1) 211028.823-⨯==kT w J()5211014.423⨯=+==kT N N w N E K J (2) p = n kT =2.76×105 Pa 11. 解:根据卡诺循环的效率121T T -=η 1分 由绝热方程:212111T p T p --=γγ 1分 得 γγ11212)(-=p p T T氢为双原子分子, 40.1=γ, 由2112=p p 1分 得82.012=T T 1分 %18112=-=T T η 1分12. 解:kT w 23= 29032==k w T K5m o l He He 1004.923⨯==RT M M E J2分而 6He H 1055.12⨯=-=E E E J 又RT M ME mol H 252= ∴ 51.02H =M kg 3分。
哈工大热力学大作业

黑体辐射杨威1221102 1122110212摘要:黑体辐射问题是经典物理学遇到的极大的挑战,普朗克利用能量子假设成功的解决了这一问题,从而引发了物理学重大的变革。
本文主要就黑体辐射问题的来源、普朗克如何解决问题加以介绍。
关键词:黑体辐射、紫外灾难、普朗克、能量子假设一、问题来源与困难1.1热辐射的基本概念一切物质的分子都包含带电粒子,分子的热运动导致物体不断地向外发射电磁波,我们称它为热辐射。
一切温度高于绝对零度的物体都能产生热辐射,温度越高,辐射出的总能量就越大,短波成分也越多。
我们定义辐射出射度M(T)为在温度为T时,单位时间内从辐射源表面单位面积上辐射出的能量的总和。
单位波长间隔内的辐射出射度称单色辐射出射度,用Mλ(T)表示。
物体除了能发射电磁波,同时还能吸收或反射电磁波,我们定义单色吸收比为物体吸收单位波长内电磁波能量与相应波长入射电磁波能量之比,用αλ(T)表示。
德国物理学家基尔霍夫于1859年提出了热辐射定律,它用于描述物体的辐射与吸收比之间的关系。
表示如下:Mλ(T)⁄=Iλ(T)αλ(T)其中Iλ(T)是温度和波长的函数,与物体的具体形式无关。
1.2黑体在任何条件下,对任何波长的外来辐射完全吸收而无反射的物体,即吸收比为1的物体就称为绝对黑体,简称为黑体。
事实上当然不存在绝对黑体,但有些物体可以近似地作为黑体来处理,比如,一束光一旦从狭缝射入空腔体内,就很难再通过该狭缝反射回来,那么这个开着狭缝的空腔体就可以看作是黑体。
根据基尔霍夫热辐射定律,由于Iλ(T)与物体的具体形式无关,当αλ(T)为1时,Mλ(T)达到最大,所以黑体既是吸收能量最强的物体也是辐射能力最强的物体。
1.3实验现象物理学家根据黑体模型得到了黑体辐射的实验现象,如下图1所示。
1879年,斯特藩根据实验曲线总结出一个定律:黑体的辐射出射度与黑体的绝对温度四次方成正比,即M (T )=σT 4,称为斯特藩-玻耳兹曼定律。
大学物理习题详解 热力学第二定律

©物理系_2012_09《大学物理AII 》作业 No.12 热力学第二定律一、判断题:(用“T ”和“F ”表示)[ T ] 1.任何可逆热机的效率均可表示为:高低T T -=1η 解:P301,根据卡诺热机的效率[ F ] 2.若要提高实际热机的效率, 可采用摩尔热容量较大的气体做为工作物质。
解:P294-295,根据热机效率的定义吸净Q A =η,显然工作物质从高温热源吸收的热量越少,对外作的功越多,其效率越高。
根据热量的定义T C MmQ ∆=,温差一定的时候,摩尔热熔C 与热量成正比。
[ F ] 3.一热力学系统经历的两个绝热过程和一个等温过程,可以构成一个循环过程 解:P308题知循环构成了一个单热源机,这违反了开尔文表述。
[ F ] 4.不可逆过程就是不能沿相反方向进行的过程。
解:P303 [ T ] 5.一定量的理想气体向真空作绝热自由膨胀,体积由1V 增至2V ,在此过程中A =0,Q =0,0=∆T ,0>∆S 。
解:P292,P313二、选择题:1.如果卡诺热机的循环曲线所包围的面积从图中的a b c d a 增大为 a b ′c ′d a ,那么循环a b c d a 与a b ′c ′d a 所作的功和热机效率变化情况是: [ D ] (A) 净功增大,效率提高(B) 净功增大,效率降低(C) 净功和效率都不变 (D) 净功增大,效率不变 解:卡诺循环的效率121T T-=η只与二热源温度有关,曲线所围面积在数值上等于净功,所以净功增大,效率不变。
2.对于循环热机,在下面节约与开拓能源的几个设想中,理论上可行的是: [ B ] (A) 改进技术,使热机的循环效率达100%(B) 利用海面与海面下的海水温差进行热机循环作功 (C) 从一个热源吸热,不断作等温膨胀,对外作功 (D) 从一个热源吸热,不断作绝热膨胀,对外作功解:根据热力学第二定律,(A)是第二类永动机,是不可能制成的;(C)是单热源机;(D)是从热源吸热怎么作绝热膨胀。
(完整版)大学物理热学习题附答案

一、选择题1.一定量的理想气体贮于某一容器中,温度为T ,气体分子的质量为m 。
根据理想气体的分子模型和统计假设,分子速度在x 方向的分量平方的平均值 (A) m kT x 32=v (B) m kT x 3312=v (C) m kT x /32=v (D) m kT x /2=v2.一定量的理想气体贮于某一容器中,温度为T ,气体分子的质量为m 。
根据理想气体分子模型和统计假设,分子速度在x 方向的分量的平均值 (A) m kT π8=x v (B) m kT π831=x v (C) m kT π38=x v (D) =x v 03.温度、压强相同的氦气和氧气,它们分子的平均动能ε和平均平动动能w 有如下关系:(A) ε和w都相等 (B) ε相等,w 不相等 (C) w 相等,ε不相等 (D) ε和w 都不相等4.在标准状态下,若氧气(视为刚性双原子分子的理想气体)和氦气的体积比V 1 / V 2=1 / 2 ,则其内能之比E 1 / E 2为:(A) 3 / 10 (B) 1 / 2 (C) 5 / 6 (D) 5 / 35.水蒸气分解成同温度的氢气和氧气,内能增加了百分之几(不计振动自由度和化学能)?(A) 66.7% (B) 50% (C) 25% (D) 06.两瓶不同种类的理想气体,它们的温度和压强都相同,但体积不同,则单位体积内的气体分子数n ,单位体积内的气体分子的总平动动能(E K /V ),单位体积内的气体质量ρ,分别有如下关系:(A) n 不同,(E K /V )不同,ρ不同 (B) n 不同,(E K /V )不同,ρ相同(C) n 相同,(E K /V )相同,ρ不同 (D) n 相同,(E K /V )相同,ρ相同7.一瓶氦气和一瓶氮气密度相同,分子平均平动动能相同,而且它们都处于平衡状态,则它们(A) 温度相同、压强相同 (B) 温度、压强都不相同(C) 温度相同,但氦气的压强大于氮气的压强(D) 温度相同,但氦气的压强小于氮气的压强8.关于温度的意义,有下列几种说法:(1) 气体的温度是分子平均平动动能的量度;(2) 气体的温度是大量气体分子热运动的集体表现,具有统计意义;(3) 温度的高低反映物质内部分子运动剧烈程度的不同;(4) 从微观上看,气体的温度表示每个气体分子的冷热程度。
热力学习题——精选推荐

热⼒学习题⼤学物理精品课程热⼒学习题⼀、选择题:1.在下列说法中,哪些是正确的()(1)可逆过程⼀定是平衡过程. (2)平衡过程⼀定是可逆的.(3)不可逆过程⼀定是⾮平衡过程. (4)⾮平衡过程⼀定是不可逆的.(A) (1)、 (4). (B) (2)、(3).(C) (1)、 (2)、(3)、(4). (D) (1)、 (3).2.⼀定量的理想⽓体,开始时处于压强,体积,温度分别为的平衡态,后来变到压强,体积,温度分别为的终态.若已知>,且111,,T V p 222,,T V p 2V 1V 12T T =,则以下各种说法中正确的是()(A)不论经历的是什么过程,⽓体对外净作的功⼀定为正值.(B)不论经历的是什么过程,⽓体从外界净吸的热⼀定为正值.(C)若⽓体从始态变到终态经历的是等温过程,则⽓体吸收的热量最少.(D)如果不给定⽓体所经历的是什么过程,则⽓体在过程中对外净作功和从外界净吸热的正负皆⽆法判断.3.⼀定量的理想⽓体,从a 态出发经过①或②过程到达b态,a c b 为等温线(如图),则①、②两过程中外界对系统传递的热量、是()1Q 2Q 1(A) >0,>0. (B)<0,<0. 1Q 2Q 1Q 2Q (C) >0,<0. (D) <0,>0.1Q 2Q 1Q 2Q 4.两个卡诺热机的循环曲线如图所⽰,⼀个⼯作在温度为T 与的两个热源之间,另⼀个⼯作在温度为T 与T 的两个热源之间,已知这两个循环曲线所包围的⾯积相等.由此可知()13T 23(A)两个热机的效率⼀定相等.(B)两个热机从⾼温热源所吸收的热量⼀定相等.(C)两个热机向低温热源所放出的热量⼀定相等.(D)两个热机吸收的热量与放出的热量(绝对值)的差值⼀定相等.5.所列四图分别表⽰某⼈设想的理想⽓体的四个循环过程.请选出其中⼀个在物理上可能实现的循环过程的图的标号()6.设有以下⼀些过程:(1)两种不同⽓体在等温下互相混合. (2)理想⽓体在定容下降温.(3)液体在等温下汽化. (4)理想⽓体在等温下压缩.(5)理想⽓体绝热⾃由膨胀.在这些过程中,使系统的熵增加的过程是()(A) (1)、(2)、(3). (B) (2)、(3)、(4).(C) (3)、(4)、(5). (D) (!)、(3)、(5).7.⼀绝热容器被隔板分成两半,⼀半是真空,另⼀半是理想⽓体.若把隔板抽出,⽓体将进⾏⾃由膨胀,达到平衡后()(A)温度不变,熵增加. (B)温度升⾼,熵增加.(C)温度降低,熵增加. (D)温度不变,熵不变.2e d c →→e c →→8.如图所⽰,设某热⼒学系统经历⼀个由的过程,其中,ab 是⼀条绝热曲线,、在该曲线上.由热⼒学定律可知,该系统在过程中()(A)不断向外界放出热量. (B)不断从外界吸收热量.(C)有的阶段吸热,有的阶段放热,整个过程中吸的热量等于放出的热量.(D)有的阶段吸热,有的阶段放热,整个过程中吸的热量⼤于放出的热量.(E)有的阶段吸热,有的阶段放热,整个过程中吸的热量⼩于放出的热量.9.如图所⽰,设某热⼒学系统经历⼀个由b 的准静态过程,a、b 两点在同⼀条绝热线上.该系统在过程中()a c a cb →→(A)只吸热,不放热. (B)只放热,不吸热.(C)有的阶段吸热,有的阶段放热,净吸热为正值.(D)有的阶段吸热,有的阶段放热,净吸热为负值.10.⽓缸中有⼀定量的氦⽓(视为理想⽓体),经过绝热压缩,体积变为原来的⼀半,问⽓体分⼦的平均速率变为原来的⼏倍() (A) 522 (B) 512 (C) 322 (D) 312⼆、填空题:1.⽤绝热材料制成的⼀个容器,体积为,被绝热板隔成A、B 两部分,A 内储有1 mol 单原⼦理想⽓体,B 内储有2mol 双原⼦理想⽓体,A、B 两部分压强相等均为,两部分体积均为V ,则02V 0p 0(1)两种⽓体各⾃的内能分别为 =A E ;=B E ;(2)抽去绝热板,两种⽓体混合后处于平衡时的温度为T= .2.某种⽓体(视为理想⽓体)在标准状态下的密度为0894.0=ρkg/3m ,则该⽓体的定压摩尔热容 =p C ,定容摩尔热容=v C .(摩尔⽓体常量)-11K J 31.8??=?mol R 3.同⼀种理想⽓体的定压摩尔热容⼤于定容摩尔热容,其原因是 p C v C . 4.处于平衡态A 的热⼒学系统,若经准静态等容过程变到平衡态B,将从外界吸收热量416J,若经准静态等压过程变到与平衡态B 有相同温度的平衡态C,将从外界吸收热量582J.所以,从平衡态A 变到平衡态C 的准静态等压过程中系统对外界所作的功为.5.⼀定量的某种理想⽓体在等压过程中对外作功为200J,若此种⽓体为单原⼦分⼦⽓体,则该过程中需吸热 J;若为双原⼦分⼦⽓体,则需吸热 J.6.1mol 理想⽓体(设v p C =γ为已知)的循环过程如T—V 图所⽰,其中CA 为绝热过程,A 点状态参量()和B 点的状态参量()为已知.试求C 点的状态参量:11,V T 21,VT =c V ,=c T ,=c P . 7.所谓第⼆类永动机是指,它不可能制成是因为违背了.三、计算题:1.温度为25℃、压强为1 a t m 的1 mol 刚性双原⼦分⼦理想⽓体,经等温过程体积膨胀⾄原来的3倍.(1)计算这个过程中⽓体对外所作的功.(2)假若⽓体经绝热过程体积膨胀为原来的3倍,那么⽓体对外作的功⼜是多少?(摩尔⽓体常量,-11K J 31.8??=?mol R 0986.13ln =)2.如图所⽰,C 是固定的绝热壁,D 是可动活塞,C、D 将容器分成A、B 两部分.开始时A、B 两室中各装⼊同种类的理想⽓体,它们的温度T、体积V、压强p 均相同,并与⼤⽓压强相平衡.现对A、B 两部分⽓体缓慢地加热,当对A 和B 给予相等的热量Q 以后,A 室中⽓体的温度升⾼度数与B 室中⽓体的温度升⾼度数之⽐为7∶5,(1)求该⽓体的定容摩尔热容和定压摩尔热容.V C p C (2)B 室中⽓体吸收的热量有百分之⼏⽤于对外作功?3.汽缸内有2mol 氦⽓,初始温度为27℃,体积为20,先将氦⽓定压膨胀,直⾄体积加倍,然后绝热膨涨,直⾄回复初温为⽌.若把氦⽓视为理想⽓体.试求:l (1)在p—V 图上⼤致画出⽓体的状态变化过程.(2)在这过程中氦⽓吸热多少?(3) 氦⽓的内能变化多少?(4) 氦⽓所作的总功是多少?4. 1 mol 刚性双原⼦分⼦的理想⽓体,开始时处于,的状态.然后经图⽰直线过程I 变到,的状态.后⼜经过程⽅程为Pa 1001.151×=p 331m 10?=V Pa 1004.452×=p 332m 102?×=V C =2pV 1(常量)的过程Ⅱ变到压强的状态.求:Pa 1001.1513×==p p (1)在过程I 中⽓体吸的热量.(2)整个过程⽓体吸的热量.5.某理想⽓体在P—V 图上等温线与绝热线相交于A 点,如图。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
11
11 热力学
班号 学号 姓名 成绩
一、选择题
(在下列各题中,均给出了4个~6个答案,其中有的只有1个是正确答案,有的则有几个是正确答案,请把正确答案的英文字母序号填在题后的括号内)
1. 在下列说法中,正确的是: A .物体的温度愈高,则热量愈多; B .物体在一定状态时,具有一定的热量; C .物体的温度愈高,则其内能愈大;
D .物体的内能愈大,则具有的热量愈多。
(C ) [知识点] 内能和热量的概念。
[分析与解答] 内能是物体内部所有分子的热运动动能和分子间相互作用势能的总和,是系统状态(或温度)的单值函数,系统的温度愈高,其内能愈大。
热量是由于系统与外界温度不同而进行的传热过程中所传递的能量的多少,同样温差情况下,不同的传热过程其热量不同,热量是过程量,不是状态的函数。
作功与传热可以改变系统的内能,若系统状态不变(内能也不变),就无需作功与传热,功与热量不会出现。
2. 在下列表述中,正确的是:
A .系统由外界吸热时,内能必然增加,温度升高;
B .由于热量Q 和功A 都是过程量,因此,在任何变化过程中,(Q +A )不仅与系统的始末状态有关,而且与具体过程有关;
C .无摩擦的准静态过程中间经历的每一状态一定是平衡状态; D
能增量为T C M
m
E m p ∆=
∆,。
(C ) [知识点] 热量、作功和内能的概念。
[分析与解答] 根据热力学第一定律E A Q ∆+=,系统由外界吸热时,可以将吸收的热量全部对外作功,内能不变,等温过程就是这种情况。
p
系统所吸收的热量和外界对系统做功的总和为系统内能的增量,内能的增量仅与系统始末状态有关,而与过程无关。
准静态过程就是在过程进行中的每一个状态都无限地接近平衡态的过程。
由于准静态过程是无限缓慢的,无摩擦的(即无能量耗散),则各中间态都是平衡态。
无论何种过程,只要温度增量T ∆相同,内能增量均为
T R M m i E ∆=
∆2T R C M m
m V ∆=1
,与过程无关。
3. 一定量某理想气体,分别从同一状态开始经历等压、等体、等温过程。
若气体在上述过程中吸收的热量相同,则气体对外做功最多的过程是:
A .等体过程; B. 等温过程;
C. 等压过程;
D. 不能确定。
(B ) [知识点] 热力学第一定律在等值过程中的应用。
[分析与解答] 设在等压、等体和等温过程吸收的热量为0Q ,则 等压过程 T R i T C Q m p ∆+=∆=2
2
10ν
ν 00
2
2Q i Q T R V p A p <+=
∆=∆=ν 等体过程 0=Q A ,吸收的热量全部用于增加的内能 等温过程 0=T A ,吸收的热量全部用于对外做功
由热力学第一定律E A Q ∆+=知,等压过程,气体吸收来的热量既要对外做功,又要使内能增加;等体过程,气体不对外做功,吸收的热量全部用于增加内能;等温过程,气体吸收的热量全部用于对外做功。
因此,当吸收的热量相同时,等温过程对外做功最多。
4. 如图11-1所示,一定量理想气体从体积V 1膨胀到V 2,ab 为等压过程,ac 为等温过程,ad 为绝热过程,则吸热最多的是:
A .ab 过程; B. ac 过程;
C. ad 过程;
D. 不能确定。
(A ) [知识点] 热力学第一定律的应用。
[分析与解答] 由热力学第一定律E A Q ∆+=知
E
图11-2
图11-3
在ab 等压过程中, 21V abV p S A =,0>∆ab E 21V abV p p S A Q =>
在ac 等温过程中,21V acV T S A =,0=∆E 21V acV T T S A Q == 在ad 绝热过程中,0=Q
由图知,2121V acV V abV S S >,即0>>T p Q Q ,则ab 过程吸热最多。
5. 某理想气体状态变化时,内能随压强的变化关系如图11-2中的直线ab 所示,则a 到b 的变化过程一定是:
A .等压过程;
B .等体过程;
C .等温过程;
D .绝热过程。
(B ) [知识点]
E -p 图分析。
[分析与解答] 理想气体的内能为 pV i
RT i M m E 2
2==
只有当恒量=V 时,E 和p 才成线性关系,故ab 过程为等体过程。
6. 如图11-3所示,理想气体卡诺循环过程中两条绝热线下面的面积分别为S 1和S 2,则
A .S 1 > S 2;
B .S 1 < S 2;
C .S 1 = S 2;
D .无法确定。
(C )[知识点] 卡诺循环概念,热力学第一定律在绝热过程中的应用。
[分析与解答] 如图11-3所示,理想气体卡诺循环过程中两条绝热线下面的面积1S 表示绝热膨胀过程系统对外界所作的功,
2S 表示绝热压缩过程外界对系统所作的功。
绝热膨胀过程,0=Q ,系统对外界所作的功等于系统内能的减少。
()02
A 12<-=
∆-=T T R i
M m E 绝热压缩过程,0=Q ,外界对系统所做的功等于系统内能的增加。
图11-4
()02
A 12>-=
∆=-T T R i
M m E 比较可知,绝热膨胀过程系统对外界做功与绝热压缩过程外界对系统做功数值相等,则 21S S =
7. 某理想气体分别进行了如图11-4所示的两个卡诺循环Ⅰ)(abcda 和Ⅱ
)(a d c b a ''''',已知两低温热源的温度相等,且两循环曲线所围面积相等,设循环Ⅰ的效率
为η,从高温热源吸热Q ,循环Ⅱ的效率为η',从高温热源吸热Q '。
则
A .ηη'<,Q Q '<; B. ηη'>,Q Q '<;
C .ηη'<,Q Q '>; D. ηη'>,Q Q '>。
(C ) [知识点] 1
121Q A T T η=-
=卡。
[分析与解答] 两循环曲线所围面积相等,表示两循环过程对外做的净功相等。
两个卡诺循环的效率为
121T T η-=, 121T T η'
'
-='
由于22T T '=,11T T '<,则ηη'<。
再根据热机效率的定义有 吸Q A η=
,吸
Q A η''
='
由于两循环过程对外做的净功相等 A A '=,ηη>',则 Q Q <'。
8. 在热力学系统中,若高温热源的温度为低温热源温度的n 倍,以理想气体为工作物质的卡诺机工作于上述高、低温热源之间,则从高温热源吸收的热量与向低温热源放出的热量之比为:
A.
n n 1+; B. n
n 1
-; C. n ; D. 1-n 。
(C ) [知识点] 1
21211T T
Q Q η-=-
=。
[分析与解答] 对于卡诺循环有 1
21211T T
Q Q η-=-
=
若 21nT T =,1
211
1Q Q n η-=-
= 则从高温热源吸收的热量1Q 与向低温热源放出的热量2Q 之比为
n Q Q =2
1
9. 在下列有关热力学过程进行的方向和条件的表述中, 正确的是: A. 功可以全部转化为热量,但热量不能全部转化为功;
B. 热量可以从高温物体传到低温物体,但不能从低温物体传到高温物体; C .对封闭系统来讲,自发过程总是按系统熵值增加的方向进行;
D .对封闭系统来讲,其内部发生的过程,总是由概率小的宏观态向概率大的宏观态进行;
E. 不可逆过程就是不能向相反方向进行的过程;
F. 一切自发过程都是不可逆的。
(C 、D 、F ) [知识点] 热力学第二定律的概念。
[分析与解答] 热力学第二定律指出了热传导过程和热功转换过程的不可逆性,表述中强调的是“热量不能自动地从低温传到高温”和“热量不可能完全变为有用功而不产生其他影响”,例如等温膨胀,热可以完全转变为功。
自然界中自发的热力学过程都是不可逆过程;不可逆过程可以反向进行,但系统与外界无法复原;不可逆过程是一个由热力学概率小的状态向热力学概率大的状态转变的过程;孤立系统中的一切自发宏观过程总是沿着熵增大的方向进行。
10. 某理想气体的初始温度为T ,初始体积为V 。
气体取3个可逆过程构成一循环:绝热膨胀到2V ;等体过程到温度T ;等温压缩到初始体积V ,如图11-5所示,则下列叙述中正确的是:
A .在每个过程中,气体的熵不变;
B .在每个过程中,外界的熵不变;
C .在每个过程中,气体和外界的熵的和不变;
D .整个循环中,气体的熵增加。
(C ) [知识点] 熵增加原理的理解。
[分析与解答] 由题意知,图中的3个过程为可逆过程,即该循环也是可逆过程。
由熵增加原理知,孤立系统中的可逆过程,其熵不变。
则把气体和外界构成孤立体系,在以上3个可逆过程中,气体和外界的熵的和不变。
