化学立体化学基础
立体化学基础
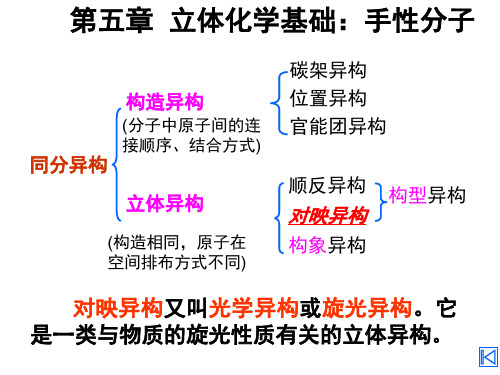
Cl大 HOCH2
Cl
键上,纸面 走向与实际
CH2Cl 走 向 相 同 ,
S-2,3-二氯丙醇
R-2,3-二氯丙醇
顺时针为R型, 逆时针为S型。
直接根据Fischer投影式命名的简便方法介绍
Problem 6: Give the names of the following compounds。(by R/S nomenclature)
有相等的距离。实物与镜像的关系叫对映关系。
镜面
实物与镜像
若实物与其镜像能够完全重合,则实物与镜像所 代表的两个分子为同一个分子。
OH
OH
CH H
CH3
HC H
CH3
OOHH
HH
CC HH 所有基团都重合 CCHH3 3
乙醇分子模型的重叠操作
对于某些分子,两个互为实物与镜像关系的分 子不能重合,如乳酸。
CO2H
CO2H
CO2H
NH2
NH2
H CH3
NH2 H
CH3 H
CO2H
CH3
H
NH2
CH3
即:固定*C上某个基团,其它三基团顺序轮换,不 改变其构型。
Problem 3: 下列Fischer式是否表示同一化合物?
COOH
CH2OH
H
OH
HO
H
--
CH2OH
COOH
镜 像
1
2
关
旋转180℃后可重叠
丙酸分子 的对称面
分子的对称面 具有对称面的分子为非手性分子
四、判断对映体的方法
1、看分子和它的镜像能不能重合。如果 不能重合,就具有对映异构现象。
2、寻找对称面和对称中心。如果分子没 有对称因素(对称面和对称中心),就 具有对映异构现象。
有机化学基础知识点整理立体化学基础概念

有机化学基础知识点整理立体化学基础概念有机化学基础知识点整理——立体化学基础概念引言:有机化学是研究碳元素化合物的构造、性质和变化的一门学科,而立体化学则是有机化学中重要的基础概念之一。
在有机化学中,分子的立体构型对于反应性、性质和生物活性有着重要影响。
本文将着重整理一些有机化学中的立体化学基础概念,以帮助读者更好地理解有机化学中的立体结构,进而对有机化学进行深入学习。
一、手性与手性中心手性是指分子或物体与其镜像体不可重合的性质。
在有机化学中,手性分子是指拥有手性中心或手性轴的分子。
手性中心是指一个碳原子上连接着四个不同基团的碳原子,它使得分子无法与自身的镜像体重合。
手性分子在光学活性、药物作用和化学性质等方面具有独特的特性。
二、立体异构与构象异构1. 立体异构立体异构是指分子的空间排列方式不同而产生的异构体。
常见的立体异构有以下两种类型:(1) 旋转异构:由于单键的自由旋转,骨架构型可以发生一定程度的旋转,产生旋转异构体。
(2) 互变异构:由于键的旋转受到某些限制,使分子无法通过旋转达到立体异构体之间的互变。
2. 构象异构构象异构是指分子在空间中采取不同的构象,但化学键没有发生断裂或形成新的键。
构象异构分为以下几种类型:(1) 键的旋转构象异构:分子在有某些限制的情况下,通过键的旋转而形成的构象异构。
(2) 环的变形构象异构:分子中含有环系统,通过环的弯曲或平面变形产生的构象异构。
(3) 键的翻转构象异构:分子中存在于键的两个端点之间的三个最佳位置,通过在这三个位置间进行翻转形成的构象异构。
三、立体化学的表示方法1. 常用的立体表示方法(1) 空间结构式:通过笛卡尔坐标系中的三维坐标表示分子的立体构型。
(2) 键切式:通过表示分子和化学键之间关系的切面图形来表示立体构型。
(3) 投影式:通过投影方式来表示立体构型,包括斜投影式、哈维利投影式等。
2. 立体异构体的命名方法(1) IUPAC命名法:使用希腊字母(R和S)来表示手性异构体,其中R表示顺时针方向,S表示逆时针方向。
化学第三章立体化学

C=Y
CY (Y) (C)
Y为C、O、N等常见原子,是几重键就相当于连几 个相同的原子。
H (C) CH CH2 相当于 C C H
(C) H
H(C) H(C)
相当于 (C)
H
( C)
(C)
H
H (C)
(C) (C) C CH 相当于 C C H
(C) (C)
(N) (C) C N 相当于 C N
H
H
CC C6H5
CH3 CC
H
H
(顺,顺)
H CC
C6H5
H H
CC
H
CH3
(顺,反)
H
C C6H5
H
CH3
CC
C
H
H
(反,反)
H
H
H
CC
CC
C6H5
H
CH3
(反,顺)
H
CH2CH3 CH3CH2
CH(CH3)2
CC
CC
CH3
CH2CH2CH3 CH3
CH2CH2CH3
(三) Z , E - 命名法
H5 4 H
CC
CH3
3 2H CC 1
H
COOH
(2E,4Z) – 2,4- 己二烯酸
(四)顺反异构体的性质(一般规律的比较)
顺、反-丁烯二酸的物理性质
异构体
熔点/℃ 密度
溶解度( 25℃) /(g/100g·H2
O)
顺-丁烯二酸 130
1.590
78.8
反-丁烯二酸 287
1.625
0.7
1.构造式(结构式)相同(分子的结构相同,构型不同)
2. 比较各种取代原子或原子团的排列顺序时,先比 较直接相连的第一个原子的原子序数。如果是相同 原子,那就再比较第二个、第三个……原子的原子 序数。 C(CH3)3 > CH(CH3)2 > CH2CH3 > CH3
立体化学基础.
丙 丙 异构
二,对映异构体和手性分子 (一)对映异构体和手性分子
下图为一对互为镜像关系的乳酸分子的立体结构式(透视式 : 下图为一对互为镜像关系的乳酸分子的立体结构式 透视式): 透视式
镜子 C2OH C HO H CH3
a
C2OH H C CH3 OH
b
a和b互为镜像的一对乳酸分子 实线代表位于纸平面上的键; 实线代表位于纸平面上的键; 虚线… 代表伸向纸平面后面的键, 虚线… 代表伸向纸平面后面的键, 楔形线代表伸向纸平面前方的键
第三章 立体化学基础
立体化学是现代有机化学的一个重要分支, 立体化学是现代有机化学的一个重要分支,是从三 维空间来研究有机物的结构以及结构与性质之间的关系. 维空间来研究有机物的结构以及结构与性质之间的关系. 一,同分异构现象 碳 链异 构
构 造异 构 异 构现 象 立 丙异 构
位 置异 构 官 能团 异构 互 变异 构 构 丙 异构 构 象 异构
12
可用不同的方法表示同一立体异构体的立体结构 三羟基丁醛: 例:2R, 3S-2, 3, 4-三羟基丁醛: 三羟基丁醛
CHO H OH HO H CH2OH HO H HOH OH CHO H CH2OH OHC CH2OH H OH
Fischer投影式 投影式
锯架式
Newman投影式 投影式
13
-CH3 < -CH2CH3 < -CH2CH2CH3 < -CH(CH3)2
H3C C2H5 H OH
-OH >-CH2CH3 >-CH3 > H
R-2-丁醇 丁醇
18
(3)若手性碳连有含重键的基团时,则可看 若手性碳连有含重键的基团时, 作多次与同一原子相连.例如: 作多次与同一原子相连.例如:
《有机化学(第二版)》第6章:立体化学基础

第六章
立体化学基础
19:21
第一节 顺反异构 一、顺式和反式 二、Z—型和E—型 三、顺反异构的性质
19:21
第一节 顺反异构
1、 顺反异构
重点介绍顺反异构体的Z/E标记法。 哪些化合物存在顺反异构体:
(1). 含有 C =C 、 C =N 、 N =N 双键的化合物。
(2). 环状化合物。
顺反异构现象。
顺反异构体的命名方法: 1. 顺/反标记法:
相同的原子或基团位于双键(或环平面)的同侧为“顺 式”; 否则为“反式”。
a C=C b b b a a C=C a b b b b a a a
19:21
b a
_ 顺式 (cis )
_ 反式 (trans )
_ 顺式 (cis )
_ 反式 (trans )
2. Z / E标记法:
该法是1968年IUPAC规定的系统命名法。
规定按“次序规则”,若优先基团位于双键的同侧为 Z
式(德文Zusammen的缩写,中文意为‘在一起’);否
a C=C b (Z)
c d
a c
b d
a C=C b (E)
d c
19:21
应用举例: 含C=C双键的化合物:
H Cl _ C=C H Cl H Cl C=C Cl H
翻 转
CO O H HO H C H3
翻 转
(2) 可以旋转n180。(n>=1),但不能旋转90。或270。。
19:21
CO O H H OH C H3
旋 转180
C H3 。 HO H CO O H
19:21
旋转180 。
CO O H H OH C H3
立体化学

COOH H (S) HO HO H (R) COOH
COOH
COOH HO H
(R) (S)
H H
OH OH COOH
(R) H (R) HO
OH H COOH
(S) H OH (S)
COOH
(I)
(I)
(2) (+)-酒石酸
(3) (-)-酒石酸
mp
[]D(水)
溶解度(g/100ml)
含有两个(或两个以上)手性碳原子的化合物透视 式、纽曼投影式和锯架式,实际上是这个化合物的 构象式。之所以可以用某一个构象式来表示分子的 构型,是由于构象比构型更为精细的缘故。
对于环状分子来说,通常的规定是随意地把环 表述为平面的(不管它们的真实形象),环上 取代基的取向就可参照透视法表示其取向。环 所在的平面可以在纸面上也可以与纸面相垂直。 例如反-1,2-二甲基环丁烷构型式为:
pKa1
pKa
(+)-酒石酸
(-)-酒石酸
170oc
170oc
+12.0
-12.0 0
139
139 20.6
2.98
2.98 2.96
4.23
4.23 4.24
()-酒石酸 (dl) 206oc
meso-酒石酸
140oc
0
125
3.11
4.80
3.分子构型的表示方法(构型式)及构型的标 记 构型的表示方法: 表示分子构型的化学式子叫做构型式。虽 然每种分子都具有确定的构型,在一般情况 下通常是用构造式来表示分子的结构,在讨 论分子与构型有关的性质时则必须应用构型 式。 构型的表示方法很多,最原始的方法就是 用凯库勒模型图(棍球式)。
立体化学基础笔记

立体化学基础笔记立体化学是有机化学中的重要分支之一,它探究分子中化学键的立体构型与空间关系,并以此为基础研究分子的反应性质和反应机制。
在理解立体化学之前,我们先来回顾一下化学键的本质。
化学键基础化学键是由原子间的电子相互作用而形成的连接,共价键是其中一种最常见的化学键。
共价键是两个原子之间共用一对电子,以达到每个原子的电子壳层的填满。
共价键的角度和键长是由多种因素决定的,包括原子的轨道混杂程度、原子间的间隔、原子间的电子云分布等。
因为这些因素的复杂性,实际上相同的原子对,在不同的化合物中形成的键的长度和角度都有所不同。
对于分子中含有多个原子的化合物来说,所有的原子的相对位置以及它们之间的键的相对位置规定了分子的结构,从而影响着反应的特性。
立体化学基础分子中化学键的立体构型有时被称为分子的空间取向。
立体取向对于分子的各种反应起到关键的作用。
例如,在糖的立体构型中,差异仅仅在于单个羟基或氢原子的位置,但这种稍微的变化引起了巨大的影响。
当人体消化食物时,他的消化系统会针对特定的立体形态进行分解,并且对于其他立体异构体则不同程度地吸收和代谢。
立体异构体分子中的立体异构体是由同种原子的连接方式不同而引起的。
结构上的异构体共有两种:平面异构体和空间异构体。
平面异构体是由于有相同的平面结构,而其立体结构的位置不同。
例如,在香草与许多其他植物中,存在两种主要的香草酮异构体:顺式香草酮和反式香草酮,它们具有同一种化学式,但它们的立体异构关系是在平面上,而不是在空间中。
空间异构体是由于分子组分的立体构造引起的不同。
空间异构体又称对映异构体、手性异构体或手性分子。
因为两种异构体之间的物理、化学、生物学特性几乎完全相同,所以通常只用一种形式的分子来制备,这就通常引起了产品失效的问题。
手性分子手性分子是立体异构体的一种形式。
手性分子是指每个分子都具有镜像对称体形,而两个镜像分子不能通过旋转和翻转互相重合。
手性分子有两个对称体,其中一个形体是左旋性,另一个是右旋性。
有机化学基础知识点整理立体化学的基本概念与应用

有机化学基础知识点整理立体化学的基本概念与应用在有机化学中,立体化学是一个重要的分支领域,它研究的是分子和化合物的三维结构及其对化学性质的影响。
立体化学的概念和应用在有机化学领域具有举足轻重的地位。
本文将对有机化学中的立体化学进行基本概念的整理,并探讨其在化学研究与应用中的重要性。
一、立体化学的基本概念1. 手性:手性是立体化学的一个重要概念,指的是分子或离子的不可重合的镜像异构体。
手性分子无法通过旋转或挪动使其镜像与原分子完全重合,就好像左手和右手无法完全重合一样。
2. 构象异构体:构象异构体指的是同分子式、同结构式但不同空间构型的异构体。
构象异构体的存在是由于分子的键旋转或自由转位所引起的。
典型的构象异构体如反式异构体和顺式异构体等。
3. 立体异构体:立体异构体指的是具有不同立体构型的分子或化合物。
常见的立体异构体有立体异构体、顺反异构体、环异构体等。
立体异构体的存在表明分子或化合物在空间上具有多种不同的构型。
4. 立体中心:立体中心是指一个分子中与不同基团相连的一个原子。
立体中心通常是由于其所连接的基团不对称而导致的。
一个分子可以有一个或多个立体中心。
5. 伪旋光体系:伪旋光体系是一种没有旋光性质的化合物与另一种旋光体系混合而形成的旋光体系。
这种混合体系的旋光性质来源于两个(或多个)异构体存在的旋光性质的合成。
二、立体化学的应用1. 手性药物:手性药物是指那些由手性分子构成的药物。
由于手性药物和其镜像异构体具有不同的生物活性,所以对于手性药物的合成和分离有着重要的意义。
立体化学在药物研发和制备中发挥着重要作用。
2. 光学活性物质:光学活性物质是指那些能够旋转平面偏振光的化合物。
通过立体异构体的性质,光学活性物质可以用于制备偏光镜、偏振片等光学器件,同时也广泛应用于化学分析和手性分离等领域。
3. 反应立体化学:立体化学对于有机反应的研究和理解具有重要意义。
通过研究反应的立体选择性、选择性和环境中对于反应物立体异构体的识别能力,可以更好地设计有机反应和催化剂的设计。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Cl
CH3
H
H
CH3
CH3
H
CH3
Cl
COOH
CH3
H
Cl = H
Cl
CH3
OH
CH3
CH3
COOH
OH
COOH
H
Cl
CH3
OH
CH3
H Cl
CH3
CH3 COOH
OH
H CH3
COOH Cl
OH CH3
CH3
H
Cl
CH3
COOH
OH
五、构型的命名
1、相对构型与D、L命名
人为选定一个简单化合物为标准,并假 定它的构型,其它旋光性化合物用联系 法确定构型,其构型为相对构型。
1 CHO
甘
D
油 H 2 OH
醛
3 CH2OH
CHO
L
HO
H
CH2OH
D、L命名时,费歇尔投影式的写法: 碳链竖向排列,氧化态高者在上方, 低者在下方。
H3C
CH3
H3CBiblioteka cistrans CH3
顺反异构
(可分离,不能通过键旋转相互转化)
对映异构(旋光异构)
COOH
COOH
C CH3H OH
C
HO
CH3
H
镜像
F
F
H
Br
Cl
Br
H
Cl
基 相本 同相 的同 物的 理化 性学 质性
质
实物和其镜像不能重叠
左旋体
CH2OH
Cl2CHCOHN H
合
H OH
霉
Cl Cl
NH2
Cl
NH2
H
NHCH3
C
CH3 Ph
Ph H
Ph
NHCH3
NHCH3
HH
CH3
CH3
Ph
CH3
CH3
H
Ph
NHCH3
NHCH3
H
CH3
H
3
HO 2
H
OH CH3
H OH H3C
OH H CH3
CH3
2
HO
H
3
H
OH
CH3
2
HO
H
3
H
OH
CH3
CH3
横前竖后
Fischer (费歇尔)投影式中各基团 的相互位置必须遵守下列规则:
棱镜(检偏镜)旋转的角度叫旋光度,用α 表 示。
二、旋光度与比旋光度
t
[α]λ =
α
C.L
C为浓度,单位:g / ml
L为管长,单位:dm
三、旋光性与化学结构的关系
CH3
C2H5
H C OH H C* OH
无 旋
CH3
光 性
COOH
有
CH3 旋
光
COOH 性
H C H H C* OH
CH3
CH3
致盲
HO
NH2
HO
COOH
(-)-L-DOPA 治疗帕金森氏病
HO
NH2
HO
COOH
(+)-D-DOPA 在体内集聚,不能被代谢
Thalidomide(反应停) —— 镇静和止吐药物
O
O
O HN
N OO
右旋体 (R)型, 有效。
N OO
O NH
左旋 (S)型,致畸形
第一部分 : 旋光异构(对映异构) 一、偏振光与旋光性
COOH
交换一次
HO
H
H
COOH OH
CH2OH 对映异构体
CH2OH
交换一次 对映异构体
同一化合物
COOH
H
CH2OH
OH
3、费歇尔投影式与纽曼投影式的转换
CH3
H
Cl =
H Cl
CH3
Cl
CH3
H
H
CH3
Cl
CH3
2
H
Cl
H
Cl
H
CH3
H
Cl Cl
3
H
Cl H
Cl
CH3
CH3
CH3CH3
Cl H Cl
Cl
CC
Cl H H
Cl
Cl
C
H
CH3
H
Cl
2、对称中心
H
H
Cl
F
F
Cl
H
H
H
H
H
H
F
Cl
Cl
F
180o
Cl
F
F
Cl
H
H
与镜像重合
H
H
四、旋光异构体的表示方法 1、立体图式(伞形)
NHCH3
C
CH3
H
Cl
COOH
C
HO
CH3
H
CH3
H
3
HO 2
H
OH CH3
CH3 COOH
H
H
HO CH3
2、Fischer (费歇尔)投影式 横前竖后
① 投影式不离开纸平面旋转180°, 构型不变。(不能翻转)
② 投影式不离开纸平面旋转90°, 变为对映体。
③ 同一手性碳上任何两个原子或基团 经偶数次交换,构型不变。
COOH
180°
CH2OH
HO
H
H
OH
CH2OH 同一化合物
COOH
COOH
90°
OH
HO
H
HOH2C
COOH
CH2OH
H
对映异构体
CH3
H HO
C2H5
CH3
H HO
CH2Cl
CH3
H HO
CH2Cl
CH3 H C OH
C2H5
CH3 H C OH
CH2Cl CH2Cl HO C H CH3
CH3
H
OH
C2H5
CH3
H
OH
CH2Cl
CH2Cl
OH
H
CH3
COOH
COOH
H
OH
C
H
OH
CH3
CH3
CH3
CH3
CH3
C H
H
NH2
CH3C* HC* HCH3 Cl Cl
CH3C* HOHCOOH 手性分子
COOH
COOH
C*
CH3H OH
C*
HO
CH3
H
[α]= -3.8°
[α]= +3.8°
对映异构体或旋光异构体
对映异构体:互为镜像不能重合
外消旋体:等量对映体混合在一起
对称因素:有对称面或对称中心的 无旋光性。
1、对称面:
Chapter 3 Stereochemistry
立体化学
立体化学(Stereochemistry):
以三维空间研究分子结构和性质的科学
立体异构
构象异构 构型异构
H
HH
H
H
H
H
H
HH
HH
不可分离
通过键旋转可互相转化
构型异构
顺反异构 对映异构(旋光异构、光学异构)
H H3C
H
H3C
CH3
H
H CH3
光源
普通光 尼柯尔棱镜 偏振光
旋光仪基本构造
有旋光性
0
α
。
-90
。
+90
。
180
钠
起
盛
检目
光
偏
液
偏视
灯
镜
管
镜镜
使偏振光的振动平面旋转的现象叫 旋光现象。
有旋光现象的物质为旋光性物质。 棱镜(检偏镜)旋转的方向代表旋光物质 的 旋光方向。右旋的为右旋物质,左旋的为 左右旋旋用物(质+。)或 “d” 表示(dextro-rotatory) 左旋用(-)或 “l” 表示(levo-rotatory)
CH3 N
O
O
Ph n-Bu
O
O
n-Bu Ph
麻醉剂
致痉挛
巴比妥酸衍生物
( R,R,) (+)乙胺丁醇 抗结核药
右旋体 CH2CH3
CH2OH
HOCH2 C NHCH2CH2HN C CH2CH3
H
H
H
H
HOCH2 C NHCH2CH2HN C CH2CH3
左旋体 CH2CH3
CH2OH
( S,S,)( )乙胺丁醇
无 旋
H
光H
性
COOH CH CH COOH
COOH
有手
H C H 旋性
H
C*
OH
光 性
分 子
COOH
手性碳原子 (chiral carbon atom):*
不对称碳原子(asymmetric ~):*
手性中心 (chiral center):*
F
H
Br
Cl
F
Br
H
Cl
F H C Br
Cl
手性碳 —— 手性分子的特征
+
素
右旋体
CH2OH H NHCOCHCl2 HO H
NO2
药效: 有活性 氯霉素
NO2
无活性
药效:左旋体 > 右旋体 8~135倍
氟 嗪 酸 CH3 N
O
F
COOH
N
N
O
CH3
H2N O
