第九章 液体精馏
9 精馏分知识点复习题
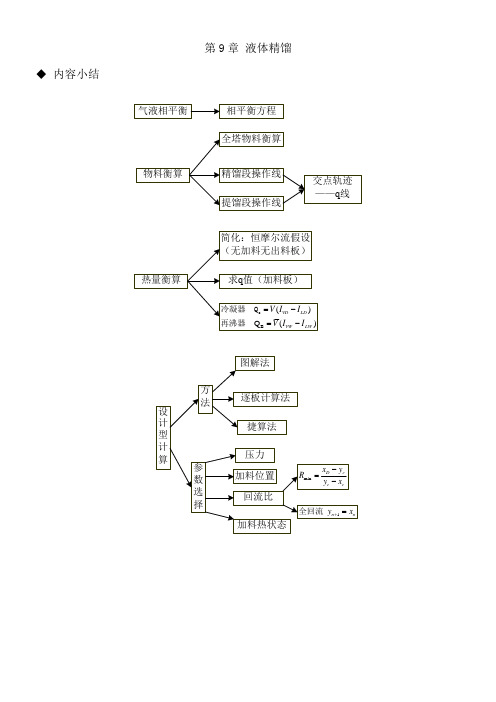
第9章液体精馏 内容小结复习题1 蒸馏概述蒸馏操作是借混合液中各组分挥发性的差异而达到分离目的。
轻组分:混合物中的易挥发组分;重组分:混合物中的难挥发组分例:蒸馏是分离的一种方法,其分离依据是混合物中各组分的,分离的条件是。
答:均相液体混合物,挥发性差异,造成气液两相系统精馏操作压力的选择减压蒸馏:降低了液体的沸点。
应用场合:分离沸点较高的热敏性混合液,混合物沸点过高的物系(避免采用高温载热体)。
加压蒸馏:提高冷凝温度避免使用冷冻剂。
应用场合:分离常压下呈气态的物系,馏出物的冷凝温度过低的物系。
举例:脱丙烷塔操作压力提高到1 765kPa时,冷凝温度约为50℃,便可使用江河水或循环水进行冷却,石油气常压呈气态,必须采用加压蒸馏。
2 双组分溶液的气液相平衡例:当混合物在t-x-y图中的气液共存区内时,气液两相温度,但气相组成液相组成,而两相的量可根据来确定。
答: 相等,大于,杠杆规则例:当气液两相组成相同时,则气相露点温度液相泡点温度。
答:大于例:双组分溶液的相对挥发度α是溶液中的挥发度对的挥发度之比,若α=1表示。
物系的α值愈大,在x-y图中的平衡曲线愈对角线。
答:易挥发组分,难挥发组分,不能用普通蒸馏方法分离,远离理想溶液的含义例:理想溶液满足拉乌尔定律,也满足亨利定律;非理想稀溶液满足亨利定律,但不满足拉乌尔定律;服从亨利定律并不说明溶液的理想性,服从拉乌尔定律才表明溶液的理想性例:精馏塔分离某二元物系,当操作压强降低时,系统的相对挥发度α_____,溶液的泡点_____,塔顶蒸汽冷凝温度______。
答:增大,减小,减小例. 已知75℃时甲醇(A)、水(B)的饱和蒸汽压为p A0=149.6kPa,p B0=38.5kPa,平衡的气液两相浓度分别为y=0.729,x=0.4,则其相对挥发度之值为_____.(4.035)3 平衡蒸馏与简单蒸馏简单蒸馏过程中,釜内易挥发组分浓度____,其沸点则_____.答:不断降低不断升高4 精馏例:精馏塔的作用是。
化工原理复习必看 第9章_液体精馏(定稿)
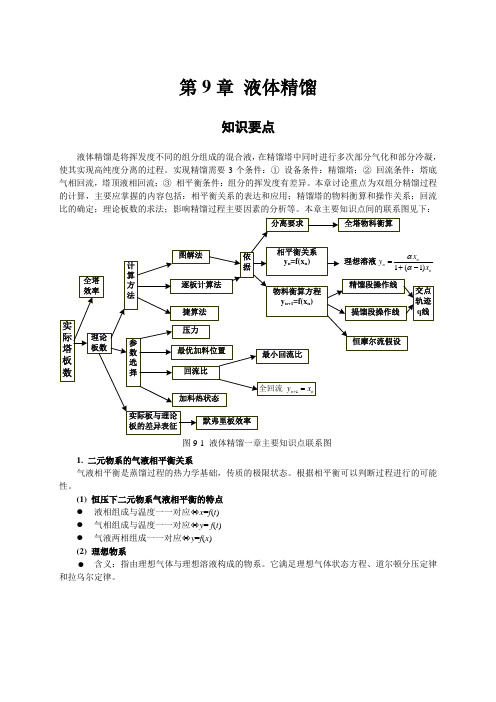
第9章液体精馏知识要点液体精馏是将挥发度不同的组分组成的混合液,在精馏塔中同时进行多次部分气化和部分冷凝,使其实现高纯度分离的过程。
实现精馏需要3个条件:①设备条件:精馏塔;②回流条件:塔底气相回流,塔顶液相回流;③相平衡条件:组分的挥发度有差异。
本章讨论重点为双组分精馏过程的计算,主要应掌握的内容包括:相平衡关系的表达和应用;精馏塔的物料衡算和操作关系;回流比的确定;理论板数的求法;影响精馏过程主要因素的分析等。
本章主要知识点间的联系图见下:图9-1 液体精馏一章主要知识点联系图1. 二元物系的气液相平衡关系气液相平衡是蒸馏过程的热力学基础,传质的极限状态。
根据相平衡可以判断过程进行的可能性。
(1) 恒压下二元物系气液相平衡的特点●液相组成与温度一一对应⇔x=f(t)●气相组成与温度一一对应⇔y= f(t)●气液两相组成一一对应⇔y=f(x)(2) 理想物系含义:指由理想气体与理想溶液构成的物系。
它满足理想气体状态方程、道尔顿分压定律和拉乌尔定律。
拉乌尔定律相对挥发度/1/1A A A B B B p x y xp x y xναν-===⋅- (9-1)11y xy xα-=⋅- (气相服从道尔顿分压定律) 相对挥发度α愈是大于1 ,则y 愈是大于x ,物系愈容易分离。
● 泡点方程x -toB ooA Bp p x p p -=- (9-2) ● 露点方程y -to A BA A Bp p p y p p p -=⋅- (9-3) ● 相平衡方程y-x()11xy xαα=+- (9-4)● t -y (x )相图两端点A 与B :端点A 代表纯易挥发组分A(x =1),端点B 代表纯难挥发组分B(x =0)。
两线:t -x 线为泡点线,泡点与组成x 有关;t-y 线为露点线,露点与组成y 有关。
3区:t -x 线以下为过冷液体区;t-y 线以上为过热蒸汽区;在t-x 与t -y 线之间的区域为气液共存区,只有体系落在气液共存区才能实现一定程度的分离。
化工原理-第九章-液体精馏资料

化工原理-第九章-液体精馏(一)测试一一.选择题1. 蒸馏是利用各组分( )不同的特性实现分离的目的。
CA 溶解度;B 等规度;C 挥发度;D 调和度。
2.在二元混合液中,沸点低的组分称为( )组分。
CA 可挥发;B 不挥发;C 易挥发;D 难挥发。
3.( )是保证精馏过程连续稳定操作的必不可少的条件之一。
AA 液相回流;B 进料;C 侧线抽出;D 产品提纯。
4.在( )中溶液部分气化而产生上升蒸气,是精馏得以连续稳定操作的一个必不可少条件。
CA 冷凝器;B 蒸发器;C 再沸器;D 换热器。
5.再沸器的作用是提供一定量的( )流。
DA 上升物料;B 上升组分;C 上升产品;D 上升蒸气。
6.冷凝器的作用是提供( )产品及保证有适宜的液相回流。
BA 塔顶气相;B 塔顶液相;C 塔底气相;D 塔底液相。
7.冷凝器的作用是提供塔顶液相产品及保证有适宜的( )回流。
BA 气相;B 液相;C 固相;D 混合相。
8.在精馏塔中,原料液进入的那层板称为( )。
CA 浮阀板;B 喷射板;C 加料板;D 分离板。
9.在精馏塔中,加料板以下的塔段(包括加料板)称为( )。
BA 精馏段;B 提馏段;C 进料段;D 混合段。
10.某二元混合物,进料量为100 kmol/h ,x F = 0.6,要求塔顶x D 不小于0.9,则塔顶最大产量为( )。
(则W=0) BA 60 kmol/h ;B 66.7 kmol/h ;C 90 kmol/h ;D 100 kmol/h 。
11.精馏分离某二元混合物,规定分离要求为D x 、w x 。
如进料分别为1F x 、2F x 时,其相应的最小回流比分别为1min R 、2min R 。
当21F F x x >时,则 ( )。
AA .2min 1min R R <;B .2min 1min R R =;C .2min 1min R R >;D .min R 的大小无法确定12. 精馏的操作线为直线,主要是因为( )。
第9章 化工原理液体精馏

9.1 9.2 9.3 9.4 9.5 9.6 9.7 9.8
蒸馏概述 双组分溶液的气、液相平衡 平衡蒸馏与简单蒸馏 精馏 双组分精馏的设计型计算 双组分精馏的操作型计算 间歇精馏 恒沸精馏与萃取精馏
9.1蒸馏概述
(Introduction of Distillation )
9.2.2 非理想物系的气液相平衡
正偏差:aAB<aAA,aAB<aBB,即异分子间的排斥倾向起了
主导作用,使溶液的两个组分的平衡分压都比拉乌尔定律 所预计的高,如下图所示。
9.2.2 非理想物系的气液相平衡
正偏差严重时形成具有最低恒沸点的溶液,图9-7苯乙醇溶液就是这种溶液,其最低恒沸点为tm=68.3℃,最 低恒沸点的恒沸物组成为xm=0.552。图9-9为乙醇-水溶 液的相平衡曲线也是这种情况,其tm=78.15 ℃, xm=
1、蒸馏分离的依据 利用混合物在一定压力下各组分相对挥发度(沸点) 的不同进行分离的一种单元操作。 yA xA y B xB
易挥发组分 : 沸点低的组分 难挥发组分 : 沸点高的组分
9.1蒸馏概述
(Introduction of Distillation )
2、蒸馏的分类
简单蒸馏
平衡蒸馏 (闪蒸) 按蒸馏方式 精馏 恒沸蒸馏 特殊精馏 萃取蒸馏 水蒸汽蒸馏 较易分离的物系 或对分离要求不 高的物系 难分离的物系 很难分离的物
9.2.2 非理想物系的气液相平衡
实际生产中所遇到的大多数物系为非理想物系。非理 想物系的气液相平衡关系的计算要涉及逸度、活度系数等参 数,计算复杂, (1)非理想溶液 溶液的非理想性来源于异种分子之间的作用力aAB不同 于同种分子间的作用力aAA、aBB,其表现是溶液中各组分的 平衡蒸汽压偏离拉乌尔定律。此偏差可以是正偏差,也可以 是负偏差,实际溶液尤以正偏差居多。
济南大学化学化工学院化工原理课件第9章 液体精馏(5)

(1 q )F
V V (1 q)F
L L qF
L
F
V
F L V V L
F L V V L qF
qF
L L qF
L
V
V V (1 q)F
2019/1/30 第 9 章 液体精馏 12
9.4 精馏 9.4.1 精馏操作过程
精馏的目的:为满足高纯度分离的要求。 操作方式
y1 x D
y1
V
L 1
xD
L
L
xD
D
y i 1
i
yi xi
xi 1
F , xF
N
W
xw
2019/1/30 第 9 章 液体精馏 1
精馏高纯度分离的原理: 在每块塔板上汽、液两相之间发生传热和传质。汽相混合物在塔内上升的 过程中重组分逐渐冷凝进入液相,液相混合物在塔内下降的过程中轻组分逐 渐汽化进入汽相。是上升汽相发生多次冷凝、下降液相多次汽化的过程。上 升汽相混合物中轻组分的浓度逐渐增加,下降液相混合物中重组分的浓度逐 渐增加。故塔顶得到高纯度的轻组分产物,故塔底得到高纯度的重组分产物。
y1
V
L 1
xD
L
L
xD
D
V ( y1 yi ) L( xD xi 1 )
V ( xD yi ) L( xD xi 1 )
x D yi L V x D x i 1
y i 1
i
yi xi
xi 1
F , xF
N
y A,i x A,i 1
2019/1/30
2019/1/30 第 9 章 液体精馏 4
9.4.2 精馏过程的数学描述
化工原理第九章液体精馏

FiF Li V I Li VI
由恒摩尔假定,不同温度和组成的饱和液体焓i和汽 化潜热均相等。
20
联立上二式,得 定义:
L L I iF F I i
q
I iF分子:1kmol原料变成饱和蒸气所需的热 I i 分母:原料的摩尔汽化热
可得
L L qF
V V (1 q)F
q为加料热状态参数 q=0,饱和气体(露点);q=0,饱和液体(泡点) q<0,过热蒸气;0<q<1,气液两相,q>1,冷液
不管加料板上状态如何,离开加料板的两相温度相
等,组成互为平衡。
V,I,ym
L,i,xm-1
物料衡算式
F,iF,xF
FxF V ym1 Lxm1 Vym Lxm 相平衡方程
ym f (xm )
3)精馏段和提馏段流量的关系
V’,I,ym+1
L’,i,xm
列加料板物料和热量衡算式
F LV LV
临界压强时,气液共存区 缩小,分离只能在一定范 围内进行,不能得到轻组 分的高纯度产品。
8
9.3 平衡蒸馏和简单蒸馏
D
9.3.1 平衡蒸馏
令W q, F
则D 1q F
物料衡算:F xF D y W x
F
F DW
xF
联立得:y q x xF q 1 q 1
热量衡算:忽略组成对比热影响,
2)对理想物系
A / B
pA / xA pB / xB
p
0 A
xA
/
xA
pB0 xB / xB
pA0
pB0
3)对物系相对挥发度 1和相差2 不大
m
1 2
(1
化工原理-9章液体精馏-课件PPT
两相区特点:当两相温度相同时 y > x 当组成相同,t露点>t泡点
t/C
在总压一定的条件下,将组成为 xf
的溶液加热至该溶液的泡点 TA,产
2
9.1 概 述
工业乙醇的蒸馏(有机化学实验)
3
思考:混合物的分类? 均相混物:物系内部各处物料性质均匀而且不存在相界面的
混合物。 化工生产过程中所遇到的物料有许多是两个或两个以上 组分的均相混合物。
如:石油、空气、粗甲醇
4
蒸馏操作在工业生产中的应用
5
世界六大蒸馏酒的制备 白兰地(Brandy)、威士忌(Whisky)、伏特加(Vodka)、
N ——组分数 φ ——相数
一定压力下: 组成xA(yA)与温度t存在一一对应关系; 气液组成之间xA~yA存在一一对应关系。
21
二、 拉乌尔定律( Raoult’s Law)
法国物理学家拉乌尔在1887年研究含有非挥发性溶质的 稀溶液的行为时发现的,可表述为:“在某一温度下,稀溶 液的蒸气压等于纯溶剂的蒸气压乘以溶剂的摩尔分数”。
填料塔
规整填料 塑料丝网波纹填料
散装填料 塑料鲍尔环填料
19
9.2 双组分溶液的气液相平衡
9.2.1 双组分理想物系的气液相平衡
理想物系:液相为理想溶液,气相为理想气体且服从 道尔顿分压定律的物系。
理想液体:没有黏性、不可压缩的液体。 理想气体:严格遵从气体状态方程的气体 。 道尔顿分压定律:理想气体混合物的总压力为各组元
原料液 加热器 减压阀 Q
塔顶产品
yA
闪 蒸 罐 xA
特点:闪蒸是连续、稳定的单级蒸 馏程,生产能力大,不能得 到高纯产物,常用于只需粗 略分离的物料。
液体精馏
第9章 液体精馏(选讲)例9-1 理想物系泡点与平衡组成的计算某蒸馏釜的操作压强为106.7kPa ,溶液含苯的摩尔分数为0.2,甲苯的摩尔分数为0.8,求此溶液的泡点和平衡的气相组成。
苯-甲苯组成理想溶液,其安托因方程为苯 8.2201211031.6log 0+-=t p A 甲苯 5.2191345080.6log 0+-=t p B 解:已知x A =0.2,p=106.7kPa ,代入方程000B A B A p p p p x --= 或 0007.10620.0BA B p p p --= 设泡点温度t = 103.9℃,用安托因方程计算饱和蒸汽压苯 8.2209.1031211031.6log 0+-=A p p A o = 200.2 kPa 甲苯 5.2199.1031345080.6log 0+-=B p p B o = 83.3 kPa 2.03.832.2003.837.1067.106000=--=--BA B p p p 假设成立,则375.07.1062.20020.00=⨯==p p x y A A例9-2 简单蒸馏与平衡蒸馏的比较将苯-甲苯混合液中x(苯) = 0.70的溶液加热气化,气化率为1/3。
已知物系的相对挥发度为2.47。
试求简单蒸馏与平衡蒸馏的馏出液的量和组成。
解:(1)简单蒸馏为了计算方便,设总量W 1为100kmol ,W 2为100×2/3=66.7 kmol ,则⎪⎪⎭⎫ ⎝⎛--+-=12212111ln ln 11ln x x x x W W αα⎪⎪⎭⎫ ⎝⎛--+-=7.011ln 47.27.0ln 147.217.66100ln22x x 解出 x 2 = 0.633834.07.66100633.07.667.010*******=-⨯-⨯=--=W W x W x W y (2)平衡蒸馏q = 2/310.2213/27.013/23/211+-=---=---=x x q x q qx y F xx x x y 47.1147.2)1(1+=-+=αα 解出 x = 0.642 y = 0.816比较平衡蒸馏和简单蒸馏,在气化率相同的条件下,简单蒸馏得到的气相平均浓度比平衡蒸馏的浓度要大。
化工原理 第9章 液体精馏 典型例题题解(2)
yn1
R x x D 第2段:操作线方程 R1 R1 Wxw L xn 得:所需理论板10块,自顶数第5块进料。 V V
2段
W , xw
例:2000年华东理工大学硕士入学考试试题
用连续精馏塔分离某双组分混合液,混合液中含易挥发组分 xF=0.4(摩尔分率,下同),原料以饱和液体状态加入塔中部,塔 顶全凝,泡点回流。操作条件下物系的相对挥发度α=2 . 5 ,要求 塔顶产品浓度xD=0.8 ,塔顶易挥发组分的回收率η=0. 9 。塔釜间接 蒸汽加热。试求:(1)完成上述分离任务的最小回流比;
W , xw
第2段:操作线方程
V ' ' y F1 x f 1 L' ' x Dx D
Dx D Fx f L' ' y x V '' V ''
Wxw L 第3段:操作线方程 yn1 xn V V 得:所需理论板8块,自顶数第3块为F1进料,第6块 为F2进料。
(2)将两股原料混合后在其泡点下进入相应浓 度的塔板上 两股原料混合后的组成xf F、q=1
y1
V0
L0
D
xD
xD
V
L
F
结论:冷回流时精馏段的操作线方程形式不变。
例: 有两股原料,一股为100kmol/h含苯0.6(摩尔分率,下同)和含甲苯0.4的 混合液。另一股为100kmol/h含苯0.2(摩尔分率,下同)和含甲苯0.8的混合液。 拟用精馏操作进行分离,要求馏出液含苯0.9 ,釜液含苯0.05 。塔顶设全凝器, 塔釜为水蒸气间接加热。操作回流比为2 。问下述两种方案哪种方案所需的理论 板数少?(1)两股原料分别在其泡点下进入相应浓度的塔板上; (2)将两股原料混合后在其泡点下进入相应浓度的塔板上。 解: (1)两股原料分别在其泡点下进入相应浓度的塔板上
化工原理 第9章 液体精馏 典型例题题解(1)
第9章 精馏 典型例题例1:逐板法求理论板的基本思想有一常压连续操作的精馏塔用来分离苯-甲苯混合液,塔顶设有一平衡分凝器,自塔顶逸出的蒸汽经分凝器后,液相摩尔数为汽相摩尔数的二倍,所得液相全部在泡点下回流于塔,所得汽相经全凝器冷凝后作为产品。
已知产品中含苯0.95(摩尔分率),苯对甲苯的相对挥发度可取为2.5 。
试计算从塔顶向下数第二块理论板的上升蒸汽组成。
解: 884.095.05.15.295.05.115.20000=⨯-=→=+=x x x x y DR=L/D=2905.03/95.0884.0323/95.032:11=+⨯=+=+y x y n n 精馏段方程845.03/95.0793.032793.0905.05.15.2905.05.15.22111=+⨯==⨯-=-=y y y x例2:板数较少塔的操作型计算拟用一 3 块理论板的(含塔釜)的精馏塔分离含苯50%(摩尔分率,下同)的苯-氯苯混合物。
处理量F=100 Kmol/h ,要求 D=45 Kmol/h 且 x D >84%。
若精馏条件为:回流比R=1 ,泡点进料,加料位置在第二块理论板,α=4.10 ,问能否完成上述分离任务? 解:W=55kmol/h精馏段操作线方程:y n+1=0.5x n +0.42提馏段的操作线方程:Fq D R Wx x F q D R qFRD y w )1()1()1()1(--+---++=将相关数据代入得提馏段操作线方程:134.061.1-=x y 逐板计算:y 1=x D =0.84y 2=0.5×0.56+0.42=0.7057.0134.036.061.13=-⨯=y.22.05584.04550=⨯-=-=WDx Fx x Df w ()56.084.01.31.484.01111=⨯-=--=y y x αα36.07.01.31.470.02=⨯-=x22.024.057.01.31.457.03≥=⨯-=x所以不能完成任务。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第九章液体精馏
1.
蒸馏分离的依据是什么?2.
沸点和泡点都是液相达到沸腾时的温度,二者没有本质的不同,对吗?3.
相对挥发度的大小与物系分离的难易有何关系?4.
二元连续精馏过程中,进料状态的变化是否会引起操作线的变化?5.
在板式精馏过程中,进料温度与q值之间有什么关系?对进料板数又有什么影响?6.
精馏塔的塔顶分凝器及塔釜均可当作一块理论塔板,对吗?7.
观察精馏塔的温度分布,发现塔顶温度总是低于塔底温度,这是由于塔底装有再沸器的缘故,对吗?8.
R增大,精馏段操作线斜率、提留段操作线斜率、所需理论板数等如何变化?9.Q值与加料板位置有什么关系?
10.最小回流比只与平衡线的形状有关,对吗?
11.理论板是一理想化的塔板,其特点是什么?
12.精馏过程的核心是什么?精馏过程的代价是什么?
13.精馏过程中若总热耗固定,何种进料状态有利于提高产品分离纯度?
14.精馏塔产品纯度的高低,一般可用什么方法检测出来?如果塔顶产品纯度不符合要求,一般应调节什
么?
15.加料板的位置与达到指定分离任务所需要的理论板数目有无关系?
16.最优加料板位置如何确定?
17.加料热状态参数q的物理意义是什么?
18.全回流的特点是什么?什么情况下采用全回流?
19.在轻组分回收率相同的条件下,比较直接蒸汽加热与间接蒸汽加热,二者所需要的理论板数是否相
同?
20.精馏过程的主要操作费用是什么?
21.恒摩尔流假定的内容是什么?
页码,1/1第九章 液体精馏2012/10/9ht t p://j pkc.nw /hgyl /C our s e/C ont ent /N 70/200507200039.ht m。
