第十一章 环醚二
合集下载
第十一章 醚

CHCH2 HO R
XMgO R
◇酸性开环: 酸性开环:
◎ 例:
H2 O
H +
CH3
+
CHCH2 HO OH
H
CH3
CH CH2 O
+
CH3OH
H3 CO CHCH2 H3C OH
HX
CH3
CH CH2 X OH
反应机理: ◇反应机理: ◎例:
▲前者SN2,亲核试剂进攻取代基数少从而空间位阻较小的环C , 前者S 亲核试剂进攻取代基数少从而空间位阻较小的环C
重排( 重排的特例, [3,3]σ迁移 迁移) (4)Claisen重排(为Corpe重排的特例,属[3,3]σ迁移) 重排 重排的特例
机理: ◇机理:协同反应
◇即:
无氢
三、制法
(1)Willamson合成法 Willamson合成法
◇通式: 通式:
◇机理:一般为SN2 机理:一般为S
两个试剂中的烷基结构对反应很有影响, ◎两个试剂中的烷基结构对反应很有影响,如:
例子: ◇例子:
醚链断裂机理:一般为S ◇醚链断裂机理:一般为SN2
◎如 :
特别注意: ◇特别注意:烷芳混合醚 ◎例:
+
HI
→
碘代烷 + 酚
芳基与氧的孤电子对共轭( C(芳环 芳环) ∵芳基与氧的孤电子对共轭(p-π)使C(芳环)-O具有部分双键 性质,难于断裂。 性质,难于断裂。
(3)自动氧化(automatic oxidation) 自动氧化( )
(2)反应
①酸性 ◎酸性:硫醇(酚)>相应醇(酚) 酸性:硫醇( 相应醇( 例: pKa C2H5OH 15.7 C2H5SH 10.6 C6H5OH 10.00 C6H5SH 7.8
第十一章 醚

很少重排
OC(CH3)3
第四节 环醚
一、环氧化合物
H H
O
H
张力能114.1kJ/mol 张力能
H
反应: 反应:
碱催化下的 开环反应 反式产物 亲核基团 连接在 取代基较少 的碳上 酸催化下的 开环反应 反式产物 亲核基团 连接在 取代基较多 的碳上
制法: 制法:
OH Br
NaOH H2O
O
红外(IR): 1275~1020cm-1 C-O-C 红外 H 1H NMR): 核磁( 核磁 C O :3.3δ:3.3-3.7ppm 质谱: 峰较小, 质谱:M+峰较小, (M+1)+峰较大 R CH O R'' 基峰常为: 基峰常为: R CH O R''
R' - R'
第二节 醚的反应 一、碱性
OCH3
二、醇脱水
15%H2SO4 % (CH3)3COH+C2H5OH(过量) (CH3)3COC2H5 + 过 o 70 C
三、醇与烯烃的加成
SN 1
中间体为碳正离子, 中间体为碳正离子,有重排可能
(1)Hg(OAc)2,R'OH RCHCH3 RCH=CH2 (2)NaBH4,OHOR'
(1)Hg(OOCCF3)2,(CH3)3COH (2)NaBH4,OH-
[O]
四、克莱森重排(Claisen) 克莱森重排
协同反应
OCH2CH=CH2 CH=CH2
OH CH=CHCH2CH=CH2
OCH2CH=CHCH3 H3C CH3
H3C
O=CHCH2CH2CH=CH2
OH CH3
CH2CH=CHCH3
【有机化学】第十一章 醚【配套胡宏纹教材】

O + H2O
H+
HOCH2CH2OH O
HOCH2CH2OCH2CH2OH
H+
一缩二乙二醇 (二甘醇)
H+ O + CH3OH or OH-
CH2CH2OCH3 OH
O H+
HOCH2CH2OCH2CH2OCH3
乙二醇单烷基醚
二聚乙二醇单烷基醚
n-C12H25OH + n O
OHn-C12H25O(CH2CH2O)nH
O
O
O
O
O
O
18-冠-6环中氧原Fra bibliotek数环的总原子数目
冠醚中心是一个空穴,可对某些金属离子进行络合。用作相转移催化剂(加速 水-油两相体系的化学反应)。
4. 环氧乙烷的制备
a, 直接氧化法:
CH2 CH2
O2 / Ag
220-280 oC
O
b, 氯乙醇法
CH2 CH2 + Cl2 + H2O HOCl
CH2CH2 Ca(OH)2
OH Cl
O
5、冠醚
模型的形状与王冠相似,故得名。
大环多元醚(含≥3个-OCH2CH2-重复单元),是乙二醇的环状聚合物。
2. 环氧乙烷的开环反应
O H2C CH2
NaOH HO H2C CH2 OH H2O HX HO H2C CH2 Cl
B-:OH-,RO-,NH3
RMgX
H2O
RCH2CH2 O MgX H+
RCH2CH2OH
特点:1)能形成含有两个官能团的化合物; 2)和RMgX反应,制备比RMgX多2个碳的伯醇
H2C CH2 H2C CH2 H2C CH2
医学有机化学--第十一章 杂环化合物

O N N N H
鸟嘌呤(G)(2-氨基-6-羟基嘌呤)
2、尿酸
O HN O N H N H NH O HO N N H N OH N OH
尿酸
2,6,8-三羟基嘌呤
尿酸难溶于水。正常人血浆中含尿酸 2~6mg%。每天由尿中排出0.5~1g。
第十四章
要点
1、杂环化合物的命名结构式的写法
2、五元杂环和六元杂环的化学性质
4-甲 基 嘧 啶
2-羟 基 噻 唑
2-氨 基 咪 唑
5 6 7 8
4 3 N 1 2
CH3
1N
6
NH2
5 3 9 4 7
பைடு நூலகம்
N N H
N
3-甲基异喹啉
6-氨基嘌呤
2、当侧链为羧基、磺酸基、醛基等时:一般把杂环作取代基。
C OOH
C HO O
N
2-呋喃甲醛(糠醛)
3-吡啶甲酸
第二节 五元杂环化合物
一、吡咯、呋喃和噻吩的结构
NO2 N H
O
C H3
N
2-甲基呋喃
α-甲基呋喃
4-丙基吡啶
γ-丙基吡啶
4 3
3-硝基吡咯
β -硝基吡咯
5 6 7 8
C H3
2
3-甲基异喹啉
N
1
②含多个杂原子时:按 O,S,NH,N 的顺序使杂原子的 编号最小。有固定编号的例外。
CH3 4 5 6 N 1 N 3 2
4 5 S 1 N 3 2 OH 4 5 N1 H N3 2 NH2
4.8
8.8
N HC l 或
9.4
+
13.6
N HC l
吡啶盐酸盐
有机化学 11
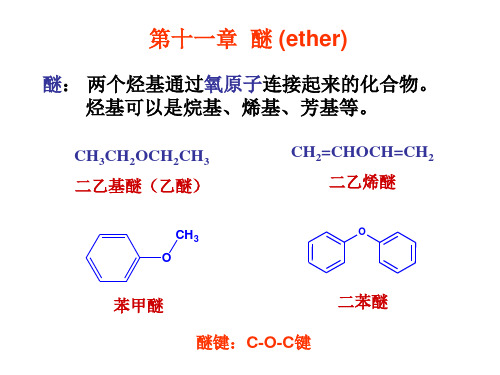
氧与二个1 相连 发生S , 相连, 氧与二个 oC相连,发生 N2, 氧与2 、 相连, 氧与 oC、 3oC相连,发生 N1。 相连 发生S 。
烷基芳基混合醚: 烷基芳基混合醚: 一起加热生成碘代烷和酚 与HI一起加热生成碘代烷和酚,酚不与氢碘酸作用 。 一起加热生成碘代烷和酚,
O
CH3 + HI
O
-
Cl
-Cl-
O
Cl
Cl
+ HOCl
OH
NaOH
O-
分子内S 分子内 N2
O
Cl OH H
NaOH E2
HO
(4) 冠谜的合成
HO-CH2-CH2-OH + 2
O
苯甲醚 醚键: 醚键:C-O-C键 键
二苯醚
醚的结构、 第一节 醚的结构、命名和物理性质 1. 分类
开链醚:没有环的醚。 开链醚:没有环的醚。
CH 3 O
CH2=CHOCH=CH2
O O O
15 16 17 14 18 O 13 O1 2 12 O 11 O 10 9 O 8 7 6 O4 3 5
链增长: 链增长:
• (CH3)2COCH3 + O2
优先形成稳定 的自由基。 的自由基。
(CH3)2COCH3 OO •
(CH3)2COCH3 + (CH3)2CHOCH3 OO • • (CH3)2COCH3 + (CH3)2COCH3 OOH
关键中间体
3. 醚的碳氧键断裂反应
CH3OCH3 + HI (1mol)
RO
- ...
... CH2
X
取代
ROCH2CH2R' + X-
第十一章 环醚二
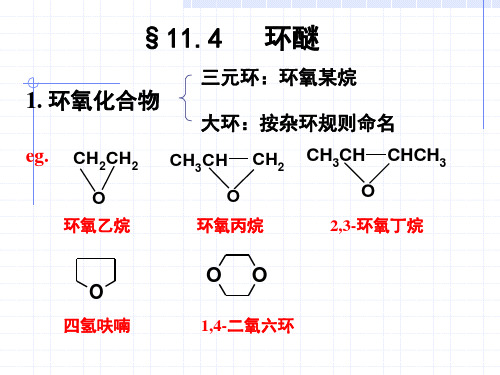
(2)酸催化开环(更容易)
过程:环氧化合物 酸
盐
O
+
H O
+
..
H
ROH
H2C CH2
H2C CH2
SN2 开环
δ+
OH
≠
H2C CH2
δ+OR
H
OH -H+
H2C CH2
+OR H
OH H2C CH2
OR
•不对称环氧化合物:亲核试剂进攻能生成较稳 定的碳正离子,即烃基取代基较多的碳原子;
•立体化学:若被进攻的环碳原子是手性碳,则 构型转化
CH3CHCH2R OMgX
CH3CHOHCH2NH2(R) [(CH3)2CHO]4AlLi
(2)酸催化反应:试剂进攻烃基取代基较多的 环碳原子(能形成稳定碳正离子)
CH3*CH
CH2 +
H2O H+ CH3 *CHOHCH2OH
H+
Hale Waihona Puke CH3OHCH3O*CHCH2OH
OH H+
CH3 CH3
O*CHCH2OH
Cl NaOH OH
NaOH
O 异构化
Cl OH
CH3 HO H (R) Br H (S)
C2H5
OH
CH3 H
HO
O
Br OH-
H C2H5
CH3
RR
H
O
H C2H5
5. 重要的环醚 (1)环氧乙烷
(2)四氢呋喃 (3)二氧六环
练习:用不超过三个碳的有机物及必要的试 剂合成:
1、(CH3)2CHCH2CH2OH 2、CH3O(CH2CH2O)2CH3 3、 CH3O CH2CH(CH3)OCH2CH(CH3 )OH 4、 CH3 CH2OCH2CH2OCH2CH2O CH3
第三节 醚
第十一章 醇酚醚
第 三 节 醚
本节要求
1、掌握醚的结构、分类和命名。 2、了解醚性质。
3、了解常见的醚。
醚的概念:
醚:两个烃基通过氧原子相连而成的化合物是醚。 通式: R—O—R/、R—O—Ar、Ar—O—Ar/ 官能团:—O— 称为醚键,是醚的官能团。
一、醚的分类和命名 (一)分类 与氧相连的两个烃基相同,称作单醚 如 C2H5-O-C2H5 与氧相连的两个烃基不同,称作混醚 如 CH3-O-C2H5
乙醚在空气的作用下能氧化成过氧化物、醛和 乙酸,暴露于光线下能促进其氧化。当乙醚中含有 过氧化物时,在蒸发后所分离残留的过氧化物加热 到100℃以上时能引起强烈爆炸; 这些过氧化物可 加5%硫酸亚铁水溶液振摇除去。与无水硝酸、浓硫 酸和浓硝酸的混合物反应也会发生猛烈爆炸。 乙醚对人的麻醉浓度为109.08~196.95g/m3, 当浓度为212.1~303g/m3时可致呼吸停止,当浓度 超过10%时通常可以致命。 乙醚是低毒物质,对皮肤及呼吸道粘膜有轻微 的刺激作用。长期接触低浓度乙醚蒸气时可出现头 痛、头晕、易激动或淡漠、嗜睡、忧郁、体重减轻、 食欲减退、恶心、呕吐、便秘等症状。吸人较高浓 度乙醚蒸气时可出现头晕、癔病样发作、精神错乱、 嗜睡、面色苍白、恶心、呕吐、呼吸不规则等短时 间大量接触后发生的中毒症状,一经脱离现场,稍 待休息,经对症处理后就可恢复。
2-甲氧基-5-氯-3-己醇
二、常见的醚 —— 乙醚
乙醚是最常见的和最重要的醚。它是易挥发的无色透明 液体,有特殊气味,沸点34.5℃。 非常易燃,乙醚蒸气与空气混合达到一定比例时,遇火 可引起爆炸,因此在制备和使用时,周围要避免明火,并采 取必要的安全措施。 乙醚比水轻,微溶于水。其蒸汽比空气重2.5倍。能溶 解多种有机物,是一种良好的有机溶剂,常用于提取中草药 的有效成分。 乙醚有麻醉作用,医用乙醚是高效麻醉药品,只要5到 10秒钟就让人昏迷,曾用作吸入式全身麻醉剂,由于可引起 恶心、呕吐等副作用,现已被更高效、安全的麻醉剂所代替。
第 三 节 醚
本节要求
1、掌握醚的结构、分类和命名。 2、了解醚性质。
3、了解常见的醚。
醚的概念:
醚:两个烃基通过氧原子相连而成的化合物是醚。 通式: R—O—R/、R—O—Ar、Ar—O—Ar/ 官能团:—O— 称为醚键,是醚的官能团。
一、醚的分类和命名 (一)分类 与氧相连的两个烃基相同,称作单醚 如 C2H5-O-C2H5 与氧相连的两个烃基不同,称作混醚 如 CH3-O-C2H5
乙醚在空气的作用下能氧化成过氧化物、醛和 乙酸,暴露于光线下能促进其氧化。当乙醚中含有 过氧化物时,在蒸发后所分离残留的过氧化物加热 到100℃以上时能引起强烈爆炸; 这些过氧化物可 加5%硫酸亚铁水溶液振摇除去。与无水硝酸、浓硫 酸和浓硝酸的混合物反应也会发生猛烈爆炸。 乙醚对人的麻醉浓度为109.08~196.95g/m3, 当浓度为212.1~303g/m3时可致呼吸停止,当浓度 超过10%时通常可以致命。 乙醚是低毒物质,对皮肤及呼吸道粘膜有轻微 的刺激作用。长期接触低浓度乙醚蒸气时可出现头 痛、头晕、易激动或淡漠、嗜睡、忧郁、体重减轻、 食欲减退、恶心、呕吐、便秘等症状。吸人较高浓 度乙醚蒸气时可出现头晕、癔病样发作、精神错乱、 嗜睡、面色苍白、恶心、呕吐、呼吸不规则等短时 间大量接触后发生的中毒症状,一经脱离现场,稍 待休息,经对症处理后就可恢复。
2-甲氧基-5-氯-3-己醇
二、常见的醚 —— 乙醚
乙醚是最常见的和最重要的醚。它是易挥发的无色透明 液体,有特殊气味,沸点34.5℃。 非常易燃,乙醚蒸气与空气混合达到一定比例时,遇火 可引起爆炸,因此在制备和使用时,周围要避免明火,并采 取必要的安全措施。 乙醚比水轻,微溶于水。其蒸汽比空气重2.5倍。能溶 解多种有机物,是一种良好的有机溶剂,常用于提取中草药 的有效成分。 乙醚有麻醉作用,医用乙醚是高效麻醉药品,只要5到 10秒钟就让人昏迷,曾用作吸入式全身麻醉剂,由于可引起 恶心、呕吐等副作用,现已被更高效、安全的麻醉剂所代替。
第十一章 醚PPT课件
❖环醚的命名,看作是烃的环氧衍生物,也常用习惯命名法。
含有三元环的环醚,英文名用epoxy(环氧)作词头,其他多采用杂环化合 物的命名法。
CH3CH CH2 O
环氧丙烷 epoxypropane
OO O
四氢呋喃 1,4-二氧六环(二噁烷)
tetrahydrofuran(THF) 1,4-dioxane
❖核磁共振谱:连在醚键碳上的H,δ值增大。 乙基苄基醚的核磁共振谱:
a. b. c. d.
a.
CH2OCH2CH3
d.
b.
c.
3 化学性质
❖醚的化学性质稳定,可用金属钠干燥醚类,醚在许多有机反应中可作溶剂。
❖官能团:醚键C—O—C,在一定条件下能发生反应。
Lewis碱与酸反应
强酸作用下醚键断裂
··
例:利用简单的化学方法除去正溴 丁烷中少量的正丁醇、正丁醚、1丁烯。
(2) 醚键的断裂 ❖钅羊盐的生成,使醚分子中的碳氧键变弱,因此在较高的温度下,强酸能使 醚键断裂。 氢卤酸最有效,其中氢碘酸作用最强,可在常温下作用。
C H 3 C H 2 O C H 3 +H I C H 3 C H 2 O H +C H 3 I
CH3CHCH2CH2CH3 OCH3
2-甲氧基戊烷 2-methoxypentane
CH3CHCH2CHCH3 CH3 OCH3
2-甲基-4-甲氧基戊烷 2-methoxy-4-methylpentane
CH2CH CH2
OCH3
3-甲氧基-1-丙烯 3-methoxyprop-1-ene
OCH(CH3)2
2 物理性质和光谱性质
❖物态:甲醚、甲乙醚为气体,大多数醚在室温下为液体,有香味,易燃。
第十一章 醚
CH3
OCH3 重排产物
溶剂汞化反应——水化,醇化
(1) Hg(OAc)2 (CH3)3CC CH2 + CH3OH (2)NaBH4,OH(CH3)3CC CH2 OCH3
羟汞化-脱汞反应(不重排)
11.4 环醚
一、环氧化合物
碳正离子,SN1
位阻小 SN2
O CH3CH2CH CH2
二、命名
1、先写出两个烃基的名称,再加上醚字; 2、醚也可以当作烃氧基衍生物;
三、物理性质
11.2 醚的反应
一、碱性 与路易斯酸(缺电子物种)形成盐 活性:二烷基醚>芳烷基混合醚>二芳基醚
二、醚链的断裂 1、与H-X 反应 R-O-R’ + HX → RX + R’X + H2O 活性: HI > HBr > HCl
第十一章 醚
结构、命名和物理性质 醚的反应 醚的制法 环醚 醚的来源和用途
11.1 醚的结构、命名和物理性质
醚,可以看成是水分子中的两个氢原子被烃基取 代而生成的化合物。分为简单醚(两个烃基相同, R-O-R)、混合醚(两个烃基不同,R-O-R’)。 一、醚的结构 不等性SP3杂化
(CH3)2C CH(CH3)2 OCH3 重排产物
机理: (CH3)3CC CH2 H
+
CH3 CH3
+ CH3OH C C CH3 + -H CH
3
CH3OCH3 CH3 C C CH3 CH3 马氏加成产物
重排
CH3OH CH3
+
CH3 C CH3 CH3OH -H
+
C
(CH3)2C
CH(CH3)2
第11章醚2016解析
H 分解
O CC
H
O CC
H
+ ROH + R2NH
请推测上述反应合理的机理!
练习:完成下列反应,写出主要产物并指出反应类型 (1) CH3CH2OCH2CH=CH2 + HBr(48%) (2) CH3CH2OCH2CH2CH3 + HBr(48%过量) (3) (CH3CH2)3COCH2CH2CH3 + HBr(48%)
eg. CH2OCH3
CHOH CH2OH
系统命名:3-甲氧基-1,2-丙二醇 普通命名:丙三醇-1-甲醚(甘油-1-甲醚)
甘油-2-甲醚
CH2OH CHOCH3 CH2OH
3. 醚的物理性质
Hydrogen Bond !!
请解释以上化合物的水溶性的差异!!
醚中氧原子上具有孤电子对,是氢键受体 由于氢键的形成,醚也能溶于醇中:
保护酚羟基——形成苄基醚
4. 自动氧化
化学物质和空气中的氧在常温下温和地进行氧化,而 不发生燃烧和爆炸,这种反应称为自动氧化。自动氧化反 应通常在具有活泼氢的部位进行。
(CH3)2CH—O—CH3
O2 自动氧化
(CH3)2C—O—CH3
OOH
醚-位上的H
烯丙位、苯甲位、3oH、醚-位上的
H均易在C-H之间发生自动氧化。
反应机理:多数自动氧化是通过自由基机理进行的。
链引发: R• + O2
ROO•
ROO• + (CH3)2CHOCH3
ROOH + (CH3)2C•OCH3
优先形成稳 定的自由基
生成能力:ROR’ > ROAr > ArOAr
2. 醚键的断裂(与热的强酸HX作用 )
O CC
H
O CC
H
+ ROH + R2NH
请推测上述反应合理的机理!
练习:完成下列反应,写出主要产物并指出反应类型 (1) CH3CH2OCH2CH=CH2 + HBr(48%) (2) CH3CH2OCH2CH2CH3 + HBr(48%过量) (3) (CH3CH2)3COCH2CH2CH3 + HBr(48%)
eg. CH2OCH3
CHOH CH2OH
系统命名:3-甲氧基-1,2-丙二醇 普通命名:丙三醇-1-甲醚(甘油-1-甲醚)
甘油-2-甲醚
CH2OH CHOCH3 CH2OH
3. 醚的物理性质
Hydrogen Bond !!
请解释以上化合物的水溶性的差异!!
醚中氧原子上具有孤电子对,是氢键受体 由于氢键的形成,醚也能溶于醇中:
保护酚羟基——形成苄基醚
4. 自动氧化
化学物质和空气中的氧在常温下温和地进行氧化,而 不发生燃烧和爆炸,这种反应称为自动氧化。自动氧化反 应通常在具有活泼氢的部位进行。
(CH3)2CH—O—CH3
O2 自动氧化
(CH3)2C—O—CH3
OOH
醚-位上的H
烯丙位、苯甲位、3oH、醚-位上的
H均易在C-H之间发生自动氧化。
反应机理:多数自动氧化是通过自由基机理进行的。
链引发: R• + O2
ROO•
ROO• + (CH3)2CHOCH3
ROOH + (CH3)2C•OCH3
优先形成稳 定的自由基
生成能力:ROR’ > ROAr > ArOAr
2. 醚键的断裂(与热的强酸HX作用 )
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
冠醚毒性大,价钱高。
3. 1,2-环氧化合物的开环反应
(1)碱催化开环(SN2)
通式: C C
Nu-
Nu δ-
CC
O
Nu
O
δ-
CC
O
O
H2C CH2 -OC2H5 -OCH2CH2OC2H5
C2H5OH HOCH2CH2OC2H5
*反应特点:碱作为Nu-从氧环背后进攻,断键
与成键同时进行,为SN2反应。对于不对称环 氧化合物,试剂选择进攻取代基较少(即位阻
§11.4 环醚
1. 环氧化合物
三元环:环氧某烷 大环:按杂环规则命名
eg. CH2CH2
O
环氧乙烷
CH3CH CH2 O
环氧丙烷
CH3CH CHCH3 O
2,3-环氧丁烷
O
四氢呋喃
OO
1,4-二氧六环
2. 冠醚 ——结构特征:分子中具有-(OCH2CH2)n-重复单 位。形状似皇冠,故统称冠醚 ——命名:n1-冠-n2
H
eg.
S
H3CH2C
O
H+
+ CH3OH
OMe
-H+
R
C H
CH2OH
CH2CH3
+ HOCH3
C H
CH2OH
CH2CH3
小结:
(1)碱催化反应:试剂活泼,亲核性强,进攻 位阻较小的环碳原子
CH3CH
CH2 +
HOROArORMgX
O
NH3(R)
LiAlH4
CH3CHOHCH2OH CH3CHOHCH2OR CH3CHOHCH2OAr
n1:醚环内原子的总数 n2 :醚环内氧原子的数目 ——制法:威廉逊合成法 ——用途:相转移催化剂(与金属离子络合)
由于该醚能与K+络合,使高锰酸钾能以络合物形式溶 于环己烯中,使氧化剂能很好地和反应物接触,氧化 反应速率大大加快,产率也大为提高。在这个反应中 冠醚实际上是促使氧化剂由水转移到有机相,是相 转移剂。所以冠醚被称为相转移催化剂。
CH3CHCH2R OMgX
CH3CHOHCH2NH2(R) [(CH3)2CHO]4AlLi
(2)酸催化反应:试剂进攻烃基取代基较多的 环碳原子(能形成稳定碳正离子)
CH3*CH
CH2 +
H2O H+ CH3 *CHOHCH2OH
H+
CH3OH
CH3O*CHCH2OH
OH H+
CH3 CH3
O*CHCH2OH
O
HX
CH3 *CHXCH2OH
HCN
CH3 *CHCNCH2OH
B2H6
(CH3CH2CH2O)3B
4. 环氧化合物的制法 (1)过氧酸氧化烯烃:取代基的相对位置不变
H C
C6H5
H C
C6H5
H
C
C6H5CO3H,C6H6
H
O
C6H5 25 C
C6H5
O CC
H C6H5
C C6H5 CH3CO3H H
较小)的环碳原子。
eg.
H3C
H5C2
C
CH2 + -OCH3
O
CH3OH
H3C H5C2
C CH2OCH3 OH
*立体化学:若被亲核试剂进攻的碳原子为 手性碳原子,则构型转化。
CH3
eg. H
R
R
O
H3C H
NH3.H2O
H3C H
OH H2N
SH
CH3
O
C2H5OH
OH H
-OC2H5
H OC2H5
Cl NaOH OH
NaOH
O 异构化
Cl OH
CH3 HO H (R) Br H (S)
C2H5
OH
CH3 H
HO
O
Br OH-
H C2H5
CH3
RR
H
O
H C2H5
5. 重要的环醚 (1)环氧乙烷
(2)四氢呋喃 (3)二氧六环
练习:用不超过三个碳的有机物及必要的试 剂合成:
1、(CH3)2CHCH2CH2OH 2、CH3O(CH2CH2O)2CH3 3、 CH3O CH2CH(CH3)OCH2CH(CH3 )OH 4、 CH3 CH2OCH2CH2OCH2CH2O CH3
H C6H5
O CC
C6H5 H
(2)β-卤代醇的成环(分子内William son反应)
OH
NaOH,H2O
Br CH3 H
C HOBr
C CH3 H
Br
H3C
H3C
H
H
OH
O
NaOH -HBr
H3C
H3C
H
H
O
注:若-OH与-Cl处于顺型,则不符合发生SN2反应的 立体化学要求,不能生成环氧化合物。
(2)酸催化开环(更容易)
过程:环氧化合物 酸
盐
O
+
H O
+
..
H
ROH
H2C CH2
H2C CH2
SN2 开环
δ+
OH
≠
H2C CH2
δ+OR
H
OH -H+
H2C CH2
+OR H
OH H2C CH2
OR
•不对称环氧化合物:亲核试剂进攻能生成较稳 定的碳正离子,即烃构型转化
