外泌体研究概述Exosome
外泌体研究方案的正确打开方式

外泌体研究方案的正确打开方式啥是外泌体?外泌体(Exosome)是一种由活细胞分泌的圆形(dish)或杯状(cup)脂质双分子层膜微小囊泡,直径约30-100nm,可由各种类型的细胞分泌,广泛存在于血液、尿液、唾液、滑膜液、乳汁、脑脊液、眼泪、腹水、羊水等各种体液以及细胞培养上清中。
外泌体是一种活性复合体,包含复杂的蛋白质,核酸和脂质。
最常见的外泌体蛋白组成包括膜转运和融合相关蛋白、多囊泡胞内体产生相关蛋白,(Alix, TSG101等)、分子伴侣(HSP70,HSP90)、整合素和四跨膜蛋白超家族(CD63,CD9,CD81, CD82等),这些成分反映了其生物起源。
外泌体还富含胆固醇、鞘脂、神经酰胺、糖脂GM3和含长饱和脂肪酰基的甘油磷脂链。
外泌体的起源外泌体的前身含有一个秘密武器,叫泛素化蛋白,被ESCRT(转运必需内体分选复合物)识别,形成内腔囊泡(ILVs),进一步形成膜性囊泡(MVBs),其中一部分会被降解为溶酶体,当MVBs与细胞膜发生融合后这些小囊泡可被释放到细胞外空间,称为外泌体。
外泌体生物功能2013年,美国科学家James E. Rothman, Randy W. Schekman 和德国科学家Thomas C. Sudhof因细胞囊泡运输的调节机制而荣获当年诺贝尔生理学或医学奖。
研究表明:外泌体有携带与运输功能,随着体液循环到达全身各个部位,通过与受体细胞的质膜保持稳定结合或经由内吞途径被内化,释放出外泌体中的内容物。
外泌体与靶细胞融合后,靶细胞的生物学特性可以在基因水平(外泌体RNA)转录水平(外泌体miRNA)或在蛋白水平发生改变,从而实现细胞间通信。
这些相互作用可能导致有益(如增强免疫状态)或有害(如扩散发病)的结果。
外泌体分离纯化方法外泌体鉴定方法NTA鉴定纳米颗粒跟踪分析(Nanopraticle Tracking Analysis, NTA)技术可以对10-2000nm范围内的纳米颗粒进行快速实时动态检测,测量参数包括颗粒粒径、散射光强、浓度等,可对外泌体进行粒径大小及数量进行统计并做出初步质量评估。
外泌体—药物靶向治疗利器

外泌体—药物靶向治疗利器1.外泌体简介外泌体(exosomes)是一种机体内大多数细胞分泌的微小囊泡,直径约为30 ~ 150 nm,具脂质双层膜,其形成机制非常简单,简而言之:“内吞-融合-外排”,如图所示,毫无违和感(图1a)。
从1980年首次发现外泌体至今,已有30多年的历史,最初被认为是细胞的“垃圾”,是细胞排泄废物的一种方式;2013年,科学家们发现细胞囊泡运输的调节机制,获得当年诺贝尔生理学或医学奖,开启了外泌体研究的新时代,此外,外泌体和微囊泡(图1b)、凋亡小体(图1c)明显不同,有鲜明的特点和潜在价值,时至今日,已逐步成为科研热点(图2)。
图1图22.外泌体作为药物载体的优势对于普通药物而言,通常在进入体内后仅有极少一部分才能够真正作用于病变部位。
这是制约药物疗效,并导致药物毒副作用的根本原因。
获取具有像导弹一样精准靶向能力的药物是人类的一个梦想,也是药物开发的终极目标。
随着药物研发进入靶向时代,越来越多的靶向药物成功上市,其中药物载体的设计研发愈发重要。
外泌体,作为天然的胞间信息载体,以其相对较小的分子结构,天然分子转运特性及良好的生物相容性,在药物载体领域存在巨大应用潜力。
较之现有的药物载体(如人工制造的脂质体), 外泌体有其显著的优越性:(1)不同来源外泌体表面分子不一, 对受体细胞有选择性, 治疗上更有利;(2)相对脂质体对亲水性物质较低的包装效率, 外泌体显著提高包装效率;(3)特殊细胞[如未成熟的DC细胞或充间质干细胞]中的外泌体, 由于特殊的表面分子,可避免与抗体、凝血因子等产生作用, 避免体内产生免疫反应。
尽管近年来在siRNA胞内递送方面取得较大进展,但针对特定组织或细胞类型靶向递送,同时避免非特异性递送,特别是对肝脏仍然具有挑战性;其二,siRNA或递送载体的免疫原性也是一个主要障碍。
而天然存在的RNA载体,如外泌体,可能会提供一个尚未开发的有效传递策略来源。
外泌体研究策略

6、Intercellular Transfer of lncARSR by Exosomes Disseminates Sunitinib Resistance
7、AXL and c-MET Are Responsible for lncARSR-Mediated Sunitinib Resistance
Tan A Advanced drug delivery reviews, 2013, 65(3): 357-367.
外泌体研究的兴起
外泌体研究基础技术
1、外泌体分离 1)超速离心 2)磁珠免疫捕获 3)沉淀或过滤法,
2、外泌体鉴定与定量 1)鉴定:电镜或NTA来分析其大小和形态,流式细胞仪或WB检测表面标记蛋白, Western blot和ELISA检测 TSG101、CD63。 2)定量:NTA检测外泌体数量,BCA定量检测蛋白浓度。
2、Annexin V, calcium, and BMP-2 in EMPs from HUVECs stimulated by TNF-a BMP-2表面标记流式检测;SN50 nf-kb抑制剂
3、The effect of EMPs from HUVECs stimulated by TNF-a on VSMC calcification
1、lncARSR Is Highly Expressed in Sunitinib-Resistant RCC Cells
2、lncARSR Is Modulated by AKT/FOXO Axis in Sunitinib-Resistant RCC Cells
3、lncARSR Is Required for Sunitinib Resistance of RCC
外泌体是什么?外泌体检测方法

外泌体是什么?外泌体检测方法外泌体是什么?外泌体(exosome)是是一种能被大多数细胞分泌的微小膜泡,这种微小膜泡中含有细胞特异的蛋白、脂质和核酸,能作为信号分子传递给其他细胞从而改变其他细胞的功能。
从细胞中提取外泌体后可以通过透射电镜来分析exosome的大小、形态等,再经过Western Blot可以分析特定蛋白在exosome中的表达情况。
外泌体中的蛋白、RNA和脂肪成分特异,并且携带了一些重要的信号分子,其在多种疾病的早期诊断中发挥着重要的作用。
如何提取外泌体?外泌体的提取方法有很多,例如超速离心法、密度梯度离心、超滤离心、PEG-base沉淀法、磁珠免疫法和试剂盒提取。
实验室常用的提取方法是如下两种:1、超速离心法(差速离心)超离法是常用的外泌体纯化手段,采用低速离心、高速离心交替进行(如图所示),可分离到大小相近的囊泡颗粒。
超离法因操作简单,获得的囊泡数量较多而广受欢迎,但过程比较费时,且回收率不稳定(可能与转子类型有关),纯度也受到质疑;此外,重复离心操作还有可能对囊泡造成损害,从而降低其质量。
2、试剂盒提取近几年来,市场上已出现各种商业化的外泌体提取试剂盒,有的是通过特殊设计的过滤器过滤掉杂质成分,有的则采用空间排阻色谱法(SEC)进行分离纯化,也有的则利用化合物沉淀将法外泌体沉淀出来。
这些试剂盒不需要特殊设备,随着产品不断更新换代,提取效率和纯化效果逐渐提高,因而逐渐取代超速离心法并推广开来。
有些试剂盒操作简便,不用超速离心,同时可获得高纯度和高回收率的外泌体。
外泌体粒径分析、浓度检测外泌体粒径分析方法为纳米颗粒跟踪分析(Nanoparticle tracking Analysis, NT A),其原理是对每个颗粒的布朗运动进行追踪和分析,结合Stockes-Einstein 方程式计算出纳米颗粒的流体力学直径和浓度。
NT A技术已被外泌体研究领域认可为外泌体表征手段之一。
相较于其他表征方式,NT A技术的样本处理更简单、更能保证外泌体原始状态、检测速度更快。
外泌体的研究进展

外泌体的研究进展一、本文概述随着生物医学研究的深入,细胞间的信息交流机制逐渐成为研究的热点。
作为细胞间交流的重要载体,外泌体(Exosomes)的研究在近年来取得了显著的进展。
本文旨在综述外泌体的基本特征、生物学功能及其在疾病诊断和治疗中的应用,同时探讨当前面临的挑战和未来的发展趋势。
我们将简要介绍外泌体的定义、结构特点以及产生机制,帮助读者理解其作为细胞间信息传递的重要角色。
接着,我们将重点讨论外泌体在肿瘤、心血管疾病、神经退行性疾病等医学领域的研究进展,包括外泌体在疾病发生发展中的作用机制,以及作为疾病标志物的潜力。
我们还将关注外泌体在疾病诊断和治疗中的应用前景,如作为药物递送载体、肿瘤疫苗以及生物标志物等方面的研究。
我们将对当前外泌体研究面临的挑战和未来的发展方向进行深入探讨,以期为推动外泌体在生物医学领域的应用提供有益的参考。
二、外泌体的结构与功能外泌体是一种由细胞主动分泌的,直径约为30-150纳米的膜性囊泡,普遍存在于各种体液中,包括血液、尿液、乳汁、脑脊液和细胞培养基等。
这些囊泡在细胞间的物质传递、信息交流以及免疫反应等方面发挥着重要作用。
近年来,随着外泌体研究的深入,其独特的结构和功能逐渐被人们所揭示。
结构上,外泌体由磷脂双分子层膜包裹着内部的水溶液组成,其膜上嵌有多种蛋白质,包括四跨膜蛋白、热休克蛋白、整合素等。
这些蛋白质不仅参与外泌体的形成和分泌过程,还负责将外泌体与靶细胞进行特异性结合,实现精准的物质传递。
外泌体的膜上还含有丰富的糖类和脂质,这些成分对于外泌体的稳定性和功能也至关重要。
功能上,外泌体具有多种生物学活性。
外泌体可以传递信息分子,如mRNA、miRNA、蛋白质等,这些分子在细胞间的信息交流过程中发挥着关键作用。
外泌体可以参与免疫反应,通过传递抗原或免疫调节分子,影响免疫细胞的活性和功能。
外泌体还具有促进血管生成、抑制肿瘤生长等多种生物学活性。
值得一提的是,外泌体的功能与其来源细胞密切相关。
外泌体 Exosome
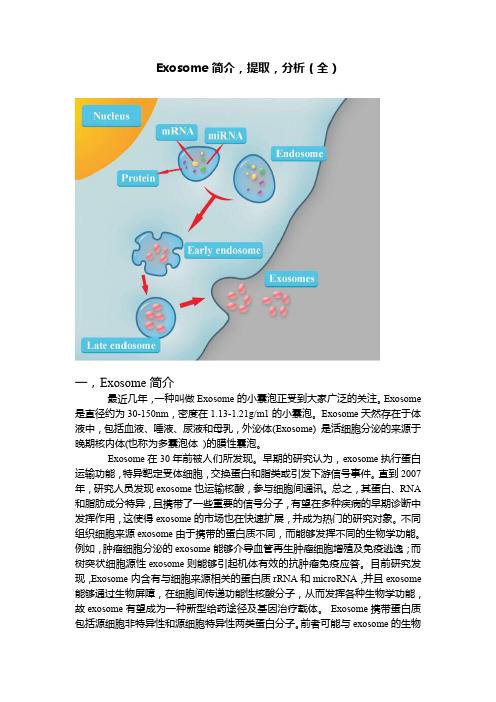
Exosome简介,提取,分析(全)一,Exosome简介最近几年,一种叫做Exosome的小囊泡正受到大家广泛的关注。
Exosome 是直径约为30-150nm,密度在1.13-1.21g/m1的小囊泡。
Exosome天然存在于体液中,包括血液、唾液、尿液和母乳,外泌体(Exosome)是活细胞分泌的来源于晚期核内体(也称为多囊泡体)的膜性囊泡。
Exosome在30年前被人们所发现。
早期的研究认为,exosome执行蛋白运输功能,特异靶定受体细胞,交换蛋白和脂类或引发下游信号事件。
直到2007年,研究人员发现exosome也运输核酸,参与细胞间通讯。
总之,其蛋白、RNA 和脂肪成分特异,且携带了一些重要的信号分子,有望在多种疾病的早期诊断中发挥作用,这使得exosome的市场也在快速扩展,并成为热门的研究对象。
不同组织细胞来源exosome由于携带的蛋白质不同,而能够发挥不同的生物学功能。
例如,肿瘤细胞分泌的exosome能够介导血管再生肿瘤细胞增殖及免疫逃逸;而树突状细胞源性exosome则能够引起机体有效的抗肿瘤免疫应答。
目前研究发现,Exosome内含有与细胞来源相关的蛋白质rRNA和microRNA,并且exosome 能够通过生物屏障,在细胞间传递功能性核酸分子,从而发挥各种生物学功能,故exosome有望成为一种新型给药途径及基因治疗载体。
Exosome携带蛋白质包括源细胞非特异性和源细胞特异性两类蛋白分子。
前者可能与exosome的生物发生和生物学作用有关,主要包括:细胞溶质蛋白、参与细胞内信号转导的蛋白、各种代谢酶、热休克蛋白和四跨膜蛋白;另一类是特殊蛋白质,这类蛋白质只存在于某种特殊的细胞分泌的exosome,而这些特定细胞源的exosome与其生物学功能有着密切联系,例如分子来源的Exosome上含有MHCII类分子。
二,Exosome提取Exosome是由活细胞分泌的,它是一种亚细胞成分,组要成分是磷脂双分子和携带的膜性分子,其界定依据形态学和生物化学及提取方式不同细胞源的exosome是不同的,这些不同的理化性质有利于exosome的提取。
不同人体细胞外泌体的特点及功能化研究-病理学论文-基础医学论文-医学论文

不同人体细胞外泌体的特点及功能化研究-病理学论文-基础医学论文-医学论文——文章均为WORD文档,下载后可直接编辑使用亦可打印——摘要:外泌体(exosomes)是一种活细胞分泌的囊性小泡,能携带脂质、蛋白质和遗传物质,在体内进行生物信息传输。
外泌体中独特的组织或细胞特异性蛋白质和遗传物质,可反映其细胞来源和细胞的生理状态,因此不同细胞来源的外泌体有不同的特点和功能。
基于其内源性、生物相容性和多功能特性,外泌体有望成为药物递送系统、免疫治疗、精准治疗的新手段。
本综述聚焦近年来报道的不同细胞分泌的外泌体的特点及功能化研究成果,对其进行归纳总结。
关键词:外泌体; 细胞来源; 药物递送载体; 疾病治疗;Abstract:Exosomes,cystic vesicles secreted by living cells,carry lipids,proteins and genetic materials,and transmits biological informations in the body. The unique tissue or cell-specific proteins and genetic materials in the exosomes generally reflect the cell origin and the physiological state of cells,so the exosomes from different cell sourcesappear to have different characteristics and functions. In view of the endogenous character,biocompatibility and functional versatility,the exosomes are expected to be a new means for the drug delivery systems,immunotherapies,and precision treatment. This review summarizes the exosomes secreted by different cells,focusing on the research achievement in their characteristics and functionalization studies in recent years.Keyword:exosomes; cell sources; drug delivery vehicles; disease treatment;外泌体(exosomes)是活细胞吞噬异源物质后以出芽方式向内凹陷形成含有多个小泡的多泡体(multivesicular body,MVB),再由多泡体与细胞膜融合而释放的小囊泡(图1)。
外泌体-活细胞吞噬异源物质后在细胞内形成内吞泡

外泌体(exosome)-活细胞吞噬异源物质后,在细胞内形成内吞泡,其中一部分内吞泡可以与溶酶体结合而降解,另一部分则在相关刺激因子的作用下,以出芽的方式向内凹陷,形成一个膜包围的结构,内含多个小囊泡外泌体(exosome)-活细胞吞噬异源物质后,在细胞内形成内吞泡,其中一部分内吞泡可以与溶酶体结合而降解,另一部分则在相关刺激因子的作用下,以出芽的方式向内凹陷,形成一个膜包围的结构,内含多个小囊泡,称其为多泡内涵体(multivesicular bodies,MVBs),小囊泡里主要成分是细胞质,由脂质双分子层包绕。
多泡内涵体泡膜最终与细胞膜融合,通过胞吐作用释放其中的小囊泡至泡外空间,即成exosome。
学术术语来源——人脐血间充质干细胞来源的外泌体:分离鉴定及生物学特性文章亮点:1 研究发现间充质干细胞是通过旁分泌有效生物学活性物质外泌体在细胞间进行信息传递,进而通过某种机制发挥组织损伤修复作用。
外泌体是间充质干细胞分泌的膜性小囊泡,含有来源细胞的膜蛋白成分,可以选择性地将含有的蛋白质、RNA等递送至受体细胞,调节细胞间的信号传导。
故可将间充质干细胞来源的外泌体开发成为一种既具有间充质干细胞的作用特点,又能规避其不良分化和肿瘤形成缺陷的新型治疗手段。
因此,通过间充质干细胞来源的外泌体促进组织损伤修复是今后具有重要探讨价值的研究方向。
2 分离提取及鉴定外泌体是进行深入研究的基础,实验主要通过超滤及差速离心法分离出外泌体,通过透射电镜及流式鉴定相结合来鉴定,为后续的外泌体功能研究奠定基础。
3偏倚或不足:人脐血间充质干细胞源性外泌体生物学功能及相关机制还需要进一步分析;人脐血间充质干细胞的外泌体最终要移入体内研究,所以尚需建立动物模型。
关键词:干细胞;脐带脐血干细胞;外泌体;人脐血间充质干细胞;分离鉴定;活性主题词:胎血;间质干细胞;外泌体;膜蛋白质类摘要背景:外泌体是间充质干细胞分泌的膜性小囊泡,越来越多的研究表明,间充质干细胞可能通过旁分泌外泌体而发挥对组织损伤的修复作用,目前人脐血间充质干细胞来源的外泌体分离鉴定尚未见报道。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
案例2
Exosome-Mediated miR-155 Transfer from Smooth Muscle Cells to Endothelial Cells Induces Endothelial Injuryr Therapy (2017)
1. 外泌体概述
2. 外泌体分离方法
(1)超速离心:
2000 g for 20 min to eliminate dead cells; 10,000 g for 30 min to remove debris; filtrated though 0.22 μm filter; 100,000 g for 70 min.
密度梯度超速离心:
蔗糖、碘克沙醇 1.15-1.19 g / mL
案例1
Adipose Tissue Macrophage-Derived Exosomal miRNAs Can Modulate In Vivo and In Vitro Insulin Sensitivity, Cell (2017)
/
EXOCARTA
/
VESICLEPEDIA
/
EVPEDIA
HTTP://STUDENT4.POSTECH.AC.KR/EVPEDIA2_XE/XE/
外泌体研究概述
exosome
| 1. 外泌体概述 | 2. 外泌体分离方法 | 3. 外泌体检测方法 | 4. 外泌体常用数据库
外泌体是细胞向胞外分泌的囊泡类小体,具有脂质双层膜结构, 可存在于细胞培养上清液、血浆、血清、唾液、尿液、羊水和恶 性腹水以及其它生物体液中。
外泌体携带特异性的蛋白质、脂质以及功能性的 mRNA、 ncRNA等生物活性物质,在体内参与细胞通讯、细胞迁移、促 血管新生和抗肿瘤免疫等生理过程,与多种疾病的发生和进程密 切相关。由于外泌体的特殊结构和功能, 使得它具有潜在的应用 价值,一方面可以作为诊断多种疾病的生物指标,另一方面也可 以作为治疗手段,未来有可能作为药物的天然载体用于临床治疗。
(3)分子筛层析:
Sepharose 2B or CL-4B,外加超速离心
Specific Isolation of Placenta‐Derived Exosomes from the Circulation of Pregnant Women and Their Immunoregulatory Consequences. American Journal of Reproductive Immunology (2006).
细胞实验一般方案
(4)共沉淀
(美国ExoQuick )
(5)免疫沉淀
外泌体不同分离方法比较
2. 外泌体检测方法
• 电镜
• 颗粒跟踪分析(particle tracking analysis)
• Western Blot
• ELISA
乙酰胆碱酯酶(AchE)
• 流式细胞仪
外泌体RNA分析
4. 外泌体常用数据库
(2)超滤:
Vivaspin 20,100 kDa MWCO (GE Life sciences)
Comparison of protein, microRNA, and mRNA yields using different methods of urinary exosome isolation for the discovery of kidney disease biomarkers. Kidney international(2012).
案例3
Circular RNA expression alteration in exosomes from the brain extracellular space after traumatic brain injury in mice, Journal of Neurotrauma(2018)
