三苯甲醇的制备
三苯甲醇

一、实验步骤及现象1 格氏试剂的制备步骤现象在三口瓶中放入0.4g镁,一粒碘,磁石;在滴液漏斗中装入2ml溴苯和7ml无水乙醚将1/3的混合液倒入溶液呈黄绿色(I2),无气泡生成开启搅拌器转动一会儿,再关闭有气泡产生继续搅拌溶液颜色逐渐变淡,最终呈无色将温度保持在32℃逐滴滴加溶液始终有汽包冒出,溶液呈微沸状态待加完溶液之后保持温度在34℃,待回流0.5h 溶液变成棕黄色从加热套中取出三口瓶让其自然冷却2 三苯甲醇的制备在滴液漏斗中装入1ml苯甲酸乙酯和2ml无水乙醚开动搅拌器滴加混合液溶液开始冒泡溶液颜色开始发生变化滴加完成后在将温度保持在34℃回流0.5h 溶液变为红色再变成黄色最终为灰绿色从加热套中取出三口瓶让其自然冷却在滴液漏斗中装入2g氯化铵和7-8ml水配成的混合溶液,并逐滴滴入三口瓶中溶液冒泡,呈绿色,混合后呈粘稠状放置一周3 水蒸气蒸馏放置一周后的溶液呈紫色安装蒸馏装置后,加热至微沸状态蒸馏有紫色的物质浮于溶液的表面一段时间后溶液呈棕黄色,在直型冷凝管中有白色的物质生成,同时再过一段时间之后,有多个黄色的球状的物质生成待直型冷凝管口的溶液出现的油状物质较少时停止蒸馏在空气中进行冷却,抽滤的粗样品。
称的出样品的质量为1.223g。
将粗产品研碎之后装入三口瓶中,向粗产品中加入8.5ml的95%乙醇,加热搅拌溶解溶液呈黄色加入活性碳溶液逐渐变为无色趁热进行过滤,放置在空气中让其自然结晶最后的看到棱状的晶体,在阳光的照射下折射出彩色的光芒待结晶完成之后进行过滤滤液仍呈黄色放置一周后称重得0.364g4 物理常数的测定取少量的晶体放到玻片上加热并记录晶体坍塌,初熔和全熔时的温度5 三苯甲醇的熔点测定数据记录熔点萎缩(℃)初熔(℃)全熔(℃)三苯甲醇1 157.8 161.3 1682 159.4 160.4 165.93 163.4 165.1二、实验步骤的图示三口瓶中放入0.4g镁,一粒碘,磁石→将1/3的混合液倒入→开启搅拌器→将温度保持在32℃逐滴滴加→待加完溶液之后保持温度在34℃,待回流0.5h→从加热套中取出三口瓶让其自然冷却→在滴液漏斗中装入1ml苯甲酸乙酯和2ml无水乙醚→开动搅拌器滴加混合液→滴加完成后在将温度保持在34℃回流0.5h→从加热套中取出三口瓶让其自然冷却→在滴液漏斗中装入2g氯化铵和7-8ml水配成的混合溶液,并逐滴滴入三口瓶中→放置一周→安装蒸馏装置→加热待直型冷凝管口的溶液出现的油状物质较少时停止蒸馏在空气中进行冷却,抽滤的粗样品→将粗产品研碎之后装入三口瓶中,向粗产品中加入8.5ml的95%乙醇,加热搅拌溶解→加入活性碳→趁热进行过滤,放置在空气中让其自然结晶→待结晶完成之后进行过滤→取少量的晶体放到玻片上加热并记录晶体坍塌,初熔和全熔时的温度三、实验结果的计算1三苯甲醇的产率以粗产品为参考,实验的产率=0.364∕1.223×100%=29.76%2 三苯甲醇的熔点熔程=(168-161.3+165.9-160.4+165.1-163.4)/3=4.63℃熔点在161.7℃到166.3℃之间四、讨论1 红色的中间产物应为。
三苯甲醇的制备课件

三苯甲醇的制备
三苯甲醇的制备
Hale Waihona Puke 三苯甲醇的制备三苯甲醇的制备
三苯甲醇的制备
三苯甲醇的制备
三苯甲醇的制备
15
三苯甲醇的制备
(1)将制备好的苯基溴化镁乙醚溶液置于冰浴中,在搅拌下 滴加1.9 mL (0.013mol)的苯甲酸乙酯和无水乙醚的混合液。滴 加完毕后,继续反应5min,然后将反应混合物在水浴加热回流 0.5小时。(反应物明显分为两层) (2)慢慢从冷凝管上口加入配好的饱和的氯化铵水溶液,改 成蒸馏装置,蒸出乙醚。然后进行水蒸气蒸馏,蒸出溴苯及副 产物。 (3)瓶中的剩余物冷却,过滤收集。再用80%的乙醇重结晶。
三苯甲醇的制备
三苯甲醇的制备
三苯甲醇的制备
此课件下载可自行编辑修改,供参考! 感谢您的支持,我们努力做得更好!
三苯甲醇的制备
实验5:三苯甲醇的制备及结构表征

实验五 三苯甲醇的制备及结构表征一、实验目的1. 了解格氏试剂的制备、应用和进行格氏反应的条件。
2. 进一步掌握搅拌、回流、萃取蒸馏(包括低沸点物蒸馏)等操作。
二、反应原理三苯甲醇可通过格氏试剂与苯甲酸乙酯与苯基溴化镁的反应制备: Br Mg MgBr+ MgBr COC 2H 5O OMgBrOC 2H5O C 2H 5OMgBr+C C +OMgBr OMgBrC +C42OHC三、实验装置图接氯化钙干燥管四、试剂及仪器仪器:半微量有机合成玻璃仪器;电动搅拌器;旋转蒸发仪;数显式熔点测定仪;红外光谱仪试剂:镁屑,溴苯,苯甲酸乙酯,无水乙醚,氯化铵,乙醇五、操作步骤1. 苯基溴化镁的制备如图安装好反应装置,瓶内放置0.8g镁屑及一小粒碘片,在滴液漏斗中混合5g溴苯及13mL无水乙醚。
先将三分之一的混合液滴入烧瓶中,反应开始后开动搅拌,缓缓滴放其余的溴苯醚溶液,滴加速度保持溶液呈微沸状态。
加毕后,继续回流1.5h。
2. 三苯甲醇的制备将已制好的苯基溴化镁试剂置于冷水浴中,在搅拌下由滴液漏斗滴加1.9mL苯甲酸乙酯和5mL无水乙醚混合液,控制滴加速度保持反应平稳地进行。
滴加完毕后,继续回流0.5h。
将反应液改为冰水浴冷却,在搅拌下由滴液漏斗滴加由3.8g氯化铵配成的饱和溶液,分解加成产物。
在旋转蒸发仪上蒸去乙醚,再将残留物进行水蒸汽蒸馏。
残留物冷却后抽滤,得到三苯甲醇粗产品。
3. 重结晶法提纯粗产物用95%进行重结晶,得三苯甲醇产品。
4. 产品表征(1)测定产品熔点。
(2)测定产品的红外光谱图。
*废液和固体废弃物倒入指定容器中。
六、注意事项1. 所用仪器、药品必须经过严格的干燥处理,否则反应很难进行,并可使生成的格氏试剂分解。
2. 卤代烃与镁的作用很难发生通常温热或用一小粒碘作催化剂,以促使反应开始。
3. 滴加的速度太快,反应过于激烈,不易控制,并会增加副产物的生成。
4. 为了使反应易于发生,故搅拌应在反应开始以后进行,若5min后反应仍不开始,可用温水浴或直接加入一小粒碘促使反应开始。
三苯甲醇的制备实验报告

三苯甲醇的制备实验目的:学习利用Grignard反应合成醇练习无水操作反应学习水蒸气蒸馏操作认识三苯甲基碳正离子反应原理:试剂药品:0.5g(0.021moI)镁屑,3.3g(2.2mL,0.021mo1)溴苯(新蒸),1.33g(1.3mL,0.009mo1)苯甲酸乙酯,无水乙醚,2.5g氯化铵,乙醇实验步骤:1.苯基溴化镁的制备如图在50mL三颈瓶上分别装置搅拌器、冷凝管及滴液漏斗,在冷凝管及滴液漏斗的上口装置氯化钙干燥管。
瓶内放置0.5g镁屑及一小粒碘片,在滴液漏斗中混合3.3g溴苯及8mL无水乙醚。
先将三分之一的混合液滴入烧瓶中,数分钟后即见镁屑表面有气泡产生,溶液轻微混浊,碘的颜色开始消失。
若不发生反应,可用水浴或手掌温热。
反应开始后开动搅拌,缓缓滴入其余的溴苯醚溶液,滴加速度保持溶液呈微沸状态。
加毕后,在水浴继续回流0.5h,使镁屑作用完全。
2.三苯甲醇的制备将已制好的苯基溴化镁试剂置于冷水浴中,在搅拌下由滴液漏斗滴加1.3mL苯甲酸乙酯和3mL无水乙醚的混合液,控制滴加速度保持反应平稳地进行。
滴加完毕后,将反应混合物在水浴回流0.5h,使反应进行完全,这时可以观察到反应物明显地分为两层。
将反应物改为冰水浴冷却,在搅拌下由滴液漏斗慢慢滴加由9mL水和2.5g氯化铵配成的溶液,以分解加成产物。
将反应装置改为蒸馏装置,在水浴上蒸去乙醚,再将残余物进行水蒸气蒸馏,以除去未反应的溴苯及联苯等副产物。
瓶中剩余物冷却后凝为固体,抽滤收集。
得三苯甲醇粗产品1.72g(淡黄色固体)。
用80%的乙醇进行重结晶,干燥后得白色颗粒状晶体1.60g。
3.三苯甲基碳正离子的检验在一洁净的干燥试管中,加入0.01g三苯甲醇和2mL冰醋酸,温热使其溶解,向试管中滴加2滴浓硫酸,立即生成橙红色溶液,然后加入2mL水,颜色消失,并有白色沉淀生成。
产率:以苯甲酸乙酯(M260)的量为基准计算产率:1.60/(0.009ⅹ260)=68%欢迎您的下载,资料仅供参考!致力为企业和个人提供合同协议,策划案计划书,学习资料等等打造全网一站式需求。
三苯甲醇的制备

三苯甲醇的制备三苯甲醇的制备一、实验目的1.了解格氏试剂的制备、应用和格氏反应的条件。
2.掌握制备三苯甲醇的原理和方法。
3.掌握搅拌、回流、萃取、蒸馏等基本操作。
二、实验原理1. 格氏试剂的制备BrMgBrI2+ Mg无水乙醚2. 格氏试剂反应合成三苯甲醇OMgBrO无水乙醚C+2OMgBrCl / HONH42COH3. 副反应BrMgBr无水乙醚+三、试剂0.75g(0.032mol)镁屑,5g(3.5ml,0.032mol)溴苯(新蒸),2g(1.9ml,0.013mol)苯甲酸乙酯,无水乙醚,4g氯化铵,乙醇。
四、物理参数1、三苯甲醇:英文名称:Triphenylmethanol, Triphenylcarbinol, Trityl alcohol Cas号:【76-84-6】MDL号:--MFCD00004445Beilstein 号:1460837 EINECS: --200-988-5分子式:CHO;(CH)COH 结构式: 1916653分子量:260.33性质:片状晶体。
熔点164.2?;沸点380?。
相对密度1.199。
折光率:1.1994溶解性:不溶于水和石油醚,溶于乙醇、乙醚、丙酮、苯,溶于浓硫酸显黄色。
化学性质:羟基很活泼,与干燥氯化氢在乙醚中生成三苯氯甲烷。
与一级醇作用成醚。
用锌和乙酸还原得三苯甲烷。
由三苯氯甲烷水解,或溴化苯基镁(格利雅试剂)与二苯甲酮(或苯甲酸乙酯)制备。
用途:有机合成中间体。
市场价:65000元,吨顺强生物科技有限公司阿里巴巴-化工 2012/3/14。
2、溴苯:中文名: 溴苯外文名: bromobenzene别名: 一溴代苯分子式: CHBr 结构式: 65相对分子质量: 157.02熔点(?): —30.7沸点(?):156.2相对蒸气密度(空气=1):5.41外观与性状: 无色油状液体,具有苯的气味。
溶解性:不溶于水,溶于甲醇、乙醚、丙酮、苯、四氯化碳等多数有机溶剂。
三苯甲醇的制备
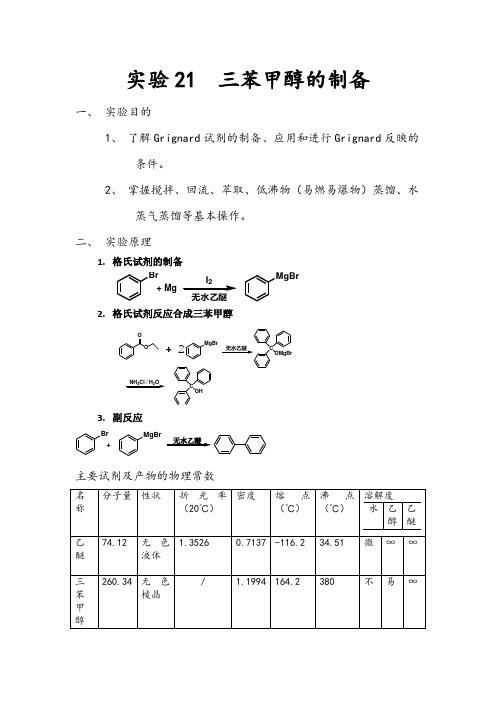
熔点:
48.5
305.4
不
溶
溶
联苯
154.21
无色片状晶体
1.5888
0.8660
71
255.9
不
溶
溶
三、实验内容
1、苯基溴化镁制备
2、 在100mL三颈烧瓶上分别装上恒压滴液漏斗、球形冷凝管(带无水CaCl2gan干燥管),放进磁石 向瓶中加入0.5g(0.02moL)剪碎的镁、一小粒碘 恒压漏斗中加入2.1mL(0.02mol)溴苯和15mL无水乙醚混合均匀 滴入约1-2mL混合液(浸没镁条),(数分钟后见溶液微沸,碘颜色消失) 开动搅拌器,继续滴加其余混合液(控制滴加速度),维持微沸状态(如果发现反应液粘稠,则补加适量乙醚) 滴完后,温水浴回流至镁条反应完全(约30min)
密度
熔点(℃)
沸点(℃)
溶解度
水
乙醇
乙醚
乙醚
74.12
无色液体
1.3526
0.7137
-116.2
34.51
微
∞
∞
三苯甲醇
260.34
无色棱晶
/
1.1994
164.2
380
不
易
∞
溴苯
157.02
无色液体
1.5597
1.4950
-30.82
156
不
易
易
二苯甲酮
182.22
白色至淡黄色结晶
1.6077
1.1146
4、引发反应时,所用碘量不能太大,以1/3粒大小为宜
5、制备格氏试剂时,溴苯和乙醚混合液滴加速度不能太快
6、所制备的格氏试剂是混浊有色液体,若为澄清可能瓶中进水没制好格氏试剂
化学实验报告——三苯甲醇的合成

三苯甲醇的合成一、 实验目的和要求1、 了解无水条件下的实验操作要求;2、 掌握无水乙醚制备方法;3、 了解Grignard 反应;4、 掌握水蒸气蒸馏操作;5、 熟练掌握混合溶剂重结晶及熔点测定。
二、 实验内容和原理卤代烷在无水乙醚中和金属镁作用后生成的烷基卤化镁RMgX ,称为Grignard 试剂。
实验中,结构复杂的醇通常由Grignard 试剂来制备。
R X + Mg + 2(C 2H 5)2OMg(C 2H 5)2O (C 2H 5)2OR XX=Cl,Br,IGrignard 试剂实际是烷基卤化镁与二烷基镁和卤化镁的混合物。
芳香族氯化物和氯乙烯类型的化合物,在上述无水乙醚为溶剂的条件下,不易生成Grignard 试剂。
但如果改用碱性比乙醚稍强,沸点较高的四氢呋喃(沸点66℃)作溶剂,它们也能生成Grignard 试剂,并且操作比较安全。
Grignard 反应必须在无水、无氧和无CO 2的条件下进行。
微量水的存在,不但会阻碍卤代烷和镁之间的反应,同时会破坏Grignard 试剂而影响产率。
因此,反应时最好用氮气赶走反应瓶中的空气。
一般在乙醚作溶剂时,由于乙醚的挥发性大,也可以借此赶走反应瓶中的空气。
此外,在Grignard 反应中,有热量放出,所以反应液滴加速度不宜过快。
必要时反应瓶需要用冷水冷却。
Grignard 试剂与醛酮等形成的加成物,在酸性条件下可以进行水解反应。
如通常用稀盐酸或稀硫酸使产生的碱式卤化镁转变成易溶于水的镁盐,以便于乙醚溶液和水溶液分层。
由于水解时放热,因此要在冷却下进行。
对遇酸极易脱水的醇或易发生卤代反应的醇,最好用饱和氯化铵溶液进行水解。
反应式如下:OMgBr42OH苯甲酸甲酯与苯基溴化镁的反应:COCH 3OMgBretherOMgBr副反应:Grignard 试剂是一个强亲核试剂,除了与羰基化合物加成外,Grignard 试剂中的烃基负离子还可以与CO 2、O 2等加成,能被活泼氢分解。
有机化学实验三苯甲醇的制备

有机化学实验三苯甲醇的制备中山大学实验报告 2010-10-29学院: 专业: 学号: 姓名:实验题目:三苯甲醇一(实验目的:1,学习用格式试剂反应制备醇2,学习无水反应~水蒸气蒸馏~有机溶剂重结晶操作二(反应原理及反应方程式:概述:格式试剂与羰基化合物加成生成醇实验室制备醇的重要途径之一利用羰基化合物,醛>酮>酯,与格式试剂反应生成醇。
利用格式试剂与甲醛~环氧乙烷或者是卤代醇的反应制备一级醇,与醛或者甲酸酯,2倍格氏试剂,的反应制备二级醇,与酮~酯~酰氯~不饱和酸酯或者酸酐反应制备三级醇反应制备三级醇。
本实验采用格氏试剂与苯甲酸甲酯制备三苯甲醇~而格氏试剂则用镁和溴苯作为反应原料在无水乙醚的溶剂中~和一小粒碘来活化镁。
来反应制备格氏试剂。
1, 格氏试剂的制备格氏试剂很活泼可以与水和含有酸性氢的有机化合物,ROH,RSH,RCOH,RNHH,RCONHH,RCCH,RSOH,反应也可以和 2223氧发生反应。
反应式如下RMH+HOR-H+XMOH g2gRMH+[O] ROMXR—H+XMOH ggg反应之前需要通入氮气一赶走反应瓶中的空气。
乙醚则为反应溶剂严格不准见水~挥发性大~蒸气可赶走瓶中的空气~但是在需要较高温度下反应时也可以用四氢呋喃等。
镁则应用细小的镁屑或者是镁粉~事先可在60到80摄氏度下干燥30分钟~再经真空干燥保存于密闭的玻璃容器中。
必要时可用碘活化镁~将理论计算量的镁喝少量的碘放进反应瓶中~小火加热至瓶中充满碘蒸气~待冷却后再加入其它的试剂进行反应。
在制备格氏试剂的过程中注意滴加卤代烷的方法。
之前先加入少量的卤代烷乙醚溶液和镁作用~待反应引发之后~再将其他剩余的卤代烷缓慢的滴入~使乙醚保持微沸腾~若是一次加入太多的卤代烷反应剧烈且不易控制~也会有自身的耦合反应。
必要时可用冷水冷却~而对于引发反应很难可以适当的加热2, 三苯甲醇的制备格氏试剂与醛酮等形成的加成产物进行酸性水解的时候镁变为易溶于水的镁盐便于乙醚与水分层。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三苯甲醇的制备
一、 实验目的
1.了解格氏试剂的制备、应用和格氏反应的条件。
2.掌握制备三苯甲醇的原理和方法。
3.掌握搅拌、回流、萃取、蒸馏等基本操作。
二、 实验原理
1. 格氏试剂的制备
Br
MgBr + Mg 2. 格氏试剂反应合成三苯甲醇 MgBr O O
C OMgBr +C OH NH 4Cl / H 2O
2
3. 副反应 MgBr Br
无水乙醚+
三、 试剂
0.75g (0.032mol )镁屑,5g (3.5ml ,0.032mol )溴苯(新蒸),2g (1.9ml ,0.013mol )苯甲酸乙酯,无水乙醚,4g 氯化铵,乙醇。
四、物理参数
1、三苯甲醇:
英文名称:Triphenylmethanol, Triphenylcarbinol, Trityl alcohol Cas 号:【76-84-6】
MDL 号:--MFCD00004445
Beilstein 号:1460837 EINECS: --200-988-5
分子式:C
19H
16
O;(C
6
H
5
)
3
COH 结构式:
分子量:260.33
性质:片状晶体。
熔点164.2℃;
沸点380℃。
相对密度1.199。
折光率:1.1994
溶解性:不溶于水和石油醚,溶于乙醇、乙醚、丙酮、苯,溶于浓硫酸显黄色。
化学性质:羟基很活泼,与干燥氯化氢在乙醚中生成三苯氯甲烷。
与一级醇作用成醚。
用锌和乙酸还原得三苯甲烷。
由三苯氯甲烷水解,或溴化苯基镁(格利雅试剂)与二苯甲酮(或苯甲酸乙酯)制备。
用途:有机合成中间体。
市场价:65000元/吨顺强生物科技有限公司阿里巴巴-化工2012/3/14。
2、溴苯:
中文名:溴苯
外文名: bromobenzene
别名:一溴代苯
分子式: C
6H
5
Br 结构式:
相对分子质量: 157.02
熔点(℃):—30.7
沸点(℃):156.2
相对蒸气密度(空气=1):5.41
外观与性状:无色油状液体,具有苯的气味。
溶解性:不溶于水,溶于甲醇、乙醚、丙酮、苯、四氯化碳等多数有机溶剂。
用途:用作压敏和热敏染料的原料;二苯醚系列香料的原料;农药原料,生产杀虫剂溴螨酯;医药原料,生产镇痛解热药和止咳药。
市场价:27000/吨盐城市云峰化工有限公司阿里巴巴-化工2012/3/14 。
3、苯甲酸乙酯:
中文名:苯甲酸乙酯
外文名: ethyl benzoate
分子式: C
9H
10
O
2
结构式:
相对分子质量: 150.17
熔点(℃):—34.6
沸点(℃):212.6
相对密度(水=1):1.05
外观与性状:无色澄清液体,有芳香气味。
低毒,半数致死量(大鼠,经口)2100mG/kG。
化学性质:遇明火、高热可燃。
溶解性:微溶于热水,与乙醇、乙醚、石油醚等混溶。
用途:常用于较重花香型中,尤其是在依兰型中,其他如香石竹、晚香玉等香型香精。
亦适用于配制新刈草、香薇等非花香精中。
可与岩蔷薇制品共用于革香型香精。
也用做食用香料,在鲜果、浆果、坚果香精中均可适用,如香蕉、樱桃、梅子、葡萄等香精以及烟用和酒用香精中。
市场价:13800元/吨上海昊天化工有限公司阿里巴巴-化工2012/3/14 。
4、无水乙醚:
中文名称:无水乙醚
英文别名:Diethyletheranhydrous,Diethyletherabsolute,Etheranhydrous
分子式: C
4H
10
O 结构式:
相对分子质量:74.12
性状:同乙醚,但水分含量较少。
剧烈振摇时可能产生静电而起火沸点:34.5℃
凝固点:-116.3℃
溶解性:溶于乙醇、苯、氯仿及石油,微溶于水。
用途:主要用作溶剂、麻醉剂和化学试剂
3.6—6.5%的乙醚就可导致人的昏迷,起麻醉作用
7~10%的乙醚可导致人的呼吸停止
10%以上的乙醚会导致人的死亡
分式C
4H
10
O,结构简式CH
3
CH
2
—O—CH
2
CH
3
是无色易挥发有特殊气味的液
体,使用时应避开火源,注意安全。
乙醚微溶于水,能溶解多种有机物是良好的有机溶剂。
纯净的乙醚在
医疗上用做手术时的全身麻醉剂。
工业上乙醚可由乙醇分子间脱水制
得:
随着石油工业发展,乙醚亦可由石油化工产物乙烯制取,其方法是用
硫酸吸收乙烯,形成硫酸乙酯,再水解得到乙醇和乙醚。
通过改变温
度和试剂浓度,可控制生成醇和醚的比例。
市场价:12.4元/500ml 南京化学试剂有限公司阿里巴巴-化工 2012/3/14 5镁屑
市场价:17800元/吨北京元创镁业有限公司阿里巴巴-化工 2012/3/14 6氯化铵
市场价:1300元/吨武汉市楚江化工有限公司阿里巴巴-化工 2012/3/14
五、实验步骤
1、苯基溴化镁的制备
在100ml的三颈烧瓶加入0.75g镁屑,一小粒碘和搅拌磁子,烧瓶上安装冷凝管和滴液漏斗,在冷凝管及滴液漏斗的上口装置氯化钙干燥器,在滴液漏斗中混合5g溴苯及16ml乙醚。
,将其1/3由恒压滴液漏斗滴加到反应瓶中,用手温热反应瓶,使反应尽快发生。
若反应仍不能发生,加一粒碘诱发反应。
当反应较为平稳后,将剩余的溶液慢慢滴入反应瓶(保持微沸)。
滴加完毕后,继续将反应瓶置于40ºC水浴上保持微沸回流使镁几乎完全溶解。
(约1 h)
2、三苯甲醇的制备
用冷水冷却反应瓶,搅拌下将1.9 ml苯甲酸乙酯与7 ml无水乙醚混合液逐滴加入其中。
滴加完毕后,将反应混合物在水浴回流约1 h,使反应完全。
将反应物改为冰水浴冷却。
反应物冷却后向其中慢慢滴加由4 g氯化铵配成饱和水溶液(约15 ml),然后改为水蒸气蒸馏装置,水浴蒸出乙醚。
瓶中剩余物冷却后凝为固体,抽滤,烘干,称重。
粗产物用80% 的乙醇进行重结晶,干燥称量后的产物约2—2.5g。
熔点在161—162℃纯三苯甲醇的熔点为162.5ºC。
3、实验装置
六、实验数据记录
实验时间: 2012/3/22
14:30实验开始及投料。
14:32有气泡产生并溶液成暗红色。
14:34暗红色开始消失。
15:30苯基溴化镁制备完成且在1h内温度始终保持在35~40℃。
15:40搅拌下由滴液漏斗滴加1.9 ml苯甲酸乙酯和7 ml无水乙醚混合液,水浴回流1h,反应物溶液颜色由灰绿变为紫红色。
16:40 冰水浴冷却后在搅拌下由滴液漏斗滴加由4g氯化铵配成的约15ml 饱和水溶液,反应物变成浅绿色。
16:55 开始蒸馏,5 min后开始有溜出液;20 min后抽滤,干燥后粗产品为1.18g。
2012/3/23 13:30用80%乙醇重结晶,抽滤、烘干,得精产品1.02g.
七、实验数据处理
2
C
OH
157.02*2 260.34
5g M理论
所以M理论=4.15g
实际产品=1.02g
产率(W%)=实际产品÷理论产品×100%=1.02÷4.15×100%=24.8%
成本=(0.75*17800+5*27000+2*13800+4*1300) ÷2*106+(16+7)*12.4÷500=0.75元
产值=1.02*65000÷2*106=0.063
亏本=产值-成本=0.063-0.75=-0.69元
八、注意事项
[1] 反应所用溶剂是乙醚,易燃、易爆、易挥发,所以整个实验过程严禁使用明火。
[2] 反应过程中,乙醚会挥发较多,需要补充一定的乙醚。
[3] 二苯甲酮和苯基溴化镁反应时,反应液会出现淡红色,并且有可能整个反应液固化,这
都是正常现象。
九、讨论
本实验的关键步骤是制备Grigand试剂,所以制备Grigand试剂时滴加速度不能太快,
否则反应过于剧烈不易控制,增加副产物的生成。
所制备的Grigand试剂是呈混浊有色溶液,若为澄清可能瓶中进水没制好格式试剂。
[思考] P.103 第1,2题
[1] 本实验的成败关键何在?为什么?为此采取什么措施?
答:本实验的成败关键是,整个反应体系和所使用试剂都要求无水。
如果在反应过程中有水引入,Grignard试剂将难于制得,或者所制得的Grignard试剂质量较差,会直接导致产物产率低。
为使反应能顺利进行,所使用的仪器都必须彻底烘干,反应体系要装上干燥管;所使用的药品均要进行无水处理。
[2] 本实验中溴苯滴加太快或者一次加入,有何影响?
答:本实验中溴苯滴加太快或者一次加入,会导致反应剧烈不易控制,可能会使反应液冲出,导致反应失败;同时会有大量副产物生成,使产物产率低,产物难于提纯。
