第十三章羧酸(不饱和,取代羧酸)
大学有机化学第十三章羧酸

CH3-C CH-COOH CH3
4
3
2
1
3-甲基-2-丁烯酸
取代酸
CH
CHCOOH
3-苯基丙烯酸(肉桂酸) ( -苯基丙烯酸)
◆ 羧酸的物理性质
O R C
=
O
H O
H H H
R C
=
O
H O O
O H
O H
=
C R
羧酸是极性分子,能与水形成氢键,故低级一元酸可 与水互溶,但随M↑,在水中的溶解度↓,从正戊酸开始 在水中的溶解度只有3.7 %,>C10的羧酸不溶于水。
O CH3C OH + NH3
CH3COOH + NH3
O
CH3C O.NH4 200℃CH C NH 3 2
CH3COONH4 Δ CH3CONH2 + H2O
-+
O
二元酸的二铵盐受热则发生分子内脱水兼脱氨,
生成五元或六元环状酰亚胺。
C H2C O O NH 4 C H2C O O NH 4
O
300℃
回流
ClCH2COOH
Cl2 , P
一氯乙酸
Cl2CHCOOH
回流
Cl2 , P Cl3CCOOH
二氯乙酸
回流
三氯乙酸
α-卤代酸是一种重要的取代酸,它可以发生与卤代烃相 似的亲核取代或消去反应,从而转变成其它的取代酸。
如:
CH3COOH Br2 ,P BrCH2COOH NaCN NCCH2COOH α-氰基乙酸
b.p: 羧酸 > M 相同的醇。
IR谱:
OH伸缩振动—
二聚体:2500~3300cm-1(宽而散);
单体: 3550cm-1(气态或非极性溶剂的稀溶液)。 C=O伸缩振动——脂肪族羧酸:1700~1725cm-1 芳香族羧酸:1680~1700cm-1
第十三章 羧酸

O
BrCH2CH2CH2COOH CH3CH CHCH2CH2C OH
4–溴丁酸 溴 (4-bromobutanoic acid)
COOH
1 5 4 2 3
4–己烯酸 己烯酸 (4-hexenoic acid)
COOH
1–环戊烯甲酸 环戊烯 环戊 (1-cyclopentenecarboxylic acid)
O H C O
O H C O
-
1.27Å
两个碳氧键等长,完全离域。 两个碳氧键等长,完全离域。
羧酸的分类: 羧酸的分类:
O R C OH
按羧基数目分:一元,二元,三元, 按羧基数目分:一元,二元,三元,多元酸 按烃基类型分:脂肪酸,芳香酸,饱和酸, 按烃基类型分:脂肪酸,芳香酸,饱和酸,不饱和酸
13.1.2 一元羧酸的命名
羧酸的命名: 羧酸的命名:
• 选择含羧基的最长的C链为主链,称“某酸”。 选择含羧基的最长的C链为主链, 某酸” • 含脂环和芳环的羧酸:当羧基直接与环相连时,“环的 含脂环和芳环的羧酸:当羧基直接与环相连时, 甲酸” 当羧基与侧链相连时,环作为取代基; 名称 + 甲酸”;当羧基与侧链相连时,环作为取代基;当 环上和侧链都连有羧基时,以脂肪酸为母体。 环上和侧链都连有羧基时,以脂肪酸为母体。 • 英文命名:将烷烃命名的后缀“e”改为“oic acid”。 英文命名:将烷烃命名的后缀“ ”改为“ ”
O R-C-O
-
O
NH4+
t
室温
RC-OH + NH3
P2O5 t
t -H2O
O RC-NH2
RC≡N + H2O ≡
反应是可逆的,加热、脱水有利于正反应, 反应是可逆的,加热、脱水有利于正反应, 为了使正反应顺利进行,常采用苯、 为了使正反应顺利进行,常采用苯、甲苯带水的 方式除去反应体系中产生的水。 方式除去反应体系中产生的水。
第十三章 取代羧酸
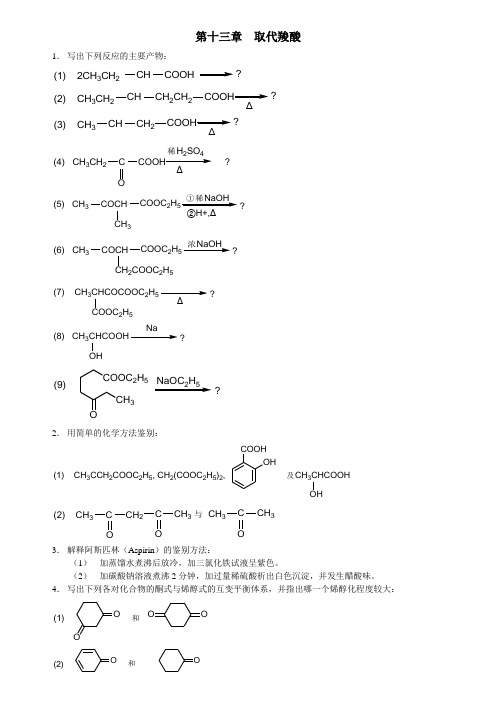
第十三章 取代羧酸1. 写出下列反应的主要产物:(1) 2CH 3CH 2CH COOH ?(2) CH 3CH 2CH CH 2CH 2?COOH Δ (3) CH 3CH CH 2?COOHΔ (4) CH 3CH 2C ?Δ稀H SO O (5) CH 3COCH?COOC 2H ②H+,Δ①稀NaOH CH 3 (6) CH 3COCH ?COOC 2H 浓NaOH CH 2COOC 2H 5(7) CH 3CHCOCOOC 2H 5?COOC 2H 5(8) CH 3CHCOOH?OH (9)COOC 2H 5CH 3O ?NaOC 2H 52. 用简单的化学方法鉴别:(1) CH 3CCH 2COOC 2H 5, CH 2(COOC 2H 5)2,COOH OH及CH 3CHCOOHOH(2) CH 3CCH 2C CH 3 与 CH 3C CH 3O O O3. 解释阿斯匹林(Aspirin )的鉴别方法:(1) 加蒸馏水煮沸后放冷,加三氯化铁试液呈紫色。
(2) 加碳酸钠溶液煮沸2分钟,加过量稀硫酸析出白色沉淀,并发生醋酸味。
4. 写出下列各对化合物的酮式与烯醇式的互变平衡体系,并指出哪一个烯醇化程度较大: (1)O O 和O O (2)O 和O(3) CH3COCH2COCH3和CH3COC(CH3)2COCH35.由乙酰乙酸乙酯或丙二酸二乙酯及其他原料合成下列化合物:(1)3-甲基-2-戊酮(2)2-甲基丁酸(3)α,β-二甲基丁二酸(4)环戊烷-1,2-二羧酸6.由指定原料合成下列化合物:(2)由环戊酮合成(i)OHCOOH(ii)OHCH2COOH(2)由CH3(CH2)3COOC2H5合成CH3(CH2)3COCOOH(3)由环己酮合成OCOOC2H57.提出一个反应历程以解释下列反应的结果:8.化合物A(C5H8O3)的IR谱在3400cm-1~2400cm-1和1760cm-1,1710cm-1有强吸收峰。
有机化学:第十三章羧酸及其衍生物

2. 酸酐的生成
用P2O5作脱水剂制备酸酐
O CH3 C OH O O P2O5 CH3 C O O C CH3
+
HO
C CH3
+
H2O
用低沸点酸酐作脱水剂制备较高沸点的酸酐
O 2 COOH + (CH3CO)2O
(
C
) 2O + 2 CH COOH
3
能形成五元、六元环酸酐的二元羧酸可直接加热制备酸酐
羧酸与PX3 、PCl5(X=Cl、Br)、SOCl2反应
3CH3COOH + PCl3
3 CH3 COCl + H3PO3
COOH+PCl5
(CH3)2CHCH2COOH + SOCl 2
COCl + POCl3+ HCl
(CH3)2CHCH2COCl
+
SO2
+ HCl
注:HX不能与羧酸反应生成酰卤 。 应用:酰卤的反应活性比较高,广泛应于药物合成中 。
( 2)编号:从羧基碳原子开始用阿拉伯数字编号,按所含碳原
子数目称为某酸,取代基名称及位次写在某酸之前。
( 3)简单的酸酸,常用希腊字母表明取代基的位置,从羧基相 邻碳原子开始编号为 ,依次为 、 、 等,将编号写在取代基 名称前面。
CH3CH2CHCH2COOH CH3
-甲基戊酸(3-甲基戊酸)
第十三章
羧酸及其衍生物 主要内容
1、掌握羧酸和取代羧酸的结构、命名和化学性质 2、掌握羧酸衍生物的结构、分类及命名和化学性质
3、熟悉羧酸和取代羧酸的物理性质
4、掌握羟基酸、酮酸的命名及主要化学性质。
羧酸:
有机化学第十三章 取代羧酸
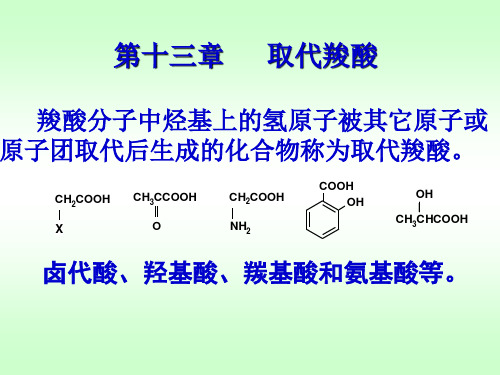
C HO 浓NaOH CH2OH COOH ’ COOH C anniz z aro 反 应 COOH + COOH
三
丙酮酸: 最简单的α -酮酸
CH3
O C COOH
CH3 CH3
O 浓 H2SO4 CO + CH3 COOH(脱羰) C COOH O 稀 H2SO4 CO + CH CHO (脱羧) 2 3 C COOH
OH O C6H5C=CHCCH 3 90.0%
2 乙酰乙酸乙酯的分解反应 稀OH-
O O CH3C-CH 2-COC 2H5
浓OH-
O CH3CCH3
酮式分解
O CH3C-OH + 其余 酸式分解
3 α-H的活性:被取代
O O CH3C-CH2-COC 2H5
RONa
O Na+ O CH3C-CH--COC 2H5
稀 OH -
CH3COCHC 2H5 CH3
1. 合成甲基酮 经乙酰乙酸乙酯合成:
引入基团
引入基团
CH3 CH3CO CHCH 2CH 3
CH3CO CH 2CH 3
分析:(1) 产物为甲基酮,合成时一定要经过酮式分解。 (2) 将TM的结构与丙酮进行比较,确定引入基团。 (3) 最后确定合成路线。
O C COOH
CO2
RCHO O
CO2
R
C
CH 3
四 醇酸的制备 1 α-羟基酸 羟基腈水解( “醛的化学性质”)
O R-C-R(H) + HCN
2 β-羟基酸(酯)
OH R-C-R(H) CN
H3O
+
OH α R-C-R(H) COOH
取代羧酸

第十三章 取代羧酸碳链或碳环上的氢被其他原子或基团取代所生成的化合物,称为取代羧酸。
常见的取代羧酸有卤代酸、羟基酸、羰基酸和氨基酸等,它们无论在有机合成或生物代谢中,都是十分重要的。
第一节 羟基酸的分类、命名和来源定义:分子中同时含有羟基和羧基得化合物叫做羟基酸。
一、 分类羟基酸可以分为醇酸和酚酸两类,羟基连接在碳链上的叫做醇酸;羟基连接在芳环上的叫做酚酸。
二、 命名羟基酸的命名常根据它的来源而采用俗名,也可以把它们看成是羧酸的羟基取代物来命名。
根据分子中羟基和羰基的相对位置,有α、β、γ……等羟基酸,或按系统命名编号,羧基碳原子编号为1,选择含羟基和羧基的最长碳链为主链。
如:COOH CH 2CH COOHCOOH CH CH COOHOH OH OH CH 3CH OHCOOHCOOHOH2-羟基丙酸(乳酸)羟基丁二酸(苹果酸)2,3-二羟基丁二酸 (洒石酸)2,3-二羟基丁二酸 (洒石酸)三、 来源羟基酸有的可用生物化学法制备,如乳酸。
化学合成法可从含羟基的化合物中引入羧基或含羧基的化合物中引入含羟基,或同时引入羟基或羧基。
1、卤代酸水解:ClCH 2COOHH 2OHOCH 2CH 2COOHH +2、氰醇水解:HOCH 2CH 2ClNaCNHOCH 2CH 2HOCH 2CH 2COOH3、Reformatsky 反应:R CHO +BrCH 2COOC 2H Zn R CHCH 2COOC 2H 5R CHCH 2COOC 2H 5OHR CHCH 2COOH OHH 2O H +4、LDA 法:CH 3C O H 2OH+LDA COOC 2H 5C OCOOC 2H 53)2C C OCOOC 2H 5(CH 3)2C第二节 羟基酸的性质羟基分子中含有羟基和羧基,两者都能和水形成氢键,所以羟基酸一般比相应的酸易溶于水。
羟基酸具有醇与酸的典型反应性能,并且由于羟基和羧基的相互影响,又表现出一些为羟基酸特有的性质。
有机化学:13 取代羧酸
2. 乙酰乙酸乙酯的互变异构
两种或以上异构体互相转变,并以动态平衡而 存在——互变异构现象(tautomerism)
O O CH3 C H 7% O CH C OC2H5
CH3CCH2COOC2H5 93%
O
COOH O OH
γ -丁内酯(1,4-丁内酯)
38
+ H2O
3.脱水反应
γ -,δ -醇酸:分子内脱水 内酯
O COOH OH O + H2O
Δ
δ -戊内酯(1,5-戊内酯)
39
3.脱水反应
γ-内酯是稳定的中性化合物 与热碱溶液作用能水解
O COONa O NaOH / H2O OH
COOH
45
(一)制备
其他酚酸:
OH +CO 2 OH NaHCO 3 OH COOH OH
46
(二)性 质
OH COOH OH 200~220℃ OH
酚酸为结晶固体,具 有酚和芳酸的性质 羧基处于羟基邻对位 时,受热易脱酸:
COOH 200℃ HO OH OH
COOH
+CO 2 HO OH
56
(二)乙酰乙酸乙酯的酸性和互变异 构
α-H的活泼性 思考:
O O CCH3
CH3C CH2
的酸性大小?
O C2H5OC CH2
O COC2H5
57
2. 乙酰乙酸乙酯的互变异构
O O CH3 C CH2 C OC 2H5
+2,4-二硝基苯肼橙色苯腙 ——羰基 +Br2-CCl4 褪色 ——不饱和键 +Na H2 ↑ ——活泼氢 +CH3COCl 酯 ——醇羟基 +FeCl3水溶液 紫红色——烯醇式结构
有机化学第13章 羧酸衍生物
35
另一方面,乙酰胺的水溶液能与氧化汞作用生成稳定的汞盐。
酰胺与金属钠在乙醚溶液中作用,也能生成钠盐,但它遇水即 分解。这些说明酰胺具有弱酸性。
O C NH C O
邻苯二甲酰亚胺
36
2.酰胺脱水
酰胺与强脱水剂共热或高温加热,则分子内脱水生成腈,这
是合成腈最常用的方法之一。常用的脱水剂有五氧化二磷和亚硫
10
IR:
11
酰卤的C=O伸缩振动在1815~1785cm-1区域有强吸收,其C—X
的面内弯曲振动在645 cm-1附近。
12
酸 酐的 C=O伸 缩 振动 吸 收 与其它 羰 基 化合物 明 显不 同 , 在 1850~1800cm-1和1780~1740 cm-1区域内有两个C=O伸缩振动的强 吸收峰。线型酸酐的高频峰强于低频峰,而环状酸酐则相反。酸酐
26
酰基化试剂中离去基团离去的难易,取决于离去基团(L)的碱 性。碱性愈弱,愈易离去。离去基团L的碱性由弱到强的次序是:
C1—<RCOO—<RO—<NH2—。因此氯原于是最容易离去的基团,
而氨基则是最难离去的基团。即酰氯是最活泼的酰基化试剂,而酰 胺是最弱者。 离去基团碱性的强弱,可从其共轭酸的酸性强弱得知(强酸的 共轭碱是弱碱):
酯的醇解亦称酯交换反应。例如:
21
腈的醇溶液和浓硫酸或盐酸共热,则发生醇解反应得到酯。 例如:
22
3.氨解
酰氯、酸酐和酯与氨或胺作用,都可以生成酰胺。例如:
23
N-未取代的酰胺与胺反应生成N-取代酰胺。例如:
以上这些反应对羧酸衍生物是发生了水解、醇解或氨解;但对 水、醇或氨则是发生了酰基化反应。酰氯、酸酐和酯都是酰基化试 剂,酰胺的酰化能力极弱,一般不用作酰基化试剂。
有机化学学习笔记 第十三章羧酸
CH2CH2COOH CH2 (CH3CO)2O CH2CH2COOH
O + CO2 + H 2O
如何将环己酮转化为环戊酮?
O HNO3 CH2CH2COOH CH2CH2COOH (CH3CO)2O O
3.羧酸的脱羧卤代反应
A. Hunsdiecker反应
O R-C-OH Ag2O
O R-C-O Ag O
O CH3 CH3C-C H CH3
COOH CH2 COOH
CH3COOH + CO2
O CH2COOH
n=2,3
CH2COOH (CH3CO)2O
O + H 2O O
CH2COOH CH2 (CH3CO)2O CH2COOH
O O + H2O O
n=4,5
O CH2CH2COOH CH2CH2COOH (CH3CO)2O + CO2 + H2O
BrCH2COOH 2.90
0.64
ICH2COOH 3.18
FCH2COOH ClCH2COOH 2.66 2.88
羧酸 pKa
羧酸 pKa
HCOOH CH3COOH CH3CH2COOH (CH3)2CHCOOH (CH3)3CCOOH 3.77 4.76 4.87 4.86
Cl CH2CH2CH2COOH 4.70
5.05
n-C3H7COOH 4.80
Cl Cl CH3CH2CHCOOH CH3CHCH2COOH 2.82 4.41
羧酸 pKa
CH=CCH2COOH 3.30
CH2COOH 4.31
CH2=CHCH2COOH 4.35
n-C3H7COOH 4.82
不饱和羧酸和取代羧酸
不饱和羧酸和取代羧酸
(Unsaturated carboxylic acid and Substituted carboxylic acid )
第十六章
不饱和羧酸和取代羧酸 (Unsaturated carboxylic acid and Substituted carboxylic acid )
H+ HO( CH2)5COO H
ε– 羟基己酸
K2CO 3
Br(CH 2)10COOH CH3COOE t
Br(CH 2)10COO
ω–卤代酸 (碳数在9以上)
O
C
(CH2)10 O
在极稀的溶液中进行
85%
大环内酯
24
2). 达让(Darzer)反应 指α-卤代酸酯在醇钠或氨基钠作用下与醛酮发生的 羟醛缩合反应,产物为αβ-环氧酸酯。
C6H5CHC Cl
ROH
Br
O
C6H5CHC OR
Br
20
2). β– 卤代酸
ቤተ መጻሕፍቲ ባይዱ
O
CH2 CH C OH + HX
CH2 CH2 COOH X
3). γ, δ 等卤代酸用二元羧酸的单酯发生汉斯狄克反应
O
AgNO 3 , KOH
O
ROC CH 2 n COOH
ROC CH 2 n COOA g
Br2 , CCl4
C6H5
H
CC
H
COOH
(E )–3–苯基丙烯酸 (肉桂酸)
H
H
CC
C6H5
COOH
(Z )–3–苯基丙烯酸
(异肉桂酸)
3
CH3(CH2)7CH CH( CH2)7COOH
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• 4)氯乙酸酯和KF反应得氟乙酸酯,水解后 得氟代羧酸。
O KF Cl O CH3 F O CH3 O
H3O
+
O F OH
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
2、卤代羧酸的性质 the properties of halocarboxylic acid 1)卤代羧酸的酸性 • 卤原子吸电子,酸酸性比羧酸强。随卤原子 与羧基距离增加迅速减弱。 2)亲核取代反应(类似于卤代烃)
13.2 13.2不饱和羧酸的化学性质 chemical properties of unsaturated carboxylic acid • 1、共轭不饱和羧酸的酸性(acidity) • 酸性略强于饱和羧酸。因为α-碳原子的sp2杂 化比饱和的sp3杂化s成分稍多,吸电子作用稍强。 共轭体系对羧酸负离子稳定性的贡献不大,(交叉 共轭体系across conjugation system所致) 。
H2C COOH
HBr Br
CH2 CH2
COOH
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
• 2)与 水的加成(反马加成):
H2C COOH H3O
+
CH2 HO CH2
COOH
• 3)与 HCN的加成
H2C COOH CNNC CH2 CH2 COOH
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
-
HO
O
R NC
OH O
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
Discussion in class • How to prepare folowing compounds using propanioc acid as the raw material?
COOH H2C
H3C
COOH
4)共轭羧酸与含N-H键的化合物的加成 addition of conjugation acid with the compounds having N-H bond • 与 氨反应生成 β—氨基酸:
H 2C COOH
NH 3 H 2N
CH 2 CH 2
COOH
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
H3C
COOH
NH2 HOOC H3C
COOH
OH
COOH
O
H3C
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
4)卤代羧酸的一些特殊性质 • γ-,δ-,ε-卤代酸 在氧化银存在下得内酯。
Br O H3C OH O AgO H2O O O CH3
γ-戊内酯 γ-pentanoic lactone δ-己内酯 δ-
催化氧化
H2C O HO
•
prop-1-ene
acrylaldehyde
acrylic acid
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
• 丙烯酸可以用来合成聚丙烯酸和聚丙烯酸酯。
H2 C
CH COOR H2C COOH
H2C
CH COOH
n
n
Polyacrylate
acrylic acid
CN H2C H3O
+
COOH H2C
• 2)卤代酸消除 • ( elemination of halocarboxylic acid) 。
H3C COOH NaOH H3C OH H2C COOH
Cl
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
缩合反应制备不饱和羧酸 to prepare the unsaturated acid by condensation • 3)芳醛和丙二酸酯缩合后水解脱羧:
华中农业大学理学院
O
CH3
第13章羧酸(不饱和和取代羧酸)
马来酸(顺丁烯二酸),工业上用苯、丁烷或丁 烯氧化制 取:
O O O O V2 O 5 O O
+
H3O
OH OH
O
benzene
Maleic anhydride
Maleic acid
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
3)马来酸的性质 properties of malaic acid • 马来酸酐或马来酸和亚硫酰氯反应不是丁烯二 酰氯,只能得γ,γ—二氯—γ—丁烯内酯。
O
OH OH
O
HO
R
OH HO R O
O
O
O
R
OH n
O
OH HO OH
O
C4H8 OH
O
O
HO
C4H8 O
O
C4H 8
OH n
聚(丁烯二酸-1,4-丁二醇酯)
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
5)丁炔二酸 but-2-ynedioic acid • 炔酸的代表化合物,由邻二卤代二酸消除得 到。
Polyacrylic acid
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
2)甲基丙烯酸甲酯和马来酸 methyl methylacrylate and maleic acid
• 甲基丙烯酸甲酯制法:
O H3C CH3 HO
HCN
CN CH3
H 2 SO 4
H3C
O HO3SO H3C CN H C OH 3 CH3 H2C CH3
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
O H2C CH2 H3C
OH
链状共轭 体系
交叉共轭体系
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
2、共轭羧酸的加成反应 addition reaction of conjugation carboxylic acid • 共轭不饱和羧酸加成反应类似共轭醛酮的加成反 应,主要1,4-加成反应。 1)与 卤化氢的加成(反马加成):
H3C H5 C6 CHO
O Na +
H3COOC COOCH3
C6 H5 H3O
+
O
COOCH3 COOCH3
C 6H 5 OH
• 4)芳香醛和乙酸酐高温缩合后水解
例:制备肉桂酸
KOAc H 5 C6 CHO (CH3CO)2O C6 H 5 O CH3 C6H5 OH
(2Z)-3-phenylacrylic acid
O H3C R OH X R OH O
R可以是0~n个亚甲基
X可以是O、OH 、NHR
• 重要:α,β-共轭(conjugated)羧酸; • 取代羧酸重要的是羰基酸和羟基酸。
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
2、不饱和羧酸制法 不饱和羧酸 preparation of unsaturated carboxylic acid • 1)烯腈水解(t hydrolyzing acrylonitrile)。
OH OH O O HO Br Br O Br HO Br H3C O NaOH OH HOOC COOH
2,3-dibromosuccinic acid
but-2-ynedioic acid
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
丁炔二酸也可以进行双烯合成:
CH2
COOH
COOH
+
CH2
COOH
COOH
cyclohexa-1,4-diene-1,2-dicarboxylic acid
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
13.3 13.3 卤代酸 halocarboxylic acid • 1、卤代酸的制备: • 1)酰氯和HX NBS催化制取α-位卤代酰氯, 水解得α-位卤代酸;卤素红磷催化制备α卤代酸。
CH2 COOH
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
• 2-丁烯酸与下列试剂反应得到什么产物?
HOOC
HBr CH3
HOOC
HCN CH3
HOOC
H3O CH3
+
COOH
HOOC
H2N
CH3
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
5)共轭羧酸的双烯合成 Diels-Alder reaction of the conjugation acid • α,β-不饱和羧酸是亲二烯体(dienophile), 与共轭二烯(conjugation diene)进行双烯合成。
O HBr H5 C6 Cl NBS H5 C 6 Cl Br O
H2O
Br
O
H5 C6
OH
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
2)β—位卤代酸的制备 α ,β-不饱和羧酸与卤化氢加成。
R
OH O
R HBr Br
OH
O
华中农业大学理学院
第13章羧酸(不饱和和取代羧酸)
卤代酸的其它制备方法 other methods for preparing halocarboxylic acid • 3)三氯乙烯水解得高纯度氯乙酸
• β-氨基丙酸还可以继续与丙烯酸反应:
CH2 H2N CH2 COOH H2C COOH HN CH2 CH2 CH2 COOH CH2 COOH
• 还可以生成胺三( β-丙酸)
CH2 HN CH2 CH2 H2C COOH COOH N CH2 CH2
CH2
COOH
CH2 COOH
CH2 CH 2 COOH
