d区过渡元素3
过渡元素课件

Cr3+的配合物有数千种,绝大多数配位数:6 常见的是:[Cr(H2O)6]3+, 配合物多有颜色
[Cr(H2O)6 ]Cl2紫色 [Cr(H2O)5Cl]Cl2 H2O蓝绿色
[Cr(H2O)4Cl2 ]Cl 2H过渡2元O素绿色
18
12.2.4 铬(Ⅵ)盐 1. Cr2O72-与CrO42-间的转化
4.形成多种配合物
过渡元素
11
12.1 过渡元素通性
过渡元素
12
12.1 过渡元素通性
5.催化性
许多过渡元素及其化合物具有独特的催化性能,Pt,Pd, Fe,Cu,V,…..,PdCl2 , V2O5….等常用的催化剂
6.磁性
多数过渡金属原子或离子有未成对电子,具有顺磁性,未 成对电子数越多,磁矩越大
Sc
Ti
Eθ M 2 /M
/
V
可溶该金属 的酸 元素
---
各种酸 Fe
-1.63
热 HCl HF Co
E / V θ M2 /M
可溶该金属 的酸
-0.44
稀 HCl H2SO4 等
-0.29
缓溶解在 HCl 等酸中
V -1.2 (估算值) HNO3,HF 浓 H2SO4 Ni
-0.25
稀 HCl H2SO4 等
Cr 2H (稀) Cr2( 蓝) H2
O2 Cr3 (紫)
2Cr
2H 2SO 4
(浓)
Cr(2 SO
)
43
3SO2
H2O
在冷、浓硝酸中钝化
2. 铬(Ⅲ)的化合物
(1)Cr2O(3 铬绿) ——两性氧化物 制备:4Cr 3O2 Δ 2Cr2O3
第九章 过渡元素

Cu(OH)2 氢氧化铜为浅兰色粉末,难溶于水,稍有两性,易溶于酸, 只溶于较浓的强碱。 Cu(OH)2 + 2OH[Cu(OH)]2-
9.2.3 银的化合物 银通常形成氧化值为+1的化合物,其中只有AgNO3易溶于水其他如Ag2O、 卤化银等均难溶。银的化合物有不同程度的感光性,银和许多配体易形成配合物。 硝酸银 AgNO3是最重要的可溶性银盐,用途广泛。它在干燥的空气中比较稳 定,潮湿状态下易见光分解,析出单质银而变黑
(1) 氧化铜和氢氧化铜 CuO 氧化铜为黑色粉末,难溶于水。它是偏碱性氧化物,溶于稀酸: CuO + 2H+ Cu2+ + H2O
由Cu(NO3)2或Cu2(OH)2CO3受热分解都能指得CuO:
2Cu(NO3)2 Δ Cu2(#43; 4NO2 + O2 2CuO + CO2 + H2O
第九章
过渡元素
9.1过渡元素的结构特点
过渡元素位于周期表中部d区ⅢB(3)—Ⅷ(8)族8个直列24个元素(不包括镧以 外的镧系,锕以外的锕系元素)。表9—1列出了第一过渡系列元素的电子构型
表9—1 第一过渡系列元素的电子构型
过渡元素电子结构的特点是具有未充满的d轨道(Pd例外),最外层 电子为1~2个,最外两个电子层都是未充满的,其特征电子构型为(n-1) d1-9ns1-2。也有把ds区的铜族,锌族元素作为过渡元素,其电子构型为 (n-1)d1-10ns1-2。最近有人只把铜族元素列入过渡元素(而锌族不列 入),因为铜的重要氧化态Cu(Ⅱ)为3d9、Ag(Ⅱ)为4d9、Au(Ⅲ) 为5d8构型,而且它们的性质与过渡元素极为相似,故过渡元素包括铜族 元素较合适。 过渡元素与典型元素不同,周期性变化规律并不明显。如同周期的金 属性递变不显著,原子半径,电离势等随原子序数增加,虽有变化但不显 著,都反映出各元素间从左至右的水平相似性(表4—6)。因之,将这些 过渡元素按周期分为三个系列。位于周期表中第四周期的Sc—Ni为第一过 渡系列元素;第五周期中的Y—Pd为第二过渡系列元素;第六周期中的 La—Pt为第三过渡系列元素。习惯上把第一过渡系列元素称为轻过渡元素, 把第二、第三过渡系列称为重过渡元素。本节主要讨论第一过渡系列元素。
d区元素一(相关知识点)
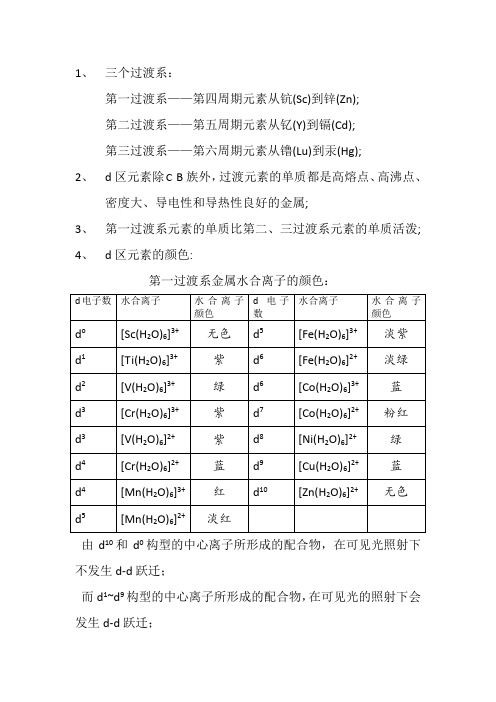
1、三个过渡系:第一过渡系——第四周期元素从钪(Sc)到锌(Zn);第二过渡系——第五周期元素从钇(Y)到镉(Cd);第三过渡系——第六周期元素从镥(Lu)到汞(Hg);2、d区元素除 B族外,过渡元素的单质都是高熔点、高沸点、密度大、导电性和导热性良好的金属;3、第一过渡系元素的单质比第二、三过渡系元素的单质活泼;4、d区元素的颜色:第一过渡系金属水合离子的颜色:由d10和d0构型的中心离子所形成的配合物,在可见光照射下不发生d-d跃迁;而d1~d9构型的中心离子所形成的配合物,在可见光的照射下会发生d-d跃迁;对于某些具有颜色的含氧酸根离子,如:VO 43-(淡黄色)、CrO 42-(黄色)、MnO 4-(紫色)等,它们的颜色被认为是由电荷迁移引起的; 5、(1)钛(Ti)是银白色金属,其表面易形成致密的氧化物保护膜,使其具有良好的抗腐蚀性,特别是对湿的氯气和海水具有良好的抗腐蚀性能;(2)加热TiO 22nH O 可得到白色粉末状的TiO 2:3002222CTiO nH O TiO nH O −−−→+;(3)自然界中存在的金红石是TiO 2的另一种存在形式,由于含少量的铁、铌、钒、钽等而呈红色或黄色;(4)TiO 2在工业上用作白色涂料和制造钛的其他化合物; (5) TiO 2+H 2SO 4(浓)=TiOSO 4+H 2O ; TiO 2+2C(s)=Ti(s)+2CO(s) ; (6)制取Ti 的方法:通常用TiO 2、碳和氯气在800C~900C 时进行反应:800~900224222C CTiO C Cl TiCl CO ++−−−−→+ ;用Mg 还原TiCl 4: TiCl 4+2Mg=Ti+2MgCl 2 ; (7)TiCl 4在加热的情况下:2TiCl 4+H 2=2TiCl 3+2HCl ;(8)Ti 4+由于电荷多,半径小,使它具有强烈的水解作用,甚至在强酸溶液中也未发现有[Ti(H 2O)6]4+的存在,Ti 4+在水溶液中是以钛氧离子(TiO 2+)的形式存在;(9)在中等酸度的Ti 4+的盐溶液中加入H 2O 2:TiO2++H2O2=[TiO](H2O2)]2+(橘黄色) ;(10)在酸性溶液中用Zn还原TiO2+时,可形成紫色的[Ti(H2O)6]3+(可简写成Ti3+):2TiO2++Zn+4H+=2Ti3++Zn2++2H2O ;(11)向含有Ti3+的溶液中加入碳酸时:2Ti3++3CO32-+3H2O=2Ti(OH)3(s)+3CO2;(12)在酸性溶液中,Ti3+是一种比Sn2+略强的还原剂,它易被空气中的氧所氧化:4Ti3++2H2O+O2=4TiO2++4H+;(13)有机化学中常用Ti3+来证实硝基化合物的存在,它可将硝基还原为氨基:RNO2+6Ti3++4H2O=RNH2+6TiO2++6H+;6、(1)钒在自然界中的存在极为分散,很少可以见到钒的富矿;(2)钒是银灰色金属,在空气中是稳定的,其硬度比刚大;(3)钒对于稀酸也是稳定的,但在室温下,它能溶于王水或硝酸中,生成VO2+;浓硫酸和氢氟酸仅在加热条件下与钒发生作用;(4)加热时。
过渡金属元素类型与应用

• 过渡元素是指长周期表中d区和ds区元素,在周期 表中包括IIIB族~IIB族。通常按同元素的性质相 近把过渡元素分成三个系列。
族
周期
IIIB IVB VB VIB VIIB
第一过渡系 Sc Ti V Cr Mn
VIIIቤተ መጻሕፍቲ ባይዱ Fe Co Ni
IB IIB Cu Zn
第二过渡系 Y Zr Nb Mo Tc Ru Rh Pd Ag Cd
-0.44 -0.277
稀HCl 稀HCl H2SO4 等
等 (缓慢)
-0.257
稀H2SO4 HCl等
Cu
0.34
浓 H2SO4
Zn -0.7626 稀HCl H2SO4等
值同I其。I一I可B活第族周溶泼一是期于性过过迅元非减渡渡速素氧元弱氧系从素化化金左中,性属过到最渡与稀金除活右属水酸元C泼素作总u类置的型用外趋和换金应释,势用出E属放E,氢(出MS(氢气Mc2+、气。/2M+Y/M、)均L)增为a 能大负
(2)水合离子的颜色 • 过渡金属的水合离子、含氧酸根离子和配离子常
是有颜色的,与此相反,主族金属的相应离子是 无色的。 • 过渡元素的离子通常在d轨道上有未成对电子,这 些电子的基态和激发态的能量比较接近,一般只 要是可见光中的某些波长的光就可使电子激发, 这些离子大都具有颜色。
过渡金属元素类型和应用
过渡元素熔点、沸点的递变规律是自IIIB至VIB依次升 高,VIB族金属的熔点、沸点最高,VIIB族以后逐渐 降低,IIB族已是低熔点金属,汞的熔点(234.13K) 最低。VIB族的铬硬度过最渡金大属元(素类9型)和应。用
IVB~VIIB族元素的单质具有高熔、沸点、高硬度的原 因,主要是它们的原子半径较小,有效核电荷较大, 价电子层有较多的未成对d电子(铬有5个),这些d电 子也参与成键,因而增过渡强金属了元素金类型属和应的用 强度和晶格能。
课件化学--d区元素

钛或钛合金的密度与人的骨 骼相近,对体内有机物不起化学 反应,且亲和力强,易为人体所 容纳,对任何消毒方式都能适应, 因而常用于接骨、制造人工关节 等。又称为生命金属。
用水浸取除去可溶盐,得海绵状钛,电弧熔 融得钛锭。
§ 2-2 钛的重要化合物
1. 二氧化钛
天然二氧化钛称“金红石”,含杂质。
人工制备纯TiO2俗称“钛白粉”,是优良的白色 涂料,着色力强,遮盖力强,化学稳定性好,优于
除s电子外,d电子可参与成金属键,自左向右未成对价电 子增多,至VIB族(铬族)可能提供6个单电子,相互作用力大, 金属键强,因此在过渡系中,铬族(Cr,Mo,W)熔点最高, 硬度也很大,除Mn和Tc外(熔点反常)随后自左向右熔点又有 规律下降。
铬族价电子层构型: (n-1)d5ns1
熔点变化示意图
此外,钛或钛合金还具有特 殊的记忆功能、超导功能和储氢 功能等。
Zr,Hf是稀有金属,锆矿主要有锆英石ZrSO4, 价电子结构(n-1)d2ns2,d0电子结构较稳定, 所以除最外层s电子,次外层d电子也参加成键, Ti,Zr,Hf最稳定的氧化态是+4。其次是+3, +2较少见。
由于镧系收缩,铪的离子半径与锆接近,所以
FeTiO3 + 2H2SO4 = TiOSO4 + FeSO4 + 2H2O TiOSO4 + 2H2O = H2TiO3 + H2SO4 H2TiO3 = TiO2 + H2O
元素周期表中的过渡金属

医学应用
01
02
03
药物合成
过渡金属在药物合成中发 挥重要作用,如铂、钴、 镍等金属的配合物用于治 疗癌症的药物研发。
诊断试剂
某些过渡金属离子如铁、 铜、锌等参与生物体内的 代谢过程,可作为生物标 记物用于诊断疾病。
医疗器械
一些具有特殊物理和化学 性质的过渡金属及其合金 用于制造医疗器械,如手 术刀具、植入物等。
环境治理
污水处理
过渡金属化合物在污水处理中具有重要作用 ,能够有效去除水中的重金属离子和有害物 质,保障水质安全。
大气治理
利用过渡金属化合物去除大气中的有害气体 ,如二氧化硫、氮氧化物等,有助于改善空
气质量。
谢谢您的聆听
THANKS
元素周期表中的过渡金属
CONTENTS
• 过渡金属的概述 • 过渡金属的化学性质 • 过渡金属的物理性质 • 过渡金属的应用 • 过渡金属的发现与开采 • 过渡金属的未来发展
01
过渡金属的概述
定义与特性
定义
过渡金属是元素周期表中d区和ds区 的金属元素,它们具有未填满的d电 子壳层。
特性
过渡金属具有多种氧化态,可以形成 多种复杂的化合物,具有丰富的化学 性质和物理性质。
功能材料
过渡金属化合物在磁性、光学、电学 等方面具有优异性能,可用于信息存 储、光电器件、传感器等领域。
新能源开发
燃料电池催化剂
过渡金属(如铂、钯等)具有良好的催化性能,是燃料电池中重要的催化剂,有助于提 高燃料电池的效率和稳定性。
太阳能电池
过渡金属化合物在太阳能转换方面具有潜在应用价值,能够提高太阳能电池的光电转换 效率和稳定性。
详细描述
过渡金属具有多种氧化态,这是因为它们的d电子可以轻易地参与成键,形成不 同的价态。此外,由于d电子的存在,使得相邻氧化态间的电离能差较小,这使 得过渡金属在化学反应中容易发生氧化还原反应。
d,f区元素
12.1.1 d区元素的特殊性
d区元素显示出许多区别于主族元素的性质:
• 熔沸点高、硬度密度大的金属大都集中在这一区 • 同一周期从左到右,元素化学性质的变化远不如s区p区
显著。
• 不少元素形成有颜色的化合物 • 许多元素形成多种氧化态从而导致丰富的氧化还原行为 • 形成配合物的能力比较强 ,参与工业催化过程和酶催
化过程的能力强
12.2 钒
• 钒的价电子层结构为3d34s2,5个电子都有成键作用,所以 • 在酸性介质中,钒的元素电势图为
A / V
VO2+ 主要氧化态为+5,但也存在+4,+3,+2。
-0.25 -1.2 1.0 VO2+ 0.36 V3+ V2+ V -0.25
所以V2+、V3+具有还原性,VO2+是稳定的,而VO2+具有氧化 性。 不同的氧化态的钒具有不同的颜色。例如: VO2+(黄色)可 被Fe2+、H2C2O4等还原为VO2+(蓝色)
[Cr(H2O)6]Cl3 紫色
[Cr(H2O)5Cl]Cl2· H2O 浅绿 [Cr(H2O)4Cl2]Cl· 2H2O 深绿
2. Cr(VI)的化合物
Cr(VI)的化合物通常是由自然界存在的铬铁矿Fe(CrO2)2,
借助于碱熔法制得的,即把铬铁矿和Na2CO3混合,并在空 气中煅烧。用水浸取煅烧后的熔体,Na2CrO4进入水中,浓 缩,得黄色晶体Na2CrO4;酸化得红色晶体。 4Fe(CrO2)2 + 8Na2CO3 + 7O2 8Na2CrO4 + 2Fe2O3 + 8CO2
电子分别填充在3d 亚层4d 亚层和5d 亚层上.
有效原子序数(EAN)规则和金属羰基化合物
(sp-sp反键)
(二重简并)
(sp(C))
(二重简并)
(sp-sp成键)
(sp(O))
现在分析一下CO有哪些分 子轨道上的电子能给予 中心原 子形成配位键。
在四条被电子占据的 轨道中, 4轨道由于电子 云 大 部 分 集 中 在 CO 核 之 间,不能拿出来给予其他原 子, 因此, 能授予中心金属原子电子对的只有3、1 和5的电子。其中3电子是属于氧的孤对电子, 由于 氧的电负性比碳原子大, 除少数情况之外, 氧很难将 3电子对拿出来给予中心金属原子, 因此,可能与中 心金属原子形成σ配键的分子轨道就只有1和5了。 当CO的5和1分别与金属生成配位键时,它们 的成键情况有如下几种方式:
② 估计反应的方向或产物 如: Cr(CO)6+C6H6 → ? 由于一个苯分子是一个6电子给予体,可取代出三 个CO分子,因此预期其产物为: [Cr(C6H6)(CO)3]+3CO
又如:Mn2(CO)10+Na → ? 由于Mn2(CO)10 7×2+10×2=34,平均为17,为 奇电子体系,可从Na夺得一个电子成为负离子,即产物 为: [Mn(CO)5]- + Na+
9.1 金属羰基配合物
9.1.1 概述
金属羰基配合物是由过渡金属与配位体 CO所形成的一类配合物。这类配合物无论是 在理论研究还是实际应用上,在近代无机化 学中都占有特殊重要的地位。
金属羰基配位物有三个特点,即 ① 金属与CO之间的化学键很强。如在Ni(CO)4 中,Ni-C键能为147 kJ· -1,这个键能值差不多 mol 与 I - I 键 能 (150 kJ· - 1) 和 C - O 单 键 键 能 (142 mol kJ· -1)值相差不多。 mol ② 在这类配合物中,中心原子总是呈现较低的 氧化态(通常为0,有时也呈较低的正氧化态或负氧 化态)。氧化态低使得有可能电子占满d-MO,从 而使M→L的电子转移成为可能。 ③ 大多数配合物都服从有效原子序数规则。
过渡元素
(3)还原法
原理:用还原剂还原化合物(如氧化物等)来制取单 质,一般常用的还原剂是焦炭,CO、H2、活泼金属等。
例: 高炉炼铁: Fe2O3+3CO 2Fe+3CO2 铝热剂法: Fe2O3+2Al 2Fe+Al2O3 应用范围:用于制取活泼性不是很强的金属及以正氧 化值存在的非金属单质。 氧化物能否被还原,可以用消耗1mol O2生成氧化物过 程的△G变化对温度作图(见p322图8-5,Ellingham图)来 分析。 一些金属还可以从卤化物中用还原法提取,也可采用 电解、水溶液电积等方法提取。
0 5 10 15 20 24
3d
r/a0
8.2.2(n-1)d与ns轨道能级高低
▲ 电子组态:由n,l表示的电子排布方式。 ● 多电子原子核外电子的填充顺序:
1s,2s,2p,3s,3p,4s,3d,4p,5s,4d,5p,6s,4f,5d,6p,7s,5f,6d,7p…
▲ 过渡元素在周期表中为何延迟出现?3d排在4s之后,4d 在5s后,4f,5d在6s后,5f,6d在7s后。 ● 电子在原子轨道中的填充顺序,并不是原子轨道能级高低 的顺序,填充次序遵循的原则是使原子的总能量保持最低。 填充次序表示,随Z增加电子数目增加时,外层电子排布的规 律。(见 图8-4,p317)
2、单质的制取方法 通常有五种:物理分离法,热分解法,还原法,氧
化法和电解法。 (1)物理分离法 原理:单质与杂质在某些物理性质(如密度、沸
点等)上有显著差异的特点。 例: “沙里淘金”(密度差异);
应用范围:分离、提取以单质状态存在,且某些物理 性质与杂质差异较大的元素。
过渡金属元素
2. 羰基簇合物 (分子中含有M—M键的化合物)
过渡元素能和CO形成许多羰基簇合物。 羰基簇合物中金属原子多为低氧化态并具有适宜的d轨道。 双核和多核羰基簇合物中羰基与金属原子的结合方式:
(1) 端基(1个CO和1个成簇原子相连);(2) 边桥基(1个CO
与2个成簇原子相连);(3) 面桥基(1个CO与3个成簇原子相 连)。
第7章 过渡金属元素
表7-1 过渡金属元素(d 区元素除第七周期外, 共23种)
周期\族
四
IIIB
Sc
IVB
Ti
VB
Ⅴ
VIB
Cr
VIIB
Mn Fe
VIII
Co Ni
五
六
Y
La
Zr
Hf
104Rf
Nb
Ta
105Db
Mo
W
106Sg
Tc
Re
107Bh
Ru
Os
108Hs
Rh
Ir
109Mt
Pd
Pt
110Uun
近时, 两个Re3+的dz2轨道以
“ 头碰头 ”重叠形成σ键; 两 个Re3+ 的dxz轨道、dyz轨道以
“ 肩并肩 ”重叠形成两个 d—d
π键; 而两个Re3+ 的dxy轨道以 “面对面”重叠形成δ键,说明 Re与Re之间形成四重键。
26
Re 5d56s2
-3e
Re3+ 5d4
dsp2杂化
5d4 (dsp2)0( dsp2)0( dsp2)0( dsp2)0 σ σ σ σ (3px)2 (3px)2 (3px)2 (3px)2 Cl Cl Cl Cl
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第九章d区元素(Ⅲ)—有机金属化合物簇合物要点有效原子序数(EAN)规则和金属羰基化合物类似羰基的有机过渡金属化合物过渡金属不饱和链烃配合物过渡金属环多烯化合物过渡金属的羰基簇合物过渡金属的卤素簇合物应用有机过渡金属化合物和金属原子簇化物的一些催化反应习题:1,2,7, 15; 选作题:4,5,6,8,9,11,12.(2),(4),(6)9.1 金属羰基配合物9.1.1 概述金属羰基配合物是由过渡金属与配位体CO所形成的一类配合物。
这类配合物无论是在理论研究还是实际应用上,在近代无机化学中都占有特殊重要的地位。
金属羰基配位物有三个特点,即①金属与CO之间的化学键很强。
如在Ni(CO)4中,Ni-C键能为147kJ·mol-1,这个键能值差不多与I-I键能(150kJ·mol-1)和C-O单键键能(142 kJ·mol-1)值相差不多。
②在这类配合物中,中心原子总是呈现较低的氧化态(通常为0,有时也呈较低的正氧化态或负氧化态)。
氧化态低使得有可能电子占满dπ-MO,从而使M→L的π电子转移成为可能。
③大多数配合物都服从有效原子序数规则。
最早发现的羰基化合物是Ni(CO)4,它是在1890年被Mond发现的。
将CO通过还原镍丝,然后再燃烧,就发出绿色的光亮火焰(纯净的CO燃烧时发出蓝色火焰),若使这个气体冷却,则得到一种无色的液体。
若加热这种气体,则分解出Ni和CO,其反应如下:Ni+4CO Ni(CO)4(m.p.-25℃)Ni+4CO由于Fe、Co、Ni的相似性,它们常常共存。
但是由于金属Co与金属Ni同CO的作用条件不同(Co和Fe必须在高压下才能与CO化合,Ni在常温常压就可作用),从而利用上述反应就可分离Ni和Co,以制取高纯度的Ni。
常温常压△1891年,Mond还发现CO在493K和2×107Pa 压力下通过还原Fe粉也能比较容易地制得五羰基合。
铁Fe(CO)5493K, 20MPaFe+5CO Fe(CO)5继羰基Ni及羰基Fe被发现之后又陆续制得了许多其他过渡金属羰基配合物,其中一些实例示于下页表中:一些羰基化合物的性质化合物颜色及状态熔点/K 点群其他性质1 V(CO)6黑色固体d*.343 O h真空中升华;顺磁性, V-C键长200.8 pm 1 Cr(CO)6白色晶体 d. 403 O h易升华,Cr-C键长191.3 pm 1 Mo(CO)6白色晶体―O h易升华,Mo-C键长206 pm 1 W(CO)6白色晶体―O h易升华,W-C键长206 pm 1 Fe(CO)5淡黄色液体253 D3h b.p.403 K 1 Ru(CO)5无色液体251 D3h挥发性强1 Os(CO)5无色液体258 D3h挥发性强,难制得纯净物1 Ni(CO)4无色液体258 Td b.p.316 K,易燃,剧毒, Ni-C键长183.8 pm Mn2(CO)10黄色固体427 D4d易升华,Mn-Mn键长293 pmTc2(CO)10白色固体432 D4dRe2(CO)10白色固体450 D4dFe2(CO)9金黄色固体 d. 373 D3h Fe-Fe键长246 pmOs2(CO)9橙黄色固体337-340Co2(CO)8橙红色固体 d. 324 C2v或D3d D3d,Co-Co键长254 pmRh2(CO)8橙色固体440 低温和高CO压力下稳定Ir2(CO)8黄绿色固体低温和高CO压力下稳定*d,分解9.1.2 二元羰基化合物的制备和反应1二元羰基化合物的制备(1)金属粉末与CO 直接作用如四羰基合镍、五羰基合铁的合成。
金属粉末必须是新鲜还原出来的处于非常活化的状态才行。
Ni +4CONi(CO)4(m.p.-25℃)Ni +4CO Fe +5COFe(CO)5493K , 20MPa常温常压△(2)还原和羰基化作用还原剂可用Na 、Al 、Mg 、三烷基铝、CO 以及CO +H 2等。
如:2CoCO 3+6CO +4H 2Co 2(CO)8+4H 2OCrC13+6CO +A1Cr(CO)6+A1C13OsO 4+9COOs(CO)5+4CO 2420K ,30MPa A1C13,苯420K ,25MPa(3) 通过热分解或光照分解, 可制得某些多核羰基化合物。
如:3 Os(CO)5Os3(CO)12+3CO2 Fe(CO)5Fe2(CO)9+COCo2(CO)6Co4(CO)12(4) 两种金属的羰基化合物相互作用,可以制得异核羰基配合物。
如:3Fe(CO)5+Ru2(CO)12FeRu2(CO)12+Fe2Ru(CO)12+CO△UV,汽油320K380K2羰基化合物的反应(1)可与碱作用生成含氢羰基配合阴离子Fe(CO)5+3NaOH Na[HFe(CO)4]+Na2CO3+H2O (2)与酸作用生成羰基氢化物Na[Co(CO)4]+H+H[Co(CO)4]+Na+Co(CO)4-+H+pK a≈7(3)与X2、NO的取代反应Fe2(CO)9+4NO2Fe(CO)2(NO)2+6CO (4)氧化还原反应Mn2(CO)10+Br22Mn(CO)5Br9.1.3 有效原子序数规则(EAN规则)1EAN规则EAN规则是说金属的价电子加上配体所提供的σ电子之和等于18,或等于最邻近的下一个稀有气体原子的价电子数,或中心金属的总电子数等于下一个稀有气体原子的有效原子序数。
EAN亦称为18电子规则,这个规则实际上是金属原子与配体成键时倾向于尽可能完全使用它的九条价轨道(五条d轨道、一条s、三条p轨道)的表现。
需要指出的是,有些时候,它不是18而是16。
这是因为18电子意味着全部s、p、d价轨道都被利用,当金属外面电子过多,意味着负电荷累积,此时假定能以反馈键M→L形式将负电荷转移至配体,则18电子结构配合物稳定性较强;如果配体生成反馈键的能力较弱,不能从金属原子上移去很多的电子云密度时,则形成16电子结构配合物。
因此,EAN规则在有些书上直接叫18电子和16电子规则。
*注意:这个规则仅是一个经验规则,不是化学键的理论。
举例说明18电子规则和如何确定电子的方法:①把配合物看成是给体-受体的加合物,配体给予电子,金属接受电子;②对于经典单齿配体,如胺、膦、卤离子、CO、H-、烷基R-和芳基Ar-,都看作是二电子给予体。
如Fe(CO)4H2Ni(CO)4Fe2+6Ni10 4CO4×2=8+)4CO4×2=8+)2H-2×2=410+8=18 6+8+4=18③在配位阴离子或配位阳离子的情况下,规定把离子的电荷算在金属上。
如:Mn(CO)6+:Mn+7-1=6,6CO6×2=12,6+12=18Co(CO)4-:Co-9+1=10,4CO4×2=8,10+8=18④对NO等三电子配体:Mn(CO)4(NO)NO34CO8+)Mn73+8+7=18⑤含M-M和桥联基团M-CO-M。
其中的化学键表示共用电子对,规定一条化学键给一个金属贡献一个电子。
(CO)9其中有一条Fe-Fe金属键和3条M-CO-M 如Fe2桥键,对每一个Fe:Fe=8,(9-3)/2CO=6,3M-CO=3,1Fe-Fe=1,8+6+3+1=18⑥对于ηn 型给予体如, η1-C5H5-(σ给予体),η5-C5H5-、η6-C6H6(π给予体)等。
ηn是键合到金属上的一个配体上的原子的数目为n的速记符号,η表示hapto,源于希腊字haptein,是固定的意思。
ηn型配体具体给予中心原子多少电子视配体而定。
如:Fe(CO)2(η5-C5H5)(η1-C5H5)2CO=4, η5-C5H5-=6, η1-C5H5-=2, Fe2+=6,电子总数=4+6+2+6=18Mn(CO)4(η2-CH3-CH2=CH2)4CO=8, (η2-CH2=CH2-CH3)=2, Mn=7,电子总数=8+2+7=17Cr(η6-C6H6)22(η6-C6H6)=12,Cr=6,电子总数=12+6=182EAN规则的应用①估计羰基化合物的稳定性稳定的结构是18或16电子结构,奇数电子的羰基化合物可通过下列三种方式而得到稳定:a从还原剂夺得一个电子成为阴离子[M(CO)n]-;b与其他含有一个未成对电子的原子或基团以共价键结合成HM(CO)n 或M(CO)nX;c彼此结合生成为二聚体。
②估计反应的方向或产物如:Cr(CO)6+C6H6→?由于一个苯分子是一个6电子给予体,可取代出三个CO分子,因此预期其产物为:[Cr(C6H6)(CO)3]+3CO又如:Mn2(CO)10+Na→?由于Mn2(CO)107×2+10×2=34,平均为17,为奇电子体系,可从Na夺得一个电子成为负离子,即产物为:[Mn(CO)5]-+Na+③估算多原子分子中存在的M-M键数,并推测其结构如Ir4(CO)124Ir=4×9=36,12CO=12×2=24,电子总数=60,平均每个Ir周围有15 e。
按EAN规则,每个Ir还缺三个电子,因而每个Ir必须CO CO COCO Ir CO CO Ir Ir CO CO Ir COCO CO CO 同另三个金属形成三条M-M键方能达到18电子的要求,通过形成四面体原子簇的结构,就可达到此目的。
其结构示于左。
④预测化合物的稳定性如二茂铁鎓离子Fe(η5-C5H5)2+为17电子结构,二茂钴Co(η5-C5H5)2为19电子结构,可以预料它们分别可以得到一个电子和失去一个电子成为18电子结构,故前者是一种强氧化剂,后者是一种强还原剂。
需要指出的是,有些配合物并不符合EAN规则。
以V(CO)为例,它周围只有17个价电子,预料它6(CO)12还不须形成二聚体才能变得稳定,但实际上V2稳定。
其原因是空间位阻妨碍着二聚体的形如V(CO)6成,因为当形成V(CO)12时,V的配位数变为7,配位2体过于拥挤,配位体之间的排斥作用超过二聚体中V -V的成键作用。
所以最终稳定的是V(CO)而不是二6聚体。
可以利用分子轨道理论来说明金属羰基化合物中的成键过程。
在CO 分子中,C 和O 都是以2s 和2p 原子轨道参与成键的。
由于C 和O 原子对称性相同的2s 和2p x 轨道可以混合各形成二条sp x 杂化轨道。
在C 和O 组成分子时,这四条sp x 杂化轨道中有两条组成了两条σ孤对电子轨道,其中一条是氧的sp x ,另一条是C 的sp x ,剩下两条sp x 杂化轨道进行组合,一条是CO 的σ成键轨道,一条是反键轨道。
除此之外,还有两条充满的π键轨道和两条空的反键轨道,它们是由p y 和p z 轨道重叠而成,分别位于xz 和xy 平面内。
