人教版高中化学必修一2OO6高一化学期末考试卷与答案.docx
高一必修一化学试卷及答案

高一必修一化学试卷及答案【篇一:高中化学必修1(人教版)期末考试试题及参考答案】ss=txt>可能用到的相对原子质量:h—1 c—12 n—14 o—16 na—23 mg—24al—27 si—28s—32 cl—35.5 k—39 ca—40 fe—56 cu—64 zn—65 ag—108 ba—137 注意:请将选择题的答案填写在答题卡上对应的方框内。
第i卷(选择题,共54分)一、单项选择题(每题只有一个选项符合题意,共12小题,每题2分,共24分。
)1.以下各组物质反应,其离子方程式可写成h++oh-=h2o 的是() a.盐酸和烧碱溶液 b.硫酸和氨水c.氯水和氢氧化钾溶液d.氢氧化亚铁和稀硝酸2.只用一种试剂就可将agno3、kscn和h2so4、naoh四种无色溶液区分,这种试剂是()a. fe(no3)3溶液b.fecl2溶液c. bacl2溶液d. fecl3溶液3.下列实验操作中,仪器间不应该接触的是()a.过滤时,漏斗下端管口与烧杯内壁b.使用胶头滴管时,尖嘴与试管内壁c.过滤时,盛被过滤液体的烧杯口与玻璃棒d.向试管倾倒液体药品时,试剂瓶口与试管口4.某金属m的硝酸盐受热时按下列方式发生分解反应:?2mno3?2m?2no2??o2?,加热3.40g该硝酸盐,完全分解生成no2和o2共672ml(标准状况),则m的相对原子质量为()a. 23b. 40c. 108d. 2015.下列反应不属于氧化还原反应的是( )a.2c?o2?2co c. caco高温3点燃b. 2kclo3? 2kcl+3o2↑?cao?co2d.zn+h2so4(稀)=znso4+h2↑6.1989年世界卫生组织把铝确定为食品污染源之一,加以控制使用。
铝在下列应用时应加以控制的是()。
①制铝合金②制电线③制炊具④明矾净水⑤明矾与苏打制食品膨松剂⑥用氢氧化铝凝胶剂加工成胃舒平药片⑦易拉罐⑧包装糖果和小食品a.③⑤⑦⑧b.⑥⑦⑧c.③⑤⑧d.③④⑤⑥⑦⑧7、钠与水反应的现象和钠的下列性质无关的是a、钠的熔点较低b、钠的密度小于水c、钠的硬度较小d、钠的还原性强8.下列物质中,不能使品红溶液褪色的是 ()a.cl2b.so3c.so2d.活性炭9.实验室中,要使alcl3溶液中的al3+离子全部沉淀出来,适宜用的试剂是()a、naoh溶液b、ba(oh)2溶液c、盐酸d、氨水10.下列物质中既能与naoh溶液反应,又能与盐酸反应产生氢气是()a.mgb. cl2c.sid. al11.通常情况下,既能用浓硫酸干燥,又能用碱石灰干燥的是() a . nh3b. cl2 c. no d. hcl12.下列各组离子,能在水溶液中大量共存的是( )a.oh-、k+、fe3+、no3-b.hco3-、oh-、cl-、k+c.mg2+、no3-、h+、al3+d.so42-、ag+、nh4+、cl-第ii卷(共46分)二、填空题(每空1分,共16分)23.(8分)浓硫酸具有a、酸性b、强氧化性c、高沸点、难挥发性,d、脱水性,e、吸水性等性质。
人教版高中化学必修一经典期末测试题及答案

人教版化学必修一期末试题姓名相对原子质量: Na 23 Mg 24 Al 27 Fe 56 Cu 64H 1 O 16 C 12 S 16 Cl 35.5一、选择题(包括12 小题,第1—8题每小题只有1个选项符合题意,每题4分;第9—12题每小题有1~2个选项符合题意,每小题 4分,共 48分)1、若N A 表示阿伏加德罗常数,下列说法中,正确的是( )。
A .1 mol Cl 2作为氧化剂得到的电子数为N AB .在0 ℃,101 kPa 时,22.4 L 氢气中含有N A 个氢原子C .25 ℃,1.01×105 Pa ,64 g SO 2中含有的原子数为3 N AD .N A 个一氧化碳分子和0.5 mol 甲烷的质量比为7∶421、根据广州中心气象台报道,近年每到春季,我省沿海一些城市多次出现大雾天气,致使高速公路关闭,航班停飞。
雾属于下列分散系中的A .溶液B .悬浊液C .乳浊液D .胶体3、下列常用实验仪器中,能直接加热的是( )。
A .分液漏斗B .普通漏斗C .蒸馏烧瓶D .试管4、为了检验某氯化亚铁溶液是否变质,最好向溶液中加入( )A 、NaOH 溶液B 、铁片C 、KSCN 溶液D 、石蕊试液5、2.3gNa 投入97.7g 水中,所得溶液的质量分数为( )A 、2.3%B 、4%C 、<4%D 、>4%6、下列反应中必须加入还原剂才能进行的是A .Cl 2→Cl -B .Zn→ Zn 2+C .H2→H 2OD .CuO→CuCl 27、在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束后,所剩余的固体滤出后能部分被磁铁吸引(单指铜不能被磁铁吸引),则反应后溶液中存在较多的阳离子( )A 、+2CuB 、+3FeC 、+2FeD 、+H8、下列物质中,既能与强酸反应,又能跟强碱反应的是( )①3NaHCO ②Al ③32O Al ④3)(OH Al ⑤32CO NaA 、①②③④⑤B 、②③④C 、①③④D 、①②③④9、下列离子方程式中正确的是( )A 、小苏打溶液中加入烧碱溶液:↑+=+--223CO O H OH HCOB 、氯化铝溶液中加入过量氨水:↓=+-+33)(3OH Al OH AlC 、向氯化亚铁溶液中加入氯水:-+++=+Cl Fe Cl Fe 222322D 、二氧化碳通入碳酸钠溶液中:--=++322322HCO O H CO CO10、在3NO 2+H 2O =2HNO 3+NO 中,氧化剂与还原剂的分子个数比为( )。
高中化学必修一必修1期末化学测试题试卷及答案解析.doc
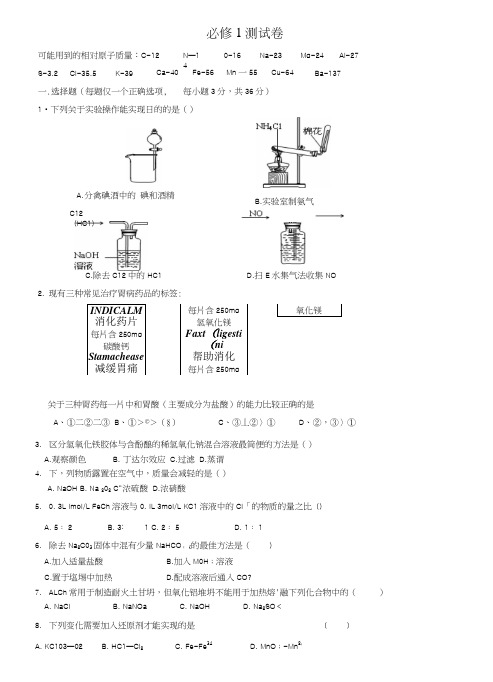
1•下列关于实验操作能实现日的的是()A. 分禽碘酒中的 碘和酒精C.除去C12中的HC1 2. 现有三种常见治疗胃病药品的标签:INDICALM 消化药片 每片含250mg 碳酸钙 Stamachease 减缓胃痛 每片含250mg 氢氧化镁Faxt(ligesti(ni帮助消化每片含250mg氧化镁关于三种胃药每一片中和胃酸(主要成分为盐酸)的能力比较正确的是A 、①二②二③B 、①>©>(§)C 、③丄②〉①D 、②,③〉①3. 区分氢氧化铁胶体与含酚酿的稀氢氧化钠混合溶液最简便的方法是()A.观察颜色B. 丁达尔效应C.过滤D.蒸谓4. 下,列物质露置在空气中,质量会减轻的是()A. NaOHB. Na 202 C“浓硫酸 D.浓硝酸5. 0. 3L lmol/L FeCh 溶液与0. IL 3mol/L KC1溶液中的Cl 「的物质的量之比()A. 5: 2B. 3: 1C. 2: 5D. 1: 16. 除去Na 2C03固体中混有少量NaHCO ;{的最佳方法是( )A.加入适量盐酸B.加入M0H ;溶液C.置于塩埸中加热D.配成溶液后通入CO?7. ALCh 常用于制造耐火土甘坍,但氧化铝堆坍不能用于加热熔'融下列化合物中的()A. NaClB. NaNOaC. NaOHD. Na 2SO <8. 下列变化需要加入还原剂才能实现的是 ( )A. KC103—02B. HC1—Cl 2C. Fe-Fe 34D. MnO ;-Mn 2' 可能用到的相对原子质量:C-12 N —14 S-3.2 Cl-35.5 K-39 必修1测试卷0-16 Na-23 Mg-24 Al-27 Ca-40 Fe-56 Mn 一55 Cu-64 Ba-137 一.选择题(每题仅一个正确选项, 每小题3分,共36分) C12(HC1)D.扫E 水集气法收集NOB.实验室制氨气9.下列关于合金的说法错误的是()A.镁铝合金的熔点比镁和铝都髙B.钠钾合金作为原子反应堆导热材料主要因为其液态范围宽和比热大C.在合金中加入适量的稀土金属能大大改善其性能D.青铜、硬铝、钢都是合金10.宇航员在升空、返冋或遇到紧急情况时,必须穿上10公斤重舱内航天服,神六宇航员所穿舱内航天服是我国科学家近年来研制的新型“连续纤维增韧”航空材料做成,其主要成分是•由碳化硅、陶瓷和碳纤维复合而成,下列相关叙述错误是()• •A.它耐高温B.它没有固定熔点C.它可以耐强碱溶液腐蚀D.它是一种新型无机非金属材料11.“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对坏境的负作用。
(精校版)人教版高一化学必修一期末考试题与答案

(直打版)人教版高一化学必修一期末考试题与答案(word版可编辑修改)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内免会有疏漏的地方,但是任然希望((直打版)人教版高一化学必修一期末考试题与答案(word版可编辑修作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为(直一期末考试题与答案(word版可编辑修改)的全部内容。
高一化学期末模拟试题(五)可能用到的相对原子质量:H—1 C —12N-14O —16NaP—31S—32Cl —35.5Mn —55Fe—56一、单项选择题(每小题只有一个正确答案,每题2 分,共40 分1。
下列实验操作:①取液体试剂,②取固体试剂,③溶解,发。
一定要用到玻璃棒的是()A。
①②③B。
②③④C。
①②⑤ D.③④⑤2.除去下列物质中的杂质 ,所用试剂和方法正确的是()选项物质杂质除杂质所用试剂和方法A KCl 溶液I2xk|b|1加热,升华B KNO 3K2SO 4BaCl 2溶液 ,过滤C Cu CuO 稀硫酸 ,过滤w w w 。
x k b 1。
c o mD CaCO 3CaO盐酸 , 过滤3。
下列说法中,不正确的是 ()23A。
磷酸(H3 PO 4)的摩尔质量与 6.02 × 10个磷酸分子上相等2323B。
6。
02 ×10个氮分子和 6。
02 ×10个比等于14∶123C。
32 g 氧气所含的原子数目为2×6。
02 × 10D.常温常压下,0.5 ×6。
02 ×10 23个一氧化碳分子所占的体积是11.4。
相同质量的下列气体,在同温同压下占有的体积最大的是(A。
H 2 B.O2C。
Cl 2D。
高中化学必修1(人教版)期末考试试题及参考答案

高中化学必修 1(人教版期末考试试题可能用到的相对原子质量:H — 1 C— 12 N — 14 O— 16 Na— 23 Mg — 24 Al—27 Si— 28S — 32 Cl— 35.5 K— 39 Ca— 40 Fe— 56 Cu— 64 Zn— 65 Ag— 108 Ba— 137 注意:请将选择题的答案填写在答题卡上对应的方框内。
第 I 卷(选择题,共 54分一、单项选择题 (每题只有一个选项符合题意,共 12小题,每题 2分,共 24分。
1.以下各组物质反应,其离子方程式可写成 H ++OH-=H2O 的是 (A. 盐酸和烧碱溶液B.硫酸和氨水C. 氯水和氢氧化钾溶液D. 氢氧化亚铁和稀硝酸2. 只用一种试剂就可将 AgNO 3、 KSCN 和 H 2SO 4、 NaOH 四种无色溶液区分 , 这种试剂是 (A. Fe(NO3 3溶液B.FeCl 2溶液C. BaCl2溶液D. FeCl3溶液3. 下列实验操作中,仪器间不应该接触的是(A. 过滤时,漏斗下端管口与烧杯内壁B. 使用胶头滴管时,尖嘴与试管内壁C. 过滤时,盛被过滤液体的烧杯口与玻璃棒D. 向试管倾倒液体药品时,试剂瓶口与试管口4. 某金属 M 的硝酸盐受热时按下列方式发生分解反应 :222322M NO M NO O =+↑+↑∆,加热 3.40g 该硝酸盐,完全分解生成 NO 2和 O 2共 672mL (标准状况 ,则 M 的相对原子质量为(A. 23B. 40C. 108D. 2015. 下列反应不属于氧化还原反应的是 (A. CO O C 222点燃=+B. 2KClO32KCl+3O2↑C . ↑+=23C O CaO CaCO 高温D. Zn+H2SO 4(稀=ZnSO4+H2↑6. 1989年世界卫生组织把铝确定为食品污染源之一,加以控制使用。
铝在下列应用时应加以控制的是( 。
①制铝合金②制电线③制炊具④明矾净水⑤明矾与苏打制食品膨松剂⑥用氢氧化铝凝胶剂加工成胃舒平药片⑦易拉罐⑧包装糖果和小食品A. ③⑤⑦⑧B. ⑥⑦⑧C. ③⑤⑧D.③④⑤⑥⑦⑧7、钠与水反应的现象和钠的下列性质无关的是A 、钠的熔点较低B 、钠的密度小于水C 、钠的硬度较小D 、钠的还原性强8.下列物质中,不能使品红溶液褪色的是 (A.Cl 2B.SO 3C.SO 2D. 活性炭9. 实验室中, 要使 AlCl 3溶液中的 Al 3+离子全部沉淀出来, 适宜用的试剂是 (A 、 NaOH 溶液B 、 Ba(OH2溶液C 、盐酸D 、氨水10.下列物质中既能与 NaOH 溶液反应,又能与盐酸反应产生氢气是(A.MgB. Cl2C.SiD. Al11.通常情况下,既能用浓硫酸干燥,又能用碱石灰干燥的是(A . NH3 B. Cl2 C. NO D. HCl12.下列各组离子,能在水溶液中大量共存的是(A . OH -、 K +、 Fe 3+、 NO 3-B . HCO 3-、 OH -、 Cl -、 K +C . Mg 2+、 NO 3-、 H +、 Al 3+D . SO 42-、 Ag +、 NH 4+、 Cl -第 II 卷(共 46分二、填空题 (每空 1分,共 16分23. (8分浓硫酸具有 A 、酸性 B 、强氧化性 C 、高沸点、难挥发性, D 、脱水性, E 、吸水性等性质。
高一化学必修一期末考试题及答案DOC

高一化学必修一期末考试题及答案DOC一、选择题(每题2分,共20分)1. 下列物质中,属于纯净物的是()。
A. 空气B. 蒸馏水C. 盐水D. 铁矿石2. 化学反应中,原子的()不变。
A. 种类B. 质量C. 数量D. 所有选项3. 根据质量守恒定律,下列说法正确的是()。
A. 化学反应前后元素的种类不变B. 化学反应前后物质的总质量不变C. 化学反应前后原子的种类不变D. 所有选项4. 以下物质中,属于氧化物的是()。
A. 二氧化碳B. 氯化钠C. 氢气D. 氧气5. 根据化学方程式,下列说法正确的是()。
A. 化学方程式可以表示反应物和生成物的质量关系B. 化学方程式可以表示反应物和生成物的微观粒子个数比C. 化学方程式可以表示反应的条件D. 所有选项二、填空题(每空1分,共20分)1. 根据化学式H2O,水分子由_____个氢原子和_____个氧原子构成。
2. 物质的量单位是_____,符号为_____。
3. 1摩尔任何物质都含有_____个粒子。
4. 根据化学方程式2H2 + O2 → 2H2O,氢气和氧气反应生成水,反应物的量比为_____:_____。
5. 根据阿伏伽德罗定律,相同温度和压强下,相同体积的任何气体都含有相同的_____。
三、简答题(每题10分,共30分)1. 请简述什么是化学变化,并给出一个生活中常见的化学变化的例子。
2. 什么是元素周期表?请列举出前20号元素。
3. 请解释什么是氧化还原反应,并给出一个氧化还原反应的例子。
四、计算题(每题15分,共30分)1. 已知某化合物中碳元素的质量分数为40%,氢元素的质量分数为6.7%,氧元素的质量分数为53.3%,求该化合物的分子式。
2. 某化学反应中,反应物A的摩尔质量为32g/mol,反应物B的摩尔质量为16g/mol,反应物A和B按照1:2的摩尔比反应,生成物C的摩尔质量为44g/mol。
若反应物A的质量为40g,求生成物C的质量。
人教版(必修1)·高一化学期末考试试题及答案
…………○号:__________…………○绝密★启用前 人教版(必修1)·高一化学期末考试试题 命题人:XXX 注意事项: 1.答题前填写好自己的姓名、班级、考号等信息 2.请将答案正确填写在答题卡上 3.本试卷满分100分,考试时间90分钟 可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 Cu 64 第I 卷(选择题,共48分)一、选择题(每小题只有一个选项符合题意。
每小题3分,共48分) 1.在汽车加油站见到的油罐车上,所贴的危险品化学品标志是( ) A . B . C . D . 2.从分类角度来看,分散系可分为溶液、胶体和浊液,则这三者的本质区别是( )A .是否有丁达尔现象B .是否能通过滤纸C .是否均一、透明、稳定D .分散质粒子的大小不同 3.下列属于电解质的是( ) A .盐酸 B .酒精 C .NH 3 D .CaCO 3 4.L /mol 是哪个物理量的单位( ) A .物质的量浓度 B .摩尔质量 C .气体摩尔体积 D .物质的量 5.以下物质不能由单质和单质直接反应生成的是( ) A .HCl B .SO 3 C .FeCl 3 D .Na 2O 2 6.下列物质都可用于漂白脱色,其原理不属于化学变化的是( ) A .新制氯水 B .活性炭 C .过氧化钠 D .SO 2 7.工业上制备硝酸的一个重要反应为:4NO +2H 2O+3O 2==4HNO 3。
下列有关该反应的说法不正确的是( ) A .O 2作氧化剂 B .HNO 3既是氧化产物也是还原产物 C .NO 失去电子 D .NO 发生还原反应 8.下列气体中,无色而有刺激性气味的是() A .SO 2 B .Cl 2 C .CO 2 D .NO 2 9.已知N A 为阿伏加德罗常数,下列说法正确的是( ) A .16g O 2和O 3的混合物中含有氧原子数为N A B .1mol H 2O 含有的电子数为9N A…外…○学…内…○C . 标况下,22.4L Cl 2含有的分子数为2N AD .CO 2的摩尔质量是44g 10.下列关于物质用途的叙述中,不正确的是( ) A .氨气易液化,可用作制冷剂 B .可用氢氟酸在玻璃上雕刻各种艺术图案 C .SiO 2是制作太阳能电池的主要材料 D .Fe 2O 3俗称铁红,常用于制红色油漆和涂料11.为了检验某FeCl 2溶液是否氧化变质,可向溶液中加入( ) A .盐酸 B .KSCN 溶液 C .稀H 2SO 4 D .铁片 12.下列物质中既有氧化性又有还原性的是( ) A .Fe 3+ B .Al C .HNO 3 D .SO 2 13.下列能大量共存于溶液中的离子组是( ) A .H +、Na +、SO 42-、CO 32- B .Cl -、H +、Na +、SO 42- C .Ag +、OH -、Cl -、K + D .Fe 2+、H +、K +、NO 3- 14.下列离子方程式的书写正确的是( ) A .铁和稀硫酸反应:2Fe + 6H + == 2Fe 3+ +3H 2↑ B .氯化镁溶液与氢氧化钠溶液反应: Mg 2++2OH - == Mg(OH) 2 ↓ C .钠和冷水反应: Na +2H 2O == Na ++2OH -+H 2↑ D .少量金属钠投入到CuSO 4溶液中:2Na +Cu 2+ == 2Na ++Cu 15.配制一定物质的量浓度的NaOH 溶液时,使所配制的溶液浓度偏小的操作是 ( ) ①烧杯中NaOH 溶液移入容量瓶后,没有洗涤烧杯和转移洗涤液 ②实验用的容量瓶洗净后未干燥,瓶底含有少量水 ③定容后摇匀,发现液面低于刻度线,再滴加蒸馏水至刻度线 ④定容时俯视 ⑤所用NaOH 已经潮解 ⑥称量时所用砝码生锈 A .①③⑤ B .①②③ C .①③④ D .②④⑥ 16.下列现象和结论一致的是( )…○…………外…………○…………内………第II 卷(非选择题,52分) 二、非选择题(每空2分,共52分) 17.(8分)用下列物质的序号填空: ①NaCl(熔融) ②铜片 ③NaCl 固体 ④盐酸 ⑤NaCl 溶液 ⑥干冰 ⑦H 2SO 4,其中能导电的是_____ _____, 属于电解质的是___ _______, 属于非电解质的是__________, 既不是电解质也不是非电解质的是_____________。
人教版高一化学必修一期末考试题及答案
人教版高一化学必修一期末考试题及答案一、选择题(每题3分,共30分)1. 下列关于化学科学的说法正确的是()A. 化学是研究物质的组成、结构、性质以及变化规律的基础科学B. 化学是研究物理现象和化学现象之间的相互联系的科学C. 化学是研究生命现象和生命过程的科学D. 化学是研究自然界的各种物质和能量的科学答案:A2. 下列属于化学变化的是()A. 碘升华B. 酒精挥发C. 铁生锈D. 水蒸发答案:C3. 下列关于原子的说法正确的是()A. 原子是化学变化中的最小粒子B. 原子是构成分子的基本单位C. 原子是不可分割的D. 原子由原子核和电子组成答案:D4. 下列关于元素的说法正确的是()A. 元素是具有相同质子数的一类原子B. 元素是具有相同中子数的一类原子C. 元素是具有相同电子数的一类原子D. 元素是具有相同质量数的一类原子答案:A5. 下列关于离子的说法正确的是()A. 离子是带电的原子或原子团B. 离子是带正电荷的原子或原子团C. 离子是带负电荷的原子或原子团D. 离子是带电的分子答案:A6. 下列关于化合物的说法正确的是()A. 化合物是由两种或两种以上元素组成的纯净物B. 化合物是由两种或两种以上原子组成的纯净物C. 化合物是由两种或两种以上分子组成的纯净物D. 化合物是由两种或两种以上离子组成的纯净物答案:A7. 下列关于氧化还原反应的说法正确的是()A. 氧化还原反应中,氧化剂和还原剂必须同时存在B. 氧化还原反应中,氧化剂和还原剂可以同时为同一种物质C. 氧化还原反应中,氧化剂和还原剂的物质的量必须相等D. 氧化还原反应中,氧化剂和还原剂的质量比必须相等答案:A8. 下列关于酸碱中和反应的说法正确的是()A. 酸碱中和反应的实质是H+和OH-结合生成水B. 酸碱中和反应的实质是H+和Cl-结合生成盐C. 酸碱中和反应的实质是OH-和Cl-结合生成盐D. 酸碱中和反应的实质是酸和碱的化学性质相互抵消答案:A9. 下列关于盐类水解的说法正确的是()A. 盐类水解是指盐在水溶液中发生电离B. 盐类水解是指盐在水溶液中发生分解C. 盐类水解是指盐在水溶液中发生氧化还原反应D. 盐类水解是指盐在水溶液中发生酸碱中和反应答案:D10. 下列关于有机物的说法正确的是()A. 有机物是指含有碳元素的化合物B. 有机物是指含有氢元素的化合物C. 有机物是指含有碳和氢元素的化合物D. 有机物是指含有碳、氢、氧元素的化合物答案:A二、填空题(每题10分,共40分)11. 填写下列物质的化学式:(1)氢氧化钠:________(2)硫酸铜:________(3)氯化钾:________(4)碳酸钙:________答案:(1)NaOH (2)CuSO4 (3)KCl (4)CaCO3 12. 填写下列反应的化学方程式:(1)铁与稀硫酸反应:________(2)氢气与氧气反应:________(3)碱式碳酸铜分解反应:________(4)乙醇与氧气反应:________答案:(1)Fe + H2SO4 = FeSO4 + H2↑(2)2H2 + O2 = 2H2O(3)Cu2(OH)2CO3 = CuO + CO2↑ + H2O(4)C2H5OH + 3O2 = 2CO2 + 3H2O13. 根据下列实验现象,填写相应的化学方程式:(1)将铜丝放入浓硝酸中,观察到铜丝逐渐溶解,溶液变为蓝色,产生红棕色气体。
人教版高中化学必修一——上学期高一期末考试.doc
高中化学学习材料唐玲出品2005——2006学年度上学期高一期末考试化学模拟试题2可能用到的相对原子质量:H -1 C- 12 N- 14 O- 16 He- 4 Na- 23 S- 32 Cl- 35.5Ca- 40 Fe -56 Zn -65 Ag -108 Ba -137一、选择题:(本题共22小题,普通中学做1~20题,重点中学做1~18、21、22题。
共60分,每小题只有一个正确答案)1、下列燃料中,不属于化石燃料的是( )A、煤矿B、石油C、天然气D、水煤气2、实验室收集Cl2,最好选用()A、向上排空气法B、向下排空气法C、排水法D、排饱和食盐水法3、在下列各组物质中,只有还原性的是( )A、Na Cl- S2-B、Cl- CO Na+C、Fe3+ SO42- NO3-D、Fe2+ O2 H2S4、见光能分解的盐.是()A、HClOB、AgBrC、氯水D、Ca(ClO)25、为高空或海底作业提供氧气的物质是()A、KClO3B、KMnO4C、Na2O2D、H2O6、下列物质的保存方法不正确的是()A、新制氯水应密封保存B、盛液溴的试剂瓶常加少量水C、少量的金属钠应保存在煤油中D、固态碘放在棕色细口瓶中7、下列叙述正确的是( )A、1mol任何气体的体积一定是22.4LB、同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同C、在标准状况下,体积为22.4L的物质都是1molD、在非标准状况下,1mol任何气体的体积不可能是22.4L8、用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )A、干燥的B、瓶塞不漏水的C、用欲配制的溶液润洗过的D、以上三项均须要求的9、被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价)( )A、NaBH4既是氧化剂又是还原剂B、NaBH4是氧化剂,H2O是还原剂C、硼元素被氧化,氢元素被还原D、被氧化的元素与被还原的元素质量比为1:110、用自来水养金鱼,在将水注入鱼缸之前,常需把水在阳光下晒一段时间,主要目的是()A、增加水中氧气的含量B、起杀菌作用C、使水中的次氯酸分解D、使水的温度升高11、下列各溶液中,Na+物质的量浓度最大的是( )A、4L0.5mol/LNaCl溶液B、1L0.3mol/LNa2SO4溶液C、5L0.4mol/LNaOHD、2L0.15mol/LNa3PO412、做焰色反应实验时所用的铂丝,每次用毕后都要()A、用水多洗几次B、先用稀盐酸洗,再用水洗C、用稀盐酸洗,再在火焰上灼烧到没有什么颜色为止D、放在火焰上灼烧,直到铂丝发红为止13、下列关于新制氯水及久置氯水的说法,不正确的是()A、新制的氯水呈黄绿色,久置的氯水无色B、新制的氯水漂白作用强,而久置的氯水漂白作用很弱C、新制的氯水所含成分多,而久置的氯水所含成分少D、新制的氯水中无氯离子,而久置的氯水中则含氯离子14、下列离子方程式中,书写不.正确..的是( )A、氯化钠溶液中加入硝酸银溶液:Ag+ + Cl- = AgCl↓B、把金属钠放入水中:Na + 2H2O = Na+ +2OH- + H2C、将溴水加入碘化钾溶液中:Br2 + 2I- = 2Br- + I2D、盐酸滴在石灰石上:CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O15、下列各组离子中,能在溶液中大量共存的是()A、H+、Ca2+、Cl-、CO32-B、I-、ClO-、K+、H+C、Na+、Fe3+、SO42-、OH-D、Na+、Cu2+、Cl-、SO42-16、将同体积同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液中的Cl-完全沉淀,则需同物质的量浓度的AgNO3溶液的体积比为()A、1∶2∶3B、 3∶2∶1C、1∶1∶1D、6∶3∶217、血红蛋白的相对分子质量约为68000,已知其中含铁0.33%,则平均每个血红蛋白的分子中铁原子数约为( )A、5B、4C、3D、2.408×102418、同温同压下,氦气、氢气和氨气的体积比为3∶2∶1,则其原子个数比为 ( )A、1∶2∶3B、4∶3∶3C、3∶4∶4D、3∶2∶119、含碘食盐中的碘是以碘酸钾(KIO3)形式存在的。
人教版必修一高中化学期末考试高一年级化学.docx
高中化学学习材料唐玲出品第一学期期末考试高一年级化学(文)《必修1》试题(考试时间:100分钟,试卷满分:100分)可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 P—31 S—32 Cl—35.5 K—39 Ca—40 Fe—56 Ag—108 Ba—137第Ⅰ卷选择题(每小题2分,共计40分)1.据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源,下列所列能源是清洁能源的是()A.太阳能 B.石油 C.天然气 D.煤2.下列物质的用途错误的是()A.硅是制造太阳能电池的常用材料 B.二氧化硅是制造光导纤维的材料C.水玻璃可用作木材防火剂 D.硅是制取水泥的原料3.下列叙述正确的是()A.纯碱、烧碱均属碱 B.SiO2、SO2均属酸性氧化物C.凡能电离出H+的化合物均属酸 D.盐类物质一定含有金属离子4.绿色植物是空气天然的“净化器”,研究发现,1公顷柳杉每月可以吸收160kgSO2,则1公顷柳杉每月吸收的SO2的物质的量为()A.164kg B.2.5mol C.2500mol D.2500g/mol5.现有两瓶溶液,新制饱和氯水和亚硫酸,下列方法或试剂(必要时可加热)能用于鉴别它们的是()①观察颜色;②石蕊试剂;③品红溶液A.①②③B.只有①③C.只有②③D.只有①②6.下列气体不能用排空气法收集的是()A.Cl2 B.SO2C.O2D.CO7.下列物质是属于非电解质的是 ( )A .NH 3B .(NH 4)2SO 4C .Cl 2D .CH 3COOH8.下列离子方程式书写正确的是( )A .Na 投入到足量的盐酸中:2Na+2H 2O ══2Na ++2OH -+H 2↑B .AlCl 3溶液中加入足量的氨水:Al 3++ 4OH - ══ AlO 2-+2H 2OC .三氯化铁溶液中加入铜粉:322Fe Cu Fe Cu ++++=+D .将氯气通入冷的氢氧化钠溶液中:Cl 2+2OH -=Cl -+ClO -+H 2O 9.下列各组中的离子,能在溶液中大量共存的是( )A .H + Na + CO 32- Cl -B .3K Al Cl OH ++--、、、C .33Fe Al SCN Cl ++--、、、D .Ag + Al 3+ NO 3-H +10.下列情况会对人体健康造成较大危害的是( )A .自来水中通入少量Cl 2进行消毒杀菌B .用SO 2漂白食品C .用食醋清洗热水瓶胆内壁附着的水垢(CaCO 3)D .用小苏打(NaHCO 3)发酵面团制作馒头11.如图所示的实验中,投入铝片后( ) 铝片A .①中产生气泡,②中不产生气泡B .①和②中都不产生气泡 稀HCl NaOH 溶液C .①和②中都产生气泡,①中是H 2,②中是O 2 ① ②D .①和②中都产生气泡,且都是H 2 12.下列物质存放方法错误的是( )A .铝片长期放置在不密封的纸盒里B .漂白粉长期放置在烧杯中C .FeSO 4溶液存放在加有少量铁粉的试剂瓶中D .金属钠存放于煤油中 13.下列实验操作中正确的是( )A .蒸馏操作时,应向蒸馏液体中加入几块沸石,以防止暴沸B .蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热C .分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出D .萃取操作时,可以选用CCl 4或酒精作为萃取剂从溴水中萃取溴14.吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断Na2SeO3的作用是()A.作还原剂 B.作氧化剂C.既作氧化剂又作还原剂 D.既不作氧化剂又不作还原剂15.在FeCl3和CuCl2混合液中,加入过量的铁粉,充分反应后,溶液中的金属离子是()A.Fe2+和Fe3+ B.Fe2+C.Cu2+ 和Fe2+ D.Cu2+16.下列物质间的转化,能经过一步化合反应直接转化的是()A.SiO2→H2SiO3B.Na2O2→Na2CO3C.Fe→FeCl2D.Al2O3→Al(OH)317.下列有关氢气与氯气反应的叙述中,不正确的是()A.纯净的氢气在氯气里安静地燃烧,发出苍白色火焰B.氢气与氯气反应生成的氯化氢气体与空气里的水蒸气结合,呈白雾状 C.氢气与氯气混合后,光照发生爆炸D.氢气与氯气的反应是化合反应,是氧化还原反应,且有电子得失18.在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中化学学习材料
(灿若寒星**整理制作)
高一化学期末复习二
相对原子质量:H—1 C—12 O—16 S—32 N—14 Na—23 Mg—24 Al—27 Fe—56 Ag—108 K —39 Ca—40 Cl—35.5
第Ⅰ卷(共60分)
一、选择题(每题有只有1个正确答案,每题2分,共60分)
1、下列反应中,属于有水参加的氧化还原反应、且水只做氧化剂的是
A .
B .
C .
D .
2、自然界里常见金属元素存在最多的是Al,其次是铁,铜的含量较少。
然而人类冶炼金属获得成功最早的反而是含量少的铜,含量最多的铝最迟冶炼出来,究其原因,合理的是
A.矿石在地下埋藏,铜矿最浅,容易开发,铝矿埋得深,难开发
B.铜矿颜色较深,易发现,铝矿颜色较浅,不易发现
C.铜矿较易还原,铝矿很难还原
D.以上说法是错误的
3、把碘从碘水里分离出来,有下列基本操作:①静置后分液②充分振荡③把碘水倒入分液漏斗,再加
入萃取剂四氯化碳。
其正确的操作顺序是
A.①②③ B.③②① C.②③① D.③①②
4、下列变化中,必须加入氧化剂才能发生的是
A.SO2→S B.SO32—→SO2
C.I—→I2D.HCO3—→CO32—
5、下列物质中属于电解质的是
① KOH ② CuSO4 ③ Al ④HCl ⑤蔗糖
A.①②③ B.②③④ C.③④ D.①②④
6、能用CO32- + 2H+ = H2O + CO2↑离子方程式表示的反应是
A.CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
B.NaHCO3 + HNO3 = NaNO3 + H2O + CO2↑
C.Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑
D.BaCO3 + H2SO4 = BaSO4↓ + H2O + CO2↑
7、下面的离子方程式正确的是
A.碳酸钡和稀硫酸 BaCO3 + 2H+= Ba2+ + H2O + CO2↑
B.Ba(OH)2溶液中加入CuSO4溶液:Ba2+ + SO42- = BaSO4↓
C.硫酸溶液中加入Ba(OH)2溶液:H+ + OH- == H2O
D.澄清石灰水跟盐酸H+ + OH- == H2O
8、加入KOH溶液后,下列溶液中哪种离子数目会减少
A.CO32-
B.Mg2+
C.SO42-
D.Na+
9、下列名词中,哪个名词不属于物理量
A. 长度
B. 质量
C. 摩尔
D. 时间
10、如果你家里的食用花生油混有水份,你将采用下列何种方法分离
A.过滤 B.蒸馏C.分液D.萃取
11、1molN2含有X个分子,则阿伏加德罗常数是
A、.14X B.X/14 C.X D.2X
12、某无色溶液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则溶液中溶有的离子是
A.一定溶有CO32- B.一定溶有Ag+
C.一定溶有SO42- D.可能有SO42-也可能有Ag+
13、下列有关实验的做法,正确的是
A.实验完毕自由离开实验室,想做实验随便进入实验室
B.不慎将酸溅到眼中,应立即用清水冲洗,边洗边眨眼睛
C.洒出的酒精在桌上燃烧起来,立即用干抹布扑盖
D.不报告老师随意增加别的实验,随便动用仪器、药品及其他实验材料
14、用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。
下列不易区别其真伪的方法是 A.测定密度 B.放入硝酸中
(气)
C .放入盐酸中
D .观察外观 15、下列化学方程式中,不能用H +
+OH -
=H 2O 表示的是
A . 2NaOH +H 2SO 4=Na 2SO 4+2H 2O
B . Ba(OH)2+2HCl =BaCl 2+2H 2O
C . Cu(OH)2+2HNO 3=Cu(NO 3)2+2H 2O
D . KOH +HCl =KCl +H 2O
16、在FeCl 3和CuCl 2混合液中,加入过量的铁粉,充分反应后,溶液中的金属离子是
A . Fe 2+
B . Fe 3+ 和Fe 2+
C . Cu 2+ 和Fe 2+
D . Cu 2+ 17、下列化合物不能由单质直接化合得到的是
A . 2CuCl
B . 2CO
C . HCl
D .2FeCl
18、实验室有一瓶购置时间较长绿矾(FeSO 4•7H 2O ),老师将其交给化学研究小组某同学检验药品是否有变质现象,这位同学取绿矾做了简单的检验,得出的结论是:已经开始氧化。
该同学所用的试剂和判断依据是 选项 A B
C D
试剂 氯水 氢氧化钠溶液 铁屑
KSCN 溶液
现象
出现黄褐色
生成红褐色沉淀
绿色加深 有较浅的血红色
二、填空题 (每空2分,共30分)
19、实验室盛装氢氧化钠的试剂瓶用橡皮塞而不用玻璃塞,这是为了防止发生反 应:(用化学方程式表示) ,而使瓶塞 和瓶口粘在一起。
20、工业上拟用铜和硝酸来制备Cu(NO 3)2· 3H 2O ,下面有三位同学提出了不同的生产方案: 甲方案:Cu+浓HNO 3→ 蒸发结晶 乙方案: Cu+稀HNO 3→ 蒸发结晶 丙方案:Cu+O 2→CuO+稀HNO 3蒸发结晶
你认为______方案最好,理由___________ ________
21、某溶液与碱共热,有无色、刺激性气味的气体发出,该气体使湿润的红色石蕊试纸变蓝,该溶液一定含有 ,写出该反应的离子方程式:
;
答案:31、SiO 2+2NaOH===Na 2SiO 3+2H 2O
32、C+2H 2SO 4===CO 2+2SO 2+2H 2O,氧化剂,2:1。
33、丙方案,硝酸消耗较少,且没有污染空气的气体产生。
34、NH 4+, NH 4++OH -===△
═NH 3+H 2O 35、(10分,每空2分 )
(1)3Fe +4H 2O(g)△
═ Fe 3O 4+4H 2 ( 2)检验装置的气密性 (3)干燥反应产生的气体
(4)H 2;验纯;防止点燃时,氢气因含有氧气而爆炸 (5)不需要;水槽中的水能将氢气中的水蒸气冷凝。
36、1,1.5
37、(6分)①所提出的解决方法具有可行性,不会对周边环境和人产生新的危险;(2分)
②实施时所用的物品(包括化学试剂)必须价廉易得。
(2分)。
