镁铝及其化合物知识点
镁和铝
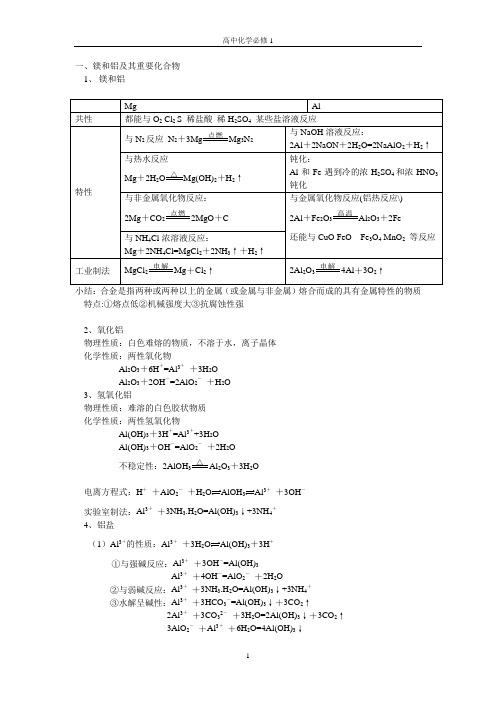
一、镁和铝及其重要化合物1、镁和铝特点:①熔点低②机械强度大③抗腐蚀性强2、氧化铝物理性质:白色难熔的物质,不溶于水,离子晶体化学性质:两性氧化物Al2O3+6H+=Al3++3H2OAl2O3+2OH-=2AlO2-+H2O3、氢氧化铝物理性质:难溶的白色胶状物质化学性质:两性氢氧化物Al(OH)3+3H+=Al3++3H2OAl(OH)3+OH-=AlO2-+2H2O△不稳定性:2AlOH3Al2O3+3H2O电离方程式:H++AlO2-+H2O33++3OH-实验室制法:Al3++3NH3.H2O=Al(OH)3↓+3NH4+4、铝盐(1)Al3+的性质:Al3++3H2O Al(OH)3+3H+①与强碱反应:Al3++3OH-=Al(OH)3Al3++4OH-=AlO2-+2H2O②与弱碱反应:Al3++3NH3.H2O=Al(OH)3↓+3NH4+③水解呈碱性:Al3++3HCO3-=Al(OH)3↓+3CO2↑2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑3AlO2-+Al3++6H2O=4Al(OH)3↓总结:AlCl 3溶液滴加到NaOH 溶液中开始无沉淀后有沉淀NaOH 溶液滴加到AlCl 3溶液中先出现沉淀后沉淀溶解 (2)AlO 2-的性质AlO 2- +2H 2O=Al(OH)3↓+OH - ① 与强酸反应: AlO 2- +H +(少量) +H 2O=Al(OH)3↓ AlO 2-+4H + (过量)=Al 3+ +H 2O②与弱酸反应:AlO 2-+CO 2+2H 2O=Al(OH)3↓+HCO 3-③与水解呈酸性的物质反应:3AlO 2- +Al 3+ +6H 2O=4Al(OH)3↓3AlO 2- +Fe 3+ + 6H 2O=3Al(OH)3↓+Fe(OH)3↓总结:将HCl 滴加到NaAlO 2中先出现沉淀后溶解 将NaAlO 2滴加到HCl 中开始无沉淀后有沉淀 (3)明矾2KAl(SO 4)2+3Ba(OH)2=2Al(OH)3↓+3BaSO 4+K 2SO 4 KAl(SO 4)2+2Ba(OH)2=2BaSO 4↓+KAlO 2+H 2O小结:Al 3+AlOH 3AlO 2AlOH 3Al 3+ 未知溶液白色沉淀白色沉淀溶解,从而未知溶液中含Al 3+未知溶液白色沉淀白色沉淀溶解,从而未知溶液含AlO 2-二、铁及其重要化合物1、铁:第四周期第Ⅷ族 26号元素 各层电子数为2 8 14 2 常见价态+2和+3(1)与弱氧化剂反应 Fe Fe 2+ S +Fe I 2+Fe 2(2)与强氧化剂反应Fe Fe 3+ 3Cl 2+2Fe=2FeCl 3 3Br 2+2Fe 3稀硝酸:Fe +4HNO 3=Fe(NO 3)3+2NO ↑+2H 2O 3Fe +8HNO 3=3Fe(ON 3)3+2NO 2↑+4H 2O特殊:3Fe +2O 23O 4 3Fe +4H 2O 3O 4+4H 2↑2、 氧化物 FeO :黑色固体不溶于水,在空气中加热会生成Fe 3O 4Fe 2O 3:红棕色固体不溶于水,俗称铁红、铁锈,可做红色染料 Fe 3O 4:黑色固体不溶于水,俗称磁性氧化铁3、 氢氧化物Fe(OH)2 白色沉淀迅速变成灰绿色,最后变成红褐色 4Fe(OH)2+O 2+2H 2O=4Fe(OH)3Fe(OH)3:红褐色沉淀 具有不稳定性,受热易分解2FeOH 3Fe 2O 3+3H 2O4、Fe 2+ Fe 3+的盐 (1)Fe 2+的性质 ①颜色:浅绿色△高温点燃△△△过量HClHCl 过量NaOH H +H +OH - OH -②易水解:Fe2++2H2O2+2H+如何保存FeSO4溶液:加几滴稀硫酸或加铁粉③强还原性:与O2Cl2Br2HNO3浓H2SO4KMnO4酸性溶液反应Fe2+检验:①加碱法(NaOH或氨水)②先加KSCN溶液,无现象再加氨水会出现血红色(2)Fe3+的性质①颜色:棕黄色②易水解:Fe3++3H2O3+3H+Fe3++3HCO3-=Fe(OH)3↓+3CO2↑(与CO32-AlO2-也双水解) ③强氧化性:氧化S2-I-SO2SO32-Cu Fe2Fe3++2S2-=2Fe2++2S↓2Fe3++2I-=2Fe2++I2 (Fe3+能使湿润的淀粉KI试纸变蓝)2Fe3++Cu=2Fe2++Cu2+④络合性:KSCN溶液--血红色Fe3++3SCN-=Fe(SCN)3↓⑤制Fe(OH)3胶体:FeCl3+3H2O=Fe(OH)3胶体+3HCl⑥与苯酚显紫色⑧Fe3+检验:溶液加碱法加苯酚法。
02镁、铝及其化合物-【化学方程式】高考重要化学方程式汇总

(1)用惰性电极电解熔融MgCl2
①化学反应:MgCl2 Mg+Cl2↑
②离子反应:Mg2++2Cl- Mg+Cl2↑
③反应应用:工业上炼镁原理
(2)用惰性电极电解MgCl2溶液
①化学反应:MgCl2+2H2O Mg(OH)2↓+Cl2↑+H2↑
②离子反应:Mg2++2Cl-+2H2O Mg(OH)2↓+Cl2↑+H2↑
①化学反应:KAl(SO4)2+2Ba(OH)2 K[Al(OH)4]+2BaSO4↓
②离子反应:Al3++2SO42-+2Ba2++4OH- 2BaSO4↓+[Al(OH)4]-
(2)向明矾溶液中滴加Ba(OH)2溶液至Al3+沉淀完全
①化学反应:2KAl(SO4)2+3Ba(OH)2 K2SO4+3BaSO4↓+2Al(OH)3↓
(3)MgCl2溶液与石灰乳反应
①化学反应:MgCl2+Ca(OH)2 Mg(OH)2↓+CaCl2
②离子反应:Ca(OH)2+Mg2+ Mg(OH)2↓+Ca2+
③反应应用:海水提镁中富集镁的原理
(4)氯化镁晶体脱水
①化学反应:MgCl2·6H2O MgCl2+6H2O
②HCl的作用:带走部分水蒸气,抑制MgCl2的水解,得到无水MgCl2
2.四羟基合铝酸盐溶液和二氧化碳反应
(1)量不同,反应不同,现象相同
①少量CO2:2[Al(OH)4]-+CO2 2Al(OH)3↓+CO32-+H2O
高中化学专题复习-镁和铝的单质及其化合物.ppt

镁
铝
结
周期表 中位置
第三周期ⅡA族
第三周期ⅢA族
金属性
镁强于铝
构 单质的 还原性
镁强于铝
共性:密度小熔点较低,硬度较小银
物理性质 白色金属.
不同点:Al的上述性质都比镁略高.
1.跟O2及 其它非金
2Mg+O2=2MgO
属反应 3Mg+N2=Mg3N2
4Al+3O2=2Al2O3 2Al+3S=Al2S3
Al(OH)3显酸性.
▪ Al(OH)3溶解度很小,无论酸式或碱式电离 的程度都很小,其碱性略强于酸性,故仍
属于弱碱.
重要的铝盐:
▪ 明矾:十二水合硫酸铝钾[KAl(SO4)2·12H2O] ▪ 结构:硫酸铝钾是由两种不同的金属离子和一种
酸根离子组成的化合物,它电离时能产生两种金 属的阳离子,是一种复盐。
▪
Al3++3AlO2-+6H2O = 4Al(OH)3↓
③有关图像:
n(沉淀)
O
n(AlCl3)
五、课堂练习:
2.跟某些 2Mg + CO2 =
2Al+Fe2O3=2Fe+Al2O3
化 氧化物
2MgO + C
(铝热反应)
学 3.跟水反 Mg + 2H2O =
性
应 Mg(OH)2 + H2↑
质
(冷水慢,沸水快)
很难反应
4.跟酸的 Mg + 2H+ =
反应
Mg2+ + H2↑
2Al+6H+=3Al3++3H2↑ (在浓H2SO4、浓HNO3 中钝化)
第二节 铝、镁及其化合物

沉淀
Mg2++2OH-===gCl2+2H2O
蒸发 结晶
析出MgCl2·6H2O
脱水 在氯化氢气流中使MgCl2·6H2O脱水制得无水氯化镁 电解熔融氯化镁制得镁:
电解
电解 MgCl2(熔融) ===== Mg+Cl2↑
[注意] ①由MgCl2·6H2O到无水MgCl2,必须在HCl气流 中加热,以防MgCl2水解。
解析:稀释浓硫酸应该是把浓硫酸慢慢注入水中,A项错误; 两者反应为Mg2++2OH-===Mg(OH)2↓,因此能够观察到沉 淀产生,B项正确;过滤应该用玻璃棒引流,而不是直接倒入 已装好滤纸的漏斗中,C项错误;氮气与镁反应生成氮化镁, 得不到镁粉,D项错误。 答案:B
4.(2020·雅礼中学月考)从海水中提取镁的工艺流程如图所示:
2.根据如图的转化关系判断,下列说法正确的是(反应条件已
略去)
()
A.生成等质量H2时,①和②反应消耗n(HCl)=n(NaOH) B.反应③中氧化剂与还原剂的物质的量之比为2∶3 C.反应③和④消耗等量的Al时,生成的n(Cu)∶n(Fe)=
3∶2 D.反应⑤的离子方程式为Al3++3OH-===Al(OH)3↓
Cr2O3等金属氧化 物
发生铝热反应
能在CO2中燃烧: 点燃
2Mg+CO2=====2MgO+C
3.用途 (1)镁合金——用于制造火箭、导弹和飞机的部件。 (2)镁——制造信号弹和焰火。
4.从海水中提取镁 (1)工艺流程
(2)基本步骤及主要反应
制熟 石灰
高温 CaCO3=====
CaO+CO2↑,CaO+H2O===Ca(OH)2
第二节 铝、镁及其化合物
考点一
镁、铝/ 理清概念 基础需抓牢
镁铝及其化合物(1)概要

反应现象:镁条剧烈燃烧,放出大量的热,发出耀
眼的白光,纸漏斗内剧烈反应,纸漏斗被烧穿,有 熔融物落入沙中。
高温
Fe2O3+2Al === 2Fe + Al2O3
铝热剂 问题 1、镁条的作用是什么?
2、氯酸钾的作用是什么? 结论:铝也是还原剂,在一定的条件下与某些金属
氧化物反应,把其中的金属还原成单质。所以一些 活泼的金属也可作还原剂。
O2
具有抗腐蚀的性能
点燃
点燃
2Mg+ O2 = 2MgO 4Al+ 3O2 = 2Al2O3
点燃
N2 3Mg+ N2 = Mg3N2
质
加热
反 S Mg+ S = MgS
加热
2Al+ 3S =Al2S3
应
点燃
点燃
Cl2 Mg+Cl2 = MgCl2
2Al+ 3Cl2 = 2AlCl3
与 氧
H2O Mg+2冷H水2O反应=△缓M慢g(OH)2↓+2HA2l↑+6H冷2O水△几= 乎2A不l(反O应H)3 ↓+3H2↑
Al(OH)3+OH-=AlO2ˉ+2H2O
类别 主要用途
中强碱,水溶液能够使酚 酞变红
两性氢氧化物
制MgO和镁盐 制备Al2O3和净水剂,治疗胃酸
实验室 制法
Mg2++2OHˉ = Mg(OH)2↓Al3++3NH3•H2O=Al(OH)3
↓+Biblioteka NH4+ 其它方法思考:
(1)Al(OH)3为何既能与酸又能与强碱液反应?
4、镁、铝的制备及用途
第2讲镁、铝及其化合物

NaOH量少:
NaOH量多:
2.与Ba(OH)2溶液反应 Ba(OH)2量少: Ba(OH)2量多:
〖典型例析〗
例1.【202X年高考上海卷】已知NaOH+Al(OH)3→Na[Al(OH)4]。 向集满CO2的铝制易拉罐中加入过量NaOH浓溶液,立即封闭罐 口,易拉罐慢慢凹瘪;再过一段时间,罐壁又重新突出。上述实
与Zn的盐溶液反应,其离子方程式为:
。
⑶用途
〖典型例析〗
例1.海水的综合利用可以制备金属镁,其流程如下图
所示:
(1)若在空气中加热MgCl2·6H2O,生成的是
Mg(OH)Cl或MgO,写出相应反应的化学方程
。
用电解法制取金属镁时,需要无水氯化镁。在干燥的
HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其
。
⑵与NaOH溶液反应的离子方程式为:
。
考点二 铝及其化合物
三、氢氧化铝
1.氢氧化铝是两性氢氧化物。这是因为氢氧化
铝在水溶液中存在两种方式的电离,其电离方程
式:
.
有关的离子方程式为:与盐酸的反应:
.
与NaOH的反应:
.
2.受热分解,化学反应方程式为:
.
考点二 铝及其化合物
3.用途 ⑴治疗胃酸过多,其原理可用离子方程式表示为:
。 。 。 。
考点一 镁及其化合物
二.镁的性质
⑴物理性质
⑵化学性质
①能与O2、Cl2、N2等非金属单质反应,产物分别 为、 、。
②与CO2反应 方程式为:
。
③与酸反应
镁与非氧化性酸如稀硫酸、盐酸等反应生成氢气,离子方程
式为:
。
镁与氧化性酸如浓H2SO4、稀HNO3、浓硝酸在常温下也能反 应,但不生成H2。 ④与盐溶液反应
第三单元金属及其化合物:镁、铝及其化合物——高考化学

示:I2+2S2O2−
,
3 =2I +S4O6 )滴定终点的现象为滴加最后一滴Na2S2O3溶液,锥形瓶
中溶液蓝色褪去,且半分钟内不恢复原色 , 该粗硼样品的纯度为 99
%。
A.5.4 g
B.3.6 g
C.2.7 g
D.1.8 g
( A )
基础测评
4.在KOH和KAlO2混合溶液中滴加稀盐酸直到过量,下列生成沉淀物质
的量与所加盐酸体积关系的图像正确的是
(
D )
方法技能
铝与酸、碱反应生成H2的量的关系
3+
反应实质:Al
+
Al ,2H
H2↑;
定量关系:2Al~3H2。
(1)等量的铝分别与足量盐酸、氢氧化钠溶液反应,产生氢气的体积比
D.海水
Mg(OH)2
MgCl2溶液
MgCl2(熔融)
Mg
基础测评
3.从海水中提取镁的工艺流程如图所示:
下列说法错误的是
( B )
A.用此法提取镁的优点之一是原料来源丰富
B.步骤⑥电解MgCl2时阴极产生氯气
C.步骤⑤可将晶体置于HCl气体氛围中脱水
D.上述工艺流程中涉及化合反应、分解反应和复分解反应
+
+
Al3 +3NH3·H2O===Al(OH)3↓+3NH4 。
-
b.向 NaAlO2 溶液中通入足量 CO2,离子方程式为 AlO2 +CO2+2H2O===
-
Al(OH)3↓+HCO3 。
c.NaAlO2 溶液与 AlCl3 溶液混合:
-
+
3AlO2 +Al3 +6H2O===4Al(OH)3↓ 。
镁和铝知识点归纳

镁和铝其化合物性质知识点归纳一Mg的化学性质1与非金属反应(1)与。
2反应。
常温下与空气中的02反应生成一层致密的氧化物薄膜,所以镁、铝都有抗腐蚀的性能。
镁、铝都能在空气中燃烧:2Mg+0? 一2Mg0。
4AI+ 30 2』2AI 2O 3(2)与卤素单质、硫等反应。
__ Mg+ C 2 门"MgCI 2AI+ 3CI 2 ' '2AICI 32AI+ 3S——AI2S3 (用于工业制备) Mg+ MgS[特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。
镁在空气中燃烧时有三个反应发生:I占烬I总堆頁烬I2Mg+O2 … 2Mg0 3Mg+N 2 … Mg 3N2 2Mg+C0 2 2Mg0+C②燃烧时都放出大量的热,发出耀眼的白光。
禾U用镁的这种性质来制造照明弹。
③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。
2. 与H20反应Mg、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气Mg+2H 2^^= Mg(0H) 2+H2T 2A1+6H 2^^= 2A1(0H) 3+3H2T3. 与酸反应置换出H2Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H2,其中铝在冷浓H2S04,冷浓硝酸中发生钝化现象。
所以可用铝制容器贮存冷的浓硫酸或浓硝酸。
4.与某些氧化物反应(1)镁与二氧化碳反应:2Mg+C0 2 * 2Mg0+C[特别提醒]: “ CQ不能助燃”的说法是不全面的,C0 2对绝大多数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。
(2)铝热反应:2AI+ Fe 2O3 11 2Fe+ AI2O3铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。
[特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金属氧化物可以是:Fe203、Fe0、Fe304、Cr 2。
3、V205、Mn0 2等。
②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
镁铝及其化合物知识点 SANY标准化小组 #QS8QHH-HHGX8Q8-GNHHJ8-
镁、铝及其化合物知识点整理
Ⅰ.课标要求
1.通过海水制镁的事例了解镁及化合物的性质.
2.通过合金材料了解铝及化合物的性质.
3.能列举合金材料的重要应用.
Ⅱ.考纲要求
1.掌握镁铝及化合物的性质.
2.了解镁铝及化合物在生活.生活中的应用.Ⅲ.教材精讲
一. Mg、Al的化学性质
1.与非金属反应
(1)与O
2反应:常温下与空气中的O
2
反应生成一层致密的氧化物
薄膜,所以镁、铝都有抗腐蚀的性能。
镁能在空气中燃烧:
2Mg+O
22MgO ,铝在纯氧中燃烧:4Al+ 3O
2
2Al
2
O
3
(2)与卤素单质、硫等反应:Mg+ Cl 2
MgCl 2
2Al+ 3Cl 2
2AlCl 3
2Al+ 3S
Al 2S 3 (用于工业制
备) Mg+ S
MgS
③集气瓶底部都要放一些细纱,以防止集气瓶炸裂。
2.与H 2O 反应
Mg 、A1和冷水都不反应,但在加热条件下与水反应生成氢氧化物和氢气
Mg+2H 2O (沸水) Mg(OH)2+H 2↑ 2A1+6H 2O
2A1(OH)3+3H 2
↑
[特别提醒]:①镁在空气中用酒精灯火焰点燃即可燃烧,而铝在空气中需要高温点燃才能燃烧。
镁在空气中燃烧时有三个反应发生: 2Mg+O 2
2MgO 3Mg+N 2
Mg 3N 2 2Mg+CO 2
2MgO+C
②燃烧时都放出大量的热,发出耀眼的白光。
利用镁的这种性质来制造照明弹。
3.与酸反应置换出H
2
Mg、A1与浓、稀盐酸、稀硫酸、磷酸等酸反应置换出H
2
,其中铝
在冷浓 H
2SO
4
,冷浓硝酸中发生钝化现象。
所以可用铝制容器贮存冷
的浓硫酸或浓硝酸。
4.与某些氧化物反应
(1)镁与二氧化碳反应:2Mg+CO
2
2MgO+C
[特别提醒]:“CO
2不能助燃”的说法是不全面的,CO
2
对绝大多
数可燃物是良好的灭火剂,而对K、Ca、Na、Mg等可燃物却是助燃剂。
(2)铝热反应:2Al+ Fe
2O
3
2Fe+ Al
2
O
3
铝热反应可用于焊接钢轨和冶炼某些难熔金属,如:V、Cr、等。
[特别提醒]:①铝热剂是指铝粉和某些金属氧化物的混合物,金
属氧化物可以是:Fe
2O
3
、FeO、Fe
3
O
4
、Cr
2
O
3
、V
2
O
5
、MnO
2
等。
②铝热反应的特点是反应放出大量的热,使生成的金属呈液态。
③要使用没有氧化的铝粉,氧化铁粉末要烘干。
④KClO 3作为引燃剂,也可以用Na 2O 2代替。
实验时可以不用镁条点燃,而用在氯酸钾和白糖的混合物上滴加浓硫酸的方法来点燃。
5.与碱反应
镁不与碱反应,铝与碱液反应:2Al+2NaOH+6H 2O
2NaAlO 2+4H 2O+3H 2↑
简写:2Al+2NaOH+2H 2O 2NaAlO 2+3H 2↑
二.氢氧化铝
1.物理性质:A l (O H )3是几乎不溶于水的白色胶状固体,具有吸附性。
2.化学性质
①与酸反应:Al(OH)3 +3HCl =AlCl 3+3H 2O 离子反应方程式:Al(OH)3+3H +=Al 3++3H 2O ②与碱反应:Al(OH)3+NaOH =NaAlO 2+2H 2O 离子反应方程式:Al(OH)3+OH =NaAlO 2+2H 2O
3.Al(OH)
3
的制取
①铝盐与碱反应:实验室制取氢氧化铝时采用过量的氨水,而不
用强碱与可溶性铝盐溶液反应是因为氢氧化铝是两性氢氧化物,能溶于强碱溶液,不溶于弱碱溶液
②偏铝酸盐与酸反应:一般用向偏铝酸盐溶液中通入CO
2
的方法
制取Al(OH)
3。
当CO
2不足或适量时:2AlO
2
+CO
2
+3H
2
O=2Al(OH)
3
↓+CO
3
2
当CO
2过量时:AlO
2
+CO
2
+2H
2
O=Al(OH)
3
↓+HCO
3
4.Al(OH)
3的用途:由于A l(O H)
3
具有吸附性,既能凝聚水中悬
浮物,又能吸附色素,因此A l(O H)
3
可作净水剂和色素吸附剂。
[特别提醒]:(1)制取Al(OH)
3
也可用铝盐与强碱作用,但应严
格控制加入碱的量,因为强碱过量会使制得的Al(OH)
3
转化为偏铝酸盐。
(2)一般不用强酸,因为强酸的量控制不当会使制得的Al(OH)
3溶解。
三.镁铝及其化合物的转化关系图 1.镁及其化合物的知
识主线
上图的1~13中的
有关化学方程式如下:
1、
2、
3、
4、
5、 MgO+H
2O ==== Mg(OH)
2
6、7、8、9、
10、 MgCO
3+H
2
O===Mg(OH)
2
+CO
2
↑
11、 Mg
3N
2
+6H
2
O=3Mg(OH)
2
+2NH
3
↑
12、
13、
2.铝及其化合物的知识主线(重点)(创新设计P37 “铝三角”相关图像)
上图1~12的有关化学方程式如下:
1、
2、
3、
4、
5、
6、
7、
8、9、
10、
11、
12、 2KAl(SO
4)
2
+ 6NH
3
·H2O = 2Al(OH)
3
↓ + K
2
SO
4
+3(NH
4
)
2
SO
4。
