微生物实验室的检验报告时限(TAT)
2017-2018年福建省临床检验中心质控检查评价标准

2017-2018年福建省临床检验中心质控检查评价标准
评价标准
评价要点
适用医疗机构
1.开展标本类型错误率评价,建立质量控制指标。
【C】
1.有相关制度或工作流程。
2.汇总各专业每月所有标本(血液、尿液、胸腹水等)的总数。
3.汇总各专业标本类型与申请检验项目要求不相同的标本总数
4.计算出错误率(注:如申请生化检验,但送检标本为血常规标本,已导致标本类型发生错误,归为此类差错)。
【A】符合“B”并
1..根据实验室间比对率的分析报告和“临床检验专业医疗质量控制指标”室间质量评价结果,采取纠正措施,对纠正效果跟踪评价,成效良好。
18.开展分析设备故障数评价,建立质量控制指标。
【C】1.有相关制度或工作流程。2.汇总该年度分析设备故障导致检验报告延迟的次数。3.计算出故障次数。
二级以上综合医院、中医院、专科医院、妇幼保健院
二级以上综合医院、中医院、专科医院、妇幼保健院
【B】符合“C”并
1.每月评估分析检验前周转时间符合率,并有记录。
2.每月按专业评估分析检验前周转时间,并有记录。
【A】符合“B”并
1.根据检验前周转时间符合率、检验前周转时间的分析报告和“临床检验专业医疗质量控制指标”室间质量评价结果,采取纠正措施,对纠正效果跟踪评价,成效良好。
二级以上综合医院、中医院、专科医院、妇幼保健院
【B】符合“C”并每月按相关专业评估分析标本溶血率,并有记录。
【A】符合“B”并根据标本溶血率分析报告和“临床检验专业医疗质量控制指标”室间质量评价结果,采取纠正措施,对纠正效果跟踪评价,成效良好。
6.开展标本丢失率评价,建立质量控制指标。
【C】1.有相关制度或工作流程。2.汇总各专业每月标本(血液、胸腹水、脑脊液等)总数。3.汇总各专业丢失标本总数。4.计算出丢失率。
检验科质量控制考核标准
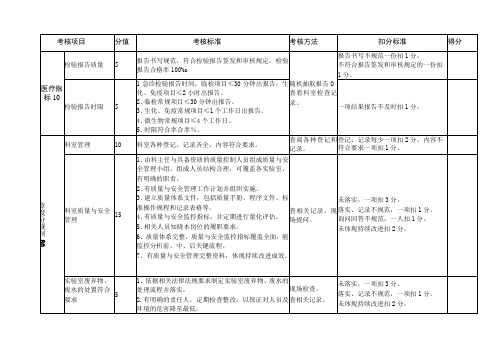
现场检查。
查相关记录。
未落实,一项扣3分。
落实、记录不规范,一项扣1分。
未体现持续改进扣2分。
度
3.对标本能全程跟踪,检验结果回报时间(TAT)明确可查。
4.标本处理和保存专人负责,标本废弃有记录,储存标本冰箱有温度24小时监控。
检验报告格式规范、统一
10
L检验报告单格式规范、统一,有书写制度。
2.报告单提供中文或中英文对照的检测项目名称,项目名称符合相关规定。
3.检验报告采用国际单位或权威学术机构推荐单位,并提供参考范围。
4.检验报告单包含充分的患者信息,标本类型、样本采集时间、结果报告时间。
5.有双签字。
6.科室有专门人员定期自查、反馈、整改。
3.指定专门的储存地点,专人管理,对使用情况做详细记录。
4.有化学危险品溢出与暴露的应急预案。
5.相关人员对制度和预案的知晓率100%o
6.、针对职能科室监管,有持续改进危险品管理工作。
现场检查。
现场询问。
查相关记录。
未落实,一项扣3分。
落实、记录不规范,一项扣1分。
询问回答不规范一人扣1分。
未体现持续改进扣2分。
2.临检常规项目≤30分钟出报告。
3.生化、免疫常规项目≤1个工作日出报告。
4.微生物常规项目≤4个工作日。
5.时限符合率合率%。
一项结果报告不及时扣1分。
章度分规制80
科室管理
10
科室各种登记、记录齐全,内容符合要求。
查阅各种登记和记录。
登记、记录每少一项扣2分。内容不符合要求一项扣1分。
科室质量与安全管理
临床实验室质量指标

临床实验室质量指标
为加强医疗质量管理与控制,完善我国医疗质量管理与控制指标体系,规范医疗机构和医务人员执业行为,保障人民群众身体健康和生命安全,依据卫生部办公厅关于委托制订临床实验室质量管理与控制指标体系函[卫办医政函〔2009〕723号]的精神,卫生部临床检验中心已组织有关专家,根据美国病理学家学会(CAP)的质量探索(Q-Probes)和质量跟踪(Q-Tracks)计划中所制定和监测的质量指标、美国临床和实验室标准化研究院(CLSI)有关文件、我国《医院管理评价指南》(卫医发〔2008〕27号)、《综合医院评价标准》(2009年版)、《患者安全目标》(2010年版)及《医疗机构临床实验室管理办法》(卫医发[2006]73号)中对临床实验室质量和管理的规定要求,并结合我国的基本国情来制定了如下的临床实验室质量管理与控制指标。
按照分析过程的不同阶段,可将制定的临床实验室质量指标分为分析前、分析中和分析后的质量指标。
在各个分析阶段中,又着眼于可能对实验室报告结果有影响的关键步骤将指标再细分。
目前提出的质量指标有分析前20项,分析中11项,分析后29项,共60项。
各阶段具体指标如下:
表1分析前质量指标
表2分析中质量指标
表3分析后质量指标。
检验科管理与持续改进记录

四棉临床检验管理与持续改进时间:地点:负责人:质控人员:一、检验质量与安全管理((★)(★)为核心条款,(★)为核心制度)(一)部门设置、布局、设备设施;服务项目;急诊检验1、设置、布局、设备设施符合《医疗机构临床实验室管理办法》;合作单位服务协议;(1)以前存在的问题及改进情况2)目前存在的问题及对策2、定期网络通报细菌耐药、临床标本菌种分布( 1 次/ 季度);三年开展的检验新项目一览表 4.15.11)以前存在的问题及改进情况精品(2)目前存在的问题及对策3、临床合理性建议、新项目设置合理性及急诊检验满意度调查表(2次/ 年);(1)以前存在的问题及改进情况(2)目前存在的问题及对策4、急诊项目报告时间对外公示(急性心肌标志物、凝血和感染)(1)以前存在的问题及改进情况2)目前存在的问题及对策精品5、检验项目、设备、试剂管理:三证齐全;分子诊断项目(外送);应急检测能力和技术储备;方法学验证及评价记录(1)以前存在的问题及改进情况(2)目前存在的问题及对策6、新项目审批及实施流程:步骤;新项目实施后的跟踪,听取临床对新项目设置合理性的意见,改进项目管理(1)以前存在的问题及改进情况2)目前存在的问题及对策(二)实验室安全程序,制度及相应的标准操作程序,遵照实施并记录1、《实验室安全管理制度和流程》、科主任负责、记录、培训;实验室生物安全分区、实验室生物安全等级标志、工作流程避免交叉污染;精品(1)以前存在的问题及改进情况2)目前存在的问题及对策2、洗眼器、冲淋装置及其他急救设施及耗材、警示标识、《实验室工作人员健康档案》;(1)以前存在的问题及改进情况(2)目前存在的问题及对策3、《传染病职业暴露应急预案》培训演练;《标本溢洒处理流程》消毒记录、检测;废水废物专人负责、记录、整改(1)以前存在的问题及改进情况(2)目前存在的问题及对策精品4、《微生物菌种、毒株的管理规定与流程》专人负责、应急预案、记录;《化学危险品的管理制度》《化学危险品清单和安全数据表》储存、记录《化学危险品溢出与暴露的应急预案》(1)以前存在的问题及改进情况(三)具备临床检验专业资质的人员进行检验质量控制活动,解释检查结果4.15.31、生化室≥80%的员工持卫生部核发的大型生化分析仪上岗证、科主任资质(副高以上)、《实验室上岗、轮岗、定期培训及考核》、检验全程质量控制授权及动态管理(1)以前存在的问题及改进情况2)目前存在的问题及对策四)检验报告及时、准确、规范,严格审核制度1、量值溯源、校准验证、能力验证、室内质控、室间质评1)以前存在的问题及改进情况2、检验报告时限(TAT):临检常规项目≤30分钟;生化、2)目前存在的问题及对策免疫常规项目≤1个工作日;微生物常规项目≤4个工作日;时限符合率≥90%;《检验结果报告时间定期评估》(1)以前存在的问题及改进情况2)目前存在的问题及对策3、《检验报告双签字制度》及审核《复检制度》及记录;《检验报告单书写制度》书写规范、统一,检查内容:格式、检验项目名称中英文对照、报告单位、参考范围、患者信息、标本类型、标本采集时间、结果报告时间、双签名等(1)以前存在的问题及改进情况4、《实验室与临床沟通机制》宣传、咨询、沟通、记录;《检验与临床的科间协调会议制度》每年1-2 次(1)以前存在的问题及改进情况2)目前存在的问题及对策2)目前存在的问题及对策五)试剂与校准品管理:《试剂与校准品管理制度》1)以前存在的问题及改进情况2)目前存在的问题及对策(六)检验质量与安全管理小组1、《检验质量与安全管理小组名册》及组织结构图2、《检验质量与安全管理工作计划》并组织实施(工作记录、佐证材料)3、《检验质量与安全监控指标》、定期量化评估4、质量体系包括质量手册、程序文件、标准操作规程和记录表格等(1)以前存在的问题及改进情况精品(七)《标本采集运输指南》:标本接收、拒收标准与流程及记录;标本全程跟踪、检验结果回报时间(TAT)查询;标本处理、保存专人负责(1)以前存在的问题及改进情况2)目前存在的问题及对策(八)室内质控:室内质控项目一览表、质控记录、质控规则、质控报告负责人签字、质控重点项目流程和记录及评价1、《临床化学、免疫学、血液学和凝血试验的质量控制流程》2、《血涂片评价和分类计数的质量控制流程》3、《细菌、分枝杆菌和真菌检测的质量控制流程》4、《尿液分析和临床显微镜检查的质量控制流程》5、《采用质量控制鉴别病毒鉴定试验中的错误检验结果》(1)以前存在的问题及改进情况精品(九)参加室间质评或能力验证活动:室间质评记录、室间质评项目一览表、无室间质评检验项目的替代评估方案;(1)以前存在的问题及改进情况2)目前存在的问题及对策(十)保证检测系统的完整性和有效性;POCT项目均应开展室内质控,并参加室间质评;(1)以前存在的问题及改进情况2)目前存在的问题及对策十一)实验室信息管理1)以前存在的问题及改进情况精品(十二)新技术准入制度(★)1)以前存在的问题及改进情况(2)目前存在的问题及对策(十三)专项督查1、患者知情同意与告知、医患沟通、隐私保护、私密沟通场所(★)(★)(1)以前存在的问题及改进情况(2)目前存在的问题及对策精品2、危急值(★)(★)1)以前存在的问题及改进情况(2)目前存在的问题及对策3、不良事件(★)(★)(1)以前存在的问题及改进情况(2)目前存在的问题及对策4、培训(1)以前存在的问题及改进情况2)目前存在的问题及对策精品(十四)补充项目:(1)以前存在的问题及改进情况(2)目前存在的问题及对策三、其它1、急救设施、设备、药品管理(1)以前存在的问题及改进情况(2)目前存在的问题及对策2、人员配备与培养1)以前存在的问题及改进情况精品(2)目前存在的问题及对策3、病人投诉及医疗纠纷(1)以前存在的问题及改进情况(2)目前存在的问题及对策五、统计(检验质量与安全指标、本月工作量、不良事件、危急值、投诉等)如有侵权请联系告知删除,感谢你们的配合!精品。
福建省临床检验中心质控检查评价标准

二级以上综合医院、中医院、专科医院、妇幼保健院
【B】符合“C”并
1.每月按专业评估分析危急值通报及时率,并有记录。
【A】符合“B”并
1.根据危急值通报及时率的分析报告和“临床检验专业医疗质量控制指标”室间质量评价结果,采取纠正措施,对纠正效果跟踪评价,成效良好。
10.开展检验前周转时间评价,建立质量控制指标。★
4.计算出开展率。
5.保证每检测批次至少有1次室内质控结果。
6.制定实验室室内质控规则。
7.室内质控报告有负责人签字。
二级以上综合医院、中医院、专科医院、妇幼保健院
【B】符合“C”并
1.每月按专业评估分析室内质控项目开展率。
【A】符合“B”并
1.根据室内质控项目开展率分析报告和“临床检验专业医疗质量控制指标”室间质量评价结果,采取纠正措施,对纠正效果跟踪评价,成效良好。
评价标准
评价要点
适用医疗机构
1.开展标本类型错误率评价,建立质量控制指标。
【C】
1.有相关制度或工作流程。
2.汇总各专业每月所有标本(血液、尿液、胸腹水等)的总数。
3.汇总各专业标本类型与申请检验项目要求不相同的标本总数
4.计算出错误率(注:如申请生化检验,但送检标本为血常规标本,已导致标本类型发生错误,归为此类差错)。
【B】符合“C”并
1.每月按专业评估分析标本容器错误率,并有记录。
【A】符合“B”并
1.根据标本容器错误率的分析报告和“临床检验专业医疗质量控制指标”室间质量评价结果,采取纠正措施,对纠正效果跟踪评价,成效良好。
3.开展标本采集量错误率评价,建立质量控制指标。
【C】
1.有相关制度或工作流程。
临床检验科管理系统与持续改进督查

临床检验管理与持续改进时间:地点:负责人:质控人员:一、检验质量与安全管理((★)(★)为核心条款,(★)为核心制度)(一)部门设置、布局、设备设施;服务项目;急诊检验1、设置、布局、设备设施符合《医疗机构临床实验室管理办法》;合作单位服务协议;(1)以前存在的问题及改进情况(2)目前存在的问题及对策2、定期网络通报细菌耐药、临床标本菌种分布(1次/季度);三年开展的检验新项目一览表4.15.1(1)以前存在的问题及改进情况(2)目前存在的问题及对策3、临床合理性建议、新项目设置合理性及急诊检验满意度调查表(2次/年);(1)以前存在的问题及改进情况(2)目前存在的问题及对策4、急诊项目报告时间对外公示(急性心肌标志物、凝血和感染)(1)以前存在的问题及改进情况(2)目前存在的问题及对策5、检验项目、设备、试剂管理:三证齐全;分子诊断项目(外送);应急检测能力和技术储备;方法学验证及评价记录(1)以前存在的问题及改进情况(2)目前存在的问题及对策6、新项目审批及实施流程:步骤;新项目实施后的跟踪,听取临床对新项目设置合理性的意见,改进项目管理(1)以前存在的问题及改进情况(2)目前存在的问题及对策(二)实验室安全程序,制度及相应的标准操作程序,遵照实施并记录1、《实验室安全管理制度和流程》、科主任负责、记录、培训;实验室生物安全分区、实验室生物安全等级标志、工作流程避免交叉污染;(1)以前存在的问题及改进情况(2)目前存在的问题及对策2、洗眼器、冲淋装置及其他急救设施及耗材、警示标识、《实验室工作人员健康档案》;(1)以前存在的问题及改进情况(2)目前存在的问题及对策3、《传染病职业暴露应急预案》培训演练;《标本溢洒处理流程》消毒记录、检测;废水废物专人负责、记录、整改(1)以前存在的问题及改进情况(2)目前存在的问题及对策4、《微生物菌种、毒株的管理规定与流程》专人负责、应急预案、记录;《化学危险品的管理制度》《化学危险品清单和安全数据表》储存、记录《化学危险品溢出与暴露的应急预案》(1)以前存在的问题及改进情况(2)目前存在的问题及对策(三)具备临床检验专业资质的人员进行检验质量控制活动,解释检查结果4.15.31、生化室≥80%的员工持卫生部核发的大型生化分析仪上岗证、科主任资质(副高以上)、《实验室上岗、轮岗、定期培训及考核》、检验全程质量控制授权及动态管理(1)以前存在的问题及改进情况(2)目前存在的问题及对策(四)检验报告及时、准确、规范,严格审核制度1、量值溯源、校准验证、能力验证、室内质控、室间质评(1)以前存在的问题及改进情况(2)目前存在的问题及对策2、检验报告时限(TAT):临检常规项目≤30分钟;生化、免疫常规项目≤1个工作日;微生物常规项目≤4个工作日;时限符合率≥90%;《检验结果报告时间定期评估》(1)以前存在的问题及改进情况(2)目前存在的问题及对策3、《检验报告双签字制度》及审核《复检制度》及记录;《检验报告单书写制度》书写规范、统一,检查内容:格式、检验项目名称中英文对照、报告单位、参考范围、患者信息、标本类型、标本采集时间、结果报告时间、双签名等(1)以前存在的问题及改进情况(2)目前存在的问题及对策4、《实验室与临床沟通机制》宣传、咨询、沟通、记录;《检验与临床的科间协调会议制度》每年1-2次(1)以前存在的问题及改进情况(2)目前存在的问题及对策(五)试剂与校准品管理:《试剂与校准品管理制度》(1)以前存在的问题及改进情况(2)目前存在的问题及对策(六) 检验质量与安全管理小组1、《检验质量与安全管理小组名册》及组织结构图2、《检验质量与安全管理工作计划》并组织实施(工作记录、佐证材料)3、《检验质量与安全监控指标》、定期量化评估4、质量体系包括质量手册、程序文件、标准操作规程和记录表格等(1)以前存在的问题及改进情况(2)目前存在的问题及对策(七) 《标本采集运输指南》:标本接收、拒收标准与流程及记录;标本全程跟踪、检验结果回报时间(TAT)查询;标本处理、保存专人负责(1)以前存在的问题及改进情况(2)目前存在的问题及对策(八)室内质控:室内质控项目一览表、质控记录、质控规则、质控报告负责人签字、质控重点项目流程和记录及评价1、《临床化学、免疫学、血液学和凝血试验的质量控制流程》2、《血涂片评价和分类计数的质量控制流程》3、《细菌、分枝杆菌和真菌检测的质量控制流程》4、《尿液分析和临床显微镜检查的质量控制流程》5、《采用质量控制鉴别病毒鉴定试验中的错误检验结果》(1)以前存在的问题及改进情况(2)目前存在的问题及对策(九) 参加室间质评或能力验证活动:室间质评记录、室间质评项目一览表、无室间质评检验项目的替代评估方案;(1)以前存在的问题及改进情况(2)目前存在的问题及对策(十)保证检测系统的完整性和有效性;POCT项目均应开展室内质控,并参加室间质评;(1)以前存在的问题及改进情况(2)目前存在的问题及对策(十一)实验室信息管理(1)以前存在的问题及改进情况(2)目前存在的问题及对策(十二) 新技术准入制度(★)(1)以前存在的问题及改进情况(2)目前存在的问题及对策(十三)专项督查1、患者知情同意与告知、医患沟通、隐私保护、私密沟通场所(★)(★)(1)以前存在的问题及改进情况(2)目前存在的问题及对策2、危急值(★)(★)(1)以前存在的问题及改进情况(2)目前存在的问题及对策3、不良事件(★)(★)(1)以前存在的问题及改进情况(2)目前存在的问题及对策4、培训(1)以前存在的问题及改进情况(2)目前存在的问题及对策(十四)补充项目:(1)以前存在的问题及改进情况(2)目前存在的问题及对策三、其它1、急救设施、设备、药品管理(1)以前存在的问题及改进情况(2)目前存在的问题及对策2、人员配备与培养(1)以前存在的问题及改进情况(2)目前存在的问题及对策3、病人投诉及医疗纠纷(1)以前存在的问题及改进情况(2)目前存在的问题及对策五、统计(检验质量与安全指标、本月工作量、不良事件、危急值、投诉等)。
三级综合医院评审标准检验部分课件

• 2.保存完整的各项安全相关活动记录。 • 【A】符合“B”,并
• 严格执行安全规程,定期进行安全检查, 定期研究安全管理,保障实验室安全,
• 各项记录完整。
4.16.2.2 实验室进行生物安全分区并合理 安 排工作流程以避免交叉污染
• 【C】 • 1.实验室生物安全分区合理,有明确的实验室生物
• 【C】
• 1.不同实验室应组织有针对性的上岗、轮 岗、定期培训及考核,对通过考核的人员 予以适当授权。
• 2.选择并授权具有相关资质、经验丰富及 较高技术水平和业务能力的人员负责检验 全程质量控制工作及结果解释工作。
• 【B】符合“C”,并 • 1.对授权工作实行动态管理。 • 2.有主管部门监督检查,评价培训效果。
目,可委托其他三级甲等医院提供服务,或多院联合开展 服务,但应签署医院之间的委托服务协议,有质量保证条 款。
• 【B】符合“C”,并
• 1.每年都有为临床推出新项目。 • 2.微生物检验项目对院内感染控制及合理用药提
供充分支持。
• 【A】符合“B”,并
• 1.以书面或网络形式定期(至少每季)向临床科 室通报细菌耐药情况。
• 【A】符合“B”,并 • 培训及考核记录完整,有授权人员的定期
评价,工作人员无超权限范围操作。
4.16.4 检验报告及时、准确 、规范,严格审核制度
• 4.16.4.1保证每一项检验结果的准确性。 • 【C】 • 实验室应采用量值溯源,校准验证,能力验证或室
间质评,实验室间的比对等方式充分保证每一项检 验结果的准确性。 • 【B】符合“C”,并 • 开展室内质控与室间质评,保障检验质量。 • 【A】符合“B”,并 • 室内质控与室间质评结果达到质量控制目标。
医学检验科检验报告管理制度

医学检验科检验报告管理制度I目的加强检验报告管理,确保检验报告正确性。
II范围适用于医学检验科。
Ill制度一、报告的格式和内容医学检验科检验报告应规范、统一。
报告单提供中文或中英文对照的检测项目名称,项目名称符合相关规定。
每份检验报告内容至少包含下列内容。
(一)清晰明确的检验标识,适当时还包括测量方法;(二)发布报告的实验室的标识(如实验室名称,委托检验结果的标识应是委托实验室);(三)患者的唯一性标识和地点,如可能,注明报告的送达地;(四)检验申请者的姓名或其它唯一性标识和申请者的地址;(五)原始样品采集的日期和时间,当可行并与患者医疗护理有关时,还应注明实验室接收样品的时间;(六)报告发布的日期和时间,如果没有在报告中注明,也应保证在需要时可以随时查到;(七)原始样品的来源和系统(或原始样品的类型);(八)以Sl单位或可以溯源至SI单位的单位报告的结果(如适用);(九)生物参考区间(如适用);(十)结果的解释(如需要);(十一)其它注释(例如,可能影响检验结果的原始样品的质或量;委托实验室的检验结果/解释;新方法的使用);报告中应区别出作为开发新方法的、其测量性能还没有完全确定的那部分检验,需要时,应有检出限和测量不确定度资料供查询;(十二)报告单上应注明检测的方法学或检验仪器及型号(编号),便于进行同一项目不同设备结果溯源;(十三)报告审核和授权发布人的标识;(十四)检验报告的页码和页码总数,如“第1页,共2页"。
(十五)相关时,应提供原始结果和修正后的结果;(十六)如可能,应有审核并发布报告的授权人的签名。
二、检验报告发布(一)检验报告签字人授权:由医学检验科主任对科室人员教育、职业技能、执业资格证、业务能力等进行审核,对符合条件者进行授权。
通过授权签的人员允许进行检验、检验结果审核、检验报告查询、检验结果解释、咨询服务等不同的从业活动。
具体活动类型依据授权人员的职称、教育水平、执业资格、岗位要求等要素而定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
<=7天
<=7天
真菌培养
<=7天
<=7天
一般细菌培养及鉴定
<=4天
<=4天
霍乱弧菌培养
<=3天
<=3天
支原体培养及药敏
<=3天
<=3天
衣原体检测
<=2小时
<=2小时
涂片查淋球菌
<=1小时
<=0.5小时
一般细菌涂片检查
<=2小时
<=1小时
真菌涂片检查
<=2小时
<=1小时
涂片查抗酸杆菌
<=4小时
微生物实验室的检验报告时限tat检验项目报告时限tat住院门诊结核杆菌培养42天42天血培养及鉴定7天7天真菌培养7天7天一般细菌培养及鉴定4天4天霍乱弧菌培养3天3天支原体培养及药敏3天3天衣原体检测2小时2小时涂片查淋球菌1小时05小时一般细菌涂片检查2小时1小时真菌涂片检查2小时1小时涂片查抗酸杆菌4小时2小时g试验1天1天gm试验1天1天超出时限报告的处理1所有超出时限的检验报告都要在迟发报告登记本上进行登记并注明报告迟发原因
微生物实验室的检验报告时限(TAT)
检验项目
报告时限(TAT)
超出时限报告的处理
住院
门诊
结核杆菌培养
<=42天
<=42天
1、所有超出时限的检验报告都要在《迟发报告登记本》上进行登记并注明报告迟发原因;
2、做好与临床医生或患者的沟通,将报告迟发的原因跟对方解释清楚。
3、认真分析报告迟发的原因,总结经验,改进方法避免再次发生类似情况。
<=2小时
G试验
<=1天
<=1天
GM试验
<=1天
<=1天
隐球菌抗原检测
<=4小时
<=4小lt;=2天
