ACS的规范化抗凝抗血小板治疗
ACS抗血小板治疗

新型ADP受体拮抗剂
如cangrelor,可在手术过程中快速逆转抗血 小板作用,降低围手术期血栓风险。
抗血小板治疗的个体化方案研究
根据患者的基因型、危险因素和临床 特征制定个体化的抗血小板治疗方案 ,以提高治疗效果并降低不良反应。
研究不同患者对不同抗血小板药物的 反应差异,为临床提供更精确的治疗 选择。
防止血栓形成
血小板在血栓形成过程中起关键作用,通过抗血小板治疗 可有效抑制血小板聚集,预防血栓形成,从而降低心肌梗 死、中风等严重心血管事件的发生率。
改善患者预后
及时、规范的抗血小板治疗有助于改善ACS患者的临床预 后,提高患者的生活质量和生存率。
临床实践中的注意事项与挑战
01 02
出血风险
抗血小板治疗会增加出血风险,特别是消化道出血、脑出血等严重出血 事件。医生需根据患者情况谨慎评估抗血小板治疗的利弊,选择合适的 药物和剂量。
01
02
03
抑制血小板活化
抗血小板药物通过抑制血 小板表面的受体或酶,阻 止血小板活化,从而降低 血栓形成的风险。
抑制血小板聚集
抗血小板药物可以抑制血 小板之间的聚集反应,防 止血栓形成和血管阻塞。
增加血小板溶解
某些抗血小板药物可以促 进血小板溶解,从而降低 血小板数量和活性,减少 血栓形成的风险。
ACS的分类与临床表现
NSTEMI/UA
非ST段抬高型心肌梗死和不稳定型心绞痛的病理生理机制相似,冠状动脉存在 不稳定的粥样斑块,但没有完全闭塞,心电图表现为非ST段抬高。临床表现为 阵发性胸痛、呼吸困难、心悸等。
STEMI
ST段抬高型心肌梗死是由于冠状动脉完全闭塞导致心肌缺血坏死,心电图表现 为ST段抬高。临床表现为持续剧烈胸痛、心力衰竭、心律失常甚至心脏骤停。
ACS治疗新观点

NSTE-ACS治疗策略
• 危险分层 • 根据最初的危险确定抗血小板治疗策略
– 所有患者应用二联抗血小板治疗 – 中危到高危患者应用糖蛋白 IIb/IIIa受体拮抗剂
• 抗凝治疗 • 中危到高危患者进行血管重建
– 根据最初的严重程度确定血管重建时间
血栓的构成—血小板,纤维蛋白,血细胞
• 在接受磺达肝癸钠治疗的患者PCI术中加用普通肝素可最大程 度减少导管内血栓,并维持磺达肝癸钠的疗效与安全性
*围PCI 定义为PCI 后加治疗
拟72小时内进行冠状动脉造影/PCI 双盲
标准剂量普通肝素
(85 U/kg 或 60 U/kg 联用 GP IIb/IIIa)
ACT 监控* 随访30 天
NSTEACS
符合以下至少两项: • 年龄>60 • 生物标记物升高 • ECG 改变
• 接受磺达肝癸钠治疗的PCI患者使用普通肝素与单 独应用磺达肝癸钠比较,不会增加大出血事件; 与依诺肝素比较大出血事件降低。
NSTEMI- Anticoagulation
Guidelines on myocardial revascularization 2010 ESC
NSTE-ACS Very high-risk of ischaemia Anticoagulation Class Level C B C B B B B UFH(+GPIIb-IIIa antagonists) or I Bivalirudin ( monotherapy ) Medium-to-high risk of ischaemia UFH Bivalirudin Fondaparinux Enoxaparin Low-risk of ischaemia Fondaparinux I I I I IIa I
ACS患者抗血小板治疗策略

抗血小板治疗药物的演变
1988年FDA批准用于临床的抗血小板药物 单用疗效有限,增加剂量会增加出血危险
阿司匹林
第一个噻吩吡啶类
1991年FDA批准 严重不良反应:中性粒细胞减少、血栓性血小板减少性紫癜
噻氯匹定
氯吡格雷
1998年FDA批准 疗效、安全性被广泛证实
ESC2014 心肌血运重建指南对PCI术后DAPT治疗,维持剂量及时间的推荐
ESC 2014 《心肌血运重建指南》推荐
择期PCI 术前建议服用氯比格雷600mg或更大剂量的负荷剂量,75mg/日维持剂量 对于支架置入术后的抗血小板治疗,药物洗脱支架(DES)置入术后应给予双
联抗血小板治疗6 个月 接受第二代DES 置入后的高危出血风险患者应接受双重抗血小板治疗3 个月 而对于存在高缺血和低出血风险的患者,或许可以给予双重抗血小板治疗6 个
② 发病12h后接受PCI的患者,参照直接PCI用药; ③ 接受溶栓的PCI患者,溶栓后24h内口服300mg负荷剂量,24h后口服300-600mg
负荷剂量,维持剂量75mg/d,至少12个月; ④ 未接受再灌注治疗的患者,口服氯吡格雷75mg/d,至少12个月。
新进展:ESC 2014 心肌血运重建指南
血风险)
Ferreiro JL, Sibbing D, Angiolillo DJ.Thromb Haemost. 2010;103:1128-35.
抗血小板策略调整需基于缺血与出血风险的平衡
平衡策略
缺血
• 对于心脑血管事件高危患 者,如ACS、近期行PCI 者,建议继续双抗治疗
• 过早停用抗血小板药物者 临床结局更差
小结
合并CKD患者同时增加ACS患者缺血及出血风险 无禁忌征的情况下,CKD患者应该接受与其他患者相同的一线
急性冠脉综合征(ACS)的抗血小板 双联抗血小板 实用总结全

急性冠脉综合征(ACS)的抗血小板双联抗血小板实用总结急性冠脉综合征(ACS):冠脉不稳定斑块破裂或糜烂继发新鲜血栓致急性缺血综合征,包括:STEMI和非ST段抬高型心肌梗死(NSTEMI)、不稳定性心绞痛(UA),NSTEMI与UA合称NSTE-ACS o基本治疗抗血小板、抗缺血。
无论ACS是否血运重建史,接受长期DAPT(双联抗血小板)是获益的。
-:非血运重建ACS者的DAPT(双联抗血小板)建议:(目前尚缺乏ACS患者P2Y12受体抑制剂单独使用临床证据)1 :接受单纯药物治疗者建议DAPT至少12个月。
2 :既往有心梗病史且存在高缺血风险者,若12个月内耐受DAPT 且无出血并发症,可阿司匹林基础上予替格瑞洛60mgbid延长方案,最长36个月。
3 :处于高出血风险(如PREQSE-DAPT>25分或符合ARC-HBR 标准)者至少1个月DAPT o4 :P2Y12受体抑制剂建议用替格瑞洛而非氯毗格雷,除非出血风险大于潜在缺血获益。
因替格瑞洛疗效优于氯叱格雷且不增加主要出血事件。
对于未计划血运重建且无高出血风险可予P2Y12负荷量预治疗。
(注:ACS为急性冠状动脉综合征;DAPT为双联抗血小板治疗;ARC-HBR为学术研究联合会高出血风险工作组)二:ACS者接受PCI术后DAPT的建议:1:PCI术前均阿司匹林150~300mg负荷剂量联合P2Y12受体抑制剂负荷剂量预治疗:P2Y12受体抑制剂首选替格瑞洛(负荷剂量18Omg,维持剂量90mgbid),当替格瑞洛不可及、无法耐受或有禁忌证时,用氯叱格雷(负荷剂量300〜600mg,维持齐(]量75mgqd)o①替格瑞洛与氯叱格雷相比作用更强、起效更快。
PQ术前服用替格瑞洛后1年的MACE(心血管事件)发生率低于氯叱格雷组且主要出血风险无差异。
院前启用替格瑞洛较院内启用降低术后24h和30d 内支架血栓形成发生率。
在排除主动脉夹层/脑出血后,对低危出血风险者尽早予替格瑞洛预治疗。
ACS患者双联抗血小板和抗凝治疗流程图
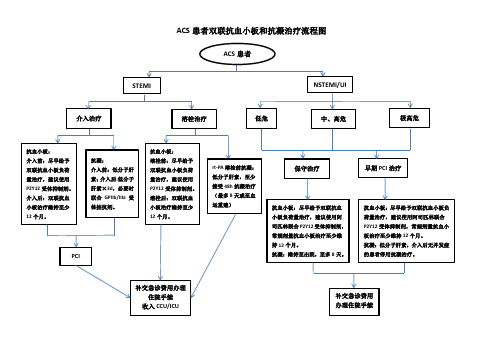
抗血小板: 溶栓前:尽早给予 双联抗血小板负荷 量治疗,建议使用 P2Y12 受体抑制剂。 溶栓后:双联抗血 小板治疗维持至少 12 个月。 rt-PA 溶栓前抗凝: 低分子肝素,至少 接受 48h 抗凝治疗 (最多 8 天或至血 运重建) 抗血小板:尽早给予双联抗血 小板负荷量治疗,建议使用阿 司匹林联合 P2Y12 受体抑制剂, 常规剂量抗血小板治疗至少维 持 12 个月。 抗凝:维持至出院,至多 8 天。 抗血小板:尽早给予双联抗血小板负 荷量治疗,建议使用阿司匹林联合 P2Y12 受体抑制剂,常规剂量抗血小 板治疗至少维持 12 个月。 抗凝:低分子肝素,介入后无并发症 的患者停用抗凝治疗。
ACS 患者双联抗血小板和抗凝治疗流程图
ACS 患者
STEMI
NSTEMI/UI
介入治疗
ห้องสมุดไป่ตู้
溶栓治疗
低危
中、高危
极高危
抗血小板: 介入前:尽早给予 双联抗血小板负荷 量治疗,建议使用 P2Y12 受体抑制剂。 介入后:双联抗血 小板治疗维持至少 12 个月。 抗凝: 介入前:低分子肝 素; 介入后:低分子 肝素×3d,必要时 联合 GPIIb/IIIa 受 体拮抗剂。
保守治疗
早期 PCI 治疗
PCI
补交急诊费用办理 住院手续 收入 CCU/ICU
补交急诊费用 办理住院手续
ACS抗凝治疗
低分子量肝素 (LMWH) 抗Xa:抗IIa 比值
Anti-Xa Anti-IIa Xa /IIa IU/mg 比值 IU/mg 克赛(依诺肝素)1 速碧林(那屈肝素)1 法安明(达肝素)2 Reviparin 1 Tinzaparin 1 Certoparin 1 UFH 3
1. European Pharmacopeia Commission (March 1994) 2. Knoll Pharma 3. Hirsh J, et al. Chest 1998;114:489S-510S 4. Bergqvist D, et al. Br J Surg 1995;82:496-501
NSTEMI
ST 段抬高
UA
NQMI
心肌梗塞
QW MI
FRIC FRAXIS ESSENCE TIMI 11B
ARHT II AMI-SK ASSENT 3 ASSENT 3 -plus ENTIRE-TIMI 23
ExTRACT-TIMI 25
急性冠脉综合征 非 ST 段抬高
NSTEMI
ST 段抬高
小时
2 1.5 1 0.5 0 Enoxaparin Nadroparin Dalteparin
克赛
速碧林
法安明
F. Collignon, A. Frydman, H. Caplain et al. Thromb Haemost 1995; 73 (4): 630-640
三、近年来有关LMWH在急性冠脉综合征的临床试验 非 ST 段抬高
急性冠脉综合征(ACS)的抗凝治疗: 低分子肝素(LMWH)的临床地位
河北医科大学第三医院 李海滨
急性冠脉综合征
非 ST 段抬高
ACS抗栓治疗指南

ACS抗栓治疗指南ACS(急性冠状动脉综合征)是指由于冠状动脉狭窄或阻塞导致的心肌缺血所引起的急性冠心病。
抗栓治疗在ACS的管理中起着至关重要的作用。
本文将介绍ACS抗栓治疗的指南,包括治疗目标、药物选择、使用时机和副作用管理等。
治疗目标:ACS的抗栓治疗的目标是恢复冠状动脉的血流,减少心肌梗死的大小和扩展,并降低再发事件的风险。
药物选择:在ACS的抗栓治疗中,通常会使用抗血小板药物和抗凝药物。
抗血小板药物:常用的抗血小板药物包括阿司匹林、氯吡格雷和普拉格雷等。
阿司匹林是首选的抗血小板药物,在怀疑ACS时即应给予患者咀嚼阿司匹林以降低心肌梗死的风险。
氯吡格雷和普拉格雷是ADP受体拮抗剂,常与阿司匹林联合使用来减少再发事件的风险。
抗凝药物:在ACS的抗凝治疗中,常用的抗凝药物包括低分子肝素和直接凝血酶抑制剂。
低分子肝素通常在ACS的初始治疗中使用,可以用于预防血栓形成。
而直接凝血酶抑制剂适用于STEMI患者,在介入治疗前进行急速对症治疗。
使用时机:ACS的抗栓治疗应尽早开始。
对于STEMI患者,应在发病后尽快实施抗栓治疗,以缩小心肌梗死的范围。
对于非STEMI患者,抗栓治疗应在确诊后的24小时内开始。
副作用管理:在ACS治疗中,抗血小板和抗凝药物可能会引起出血等副作用。
因此,在给予患者抗栓治疗时需要进行严格的剂量管理,以避免出血事件的发生。
对于发生严重出血的患者,可能需要考虑减少药物剂量或暂停治疗。
总的来说,ACS的抗栓治疗是防止心肌梗死和再发事件的关键措施。
在治疗中,应根据患者的情况和临床指南来选择合适的抗血小板药物和抗凝药物,并在尽早开始治疗的同时进行剂量管理和副作用的监测。
抗凝、抗血小板治疗在ACS中的应用

Gp IIb/IIIa 受体
COX 血小板活化
环氧化酶 抑制剂
凝血酶 胶原 5-羟色胺 肾上腺素
抗血小板药物作用机制
氯比格雷/噻氯匹啶
ADP
潘生丁
PGI2
Gs
P2T
ADP
Gi
ADP
P2X1
AC ATP
Ca++
PDE
GP IIb/IIIa 受体
?? Ca cAMP ++ COX Ca++ IP3
PIP2
急性期后患者仍处于不稳定的高危状态
延长抗凝治疗时间的理论基础
ACS患者血液持续处于不稳定的高凝状态
“发生不稳定心绞痛和急性心肌梗死的患者, 急性期治疗后,其血浆中凝血酶原片断1+2和血 纤维蛋白肽A(FPA)浓度依然显著高于稳定性 心绞痛患者及健康个体(P<0.001),这种不 稳定的高凝状态会持续六个月”
低分子肝素的优势
低分子肝素
>1 长 固定 高 无需 低 小
抗 Xa:IIa 活性比值 血浆半衰期 清除速率 生物利用度 aPTT 监测
对 PF4 的敏感性 对血小板抑制作用
普通肝素
=1 短 不固定 低 需要 高 大
Antman 1998
相关疾病抗凝治疗进展
▪ 急性冠脉综合症
▪ UA/NSTEMI ▪ STEMI
梗死后早期的不稳定心绞痛 心肌钙蛋白升高
血液动力学不稳定 主要的心律失常 (VF, VT)
糖尿病 ECG表现排除ST段变化
使用 GPIIb/IIIa拮抗剂
冠脉造影
低危患者的治疗策略
无ECG变化 第二次肌钙蛋白测量: 阴性
停用肝素 口服阿司匹林, 氯吡格雷, Beta受体阻断剂,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
非介入
首剂:1000U 后续:600~1000U/h,监测APTT,维持50-70s 疗程:<48h
LMWH的规范使用
使用简单:不同品种均有标准用法
非介入应用:皮下注射q12h
介入术中应用
术前末次给药<8h,不追加
➢ 普通肝素清除途径:
➢大分子片断有更多的负电荷,主要通过网状内皮系统 清除
➢肾脏清除 ➢ LMWH主要通过肾脏清除 ➢ 肾功能不全时,GFR导致LMWH不易被清除,在体内
产生“蓄积效应”
➢ “蓄积效应”引发LMWH的安全性问题
肾脏受损
LMWH蓄积
出血增加
Wendy Lim, et al. Thrombosis Research 2005
药物选择
LMWH:Reviparin (IA) Fondaparin (IA)
疗程?
指南推荐的抗凝药物有差别吗?
抗凝药物的特点 肝素: APTT 50~70s LMWH: 不需监测,但根据肾功能调整剂量 比伐卢定:出血少,不影响血小板 磺达肝癸钠:出血少,导管内血栓
各种药物的疗效和证据水平有差别
肾功能下降可增加LMWH的出血并发症
没有一个特定的肌酐清除率水平可以判断所有的 低分子肝素会有出血危险性的增加
不同的LMWH有差异:当采用治疗剂量给药时,依 诺肝素和那屈肝素与肌酐清除率呈线性关系,而亭 扎肝素和达肝素与肌酐清除率不呈线性关系
1Hirsh J, et al. Chest. 2004;126:188S-203S.
接受PCI的患者:
有创性治疗:
初始抗凝治疗(Class I,LOE:A) :
依诺肝素或UFH(Class I,LOE:A)
UFH或比伐卢定(Class I,LOE:C)
依诺肝素(Class I,LOE:B)
磺达肝癸钠(Class I,LOE:C)
比伐卢定或磺达肝癸钠 (Class I,LOE:B)
ACCP8: NSTE-ACS
早期介入策略 肝素优于LMWH及磺达肝癸钠
中-高危患者6h内介入:比伐卢定优于肝素
ACCP8: NSTE-ACS
早期保守或延期介入策略
磺达肝癸钠优于LMWH(1A) 如果早期选择磺达肝癸钠,术中追加肝素抗凝 及磺达肝癸钠,后者剂量为:联用2b/3a者 2.5mg,否则5mg(1B)
急性冠状动脉综合征的规范化 抗凝、抗血小板治疗
广州军区广州总医院 向定成
是否所有ACS患者都需要抗凝? 如何抗凝? 抗凝注意防出血 抗血小板问题
是否所有ACS患者需要抗凝? 如何抗凝? 抗凝注意防出血 抗血小板问题
不稳定斑块的破裂和血栓形成是ACS的共同基础
血栓 (thrombus)
初始抗凝治疗(Class I,LOE:A):
依诺肝素或UFH (Class I,LOE:A)
或磺达肝癸钠(Class I,LOE:B)
依诺肝素或磺达肝癸钠更好
溶栓后2~8d内给予辅助抗凝治疗 (Class I,LOE:C) UFH (Class I,LOE:C) 依诺肝素(Class I,LOE:A) 磺达肝癸钠(Class I,LOE:B)
在高龄患者中抗凝剂的给药
依诺肝素
< 75 y : 30 mg 负荷剂量,皮下 1.0 mg/kg q12h ≥ 75 y : 无负荷剂量, 皮下 0.75 mg/kg q12h
CrCl ≤ 30: 1.0 mg/kg q24 h
EXTRACT-TIMI 25:在75 岁以上患者剂量 调整后, 与普通肝素相比, 没有增加出血
服用阿司匹林后发生出血或有出血危险因素的患 者,选择较低剂量阿司匹林(75mg-100mg/天)
不能耐受或禁忌使用阿司匹林的患者,可考虑长 期使用氯吡格雷75mg/d替代
如果因胃肠道出血而应用氯吡格雷替代阿司匹林 时,应同时给质子泵抑制剂
事件发生率 (%)
30天出血终点(TIMI)
5
ARD 0.4% RR 1.15
UFH 依诺肝素
4
ARD 0.8%
RR 1.67
3
P<0.0001
P=0.52
3.3 2.9
ARD 0.1% RR 0.95
2
1.9
1.1
ARD 0.2% RR 1.44 p=0.06
P=0.85 1.7 1.6
1
0.5 0.7
未接受再灌注治疗者?
ACC/AHA. Circulation 2007;116;e148-e304 ACC/AHA. Circulation 2008;117;296-329
STEMI抗凝治疗策略--ACC2007
溶栓治疗者:抗凝至少48h或至出院,不超过8天
UFH:aPTT 50~70s, >48h以上者应改为LMWH LMWH:Enoxaparin Fondaparin:非特异性溶栓药物后
ExTRACT-TIMI 25中对于CrCl ≤ 30 mL/min的 患者调整了依诺肝素的使用剂量以降低出血风险
依诺肝素
< 75 y : 30 mg 负荷剂量,皮下 1.0 mg/kg q12h ≥ 75 y : 无负荷剂量, 皮下 0.75 mg/kg q12h
CrCl ≤ 30: 1.0 mg/kg q24 h
lipid corliepi(d脂c质or核e )
STEMI
NSTEMI
抗凝防栓是治疗所有ACS的必然措施
NSTEMI危险性并不低于STEMI
UA/STEMI短期死亡率可能低于STEMI,但是远期死亡率相似
Euro Heart Survey Programme ESC Quality Assurance Programme to Improve Cardiac Care in Euroe
2007ESC指南强调
1. 出血会增加死亡、心肌梗死和卒中的风险 2. NSTE-ACS的急性期,严重出血发生率与死亡率同
样高 3. 预防出血与预防缺血事件同等重要 ,并且可显著
降低死亡、心肌梗死和卒中的风险 4. 出血的风险分层应当成为决策过程中的一部分
ACS合并肾功能不全患者的抗凝治疗
肾功能不全患者使用LMWH需注意蓄积效应
抗凝不抗凝
NSTE-ACS治疗指南(ESC2007)
NSTE-ACS 患者
ASA /氯吡格雷 /UFH /LMWH/ 硝酸甘油/β阻滞剂
高危
初步计划 介入治疗
低危
初步计划 保守治疗
危险分层之前 开始抗凝治疗
不论将选择介入还是保守策略, 首先必须进行抗凝治疗
计划马上 (<120min) 行血管成形术
3小时以上
3小时内
3小时以上
90分钟不内+不同能的PC再I 灌注策略和手段有不同的抗90分凝钟内要+能求实施PCI
立刻溶栓,随后PCI (除非能立刻PCI)
立刻溶栓? 随后PCI
直接PCI
12小时内
送就近成熟的PCI中心 2b/3a拮抗剂
2007第八版
The ACS spectrum concept, organized around a common pathophysiological substrate, furnishes a useful framework for developing therapeutic strategies. Patients presenting with persistent STsegment elevation are candidates for reperfusion therapy (either pharmacological or catheter based) to restore flow in the occluded epicardial infarct-related artery. ACS patients presenting without ST-segment elevation are not candidates for pharmacological reperfusion but should receive antiischemic therapy,
followed by PCI. All patients with ACS should receive antithrombin therapy and antiplatelet therapy regardless of the presence or absence of STsegment elevation.
阿司匹林治疗建议
NSTEACS所有患者如能耐受,尽早给予阿 司匹林,负荷剂量150–300mg,随后均长期 治疗,维持剂量为75–100 mg
ACS患者拟行CABG术前不建议停药 STEMI患者无论是否接受纤溶治疗,初诊时
阿司匹林150-300mg嚼服,随后长期治疗, 每天75-150mg
阿司匹林治疗建议
结果: 出血发生率低于以往研究的发生率 颅内出血与普通肝素相比无差异
Antman EM, et al. N Engl J Med. 2006;354: 1477-88
肾功能与抗凝监测
个体化地平衡抗凝与出血 eGFR: >90 正常 60-90 适当减量 30-60 减量+监测 <30 严密监测
8~12h,追加0.3mg/kg >12h,常规剂量
特殊情况减量:
依诺肝素
< 75 y : 30 mg 负荷剂量,皮下 1.0 mg/kg q12h
≥ 75 y : 无负荷剂量,皮下 0.75 mg/kg q12h CrCl ≤ 30: 1.0 mg/kg q24 h
磺达肝癸钠的规范应用
