钠氯气方程式练习答案
高一化学必修一 化学方程式汇总练习和答案

必修1 化学方程式一、钠及其重要化合物1、钠与非金属的反应1钠与氧气常温2钠与氧气加热3钠与氯气2、钠与水反应:3、氧化钠和过氧化钠6、Na2CO3和NaHCO3①、与酸的反应Na2CO3+ HCl=NaHCO3+ HCl= 反应速率更快②、与碱的反应Na2CO3+ CaOH2=NaHCO3+ CaOH2=NaHCO3+ NaOH =③、与盐的反应Na2CO3+ CaCl2=Na2CO3+ BaCl2=④、相互转化NaHCO3加热分解向Na2CO3溶液中通入足量的CO2:二、铝及其重要化合物结合Al2O3和AlOH3的两性进行记忆1、铝与氧气:2、铝与弱氧化性酸HCl:铝与强氧化性酸:浓H2SO4、浓HNO33、铝与碱NaOH:4 ①、氧化铝与酸反应HCl:②、氧化铝与碱反应NaOH:5、氢氧化铝制备:可溶性铝盐和NH3·H2O6、氢氧化铝的不稳定性加热:7、氢氧化铝与酸反应HCl:8、氢氧化铝与碱反应NaOH:9、“铝三角”氢氧化铝的反应在上面已经提到,略:AlCl3+ NaOH少量=AlCl3+ NaOH过量=NaAlO2+ HCl少量=NaAlO2+ HCl过量=10、明矾净水原理明矾溶于水后发生电离:铝离子与水反应生成胶体:三、铁及其重要化合物1、工业炼铁原理:2、铁与氯气和氧气反应点燃:,3、与水反应高温:4、铁与HCl反应:5、铁与CuSO4溶液反应:铁与FeCl3溶液反应:6、铁的氧化物与酸反应的离子式Fe2O3 FeO7、Fe2+与Fe3+的检验①、Fe2+的检验:1 颜色:浅绿色 2加NaOH溶液:先产生白色沉淀,后变成灰绿色,最后成红褐色,3 先加KSCN溶液,不变色,再加新制氯水,溶液变成血红色离子式②、Fe3+的检验1颜色:棕黄色2加KSCN溶液:溶液变成血红色3加NaOH溶液:红褐色沉淀离子式8、氢氧化铁受热分解:9、 Fe2+与Fe3+的转化1Fe2+→Fe3+2 Fe3+→Fe2+四、硅及其重要化合物1、二氧化硅①酸性氧化物:二氧化硅和火碱:二氧化硅和生石灰:②弱氧化性:二氧化硅和氢氟酸2、硅酸盐 Na2SiO3+ HCl==Na2SiO3+ CO2+ H2O==酸性:H2CO3 H2SiO3大于\小于五、氯的重要化合物1、氯气与金属的反应铁\铜\钠,2、氯气与非金属的反应氢气3、氯气与水的反应4、次氯酸光照分解:5、Cl2与碱溶液的反应火碱酸性:H2CO3 HClO大于\小于制漂白粉漂白原理六、硫及其重要化合物1、硫的可燃性在空气中点燃2、 SO2 + O2催化剂加热3、与水反应: SO2+H2OSO3+H2O==4、与碱反应: SO2 + CaOH2=SO3 + CaOH2=5、与碱性氧化物反应:SO2+CaO ==SO3+CaO ==6、浓硫酸强氧化性C + H2SO4浓Cu+H2SO4浓七、氮及其重要化合物1、合成氨:2、NHNH3 + H2O②氨气与酸:NH3+HCl=NH3+HNO3=3、铵盐与碱反应:硝酸铵和火碱实验室制氨气4、铵盐不稳定性:氯化铵加热碳酸氢铵加热5、HNO3强氧化性:浓硝酸和铜稀硝酸和铜6、雷雨发庄稼123必修1 化学方程式汇总一、钠及其重要化合物1、钠与非金属的反应4Na +O2=2Na2O 白色 2Na + O2 △ Na2O2淡黄色2Na +Cl2点燃2NaCl2、钠与水反应:2Na + 2H2O = 2NaOH + H2↑ 浮、熔、游、响、红3、氧化钠过氧化钠Na2O+H2O=2NaOH 2Na2O2+2H2O=4NaOH+O2↑Na2O+CO2=Na2CO3 2Na2O2+2CO2=2Na2CO3+O2↑Na2O+2HCl=2NaCl+H2O 2Na2O2+4HCl=4NaCl+2H2O+O2↑6、Na2CO3和NaHCO3①、与酸的反应 Na2CO3+2HCl=2NaCl+H2O+CO2↑NaHCO3+HCl=NaCl+H 2O+CO2↑反应速率更快②、与碱的反应Na2CO3+CaOH2=CaCO3↓+2NaOH2NaHCO3+CaOH2=CaCO3↓+Na2CO3+2H2ONaHCO3+NaOH = Na2CO3+H2O③、与盐的反应Na2CO3+CaCl2=2NaCl+CaCO3↓ Na2CO3+BaCl2=2NaCl+BaCO3↓④、相互转化2NaHCO3△ Na2CO3+H2O+CO2↑加热分解Na2CO3+H2O+CO2=2NaHCO3 向Na2CO3溶液中通入足量的CO2二、铝及其重要化合物结合Al2O3和AlOH3的两性进行记忆1、铝与非金属: 4Al + 3O2 ==2Al2O32、铝与弱氧化性酸:2Al + 6HCl == 2AlCl3+ 3H2↑ 2Al+6H+== 2Al3++3H2↑铝与强氧化性酸:钝化浓H2SO4、浓HNO33、铝与碱:2Al+2NaOH +2H2O==2NaAlO2 + 3H2↑ ; 2Al+2H2O+2OH-==2AlO2-+3H2↑4 ①、氧化铝与酸反应:Al2O3 + 6HCl == 2AlCl3 + 3H2O②、氧化铝与碱反应:Al2O3 +2NaOH == 2NaAlO2 + 2H2O5、氢氧化铝制备:可溶性铝盐和NH3·H2OAlCl3+3NH3·H2O==AlOH3↓+3NH4Cl Al3++3NH3·H2O==AlOH3↓+3NH4+6、氢氧化铝的不稳定性: 2AlOH3△ Al2O3+2H2O7、氢氧化铝与酸反应:AlOH3 + 3HCl == AlCl3 + 3H2O8、氢氧化铝与碱反应:AlOH3 +NaOH == NaAlO2 + 2H2O9、“铝三角”氢氧化铝的反应在上面已经提到,略:AlCl3+3NaOH少量=AlOH3↓+3NaCl Al3++3OH-=AlOH3↓+AlCl3+4NaOH过量=2NaAlO2 + 2H2O +3NaCl Al3++4OH- = AlO2- +2H2O NaAlO2+HCl少量+H2O=AlOH3↓+NaCl AlO2- +H+ +H2O=AlOH3↓NaAlO2+4HCl过量=AlCl3+3NaCl+2H2O AlO2- +4H+ =Al 3+ + 2H2O10、明矾净水原理明矾溶于水后发生电离:KAlSO42==K++Al3++2SO42-铝离子与水反应生成:AlOH3胶体:Al3++3H2O==AlOH3胶体+3H+三、铁及其重要化合物1、工业炼铁原理:Fe2O3+3CO高温2Fe+3CO22、铁与非金属反应:2Fe+3Cl2点燃 2FeCl3 3Fe+2O2点燃Fe3O43、与水反应:3Fe+4H2Og高温Fe3O4+4H24、铁与酸反应:Fe+2HCl== FeCl2+H2↑ Fe+2H+== Fe2++H2↑5、铁与盐溶液反应:Fe+CuSO4==Cu+FeSO4 Fe+Cu2+==Cu+Fe2+Fe+2FeCl3 == 3FeCl2 Fe+2Fe3+ == 3Fe2+ 6、铁的氧化物Fe2O3 + 6H+ == 2Fe3+ + 3H2O FeO + 2H+ == Fe2+ + H2O7、Fe2+与Fe3+的检验①、Fe2+的检验:1 颜色:浅绿色 2加NaOH溶液:先产生白色沉淀,后变成灰绿色,最后成红褐色Fe2++2OH-== FeOH2↓ 白色 4FeOH2+O2+2H2O== 4FeOH3红褐色3 先加KSCN溶液,不变色,再加新制氯水,溶液变成血红色2Fe2++Cl2==2Fe3++2Cl-②、Fe3+的检验1颜色:棕黄色2加KSCN溶液:溶液变成血红色3加NaOH溶液:红褐色沉淀 Fe3++3OH-== FeOH3↓8、氢氧化铁受热分解:2FeOH3△ Fe2O3 + 3H2O9、 Fe2+与Fe3+的转化 1Fe2+→Fe3+ 2Fe2++Cl2==2 Fe3++2Cl-2 Fe3+→Fe2+ Fe+2Fe3+ == 3Fe2+四、硅及其重要化合物2、二氧化硅①酸性氧化物:SiO2+2NaOH==Na2SiO3+H2O SiO2+CaO高温CaSiO3②弱氧化性: SiO2 +4HF==SiF4↑+2H2O2、硅酸盐 Na2SiO3+2HCl==H2SiO3↓+2NaClNa2SiO3+ CO2+H2O==H2SiO3 ↓+Na2CO3酸性:H2CO3 > H2SiO3五、氯的重要化合物1、氯气与金属的反应2Fe+3Cl点燃2FeCl3 Cu+Cl点燃CuCl2 2Na+Cl点燃2NaCl2、氯气与非金属的反应 H2+Cl2 点燃2HCl3、氯气与水的反应 Cl2+H2O== HCl + HClO 次氯酸4、次氯酸光照分解:2HClO 光照 2HCl + O2↑5、Cl2与碱溶液的反应Cl2+2NaOH=NaCl+NaO+H2O2Cl2+2CaOH2=CaCl2+CaClO2+2H2O制漂白粉CaClO2+CO2+H2O=CaCO3↓+2HClO漂白原理酸性:H2CO3 > HClO六、硫及其重要化合物1、硫的可燃性 S+O2点燃SO22SO32、 2SO2 + O2催化剂加热3、与水反应: SO2+H2O2SO3 SO3+H2O== H2SO44、与碱反应SO2 + CaOH2= CaSO3 + H2O SO3 + CaOH2= CaSO4 + H2O5、与碱性氧化物反应:SO2+CaO == CaSO3 SO3+CaO == CaSO46、浓硫酸强氧化性 C + 2H2SO4浓△ CO2↑+ 2SO2↑+ 2H2OCu+2H2SO4浓△ CuSO4+SO2↑十2H2O七、氮及其重要化合物2NH31、合成氨:N2 + 3H2催化剂高温高压2、NH3①氨气与水:NH3 + H2O NH3·H2O NH4+ + OH -②氨气与酸:NH3+HCl=NH4Cl NH3+HNO3=NH4NO33、铵盐与碱反应: NH4NO3+NaOH △ NaNO3+NH3↑+H2O2NH4Cl + CaOH2△ CaCl2 + 2NH3↑+ 2H2O实验室制氨气4、铵盐不稳定性:NH4Cl△ NH3↑+HCl ↑NH4HCO3△ NH3+H2O+CO2↑5、HNO3强氧化性:4HNO3浓+Cu==CuNO33+3NO2↑+2H2O 8HNO3+3Cu==3CuNO33+2NO↑+4H2O6、雷雨发庄稼 N2 + O2放电 2NO2NO + O2 == 2NO2 3NO2 + H2O == 2HNO3 + NO。
人教版初中高中化学必修一第二章《海水中的重要元素—钠和氯》阶段练习(含答案解析)

一、填空题1.探究钠及其化合物的性质,请按要求填空:(1)Na 、Na 2O 、Na 2O 2、NaOH 久置空气中最终都是变为_______(填化学式);(2)Na 投入MgCl 2溶液中发生反应的总化学方程式_______。
(写一个方程式)(3)向足量的蒸馏水中加入一定量Na 2O 2粉末,该反应的离子方程式为_______。
2.氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a 、b 、c 、d 、e 中重合部分代表物质间反应,且氯水足量)。
()1氯水中含有的粒子有2H O 、2Cl 、___________、H+、Cl -、___________、OH -七种。
()2久置的氯水变为___________,原因是___________(用化学反应方程式表示);实验室保存饱和氯水的方法是___________。
()3b 过程中的离子方程式是___________。
()4e 过程中所发生的主要反应的化学方程式为___________。
()5能证明氯水具有漂白性的是___________填“a”、“b”、“c”或“d”)。
3.新型冠状病毒蔓延期间,为做好自我保护,我们要减少外出,避免与表现出有呼吸道疾病症状的人密切接触,外出最重要的防护措施是佩戴符合要求的口罩。
在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。
也可以在实验室进行制备84消毒液(有效成分是NaClO )。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的___________(“溶液”、“胶体”、“悬浊液”)。
(2)佩戴口罩预防疾病的原理相当于化学实验中的_________操作。
(“蒸发”、“过滤”“萃取”)(3)生成N95口罩的主要原料是聚丙烯,它属于___________(填“金属材料”或“合成材料”)(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:__________________________,氧化剂是_________,氧化产物是_________。
云阳中学高中化学必修一第二章《海水中的重要元素—钠和氯》阶段练习(含答案)

一、填空题1.同温同压下,容器A中充满CO2气体,容器B中充满N2,若V(A):V(B)=3:2,则两容器中的气体密度比为________。
2.(1)在标准状况下,4g H2、11.2L O2、1mol H2O中,含原子数最多的是____,体积最小的是______。
(2)实验室常用的浓盐酸密度为1.19g/mL、质量分数为36.5%。
此浓盐酸的物质的量浓度NO 的为_______________mol·L-1;若20 g 密度为 d g/mL 的硝酸钙溶液里含 1g Ca2+,则3浓度为_________mol·L-1(3)容量瓶上除标有规格外,还有_______、___________。
(4)在标准状况下①4.48L CH4②6.02×1022个HCl分子③10.2g H2S ④0.15mol NH3。
下列对这四种气体的关系从大到小的关系是(用序号填空):a.体积:___________ b.密度:_________ c.质量:____________ d.氢原子个数:_________(5)18g水中溶解________g的NaOH才能使100个水分子中溶有1个Na+离子。
(6)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是________,混合气体的平均相对分子质量是________。
3.实验室用高锰酸钾和浓盐酸反应制备氯气:2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O(1)用双线桥法标出上述反应方程式中电子转移的方向与数目___。
(2)上述反应中,氧化剂是___ (填化学式,下同),氧化产物___,浓盐酸体现了___性和____性,当有4mol水生成的时候,转移的电子有___mol。
(3)实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是___(填写化学式),请用化学方程式表示该反应的原理___。
成都市实验外国语学校(西区)高中化学必修一第二章《海水中的重要元素—钠和氯》经典练习题(答案解析)

一、填空题1.在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。
进行此实验,所用仪器如图所示。
(1)装置中,饱和食盐水的作用是___________;浓硫酸的作用是___________。
(2)化学实验中常用湿润的KI-淀粉试纸检验是否有Cl2产生。
如果有Cl2产生,可观察到___________,反应的化学方程式为___________。
(3)写出下列反应的化学方程式:①气体发生装置中进行的反应:___________。
②NaOH溶液中发生的反应:___________。
2.实验室中的氢氢化钠溶液在空气中放置,因密封不好会变质,有关反应的离子方程式为____;为了检测一瓶氢氧化钠溶液是否已变质,可取少量该溶液向其中加入____,若有_____现象发生,则说明烧碱溶液已经变质。
3.“84消毒液”能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示。
回答下列问题:84消毒液(有效成分) NaClO(规格) 500 mL(质量分数) 14.9%(密度) 1.1g·cm-3______,写出其在水中的电离方程式____。
(2)社团成员为探究“84消毒液”有效成分的部分化学性质,利用稀释的84消毒液进行如下实验:向淀粉KI溶液中滴加少量消毒液,无色溶液变蓝,说明NaClO具有_____性(填“氧化”或“还原”),其中每1molNaClO参加反应,转移的电子数为_______。
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18mol·L-1浓硫酸配制100mL0.9mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需用量筒量取浓硫酸的体积为_______mL;②若所配制的稀硫酸浓度偏高,则下列可能的原因分析中正确的是______。
A.配制前,容量瓶中有少量蒸馏水B.量取浓硫酸时,俯视液体的凹液面C.未冷却,立即转移至容量瓶定容D.定容时,仰视溶液的凹液面4.(1)以下为中学化学常见的几种物质①NaOH溶液②铜丝③液氯④盐酸⑤稀硫酸⑥氨水⑦CO2⑧熔融NaCl⑨蔗糖晶体⑩酒精。
高中化学必修二 第二章 钠及氯的化学方程式

高中化学无机反应★1、钠露置于空气中生成白色固体:4Na+O2= 2Na2O★2、钠在空气中燃烧(黄色的火焰):2Na+O2Na2O2(淡黄色固体)★3、钠在氯气中燃烧(白烟现象):2Na+Cl22NaCl★4、铜丝在氯气中剧烈燃烧(棕黄色的烟):Cu+Cl2CuCl2★5、铁在氯气中剧烈燃烧(棕褐色的烟):2Fe + 3Cl22FeCl36、铁在氧气中剧烈燃烧(火星四射,放出大量的热):3Fe +2O2点燃Fe3O4点燃2HCl★7、氢气在氯气中燃烧(苍白色火焰,瓶口有白雾):H2 + Cl2★8、钠与水反应(浮、熔、游、响、红):2Na + 2H2O =2NaOH + H2↑2Na + 2H2O = 2Na+ + 2OH - +H2 ↑9、氧化钠与氧气反应:2Na2O+ O2△2Na2O210、氧化钠与稀盐酸反应:Na2O+2HCl= 2NaCl + H2O(Na2O+2H+=2Na++ H2O)★11、钠与硫酸铜aq反应:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑2Na+2H2O+Cu2+=Cu(OH)2↓+2Na++H2↑9、钠与氯化铁溶液反应:6Na+6H2O+2FeCl3=2Fe(OH)3↓+6NaCl+3H2↑6Na+6H2O+2Fe3+=Fe(OH)3↓+6Na++3H2↑★12、过氧化钠与水的反应(放热反应、Na2O2是强氧化剂,用于漂白。
)2Na2O2 + 2H2O = 4NaOH + O2↑2Na2O2 + 2H2O = 4Na+ + 4OH - +O2↑(Na2O2既是氧化剂又是还原剂)13、氧化钙与水的反应:CaO + H2O = Ca(OH)2★14、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源,原因是:2Na2O2 + 2CO2 = 2Na2CO3 + O2 (Na2O2既是氧化剂又是还原剂)15、过氧化钠与稀盐酸的反应:2Na2O2 +4HCl= 4NaCl + 2H2O + O2↑2Na2O2 +4H+= 4Na+ + 2H2O + O2↑★16、苏打(纯碱)与盐酸反应:①盐酸中滴加纯碱溶液(有气泡):Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑CO32- + 2H+ = H2O + CO2↑②纯碱溶液中滴加少量盐酸(无气泡):Na2CO3 + HCl = NaHCO3 + NaCl CO32- + H+ = HCO3-★17、小苏打受热分解:2NaHCO3△Na2CO3 + H2O +CO2 ↑18、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热NaHCO3 + NaOH △Na2CO3 + H2O(若是溶液中反应有离子方程式):HCO3-+ OH - = H2O + CO32-★19、小苏打(碳酸氢钠)与盐酸反应:NaHCO3+ HCl=NaCl + H2O + CO2↑HCO3-+H+=H2O+CO2 ↑★20、饱和碳酸钠溶液通入CO2气体(晶体析出):Na2CO3+H2O+CO2=2NaHCO3↓★21、少量NaHCO3和Ca(OH)2的反应:NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOHHCO3-+OH-+Ca2+=CaCO3↓+H2O★22、足量NaHCO3和Ca(OH)2的反应:2NaHCO3+Ca(OH)2=CaCO3↓+2H2O+Na2CO32HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32-★23、氯气溶于水(新制氯水中含H+、Cl -、ClO -、OH-(少量)、Cl2、HClO、H2O):Cl2 + H2O = HCl + HClO Cl2 + H2O = H+ + Cl - + HClO★24、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂)2HClO2HCl + O2↑★25、氯气尾气的吸收原理:Cl2+2NaOH NaCl+NaClO+H2OCl 2+2OH-Cl-+ClO-+H2O★26、工业制漂白粉的原理(石灰乳与氯气反应)及漂白粉的失效:2Ca(OH)2 + 2Cl2 =Ca(ClO)2 + CaCl2 + 2H2O 2Ca(OH)2 + 2Cl2=2Ca2++2ClO- + 2Cl -+ 2H2O Ca(ClO)2 + CO2 + H2O=CaCO3↓+ 2HClO 2HClO2HCl + O2↑(此反应若在溶液中进行时有离子反应方程式):Ca2++2ClO- + CO2 + H2O=CaCO3↓+ 2HClO★27、氯气的实验室制法(仪器:分液漏斗,圆底烧瓶):MnO2 + 4HCl(浓) MnCl2 +Cl2↑+ 2H2OMnO2 + 4H+ +2Cl-Mn2+ + Cl2↑+ 2H2O★28、氯气通常用湿润的淀粉KI试纸检测:Cl2+ 2I-= I2+2Cl-29、溴水能使湿润的淀粉KI溶液变蓝:Br2+ 2I-= I2+2Br-(单质碘遇淀粉溶液变蓝色)★30、氯酸钾与浓盐酸反应:KClO3+6HCl(浓)=KCl+ 3Cl2↑+3H2O (ClO3-+6H++5Cl-=3Cl2↑+3H2O) ★31、高锰酸钾溶液与浓盐酸反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2 +5Cl2↑+8H2O2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O32、次氯酸钙溶液与浓盐酸反应:Ca(ClO)2 +4HCl(浓)=CaCl2+2Cl2↑+2H2O2ClO-+4H++2Cl-=2Cl2↑+2H2O33、酸性高锰酸钾溶液中加入双氧水:2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O。
人教版初中高中化学必修一第二章《海水中的重要元素—钠和氯》复习题(含答案解析)
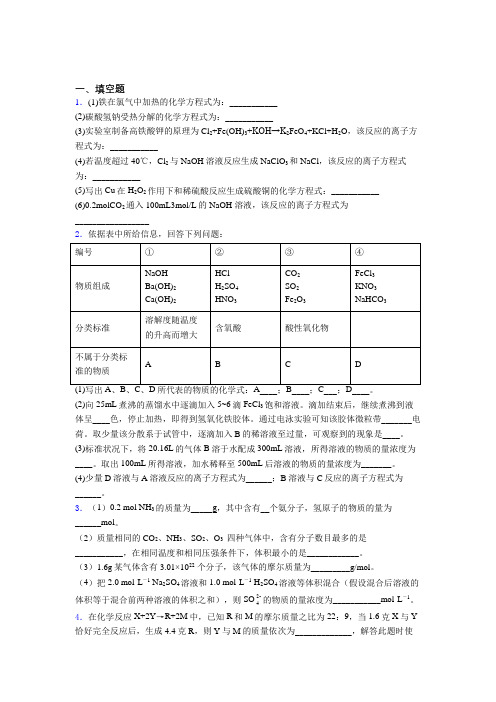
一、填空题1.(1)铁在氯气中加热的化学方程式为:___________(2)碳酸氢钠受热分解的化学方程式为:___________(3)实验室制备高铁酸钾的原理为 Cl2+Fe(OH)3+KOH→K2FeO4+KCl+H2O,该反应的离子方程式为:___________(4)若温度超过40℃,Cl2与NaOH 溶液反应生成NaClO3和NaCl,该反应的离子方程式为:___________(5)写出Cu在H2O2作用下和稀硫酸反应生成硫酸铜的化学方程式:___________(6)0.2molCO2通入100mL3mol/L的NaOH 溶液,该反应的离子方程式为_________________2.依据表中所给信息,回答下列问题:(2)向25mL煮沸的蒸馏水中逐滴加入5~6滴FeCl3饱和溶液。
滴加结束后,继续煮沸到液体呈____色,停止加热,即得到氢氧化铁胶体。
通过电泳实验可知该胶体微粒带_______电荷。
取少量该分散系于试管中,逐滴加入B的稀溶液至过量,可观察到的现象是____。
(3)标准状况下,将20.16L的气体B溶于水配成300mL溶液,所得溶液的物质的量浓度为____。
取出100mL所得溶液,加水稀释至500mL后溶液的物质的量浓度为_______。
(4)少量D溶液与A溶液反应的离子方程式为______;B溶液与C反应的离子方程式为______。
3.(1)0.2 mol NH3的质量为_____g,其中含有__个氨分子,氢原子的物质的量为______mol。
(2)质量相同的 CO2、NH3、SO2、O3 四种气体中,含有分子数目最多的是___________,在相同温度和相同压强条件下,体积最小的是____________。
(3)1.6g某气体含有 3.01×1022个分子,该气体的摩尔质量为_________g/mol。
(4)把2.0 mol·L-1 Na2SO4溶液和1.0 mol·L-1 H2SO4 溶液等体积混合(假设混合后溶液的的物质的量浓度为___________mol·L-1。
必修一钠氯气n简单练习题
必修一第一章练习题可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5一、选择题 (每小题只有一个或两个选项符合题意)1.氢气和氯气的混合气体遇强光照射时,会发生爆炸现象,并在瓶口形成( B )A .白烟B .白雾C .白色烟雾D .棕色烟2.下列关于钠的说法正确的是( C )A .金属钠与氧气反应,条件不同,产物相同B .金属钠着火可用水扑灭C .少量的钠可保存在煤油中D .钠的化学性质活泼,可从CuSO 4溶液中置换出Cu3.下列物质中,与氯气、盐酸都能发生反应且生成不同氯化物的是( A )A .FeB .AlC .CuD .Zn4.下列各组中的两种物质作用时,反应条件改变, 不会引起产物种类变化的是 ( C )A .Na 和O 2B .Ca(OH)2和CO 2C .Fe 和HClD .C 和O 2 5.下列说法错误的是( D )A .氯气是黄绿色的,氯离子是无色的B .氢气在氯气中燃烧时发出苍白色火焰C .氯气有毒,新制的氯水有漂白性,而氯离子既无毒也无漂白性D .氢气和氯气的混合气体只有在强光照射下才能迅速化合生成氯化氢6.检验HCl 气体中是否混有少量Cl 2可采用的方法是 ( D )A .凭气味和颜色B .通入AgNO 3溶液C .干燥的蓝色石蕊试纸,观察其颜色变化D .紫色石蕊试液7. 下列有关氯气的说法正确的是 ( B )A .氯气是黄绿色气体,有毒,有刺激性气味,不能溶于水。
B .将氯气持续通入紫色石蕊试液中,现象是石蕊试液先变红后褪色。
C .红热的铜丝在Cl 2 中燃烧产生棕黄色的雾;H 2 在Cl 2 中燃烧,火焰呈淡蓝色D .氯水长时间放置不会变质,还可消毒杀菌8.下列叙述中正确的是( C )A 、H 2SO 4的摩尔质量是98 gB 、2mol NO 和2mol NO 2含原子数相同C 、等质量的O 2和O 3中所含氧原子个数相同D 、等质量的CO 和CO 2中所含碳原子数相等9.下列说法错误的是 ( D )A 、1mol Na + 中含有N A 个钠离子B 、1mol H 2O 中含有6.02×1023个水分子C 、 1mol 氢中含有N A 个氢原子D 、 1mol H 2O 中含有1molH 2和 1mol O10.下列物质中分子数最多的是( A )A.标准状况下22.4L SO2 B.3.01×1023个N2分子C.0.75mol H2SO4 D.4g NaOH11.设N A代表阿伏加德罗常数,下列说法中正确的是(B)A.2.3 g金属钠所含钠原子数目为0.2N A B.2 g氢气所含原子数目为2N AC.17 g NH3所含的分子数为2N A D.N A个O2和N A个H2的所含原子数目比等于16∶1 12.下列各物质所含原子数由大到小顺序排列的是(D)①0.5 mol NH3②4 g H2③4℃时9 mL H2O ④0.2 mol H3PO4A.①④③②B.④③②①C.②③④①D.②①④③13.等物质的量的钠、镁、铁与足量稀盐酸反应生成的氢气的物质的量之比是( D )A.1:1:1 B.1:2:3 C.3:2:1 D.1:2:214.用N A表示阿伏加德罗常数的值,下列叙述正确的是( B )A.含有N A个氦原子的氦气在标准状况下的体积约为11.2LB.25℃,1.01×105Pa,64gSO2中含有的原子数为3N AC.在常温常压下,11.2L Cl2含有的分子数为0.5N AD.标准状况下,11.2LH2O含有的分子数为0.5N A15.等物质的量的氢气和氦气在同温同压下具有相等的(BC )A.原子数B.体积C.质子数D.质量16.相同状况下,下列气体所占体积最大的是(D )A.80g SO3B.16g O2C.32g H2S D.3g H217.下列说法不正确的是( B )A.标准状况下,气体摩尔体积约是22.4L/molB.非标准状况下,1mol任何气体的体积不可能为22.4LC.标准状况下22.4L任何气体都含有约6.02×1023个分子D.1mol H2和O2的混合气体在标准状况下的体积约为22.4L18.同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是( D )A.密度比为16:11 B.密度比为11:16 C.体积比为1:1 D.体积比为11:16 19下列物质里含氢原子数最多的是( C )A.1 mol H2B.0.5molNH3C.6.02×1023个的CH4分子 D.29.4gH3PO4二、填空题21.现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。
高一钠和氯气综合练习
高一钠和氯气综合练习相对原子质量:H:1 O:16 Na:23 Mg:24 Al:27 Cl:35.5 Cu:64 Fe:56一、选择题(本题包括10小题,每小题3分,共30分。
每小题只有一个选项符合题意)1.钠在自然界存在的主要形式是()A.单质B.氯化钠C.氢氧化物D.氧化物2.下列是有关钠的物理性质的叙述:①银白色金属②质软,可用小刀切割③熔点低于100℃;④密度比水小;⑤热和电的良导体,其中正确的是()A.①②④B.①②③④ C.①③④D.①②③④⑤3.取一小块金属钠,放在燃烧匙里加热,下列实验现象中,正确的描述是()①钠先熔化②在空气中燃烧,放出黄色火花③燃烧后得到白色固体④燃烧时火焰为黄色⑤燃烧后生成淡黄色固体物质A.①②B.①②③C.①④⑤D.④⑤4.钠与水反应时产生的各种现象如下:①钠浮在水面上;②钠沉在水底;③钠熔化成小球;④小球迅速游动逐渐减小,最后消失;⑤发出嘶嘶的声音;⑥滴入酚酞后溶液显红色。
其中正确的一组是()A.①③④⑤⑥B.①②③④⑤C.①②③⑤⑥D.全部5.钠与水反应时现象与钠的下列性质无关的是()A.钠的熔点低B.钠的密度小C.钠的硬度小 D.钠有强还原性6.钠与水反应的离子方程式正确的是()A.2Na+2H+=2Na++H2↑ B.Na+H2O=Na++OH-+H2↑C.2Na+2H2O=2Na++O2↑+H2↑ D.2Na+2H2O=2Na++2OH-+H2↑溶液中, 观察到的现象是()7.将一小块钠投入FeCl3A.溶液中有铁析出B.只有气体产生C.只有红褐色沉淀生成D.有气体放出并有红褐色沉淀产生8.在50mL烧杯中加入10mL煤油和10mL水(分层),再将一小块钠投入烧杯。
下列关于钠的位置及反应情况,判断正确的是()A.钠浮在煤油层上,不反应B.钠沉在煤油层下,不反应C.钠沉在煤油层下浮在水层上,在交界处剧烈反应D.钠沉在水层下剧烈反应9.将4.6克金属钠投入足量水中,得到a克溶液,将4.8克镁投入到足量盐酸中(与水等质量),得到b克溶液,则反应后两溶液质量关系是()A.a=b B.a>b C.a<b D.无法判断10.相同质量的Na、Mg、Al分别与足量稀盐酸充分反应,生成H2的质量之比为()A.1︰2︰3 B.23︰24︰27C.23︰12︰9 D.36︰69︰9211.关于钠的用途叙述不正确的是()A.工业上可用于生产纯碱和大量制备氢氧化钠B .钠是一种强还原剂,可以把钛、锆、铌、钽从其盐溶液中置换出来C .钠和钾的合金常温下为液体,可作原子反应堆的导热剂D .用来制取过氧化钠等化合物12.向含有下列离子的溶液中,加入一小块金属钠,引起离子数目减少的是( ) A .OH - B .HCO 3- C .Mg 2+ D .CO 32-13.将钠投入下列溶液中,产生气体并生成白色沉淀的是( ) A .Ca(OH)2饱和溶液 B .MgSO 4溶液C .KCl 溶液D .CuSO 4溶液14.将a g 钠投入b g 水中(足量水),反应后所得溶液中溶质的质量分数是( ) A .%100⨯+b a a B .%10040⨯+b a a C .%10020⨯+b a a D .%100232240⨯+ba a 15.一块表面已被氧化为氧化钠的钠块5.4g ,投入50g 水中,最多能产生0.10g 气体,则原来被氧化的钠是 ( )A .2.3gB .3.1gC .4.6gD .5.3g16.下列氯化物中,既能由金属和氯气反应制得,又能由金属和盐酸反应制得的是( )A. CuCl 2B. FeCl 3C. FeCl 2D. AlCl 317. 下列关于燃烧的叙述一定正确的是( )A 所有的氧化还原反应都属于燃烧B. 燃烧一定要有氧气参加C 燃烧一定要点燃或加热 D. 燃烧属于氧化还原反应18.下列物质中含有Cl -的是: ( )A. 液氯B.KClO 3溶液C. HCl 气体D. NaCl 晶体19. 下列各组物质在一定条件下反应,其中生成+3价铁盐的是( )A 铁和稀硫酸B 铁和氯化铜溶液 C.铁和氯气 D.铁和氧气20. 以下物质中,含有氯分子的是( )A.液氯B.氯水C.盐酸D.食盐21. 将H 2点燃后插入氯气集气瓶中,产生的现象是( )A.爆炸B.安静燃烧C.瓶内充满棕色烟D.火焰立刻熄灭22. 下列有关实验现象的叙述错误的是( )A .氢气在氯气中燃烧,发出苍白色火焰B .红磷在氯气中燃烧,产生白色的烟雾C .铜丝在氯气中燃烧,产生棕黄色烟雾D .钠在氯气中燃烧,产生白烟23 对氯气的性质描述不正确的是( )① 钠在氯气中剧烈燃烧时产生白烟 ② 氢气在氯气中燃烧发出苍白色的火焰③ 红热的铜丝在氯气中燃烧产生棕色的雾 ④ 氯气与水反应生成盐酸和氯酸⑤ 氯气与碱反应生成次氯酸盐和金属氯化物A. ①②B. ②④⑤C. ③④D. ①②④24.氯气可以用来消灭田鼠,使用方法是将氯气通过软管灌入田鼠洞中,这是利用了氯气以下性质中的()①黄绿色②密度比空气大③有毒④较易液化⑤能溶解于水A.①②③B.②③C.③④D.③④⑤25.市场上销售的“84”消毒液,其商品标识上注明;①本品为无色液体呈碱性;②使用时应加水稀释;③可对餐具、衣物进行消毒,可漂白浅色衣物。
江阴市敔山湾实验学校(初中)高中化学必修一第二章《海水中的重要元素—钠和氯》基础练习(含答案)
一、填空题1.按要求填空:(1)写出钠与水反应的离子方程式:___________。
(2)过氧化钠的颜色为:___________,其阳离子和阴离子的个数比为___________,写出过氧化钠与水反应的化学方程式:___________。
(3)写出氯的原子结构示意图:___________,写出工业制漂白粉的化学方程式:___________。
(4)向碳酸氢钠溶液中滴加少量的氢氧化钙,写出反应的离子方程式:___________。
2.化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,名不符实的一种物质是________(填化学式);(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时):__________,_______;(3)向一定量的Ba(HCO3)2溶液中,逐滴加入NaHSO4溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为:________,沉淀完全后,继续滴加NaHSO4溶液,此时发生反应的化学方程式为:_______。
(4)烧碱、纯碱溶液均可吸收CO2。
向含有7.2 gNaOH的溶液中通入CO2,当通入的CO2与溶液中NaOH物质的量之比为7∶9时,则所得溶液中NaHCO3的质量为______g。
3.(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B升华 C结晶 D过滤 E蒸馏 F分液①分离饱和食盐水与沙子的混合物______;②从硝酸钾和氯化钠的混合液中获得硝酸钾________;③从碘水中提取碘单质______;④分离CCl4,(沸点为76.75℃)和甲苯(沸点110.6℃)的混合物_________。
(2)实验室用NaCO3·10H2O晶体配制0. 5mol/L的Na2CO3溶液970mL,应用托盘天平称取Na2CO3·10H2O的质量是______。
金属钠铁铜铝镁方程式答案
钠及其化合物一、金属钠1.刚切开钠的断面很快变暗化学方程式:4Na+O2=2Na2O2.钠在空气中燃烧2Na+O2Na2O23.钠与硫的反应:2Na + S = Na2S钠与氯气反应:2Na+Cl22NaCl4.过量钠投入稀盐酸中,化学方程式:①2Na+2HCl=2NaCl+H2↑;②2Na +2H2O =2NaOH+H2↑离子方程式:①2Na+2H+=2Na++H2↑;②2Na+2H2O=2Na++2OH-+H2↑5.钠投入硫酸铜溶液中化学方程式:①2Na+2H2O=2NaOH+H2↑②2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 6.钠与熔融盐(如TiCl4)的反应4Na + TiCl44NaCl + Ti7.金属Na制取金属KNa + KCl NaCl+K ↑8.氧化钠与水反应Na2O + H2O = 2NaOHNa2O + H2O = 2Na+ + 2OH-9.氧化钠与CO2反应Na2O + CO2 = Na2CO310.氧化钠与盐酸反应Na2O + 2HCl = 2NaCl + H2ONa2O + 2H+ = 2Na+ + H2O11.氧化钠在空气中加热2NaO+O22Na2O2三、过氧化钠—不是碱性氧化物,是过氧化物12.过氧化钠投入水中化学方程式:2Na2O2+2H2O =4NaOH+O2↑离子方程式:2Na2O2+2H2O=4Na++4OH-+O2↑13.呼吸面具中过氧化钠做供氧剂2Na2O2+2CO2 =2Na2CO3+O214.过氧化钠与盐酸反应2Na2O2 + 4HCl = 4NaCl + 2H2O + O2↑2Na2O2 + 4H+ = 4Na+ + 2H2O + O2↑四、碳酸钠(纯碱、苏打),碳酸氢钠(小苏打)15.向纯碱溶液中逐滴滴加盐酸,至过量:化学方程式:化学方程式:①Na2CO3+HCl=NaHCO3+NaCl②NaHCO3+HCl=NaCl+H2O+CO2↑离子方程式:① CO32-+H+=HCO3-②HCO3-+H+=H2O+CO2↑16.向稀盐酸中滴加纯碱溶液化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑离子方程式:CO32-+2H+=H2O+CO2↑17.碳酸钠溶液中滴入几滴澄清石灰水化学方程式:Ca(OH)2 + Na2CO3====CaCO3↓+ 2NaOH 离子方程式:Ca2+ + CO32- ==== CaCO3↓18.向碳酸钠溶液中滴入几滴氯化钙溶液化学方程式:Na2CO3+CaCl2=CaCO3↓+2NaCl离子方程式:CO32- + Ca2+ === CaCO3↓19.向碳酸钠溶液中滴入几滴氢氧化钠溶液不反应20.除去碳酸氢钠溶液中混有的少量碳酸钠化学方程式:Na2CO3 + CO2 + H2O====2NaHCO3 21.除去碳酸钠固体中混有的少量碳酸氢钠2NaHCO3Na2CO3 +H2O+ CO2↑22.碳酸氢钠溶液与稀盐酸化学方程式:NaHCO3+HCl=NaCl+H2O+CO2↑离子方程式:HCO3-+H+=H2O+CO2↑23.碳酸氢钠溶液与烧碱.化学方程式:NaHCO3+NaOH = Na2CO3+H2O 离子方程式:HCO3-+OH-=CO32-+H2O 24.向烧碱溶液中通入少量二氧化碳.化学方程式:CO2+2NaOH = Na2CO3+H2O离子方程式:CO2+2OH-=CO32-+H2O25.向烧碱溶液中通入过量二氧化碳化学方程式:NaOH+CO2=NaHCO3离子方程式:OH-+CO2= HCO3-26.向碳酸氢钠溶液中滴入几滴氯化钙溶液不反应27.碳酸氢钠与足量氢氧化钙溶液HCO3-+Ca2+ +OH-=CaCO3↓ +H2O28.碳酸氢钠与少量氢氧化钙溶液2HCO3-+Ca2+ +2OH-=CaCO3↓ +2H2O +CO32-29.过量......Na2CO3溶液:析出NaHCO3晶体..CO2通入饱和Na2CO3 + H2O + CO2 = 2NaHCO3↓2Na++CO32- + H2O + CO2 = 2NaHCO3↓29.用饱和..NaHCO3溶液除去CO2中混有的SO2气体2NaHCO3 + SO2 = Na2SO3 + 2CO2↑+H2O30.碳酸氢钠与硫酸氢钠溶液的反应NaHCO3+ NaHSO4=Na2SO4+CO2↑+H2OHCO3--+ H+=CO2↑+H2O五、氢氧化钠(烧碱、火碱、苛性钠)32.氢氧化钠与少量CO2的反应2NaOH + CO2 = Na2CO3 + H2O2OH- + CO2 = CO32- + H2O33.氢氧化钠与醋酸的反应NaOH + CH3COOH = CH3COONa+H2OOH- + CH3COOH = CH3COO-+H2O34.少量NaOH溶液与足量Ca(HCO3)2溶液Ca(HCO3)2+NaOH=CaCO3↓+NaHCO3+H2OCa2++HCO3-+OH-=CaCO3↓+H2O35.足量NaOH溶液与少量Ca(HCO3)2溶液Ca(HCO3)2+2NaOH=CaCO3↓+Na2CO3+2H2OCa2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O七、氯化钠36、电解熔融的NaCl2NaCl(熔融)2Na+Cl2↑37、电解饱和食盐水化学方程式:2NaCl+2H2O2NaOH+H2↑+Cl2↑离子方程式:2Cl-+2H2O2OH-+H2↑+Cl2↑38、氯化钠固体与浓硫酸反应NaCl + H2SO4(浓)NaHSO4+HCl↑2NaCl + H2SO4(浓)Na2SO4+2HCl↑39、侯氏制碱法NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl2NaHCO3Na2CO3 +H2O+ CO2↑铁及其化合物1、Fe在纯O2中燃烧3Fe + 2O2Fe3O42、Fe与S的反应Fe + S FeS3、Fe与Cl2点燃2Fe + 3Cl22FeCl3(剧烈燃烧,大量棕褐色的烟)4、Fe与水蒸汽反应3Fe+4H2O(g)Fe3O4+4H25、Fe与稀硫酸反应化学方程式:Fe+H2SO4===FeSO4+H2↑;离子方程式:Fe+2H+===Fe2++H2↑;6、Fe与氯化铜溶液反应化学方程式:Fe+CuCl2===Cu+FeCl2;离子方程式:Fe+Cu2+===Cu+Fe2+;7、Fe3O4粉末和稀盐酸化学方程式:Fe3O4+8HCl====FeCl2+2FeCl3+4H2O;离子方程式:Fe3O4+8H+====Fe2++2Fe3++4H2O8、CO还原磁性氧化铁(工业炼铁)化学方程式:Fe3O4+4CO 3Fe+4CO2;9、CO还原氧化铁(工业炼铁)化学方程式:Fe2O3+3CO2Fe+3CO210、向氯化铁中滴加氢氧化钠溶液化学方程式:FeCl3+3NaOH====Fe(OH)3↓+3NaCl;离子方程式:Fe3++3OH-====Fe(OH)3↓;11、氢氧化铁胶体的制备FeCl3+3H2O Fe(OH)3(胶体)+3HCl12、向硫酸亚铁溶液滴加过量氨水,生成白色沉淀,迅速变灰绿色,最终变成红褐色,生成白色沉淀化学方程式:FeSO4+2NH3·H2O====Fe(OH)2↓+(NH4)2SO4;离子方程式:Fe2++2NH3·H2O====Fe(OH)2↓+2NH4+;白色沉淀迅速变灰绿色最终变成红褐色,化学方程式4Fe(OH)2+O2+2H2O====4Fe(OH)313、氢氧化铁受热分解化学方程式:2Fe(OH)3Fe2O3+3H2O14、除去FeCl2溶液中的FeCl3化学方程式:2FeCl3+Fe = 3FeCl2离子方程式:2Fe3+ + Fe = 3Fe2+15、除去FeCl3溶液中的FeCl2化学方程式:2FeCl2+Cl2 =2FeCl3离子方程式:2Fe2+ + Cl2 = 2Fe3+ +2Cl-16、用氯化铁溶液制作铜制印刷电路板化学方程式:2FeCl3+Cu = 2FeCl2 +CuCl2离子方程式:2Fe3++Cu=2Fe2++Cu2+17、Fe3+的检验,(1)常用硫氰酸钾溶液离子方程式:Fe3++3SCN- =Fe(SCN)3(2)加氢氧化钠溶液Fe3++3OH-====Fe(OH)3↓18、氯化亚铁中Fe2+的检验:(1)常用:先滴加硫氰化钾溶液,观察后,再加氯水,化学方程式:①2FeCl2+Cl2 =2FeCl3;②FeCl3+3KSCN=Fe(SCN)3+3KCl;离子方程式:①2Fe2+ + Cl2 = 2Fe3+ +2Cl-;②Fe3++3SCN- =Fe(SCN)3;(2)可以加氢氧化钠溶液,现象:白色沉淀迅速变灰绿色最终变成红褐色;化学方程式:①FeCl2+2NaOH====Fe(OH)2↓+2NaCl;②4Fe(OH)2+O2+2H2O====4Fe(OH)3;19、氯化铁溶液中加入KI,离子方程式:2Fe3++2I-=2Fe2++I220.氯化亚铁使酸性高锰酸钾褪色离子方程式:MnO4- + 8H+ + 5Fe2+= Mn2++ 5Fe3+ + 4H2O21.氯化亚铁中滴入双氧水离子方程式:2Fe2++H2O2+2H+=2Fe3+2H2O22.氯化铁与碳酸钠的水解互促反应离子方程式:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑23.氯化铁与碳酸氢钠的水解互促反应离子方程式:Fe3++3HCO3-=Fe(OH)3↓+3CO2↑铝及其化合物1.铝箔在氧气中剧烈燃烧化学方程式:4Al + 3O22Al2O32.表面被氧化的铝片溶于过量稀盐酸,化学方程式:①Al2O3 +6HCl =2AlCl3 + 3H2O②2Al+6HCl=2AlCl3+3H2↑离子方程式:①Al2O3 + 6H+ =2Al3+ + 3H2O②2Al+6H+=2Al3++3H2↑3.表面被氧化的铝片溶于过量氢氧化钠溶液,化学方程式:①Al2O3 + 2NaOH+3 H2O=2 Na[Al(OH)4]②2Al+2NaOH +6H2O=2Na[Al(OH)4]+3H2↑离子方程式:①Al2O3+2OH- +3 H2O== 2[Al(OH)4]-②2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑4、氢氧化铝中加稀盐酸化学方程式:Al(OH)3+3HCl=AlCl3+3H2O离子方程式:Al(OH)3 +3H+ = Al3++ 3H2O5、氢氧化铝中加烧碱溶液化学方程式:Al(OH)3+NaOH=Na[Al(OH)4]离子方程式:Al(OH)3+OH-=[Al(OH)4]-6.制备氢氧化铝(1)往硫酸铝溶液中加过量氨水,化学方程式:Al2(SO4)3+6NH3·H2O====2Al(OH)3↓+3(NH4)2SO4离子方程式:Al3+ + 3NH3·H2O =Al(OH)3↓ +3NH4+(2)往四羟基合铝酸钠溶液中通过量二氧化碳,化学方程式:Na[Al(OH)4]+CO2 = Al(OH)3↓+ NaHCO3离子方程式:[Al(OH)4]- +CO2 = Al(OH)3↓+ HCO3-7.往四羟基合铝酸钠溶液中通少量二氧化碳,化学方程式:2Na[Al(OH)4]+CO2 = 2Al(OH)3↓+ Na2CO3+H2O离子方程式:2[Al(OH)4]- +CO2 = 2Al(OH)3↓+ CO32-+H2O8.氢氧化铝受热分解2Al(OH)3Al 2O3+3H2O9.往氯化铝溶液中逐滴滴加烧碱溶液,至过量氢氧化钠不足时:AlCl3+3NaOH = Al(OH)3↓+3NaClAl3++3OH- = Al(OH)3↓氢氧化钠过量后:Al(OH)3+NaOH = Na[Al(OH)4]Al(OH)3+OH- =[Al(OH)4]-10、往氯化铝溶液中加入过量烧碱溶液化学方程式:AlCl3+4NaOH = Na[Al(OH)4]+3NaCl离子方程式:Al3++4OH- =[Al(OH)4]-11.往四羟基合铝酸钠溶液中逐滴滴加稀盐酸,至过量化学方程式:①Na[Al(OH)4]+HCl =Al(OH)3↓+ NaCl+H2O②Al(OH)3+3HCl=AlCl3+3H2O离子方程式:①[Al(OH)4]- +H+=Al(OH)3↓+H2O;②Al(OH)3 +3H+ = Al3++ 3H2O12.往四羟基合铝酸钠溶液中加入过量的稀盐酸,化学方程式:Na[Al(OH)4]+4HCl =AlCl3+ NaCl+4H2O离子方程式:[Al(OH)4]- +4H+=Al3++4H2O;13.往NaOH溶液中逐滴滴入AlCl3溶液至过量.化学方程式:AlCl3+4NaOH = Na[Al(OH)4]+3NaCl3 Na[Al(OH)4]+AlCl3=4Al(OH)3↓+3NaCl离子方程式:Al3++4OH- =[Al(OH)4]-3[Al(OH)4]- +Al3+=4Al(OH)3↓14.明矾与氢氧化钡溶液至铝离子完全沉淀化学方程式:2KAl(SO4)2+3Ba(OH)22Al(OH)3↓+K2SO4+3BaSO4↓离子方程式:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓15.明矾溶液与氢氧化钡溶液至硫酸根完全沉淀化学方程式:KAl(SO4)2+2Ba(OH)22BaSO4↓+K[Al(OH)4]离子方程式: Al3++2SO42-+2Ba2++4OH-=[Al(OH)4]-+2BaSO4↓16.氢氧化铝的碱式电离和酸式电离Al(OH)3Al3++3OH-Al(OH)3+H2O⇌[Al(OH)4]-+H+17.泡沫灭火器的原理离子方程式:Al3++3HCO3-=Al(OH)3↓+3CO2↑18.硫酸铝与碳酸钠溶液离子方程式:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑19、氯化铝与硫化钠溶液离子方程式:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑20、明矾:KAl(SO4)2·12H2O(十二水合硫酸铝钾)明矾净水:溶于水时产生Al(OH)3胶体,能吸附水中悬浮的杂质而沉淀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
钠和氯气 方程式练习答案
班级 姓名
1、金属钠与水反应的化学方程式:2Na + 2H 2O = 2NaOH + H 2↑
2、金属钠与水反应的离子方程式:2Na + 2H 2O = 2Na + + OH —
+ H 2↑ 3、钠与O 2在常温下反应的化学方程式:4Na + O 2 = 2Na 2O
4、钠在氧气中燃烧的化学方程式:2Na + O 2 Na 2O 2
5、氧化钠与水反应的化学方程式:Na 2O + H 2O = 2NaOH
6、氧化钠与CO 2反应的化学方程式:Na 2O + CO 2 = Na 2CO 3
7、过氧化钠与水反应的化学方程式:2Na 2O 2 + 2 H 2O = 4NaOH + O 2↑
8、过氧化钠与CO 2反应的化学方程式:2Na 2O 2 + 2 CO 2 = 2Na 2CO 3+ O 2↑
9、氧化钠与盐酸反应的化学方程式:Na 2O + 2HCl = 2NaCl + H 2O *10、过氧化钠与盐酸反应的化学方程式:2Na 2O 2 + 4HCl = 4NaCl + 2H 2O + O 2↑
11、金属钠与盐酸反应的化学方程式:2Na +2HCl = 2NaCl + H 2↑
12、钠在氯气中燃烧的化学方程式:2Na + Cl 2 2NaCl
13、铁在氯气中燃烧的化学方程式:2Fe + 3Cl 2 2FeCl 3
14、铜在氯气中燃烧的化学方程式:Cu+ Cl 2 Cu Cl 2
15、氢气在氯气中燃烧的化学方程式:H 2 + Cl 2 2HCl 16、氯气与水反应的化学方程式:Cl 2+ H 2O HCl + HClO
17、氯气与水反应的离子方程式:Cl 2+ H 2O H + + Cl —
+ HClO 18、氯气通入氢氧化钠溶液中反应的化学方程式:Cl 2+ 2NaOH = NaCl + NaClO + H 2O
19、氯气通入氢氧化钠溶液中反应的离子方程式:Cl 2+ 2OH — = Cl — + ClO —
+ H 2O 20、工业上制取漂白粉的化学方程式:2Cl 2+ 2Ca (OH )2 = CaCl 2 + Ca (ClO )2 + 2H 2O
21、漂白粉露置于空气中变质的原因:Ca (ClO )2 + H 2O + CO 2 = CaCO 3 + 2HClO
22、次氯酸分解的化学方程式:2HClO 2HCl+ O 2↑
23、84消毒液中加入盐酸反应的化学方程式:NaClO + HCl = NaCl + HClO
24、氯气与氯化亚铁溶液反应的化学方程式:2FeCl 2 + Cl 2 = 2FeCl 3
25、氯气与氯化亚铁溶液反应的离子方程式:2Fe 2+ + Cl 2 = 2Fe 3+ + 2 Cl — 点燃 点燃 点燃 点燃
光照。
