第2章药物的物理化学相互作用教程文件
合集下载
第2章+药物的物理化学相互作用

发生在极性分子与极性分子之间
分子的极性越大,分子间的取向力越大
2020/2/27
大连理工大学
2.诱导力(induction force )
存在于极性分子与非极性分子之间 还存在于极性分子与极性分子之间
2020/2/27
大连理工大学
3.色散力(dispersion force )
色散力存在于极性分子与极性分子之间、 极性分子与非极性分子之间、非极性分子 与非极性分子之间。
复方碘溶液
2020/2/27
大连理工大学
2.混悬剂、乳剂
由于粒子及液滴的相互作用使混悬 剂及乳剂发生聚集,造成不稳定。
需加入絮凝剂、助悬剂等稳定剂
3.高分子溶液剂、溶胶剂
大连理工大学
二、对固体制剂成型性的影响
固体制剂大多由微粉加工 · 干燥状态下固体粒子相互接触产生的范德
华力、静电力以及粉粒间接触点吸附液体薄膜 的表面张力使其发生相互的粘附,会阻碍固体 物料的混合。因此常采用交互加入少量水润湿 药物或适量表面活性剂来提高混合的效果。
2020/2/27
大连理工大学
3.对药物稳定性的影响
制成络合物提高药物稳定性 维生素B2与吡啶类络合抑制维生素B2降解 苯佐卡因与咖啡因配伍(形成分子缔合物)
2020/2/27
大连理工大学
二、药物的物理化学作用对制剂成型的影响 (一)对液体制剂成型性的影响
1.低分子溶液剂 利用助溶、潜溶制备低分子溶液剂
药物发生络合作用; 因此药物的相互作用对多种制剂的成型均
存在较大的影响。
2020/2/27
大连理工大学
一、药物的物理化学作用对物在溶剂中溶解规律“结构相似者相溶” 结构相似:分子的化学键、分子间作用力以 及分子相对大小等结构性质。
药物相互作用课件

DRUG INTERACTION 临床药学室 计 成
单击添加副标题
药物相互作用
一 基本概念
单击添加标题
单击添加标题
联合用药 同时或间隔一定时间使用两种或两种以上的药物 联合用药的目的 提高疗效 减轻副作用 减缓耐受性 延缓耐药性 治疗多种或复杂的病症
DRUG INTERACTION
由于药物之间或药物-机体-药物之间的反应,改变了药物原来的体内过程、组织对药物的感受性或药物的理化性质,而产生单种药物所没有的药理作用或不良反应(药物相互作用,或药物交互作用)
02
氯丙嗪与普萘洛尔合用时,由于前者抑制了后者药物代谢酶的活性,使普萘洛尔血药浓度上升,引起心率缓慢,血压降低,甚至休克
02
氯丙嗪抑制其他药物代谢酶活性
长期服用格列本脲的糖尿病患者因细菌感染而服用甲氧苄氨嘧啶/磺胺甲噁唑,结果导致低血糖发生 。
磺胺类药物通过肝脏代谢,竞争性地抑制了CYP2C9活性,导致磺脲类药物代谢减弱,作用增强,产生低血糖
药物相互作用的研究对象
药物相互作用的结果
药效增强或减弱
毒副作用增加或减轻
药物理化性质变化
出现始料不及的不良反应
/CONTENTS
国家药监局下发紧急通知,要求立即停用“黄柏胶囊”(“梅花K”)
黄柏
黄柏为芸香科植物黄柏或黄皮树的树皮,含有多种生物碱(小檗碱、棕榈碱、黄柏碱等),具有清热除湿、泻火解毒、清退虚热等功效; 常与抗菌药物配伍,如治疗埃希大肠杆菌所致细菌性腹泻等
04
药理效应的协同、拮抗
基本形式
01
02
03
04
普萘洛尔拮抗-肾上腺素受体激动剂
酚妥拉明拮抗-肾上腺素受体激动剂
纳络酮拮抗吗啡
单击添加副标题
药物相互作用
一 基本概念
单击添加标题
单击添加标题
联合用药 同时或间隔一定时间使用两种或两种以上的药物 联合用药的目的 提高疗效 减轻副作用 减缓耐受性 延缓耐药性 治疗多种或复杂的病症
DRUG INTERACTION
由于药物之间或药物-机体-药物之间的反应,改变了药物原来的体内过程、组织对药物的感受性或药物的理化性质,而产生单种药物所没有的药理作用或不良反应(药物相互作用,或药物交互作用)
02
氯丙嗪与普萘洛尔合用时,由于前者抑制了后者药物代谢酶的活性,使普萘洛尔血药浓度上升,引起心率缓慢,血压降低,甚至休克
02
氯丙嗪抑制其他药物代谢酶活性
长期服用格列本脲的糖尿病患者因细菌感染而服用甲氧苄氨嘧啶/磺胺甲噁唑,结果导致低血糖发生 。
磺胺类药物通过肝脏代谢,竞争性地抑制了CYP2C9活性,导致磺脲类药物代谢减弱,作用增强,产生低血糖
药物相互作用的研究对象
药物相互作用的结果
药效增强或减弱
毒副作用增加或减轻
药物理化性质变化
出现始料不及的不良反应
/CONTENTS
国家药监局下发紧急通知,要求立即停用“黄柏胶囊”(“梅花K”)
黄柏
黄柏为芸香科植物黄柏或黄皮树的树皮,含有多种生物碱(小檗碱、棕榈碱、黄柏碱等),具有清热除湿、泻火解毒、清退虚热等功效; 常与抗菌药物配伍,如治疗埃希大肠杆菌所致细菌性腹泻等
04
药理效应的协同、拮抗
基本形式
01
02
03
04
普萘洛尔拮抗-肾上腺素受体激动剂
酚妥拉明拮抗-肾上腺素受体激动剂
纳络酮拮抗吗啡
二--药物的物理化学相互作用PPT课件

药物分子络合物主要靠分子间力、氢键及电荷 转移等分子间的相互作用而形成。
种类: 传荷络合物 氢键络合物
特点:
键能较小,属于弱键型的络合物
.
11
药物传荷络合物
传荷络合物(charge transfer complex, CTC):在电荷转移 体系中,电性差别较大的两个分子间,多电子的分子(电子供体) 向缺电子的分子(电子受体)转移电 子(或迁移负电荷),这 两个分子之间产生电荷迁移力,因而结合成分子络合物,称传荷 络合物。.Biblioteka 13 络合物在制剂中的应用
络合物在制剂中 的应用
助溶
增加药物的稳定性: 少量咖啡因↑苯佐卡因在水溶 液中的稳定性。(传荷)
吡唑酮类物质抑制核黄素光照 分解。(传荷与氢键)
菸酰胺、咖啡因、吡多辛等可 防止氯丙嗪的光照分解。(传 荷)
改变药物的溶解度: 加入络作剂,生成可溶性络合 物,可增大药物的溶解度。
五、疏水相互作用
胶束(表面活性剂章节)
.
15 第二节 药物的物理化学相互作用 对药物及制剂性质的影响
溶解度
稳定性
熔点、 沸点
对药物性质的影响
.
16 对药物性质的影响
氢键对物质性质的影响 (1) 有分子间氢键的化合物的熔点和沸点比没有氢键的
同类化合物为高。
例: HF, HCl, HBr和HI中哪个物质熔沸点最高? HF的熔、沸点最高。
1
第二章 药物的物理化学相互作用
.
2 第一节 药物的物理化学 相互作用类型
一、范德华力
二、氢键
三、传荷络合作用
四、离子参与的相互作用
五、疏水相互作用
.
一、范德华力( van der Waals )
临床药学药物相互作用课件

❖ 降血糖药不宜与普萘洛尔合用,因其可加重低血 糖反应外,并掩盖低血糖先兆症象。
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
严重骨髓抑制
❖ 甲氨蝶呤与水杨酸类、磺胺类、呋塞米合用,后 者可置换甲氨蝶呤,使其对骨髓的抑制明显增强, 引起全血细胞减少。
等;
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
有不稳定性疾病,如心律失常、糖尿病、 癫痫的病人;
需要长期应用药物治疗的病人,如阿狄森 病、脏器移植患者;
服用多个医生处方药物的病人。
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
例1
塑料制品
吸 附 作 用
2020/3/15
安定、硝酸甘油、硝酸异山梨醇、
醋酸酯、华法林钠、盐酸肼酞嗪
和硫喷妥钠,抗组胺类药、吩噻
嗪类药
临床药学课件
例2
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
口服利福平、 长期外用2%盐 酸肾上腺素或1 %环硼肾上腺
素滴眼液
隐形眼镜 染色
❖奎尼丁 与氯丙嗪合用,可致室性心动过速。 ❖ 维拉帕米与β受体阻断药合用,易引起心动过缓、
低血压、房室传导阻滞、心力衰竭、甚至心脏停 搏。
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
出血
❖ 香豆素类与消胆胺、氨基糖苷类抗生素、阿司匹林、 西米替丁等药合用,可引起出血。
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
严重骨髓抑制
❖ 甲氨蝶呤与水杨酸类、磺胺类、呋塞米合用,后 者可置换甲氨蝶呤,使其对骨髓的抑制明显增强, 引起全血细胞减少。
等;
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
有不稳定性疾病,如心律失常、糖尿病、 癫痫的病人;
需要长期应用药物治疗的病人,如阿狄森 病、脏器移植患者;
服用多个医生处方药物的病人。
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
例1
塑料制品
吸 附 作 用
2020/3/15
安定、硝酸甘油、硝酸异山梨醇、
醋酸酯、华法林钠、盐酸肼酞嗪
和硫喷妥钠,抗组胺类药、吩噻
嗪类药
临床药学课件
例2
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
口服利福平、 长期外用2%盐 酸肾上腺素或1 %环硼肾上腺
素滴眼液
隐形眼镜 染色
❖奎尼丁 与氯丙嗪合用,可致室性心动过速。 ❖ 维拉帕米与β受体阻断药合用,易引起心动过缓、
低血压、房室传导阻滞、心力衰竭、甚至心脏停 搏。
2020/3/15
临床药学课件
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系网站或本人删除。
出血
❖ 香豆素类与消胆胺、氨基糖苷类抗生素、阿司匹林、 西米替丁等药合用,可引起出血。
药物相互作用DRUG-DRUG INTERACTION课件

甲氧氯普胺可加速胃肠道蠕动,进而 影响某些药物的吸收 地高辛、维生素B2只能在十二指肠和 小肠上部吸收,与甲氧氯普胺合用时,因 甲氧氯普胺加速肠道蠕动,使药物迅速通 过吸收部位,减少吸收而降低疗效
药代动力学
(3)药物互相结合后妨碍吸收
钙盐
与四环素类形成难吸收的络合物 硫糖铝 减少苯妥英钠、喹诺酮类、甲状 腺素的吸收
影响胃肠蠕动和排空的药物
延缓 阿托品及其它抗胆碱 药(普鲁本辛) 三环类抗抑郁药 吩噻嗪类抗精神病药 抗组胺药(H1拮抗剂) 促进 胃动力药:胃复安 (甲 氧氯普胺)、吗丁林 泻药:大黄、番泻叶
普鲁本辛(抗胆碱作用)+地高辛 甲氧氯普胺(D2拮抗剂,加强胃肠运动) +地高辛
甲氧氯普胺与地高辛合用
药代动力学
(2)改变胃排空或肠蠕动速度
吗丁啉加速胃排空,使某些药物的吸收减少 抗酸药、抗胆碱药和镇静催眠药 可减慢胃排空,延迟药物的吸收 阿片类可减慢乙酰氨基酚的吸收 抗胆碱药可减慢地西泮、左旋多巴的吸收 西沙必利促进环孢素、地西泮的吸收
胃排空的速度决定药物抵达小肠的速度、
影响肠道的药物吸收:胃排空慢,吸收 亦慢;胃排空快,吸收亦快 胃肠蠕动减慢,内容物停留时间延长, 会增加药物的吸收;反之,则减少药物 的吸收 互相结合 有些药物同服时可互相结合而妨碍吸收 钙盐与四环素类形成难吸收的络合物
水杨酸类、呋塞米 磺酰脲类 水合氯醛 华法林 水杨酸类 呋塞米、磺胺类 甲氨蝶呤 乙氨嘧啶 奎宁 呋塞米 水合氯醛 维拉帕米 卡马西平、苯妥英钠
药代动力学 基本规律
(2)改变组织分布量 1) 组织结合位点的竞争置换
奎尼丁将地高辛从骨骼肌的结合位点上置换 下来,使地高辛的血药浓度增高
2) 改变组织血流量 去甲肾上腺素减少肝脏血流量,使利多卡因 的代谢速度下降,血药浓度增加
药代动力学
(3)药物互相结合后妨碍吸收
钙盐
与四环素类形成难吸收的络合物 硫糖铝 减少苯妥英钠、喹诺酮类、甲状 腺素的吸收
影响胃肠蠕动和排空的药物
延缓 阿托品及其它抗胆碱 药(普鲁本辛) 三环类抗抑郁药 吩噻嗪类抗精神病药 抗组胺药(H1拮抗剂) 促进 胃动力药:胃复安 (甲 氧氯普胺)、吗丁林 泻药:大黄、番泻叶
普鲁本辛(抗胆碱作用)+地高辛 甲氧氯普胺(D2拮抗剂,加强胃肠运动) +地高辛
甲氧氯普胺与地高辛合用
药代动力学
(2)改变胃排空或肠蠕动速度
吗丁啉加速胃排空,使某些药物的吸收减少 抗酸药、抗胆碱药和镇静催眠药 可减慢胃排空,延迟药物的吸收 阿片类可减慢乙酰氨基酚的吸收 抗胆碱药可减慢地西泮、左旋多巴的吸收 西沙必利促进环孢素、地西泮的吸收
胃排空的速度决定药物抵达小肠的速度、
影响肠道的药物吸收:胃排空慢,吸收 亦慢;胃排空快,吸收亦快 胃肠蠕动减慢,内容物停留时间延长, 会增加药物的吸收;反之,则减少药物 的吸收 互相结合 有些药物同服时可互相结合而妨碍吸收 钙盐与四环素类形成难吸收的络合物
水杨酸类、呋塞米 磺酰脲类 水合氯醛 华法林 水杨酸类 呋塞米、磺胺类 甲氨蝶呤 乙氨嘧啶 奎宁 呋塞米 水合氯醛 维拉帕米 卡马西平、苯妥英钠
药代动力学 基本规律
(2)改变组织分布量 1) 组织结合位点的竞争置换
奎尼丁将地高辛从骨骼肌的结合位点上置换 下来,使地高辛的血药浓度增高
2) 改变组织血流量 去甲肾上腺素减少肝脏血流量,使利多卡因 的代谢速度下降,血药浓度增加
药物的相互作用 ppt课件

pH
0h
0.5h
1h
2h
3h
4h
色泽
淡黄 深棕 深棕 深棕 深棕 深棕
4.0
含量(%) 36.92 6.27
0.64
0.18
0.05
0.01
色泽
微黄 淡紫红 紫红 紫
紫
紫
5.0
含量(%) 68.97 56.54 39.76 18.78 10.85 4.92
色泽
无
淡蓝紫 篮紫 篮紫 篮紫 篮紫
6.0
含量(%) 67.59 65.74 58.19 53.06 44.18 41.63
PH范围
3.2-5.5 3.5-5.5 4.5-7.0 4.5-7.5 6.0-7.5 3.6-6.5 5.0-7.0
备注
含Ca2+ 含Ca2+ 含C媒的影响
5%或10%葡萄糖注射液pH为3.2~5.5,属于酸性溶液, 一些碱性药品不能加入到葡萄糖液中。
如:呋塞米注射液为加碱制成的钠盐制剂,碱性较高, 不得使用GS、GNS等偏酸性的溶媒输注,宜选用NS为溶 媒。
色泽
无
无
无
淡紫 淡紫 淡紫
7.0
含量(%) 98.97 98.70 98.12 98.89 98.86 98.81
色泽
无
无
无
无
无
淡紫
7.5
含量(%) 98.13 99.28 97.99 97.13 97.96 96.99
色泽
无
无
无
无
无
无
8.0
含量(%) 99.65 98.29 98.42 98.01 96.87 97.35
PPT课件
14
药物相互作用课件课件

关于药物相互作用课件
第1页,此课件共95页哦
现代医学和药学的发展,大大促进了患者的多药并用。 老年患者,每天同时服用4~5种药的情况极为普遍。 ADR, 尤其是药物相互作用(DDI/drug-drug interaction)所致的
ADR因此而日趋严重。
处方医师、药师和患者必须认真考虑这一重要而现实的问题。
含多价阳离子药物
氟喹诺酮类
1 含Ca2+、Mg2+、Al3+
抗酸药物
四环素类
2 Fe2+制剂
3 补钙制品
4 Bi3+
形成络合物或鳌合物
临床应避免抗生素与该类药物同时服用,必须合用 时,服药时间应间隔3小时
24
第24页,此课件共95页哦
▪ 胃肠运动的影响:
药物吸收主要部位:小肠上部 影响因素:
胃排空、肠蠕动速率
4 10
28
54
6
第6页,此课件共95页哦
联合用药:是指同时或相隔一定时间内使用两 种或两种以上的药物。
临床联合用药意义: 1 提高药物疗效;
2 减少药物的某些副作用; 3 延缓机体耐受性或病原体耐药性的产生,可延长疗
程,从而提高药物的效果。
7
第7页,此课件共95页哦
药物相互作用的结果:
加强:疗效提高,毒性也可加大 减弱:毒性减轻,疗效也可降低 理想:疗效提高,同时毒性减轻 避免:毒性加大,而疗效降低
舒普深、特治星、特美汀、强力阿莫仙等 亚胺培南+西拉司丁 泰能 磺胺甲恶唑+TMP 复方新诺明(SMZ-Co) 氯沙坦钾+氢氯噻嗪 海捷亚
10
第10页,此课件共95页哦
临床应避免产生的不良药物相互作用: 毒性加大和/或疗效降低!
第1页,此课件共95页哦
现代医学和药学的发展,大大促进了患者的多药并用。 老年患者,每天同时服用4~5种药的情况极为普遍。 ADR, 尤其是药物相互作用(DDI/drug-drug interaction)所致的
ADR因此而日趋严重。
处方医师、药师和患者必须认真考虑这一重要而现实的问题。
含多价阳离子药物
氟喹诺酮类
1 含Ca2+、Mg2+、Al3+
抗酸药物
四环素类
2 Fe2+制剂
3 补钙制品
4 Bi3+
形成络合物或鳌合物
临床应避免抗生素与该类药物同时服用,必须合用 时,服药时间应间隔3小时
24
第24页,此课件共95页哦
▪ 胃肠运动的影响:
药物吸收主要部位:小肠上部 影响因素:
胃排空、肠蠕动速率
4 10
28
54
6
第6页,此课件共95页哦
联合用药:是指同时或相隔一定时间内使用两 种或两种以上的药物。
临床联合用药意义: 1 提高药物疗效;
2 减少药物的某些副作用; 3 延缓机体耐受性或病原体耐药性的产生,可延长疗
程,从而提高药物的效果。
7
第7页,此课件共95页哦
药物相互作用的结果:
加强:疗效提高,毒性也可加大 减弱:毒性减轻,疗效也可降低 理想:疗效提高,同时毒性减轻 避免:毒性加大,而疗效降低
舒普深、特治星、特美汀、强力阿莫仙等 亚胺培南+西拉司丁 泰能 磺胺甲恶唑+TMP 复方新诺明(SMZ-Co) 氯沙坦钾+氢氯噻嗪 海捷亚
10
第10页,此课件共95页哦
临床应避免产生的不良药物相互作用: 毒性加大和/或疗效降低!
第2章 药物的物理化学相互作用2020
增加药物的稳定性:
改变药物的溶解度:
少量咖啡因↑苯佐卡因在水
加入络合剂,生成可溶性络
溶液中的稳定性。(传荷)
合物,增大药物的溶解度(
吡唑酮类物质抑制核黄素光
助溶)。
照分解。(传荷与氢键)
加入络合剂,生成难溶性或
菸酰胺、咖啡因、吡多辛等
不溶性络合物。
可防止氯丙嗪的光照分解。 (传荷)
咖啡因在水中的溶解度为1∶46,若与苯甲酸钠 以1∶1形成CTC,能使水溶性提高到1∶1.1。
氢键用 --- 表示,如 X-H --- Y,其 中 X,HY原可子以附是近同有种电原负子性,大也,可且以r是小不的同元元 素素的如原F子,。O,N 的原子,即氢键接受体
1 氢键的形成
当两个水分子充分靠 近时,带部分正电荷的氢 原子与另一分子中含有孤 电子对、带负电荷的氧原 子产生相互吸引,这种吸 引力称为分子间的氢键作 用。
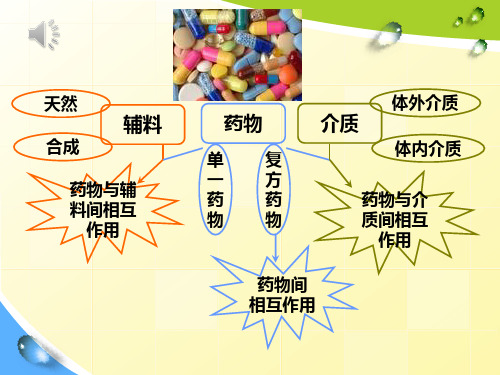
天然 合成
辅料
药物与辅 料间相互
作用
药物
单复 一方 药药 物物
介质
体外介质 体内介质
药物与介 质间相互
作用
药物间 相互作用
这些相互作用会影响到:
药物的物理化学性质。
药剂学如中熔涉点及、的沸界点面、溶现解象度、、混稳悬定剂性絮等凝 、乳剂稳定性、散剂及胶囊剂的粉体聚集、 气雾剂中粉末或液滴分散、颗粒压片等。
非极性分子在极性水中倾向于积聚 的现象就是疏水相互作用。
疏水链表面整齐地排列着一层水分子
疏水链互相聚集,把周围排列有序 的水分子排挤出来。
疏水分子的聚集是一个热力学的自发过程。
能量下降
疏水基团的相互作用对表面活性剂 在水中形成胶束起着至关重要的作用。
(二)离子-偶极作用力和 离子-诱导偶极作用力
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物发生络合作用; 因此药物的相互作用对多种制剂的成型均存
在较大的影响。
2020/6/28
2020/6/28
14
一、药物的物理化学作用对药物性质的影响
1.对药物溶解度的影响
药物在溶剂中溶解规律“结构相似者相溶” 结构相似:分子的化学键、分子间作用力以及分子 相对大小等结构性质。
溶质和溶剂能形成分子内氢键,则溶解度增加 水和乙醇可以任意比例互溶。
传荷络合物的意义:在药物配伍中可以助溶, 增加水溶性,提高稳定性。
2020/6/28
2020/6/28
10
四、离子参与的相互作用
离子键 离子-偶极作用力
离子与极性分子作用
离子-诱导偶极作用力
离子与非极性分子作用
影响药物的溶解度、溶出等。
2020/6/28
2020/6/28
11
NaCl的形成示意 图 失去电子 化合价升高 被氧化
20
三、其他
包合物 固体分散体 无定型药物系统
提高难溶性药物的溶解度及溶出速率
离子交换树脂
提高稳定性、延长作用时间、稳定释药等
2020/6/28
21
&3 药物与包材的相互作用
作用类型 迁移和吸附 评价包装的适用性,研究包装与药品间
的相容性
2020/6/28
2020/6/28
22
我国的相容性要求
分子内形成氢键,则会使药物的熔点、沸点等 物理性质降低,主要是由于分子内氢键的形成消弱 了分子间范德华引力和氢键力。
2020/6/28
2020/6/28
16
3.对药物稳定性的影响
制成络合物提高药物稳定性 维生素B2与吡啶类络合抑制维生素B2降解 苯佐卡因与咖啡因配伍
2020/6/28
2020/6/28
17
二、药物的物理化学作用对制剂成型的影响
(一)对液体制剂成型性的影响
1.低分子溶液剂 利用助溶、潜溶制备低020/6/28
18
2.混悬剂、乳剂
由于粒子及液滴的相互作用使混悬剂 及乳剂发生聚集,造成不稳定。
需加入絮凝剂、助悬剂等稳定剂
3.高分子溶液剂、溶胶剂
00
+1 -1
2Na+ Cl2 = 2NaCl
得到电子 化合价降低 被还原
Na +11 2 8 1
e-
Na+ +11 2 8
Cl +17 2 8 7
2020/6/28
2020/6/28
Cl- +17 2 8 8
Na+ Cl-
12
12
五、疏水相互作用
疏水性(Hydrophobicity Hydrophobicity):非 极性化合物在水中的溶解度非常小,与水混合时 会形成互不相溶的两相,即非极性分子有离开水 相进入非极性相的趋势。
药物分子内形氢键,在极性溶剂中溶解度减小, 在非极性溶剂中的溶解度增大。
2020/6/28
2020/6/28
15
2对药物沸点和熔点的影响
分子间形成氢键时熔点沸点增高 要使液体气化,破获分子间的氢键,需消耗更
多的能量,要使晶体破坏,也要破坏一部分分子间 氢键。 分子内形成氢键时药物的熔点、沸点降低
HF和NH3在水中的溶解度较大。
2020/6/28
2020/6/28
7
对物质熔沸点的影响
分子间氢键:物质熔点、沸点升高。 物质熔化或气化时,要克服纯粹的分子间力外,还必须 提高温度,额外供应能量来破坏分子间的氢键,所以这些 物质的熔点、沸点比同系列氢化物的高。 分子内氢键:熔、沸点常降低。 分子内形成氢键,那么相应的分子间的作用力就会减少, 分子内氢键会使物质熔沸点降低.
第2章药物的物理化学相互作用
&1 药物的物理化学相互作用类型
一、范德华力 二、氢键 三、传荷络合作用 四、离子参与的相互作用 五、疏水相互作用
2020/6/28
2020/6/28
2
一、范德华力(Van der Waals' force )
1.取向力(dipole-dipole attration )
发生在极性分子与极性分子之间
分子的极性越大,分子间的取向力越大
2020/6/28
2020/6/28
3
2.诱导力(induction force )
存在于极性分子与非极性分子之间 还存在于极性分子与极性分子之间
2020/6/28
2020/6/28
4
3.色散力(dispersion force )
色散力与相互作用的分子变形有关,变 形越大,色散力越大。
2020/6/28
19
二、对固体制剂成型性的影响
固体制剂大多由微粉加工 · 干燥状态下固体粒子相互接触产生的范德华
力、静电力以及粉粒间接触点吸附液体薄膜的表 面张力使其发生相互的粘附,会阻碍固体物料的 混合。因此常采用交互加入少量水润湿药物或适 量表面活性剂来提高混合的效果。
2020/6/28
2020/6/28
2020/6/28
8
对粘度的影响
分子间有氢键的液体,一般粘度较 大。例如甘油、磷酸、浓硫酸等多羟基 化合物,由于分子间可形成众多的氢键, 这些物质通常为粘稠状液体。
2020/6/28
9
三、传荷络合作用
概念:电性差别比较大的两个分子相互接触时, 电子多的分子(电子供体)缺电子的分子(电 子受体)转移部分电子而结合成稳定的络合物, 称为传荷络合物;或称电子转移复合物(CTC)
疏水相互作用(Hydrophobic effect) :非极性分 子在极性水中倾向于聚集的现象。
疏水基团的相互作用在表面活性剂在水中形成胶 束的中起着重要作用
2020/6/28
2020/6/28
13
&2 药物的物理化学作用对药物性质的影响
我们知道胶束的形成是通过疏水作用力; 在溶液剂设计加入助溶剂其原理是通过与药
色散力存在于极性分子与极性分子之间、 极性分子与非极性分子之间、非极性分子 与非极性分子之间。
2020/6/28
2020/6/28
5
二、氢键(hydrogen bond)
分子间氢键
分子内氢键
2020/6/28
2020/6/28
6
氢键对药物性质的影响
氢键对物质溶解度的影响
在极性溶剂中,如果溶质分子与溶剂分子之 间可以形成氢键,则溶质的溶解度增大。
相容性:Compatibility 考察药品包装材料与药物之间是否发生迁
移或吸附等现象,进而影响药物质量而进 行的一种试验 。 可控环境 实验模型 相互的或单方面的迁移、变质
2020/6/28
2020/6/28
23
玻璃容器相容性试验重点考察项目
在较大的影响。
2020/6/28
2020/6/28
14
一、药物的物理化学作用对药物性质的影响
1.对药物溶解度的影响
药物在溶剂中溶解规律“结构相似者相溶” 结构相似:分子的化学键、分子间作用力以及分子 相对大小等结构性质。
溶质和溶剂能形成分子内氢键,则溶解度增加 水和乙醇可以任意比例互溶。
传荷络合物的意义:在药物配伍中可以助溶, 增加水溶性,提高稳定性。
2020/6/28
2020/6/28
10
四、离子参与的相互作用
离子键 离子-偶极作用力
离子与极性分子作用
离子-诱导偶极作用力
离子与非极性分子作用
影响药物的溶解度、溶出等。
2020/6/28
2020/6/28
11
NaCl的形成示意 图 失去电子 化合价升高 被氧化
20
三、其他
包合物 固体分散体 无定型药物系统
提高难溶性药物的溶解度及溶出速率
离子交换树脂
提高稳定性、延长作用时间、稳定释药等
2020/6/28
21
&3 药物与包材的相互作用
作用类型 迁移和吸附 评价包装的适用性,研究包装与药品间
的相容性
2020/6/28
2020/6/28
22
我国的相容性要求
分子内形成氢键,则会使药物的熔点、沸点等 物理性质降低,主要是由于分子内氢键的形成消弱 了分子间范德华引力和氢键力。
2020/6/28
2020/6/28
16
3.对药物稳定性的影响
制成络合物提高药物稳定性 维生素B2与吡啶类络合抑制维生素B2降解 苯佐卡因与咖啡因配伍
2020/6/28
2020/6/28
17
二、药物的物理化学作用对制剂成型的影响
(一)对液体制剂成型性的影响
1.低分子溶液剂 利用助溶、潜溶制备低020/6/28
18
2.混悬剂、乳剂
由于粒子及液滴的相互作用使混悬剂 及乳剂发生聚集,造成不稳定。
需加入絮凝剂、助悬剂等稳定剂
3.高分子溶液剂、溶胶剂
00
+1 -1
2Na+ Cl2 = 2NaCl
得到电子 化合价降低 被还原
Na +11 2 8 1
e-
Na+ +11 2 8
Cl +17 2 8 7
2020/6/28
2020/6/28
Cl- +17 2 8 8
Na+ Cl-
12
12
五、疏水相互作用
疏水性(Hydrophobicity Hydrophobicity):非 极性化合物在水中的溶解度非常小,与水混合时 会形成互不相溶的两相,即非极性分子有离开水 相进入非极性相的趋势。
药物分子内形氢键,在极性溶剂中溶解度减小, 在非极性溶剂中的溶解度增大。
2020/6/28
2020/6/28
15
2对药物沸点和熔点的影响
分子间形成氢键时熔点沸点增高 要使液体气化,破获分子间的氢键,需消耗更
多的能量,要使晶体破坏,也要破坏一部分分子间 氢键。 分子内形成氢键时药物的熔点、沸点降低
HF和NH3在水中的溶解度较大。
2020/6/28
2020/6/28
7
对物质熔沸点的影响
分子间氢键:物质熔点、沸点升高。 物质熔化或气化时,要克服纯粹的分子间力外,还必须 提高温度,额外供应能量来破坏分子间的氢键,所以这些 物质的熔点、沸点比同系列氢化物的高。 分子内氢键:熔、沸点常降低。 分子内形成氢键,那么相应的分子间的作用力就会减少, 分子内氢键会使物质熔沸点降低.
第2章药物的物理化学相互作用
&1 药物的物理化学相互作用类型
一、范德华力 二、氢键 三、传荷络合作用 四、离子参与的相互作用 五、疏水相互作用
2020/6/28
2020/6/28
2
一、范德华力(Van der Waals' force )
1.取向力(dipole-dipole attration )
发生在极性分子与极性分子之间
分子的极性越大,分子间的取向力越大
2020/6/28
2020/6/28
3
2.诱导力(induction force )
存在于极性分子与非极性分子之间 还存在于极性分子与极性分子之间
2020/6/28
2020/6/28
4
3.色散力(dispersion force )
色散力与相互作用的分子变形有关,变 形越大,色散力越大。
2020/6/28
19
二、对固体制剂成型性的影响
固体制剂大多由微粉加工 · 干燥状态下固体粒子相互接触产生的范德华
力、静电力以及粉粒间接触点吸附液体薄膜的表 面张力使其发生相互的粘附,会阻碍固体物料的 混合。因此常采用交互加入少量水润湿药物或适 量表面活性剂来提高混合的效果。
2020/6/28
2020/6/28
2020/6/28
8
对粘度的影响
分子间有氢键的液体,一般粘度较 大。例如甘油、磷酸、浓硫酸等多羟基 化合物,由于分子间可形成众多的氢键, 这些物质通常为粘稠状液体。
2020/6/28
9
三、传荷络合作用
概念:电性差别比较大的两个分子相互接触时, 电子多的分子(电子供体)缺电子的分子(电 子受体)转移部分电子而结合成稳定的络合物, 称为传荷络合物;或称电子转移复合物(CTC)
疏水相互作用(Hydrophobic effect) :非极性分 子在极性水中倾向于聚集的现象。
疏水基团的相互作用在表面活性剂在水中形成胶 束的中起着重要作用
2020/6/28
2020/6/28
13
&2 药物的物理化学作用对药物性质的影响
我们知道胶束的形成是通过疏水作用力; 在溶液剂设计加入助溶剂其原理是通过与药
色散力存在于极性分子与极性分子之间、 极性分子与非极性分子之间、非极性分子 与非极性分子之间。
2020/6/28
2020/6/28
5
二、氢键(hydrogen bond)
分子间氢键
分子内氢键
2020/6/28
2020/6/28
6
氢键对药物性质的影响
氢键对物质溶解度的影响
在极性溶剂中,如果溶质分子与溶剂分子之 间可以形成氢键,则溶质的溶解度增大。
相容性:Compatibility 考察药品包装材料与药物之间是否发生迁
移或吸附等现象,进而影响药物质量而进 行的一种试验 。 可控环境 实验模型 相互的或单方面的迁移、变质
2020/6/28
2020/6/28
23
玻璃容器相容性试验重点考察项目
