铁三角的转化关系及应用优秀课件
人教版高中化学必修第一册精品课件 第3章 铁 金属材料 微专题5 “铁三角”的相互转化及应用

专题阐释 1.从物质类别和元素价态角度建构铁及其化合物的“价—类”二维图
例1 部分含铁物质的“价—类”二维图关系如图所示。下列推断不合理的 是( D ) A.c既可被氧化,也可被还原 B.a可与f反应生成c C.通过化合反应或复分解反应均能直接得到e D.g→e的转化能由一步反应实现
解析 根据含铁物质的“价—类”二维图关系可知a是Fe,b是FeO,c是亚铁盐,d是
4.某工厂的工业废水中含有大量的Fe2+、Fe3+、Cu2+和少量Na+。工厂计划 从该废水中回收硫酸亚铁和金属铜,设计如下流程。
下列说法正确的是( B ) A.加入过量A,发生的反应均为置换反应 B.固体B为混合物而固体E为纯净物 C.物质D既可以用稀硫酸也可以用稀盐酸 D.滤液C和滤液F组成完全相同
专题精练
1.[2023辽宁辽阳高一期中]向含有一定物质的量的FeCl3和CuCl2的混合溶 液中逐渐加入Fe粉至过量,该溶液的质量随加入铁粉的质量的变化关系图 为( A )
解析 FeCl3和CuCl2的混合溶液中逐渐加入Fe粉至过量,可先后发生反 应:2FeCl3+Fe ══ 3FeCl2、CuCl2+Fe ══ FeCl2+Cu。Fe先与FeCl3溶液反应, 溶液的质量增加,FeCl3反应完全后再与CuCl2溶液反应,由于Fe的相对原子 质量小于Cu的相对原子质量,导致溶液质量减小,当FeCl3和CuCl2全部反应 完全,溶液质量保持不变,故A图像正确。
铁三角转化及应用

铁三角转化及应用铁三角是一个经济学上的概念,指代三个旨在维护自身利益的角色:政府、企业和工会。
为了实现某些目标,这三方面通常会密切合作。
然而,这种紧密的合作常常会导致利益共享的问题,以及对消费者和其他利益相关者的剥夺。
在这个概念中,政府通常会通过制定政策来监管企业和工会的活动。
企业则会利用政府的支持,为自己谋取更多的利益并保护自己免于竞争。
工会则通过与政府和企业合作,获取更好的工资和福利,并确保劳动者得到公正的待遇。
铁三角可以定义为一个由政府、企业和工会组成的利益集团,他们会通过合作来影响政策制定过程,并谋求自己的利益。
虽然这种合作对于某些方面有利,但对于社会福利和公正有害。
铁三角的存在导致了很多问题。
它们通常不关注消费者的利益,而是旨在实现自己的目标。
政府和企业的合作可以导致政府政策的不公正,而工会则可能会在劳资谈判中获得更高的工资和福利,这最终会导致生产成本的上升。
铁三角的存在也就意味着利益的过度保护,这样可能会导致消费者的需要和利益被忽视。
铁三角还认为政府应该为他们服务,这意味着政府资源的过度使用,并削弱了公共服务和社会基础设施。
然而,铁三角也可以有一些优点。
政府可以通过与企业和工会合作来更好地监管企业的活动,确保企业的行为符合法律规定。
工会也能够确保劳动者得到合理的待遇和福利。
企业则可以更好地了解政策制定过程,以便更好地谋求自己的利益。
铁三角的最大问题在于,他们通常会通过利用彼此之间的势力来谋求自己的利益,以及在政策制定过程中剥夺其他利益相关者的权益。
为了解决这一问题,我们需要寻找其他形式的合作,以更好地实现公共利益和社会公正。
我们可以使用其他的办法来代替铁三角。
例如,政策制定者应该以全社会的利益为先,而非铁三角内部的利益。
政府应该与企业和工会的民间组织进行对话,以更好地理解公民的需要和合法要求。
在劳资谈判中,应着眼于结果的良好表现,而不是颠覆现有的社会协议。
企业也需要公正的机制,来确保消费者得到高质量的产品和服务。
铁三角的构建及应用(课件) -高一化学人教版(2019)必修第一册

2.补铁剂中的Fe2+在空气中很容易被氧化成Fe3+, 影响铁元素在人体中的吸收利用。如何检验补 铁剂是否部分变质?
【思考与交流】 3.为什么补铁剂与维生素C一起服用效果更好?验证补铁剂和维生素C一起服 用的科学性。
缺铁性贫血患者应补充 Fe2+ ,一些补铁剂用硫酸亚铁 制成药片时,外表包有一层特殊的糖衣,推测糖衣的作 用是_______。
二、铁极其化合物转化关系的应用
应用一:含Fe2+、Fe3+的分离、除杂方法
(1)如何除去FeCl2溶液中的少量Fe3+,写出有关反应的离子方程式。实验室中 应该怎样保存亚铁盐溶液?
一、运用价类二维图构建铁极其化合物的转化关系
资料卡片 硫酸亚铁补铁剂的有效成分 为Fe2+, Fe2+有助于人体内红 细胞执行功能,它会与氧发 生可逆反应结合,在人体内 形成氧合血红蛋白,因此, Fe2+有造血、载氧能力
如何制备补铁剂的主要成分——硫酸亚铁?请你写出尽可能多的化学方程式。
【思维建模】 运用价类二维图可从元素价态和物质类别两个角度可设计铁及其化合物的转化路径
转化思路
转化路径
价态转化
物质类别转 化
SO2 H2S S2- SO32- I-
Fe、Fe2+、Fe3+相互转化 氧化剂
还原性 O2、Cl2、Br2、 KMnO4 HNO3 H2O2
Fe2+
Fe3+
氧化性
还原剂
氧化性
Fe Cu SO2 H2S S2- SO32- I-
还原性
Fe
【思考与交流】
1.如何检验补铁剂中的铁元素的存在形式? 描述实验操作和现象。
《高二化学铁三角》课件

感谢观看
总结词:探究铁三角的性质和应用。
实验步骤
1. 将制备好的铁单质与浓硝酸反应,观察反应现象。
2. 将铁的氧化物与稀硫酸反应,观察反应现象。
实验结果:通过实验观察到铁单质与浓硝酸反应生成了氮气和二氧化氮,而铁的氧化物与稀硫酸反应可以生成相应的盐类和水。这些性质在化学工业和日常生活中有着广泛的应用。
01
04
铁三角的实验探究
总结词:通过实验探究,了解铁三角的制备方法。
实验步骤
1. 准备实验器材和试剂,如试管、烧杯、铁粉、氧化铜、硫酸等。
2. 将铁粉和氧化铜混合后放入试管中,加入适量的稀硫酸,观察反应现象。
3. 加热试管,观察反应速度和产物的变化。
实验结果:通过实验观察到铁粉和氧化铜在稀硫酸的作用下反应生成了铁的氧化物和铜的氧化物,加热后反应速度加快,生成物颜色发生变化。
02
03
04
05
05
铁三角的习题与解析
解析铁三角的概念
解析铁三角的转化
解析铁三角的应用
解析铁三角的实验
01
02
03
04
解释铁三角的定义、组成和性质,说明其在化学反应中的作用。
分析铁三角各物质之间的转化关系,说明转化的条件和原理。
解释铁三角在实际生产和生活中的应用原理,说明其重要性和意义。
分析实验设计的合理性和可行性,给出实验操作步骤和注意事项。
03
铁三角的化学性质
铁是一种过渡金属,具有多种化合价,如+2和+3价。
铁在常温下不易氧化,但在潮湿环境中容易生锈。
铁可以与酸、盐等发生置换反应,生成成铁离子。
亚铁离子在碱性溶液中不稳定,容易生成沉淀。
“铁三角”转化及应用
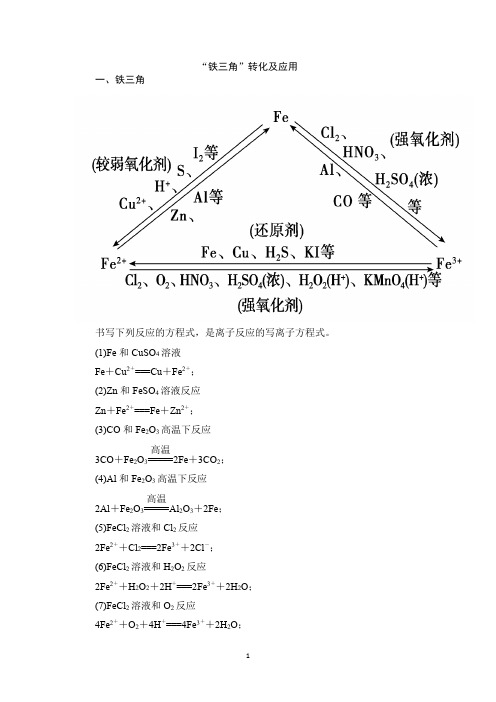
“铁三角”转化及应用一、铁三角书写下列反应的方程式,是离子反应的写离子方程式。
(1)Fe 和CuSO 4溶液Fe +Cu 2+===Cu +Fe 2+; (2)Zn 和FeSO 4溶液反应Zn +Fe 2+===Fe +Zn 2+;(3)CO 和Fe 2O 3高温下反应3CO +Fe 2O 3=====高温2Fe +3CO 2;(4)Al 和Fe 2O 3高温下反应2Al +Fe 2O 3=====高温Al 2O 3+2Fe ;(5)FeCl 2溶液和Cl 2反应2Fe 2++Cl 2===2Fe 3++2Cl -;(6)FeCl 2溶液和H 2O 2反应2Fe 2++H 2O 2+2H +===2Fe 3++2H 2O ;(7)FeCl 2溶液和O 2反应4Fe 2++O 2+4H +===4Fe 3++2H 2O ;(8)FeCl3溶液和Cu反应2Fe3++Cu===2Fe2++Cu2+;(9)FeCl3溶液和H2S反应2Fe3++H2S===S↓+2Fe2++2H+;(10)FeCl3溶液和KI反应2Fe3++2I-===2Fe2++I2;(11)FeCl2和稀HNO3反应3Fe2++4H++NO-3===3Fe3++NO↑+2H2O。
1.怎样保存含Fe2+、Fe3+的溶液?提示:(1)含Fe2+的溶液:加入少量铁粉(或铁钉、铁屑),防止Fe2+被氧化;加入少量相应的酸,防止Fe2+水解[Fe(NO3)2例外]。
(2)含Fe3+的溶液:加入少量相应的酸,防止Fe3+水解。
2.怎样用FeCl3溶液制备无水FeCl3?提示:在HCl气流中加热浓缩FeCl3溶液。
3.如何除去酸性MgCl2溶液中的Fe2+?提示:先加H2O2把Fe2+氧化为Fe3+,然后加入MgO[或Mg(OH)2或MgCO3]调节溶液的pH,使Fe3+完全水解生成Fe(OH)3沉淀,然后过滤除去。
4.向FeSO4溶液中加入Na2O2固体,有什么现象?试写出反应的离子方程式。
专题:铁三角的转化及应用

专题(4)铁三角的转化核心知识点一:一、“铁三角”1. Fe、Fe2+和Fe3+之间相互转化从Fe、Fe2+和Fe3+的结构可知:Fe只有还原性,Fe3+通常只有氧化性,Fe2+既具有氧化性又具有还原性。
上述微粒通过跟一定的氧化剂或还原剂发生氧化还原反应,才能实现不同价态的铁相互转化,如下图(常称为铁三角):(1)Fe→Fe2+或Fe3+①与弱氧化剂反应生成Fe2+与S、Fe3+、Cu2+、H+等弱氧化剂反应生成+2价的铁,例如:Fe+2Fe3+=3 Fe2+Fe+ Cu2+= Cu+ Fe2+Fe+2 H+= Fe2++ H2↑②与强氧化剂反应生成Fe3+与Cl2、Br2、HNO3(浓、稀)等强氧化剂反应生成+3价的铁,例如:2Fe+3Cl22FeCl3Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O(2)Fe2+→Fe3+或Fe①与氧化剂反应生成Fe3+与Cl2、HNO3(浓、稀)等强氧化剂反应生成+3价的铁,例如:2Fe2++Cl2=2Fe3++2Cl-②与还原剂反应生成Fe与C、Al、Zn、CO、S2-等还原剂反应生成铁单质,例如:Fe2++ Zn= Zn2+ + Fe(3)Fe3+→Fe或Fe2+①与还原剂反应生成Fe与C、Al、CO等还原剂反应生成铁单质,例如:Fe2O3+3CO2Fe+3CO2②与还原剂反应生成Fe2+与Fe、Cu、I-、S2-等还原剂反应生成Fe2+,例如:2Fe3++ Cu= 2Fe2+ + Cu2+注意:Fe3+、Fe2+、Fe的相互转化,可以应用于试剂的保存、配制和除杂,如配制硫酸亚铁溶液时加入少量的铁粉以防止Fe2+被氧化。
2. “铁三角”的应用:(1)判断离子共存:Fe2+与(H+)、ClO−、(H+),Fe3+与S2−、I−、HS−、在溶液中因发生氧化还原反应而不能大量共存。
(2)除杂方法(括号内为杂质):Fe2+(Fe3+):加过量铁粉,过滤;FeCl3(FeCl2):加氯水或H2O2;FeCl2(CuCl2):加过量铁粉,过滤;Fe(Al)、Fe2O3(Al2O3、SiO2):加过量强碱溶液,过滤;(3)盐溶液的保存:亚铁盐溶液——加入少量铁屑以防止Fe2+被氧化。
“铁三角”团队模式知识培训PPT课件

AR在铁三角团队中起着统筹规划和管理的功能, 负责项目整体规划、客户平台建设、经营指标 的实现、客户需求的达成和体验的优化,以及 客户/项目(群)铁三角组织模式的运作等内容, 是企业一线共同作战单元的大脑和协调者,并 对市场竞争的成败负有直接和第一责任。
★ 作为管理者和客户经理,负责领导面向客户的项目铁三角团队,是项目全流程运作的责任主体,并对客 户/项目的具体运营结果(格局、增长、盈利、现金流等)承担总责;
客户经理/系统部部长 (AccountResponsi
bility,AR)
产品/服务解决方案经理 (SolutionResponsibili
ty,SR)
交付管理和订单履行经理 (FulfillResponsibility,
FR)
客户经理/系统部部长 (AccountResponsibility,AR)
★ 作为客户群规划的制定者和执行者,需要具有敏锐的洞察力,基于对市场的精准判断制定最佳的目标和 策略,及时调整执行规划,并负责品牌塑造和推广等事务;
★ 作为销售项目的领导者,要根据项目销售需要组建和领导团队,制定合适的目标与策略,对执行过程和 效果进行监督把控,实现优质高效的竞争管理;
★ 作为全流程交易质量的责任者,需要完成线索管理、对机会与风险的识别和管理、质量监管、合同履行 效果的监控、工程交付、项目收入和回款等多方面的工作;
TEAMBUILD ING
ห้องสมุดไป่ตู้“铁三角“ 团队模式
team building management team building managementmanagement team building management
相互信任 承担责任 共同目标
“ 我们系统部的铁三角,其目的就是发现机 会,咬住机会,将作战规划前移,呼唤与组 织力量,实现目标的完成。系统部里的三角 关系,并不是一个三权分立的制约体系,而 是紧紧抱在一起生死与共,聚焦客户需求的 共同作战单元。”
“铁三角”的转化关系及应用 (1)

“铁三角”的转化关系及应用“铁三角”的转化关系深度思考Fe3+1.用离子方程式实现下列转化:Fe2+①Cl2、②NO-3(H+)③Fe、④Cu①2Fe2++Cl2===2Fe3++2Cl-;②3Fe2++4H++NO-3===3Fe3++2H2O+NO↑;③2Fe3++Fe===3Fe2+;④Cu+2Fe3+===Cu2++2Fe2+。
2.如何除去括号中的杂质(1)Fe2+(Fe3+):加过量铁粉,过滤;(2)FeCl3(FeCl2):加氯水或H2O2;(3)FeCl2(CuCl2):加过量铁粉,过滤;(4)Fe(Al):加过量强碱溶液,过滤;(5)Fe2O3(Al2O3、SiO2):加过量强碱溶液过滤。
3.(1)Fe2O3加入到足量的氢碘酸中,发生反应的离子方程式(用两个表示)为______________,________________________________________________________________________。
(2)Fe(OH)3加入到足量的氢碘酸中,发生反应的离子方程式(用一个表示)为__________。
答案(1)Fe2O3+6H+===2Fe3++3H2O2Fe3++2I-===I2+2Fe2+(2)2Fe(OH)3+6H++2I-===2Fe2++I2+6H2O题组一Fe2+与Fe3+的转化及应用1.下列试剂中,不能使Fe2+转化为Fe3+的是()①氯气②NaCl溶液③KMnO4溶液④稀硝酸⑤盐酸⑥NaNO3溶液A.①②③B.①③④C.②④⑤D.②⑤⑥答案D解析要实现Fe2+转化为Fe3+,必须加强氧化性物质,②NaCl、⑤HCl均没有强氧化性,⑥NO-3在酸性条件下才表现强氧化性。
2.在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是() A.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+B.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含Cu2+和Fe3+C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+答案D解析氧化性Fe3+>Cu2+>Fe2+,加入铁粉后有固体剩余,Fe3+一定不存在;若剩余固体全部都是Cu,溶液中还可能有Cu2+,也可能恰好被完全置换;若剩余固体是Cu和Fe,则溶液中不可能有Cu2+。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.“铁三角”中的转化关系
实验回顾
操作
现象
反应的离子方程式
FeCl3溶液
加入铁粉、 KSCN溶液
不显红色
2Fe3+ + Fe = 3Fe2+
上层清液加
入氯水,振 荡
变红色
2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
1.“铁三角”中的转化关系
1.Fe2+具有较强的还原性,与氧化剂反应生成Fe3+ (1)Fe2+被氯气氧化:_2_F_e_2_+_+__C_l_2_=_=_=_2_C_l_-_+__2_F_e_3_+_____________。 (2)Fe2+被溴水氧化:_2_F_e_2_+_+__B_r_2_=_=_=_2_B_r_-_+__2_F_e_3_+_____________。 (3)Fe2+被高锰酸钾氧化:5F_e_2_+_+__M_n_O_- 4_+__8_H__+=_=_=__5F_e_3_+_+__M_n_2_+_+__4_H_2。O (4)Fe2+被稀硝酸氧化:3_F_e_2+_+__N__O_- 3_+__4_H__+_=_=_=_3_F_e_3_+_+__N_O_↑ ___+__2_H_2。O (5)Fe2+被浓硝酸氧化:F_e_2+_+__N__O_- 3_+__2_H__+_=_=_=_F_e_3_+_+__N_O__2↑__+__H__2O__。 (6)Fe2+被氧气氧化:_4_F_e_2_+_+__O__2+__4_H__+_=_=_=_4_F__e3_+_+__2_H__2_O_______。
题热点。常见考查方式有离子共存(有色离子、形成沉淀、水解)、 铁铜实验、化工工艺流程等,主要考查的物质有Fe、Fe2+、Fe3+ 的相互转化,Fe2+的还原性、Fe3+的强氧化性和强水解能力, 并与氧化还原反应的知识联系起来考查。
P35 [例5] 水溶液中能够大量共存的一组离子是( A )
A.PH=1的溶液中:Fe3+、Cl-、Na+、SO42B.H+、Na+、Fe2+、MnO4C、在0.1 mol/L FeCl3溶液中:K+、NH4+、I-、SCND、K+、Fe3+、OH-、SO42-
①Fe3+、Fe2+与 HCO- 3 、AlO2-、CO23-等在溶液中因发生
(5)SO2 通入 FeCl3 溶液中:__________________________。 _______2_F_e_3+_+__S_O__2_+__2_H_2_O_=_=_=__2_F_e_2+_+__S_O__24_-_+__4_H_+___________
2.“铁三角”的应用 (1)判断离子共存
相互促进水解反应而不能大量共存。
②Fe2+与 NO3-(H+)、ClO-、MnO- 4 (H+),Fe3+与 S2-、 I-、HS-、SO23-在溶液中因发生氧化还原反应而不能大量
共存。 Fe3+与SCN- 发生络合反应不能大量共存。
2.“铁三角”的应用
(2)Fe2+和Fe3+的鉴别常用方法
(1)观察法:Fe3+的盐溶液呈棕黄色,Fe2+的盐溶液呈浅绿色 。 (2)SCN-法:滴入KSCN或其他可溶性硫氰化物溶液,呈 血红色的是Fe3+的盐溶液,不变色的是Fe2+的盐溶液。 (3)碱液法:分别加入碱液(如氨水),生成红褐色沉淀的是 Fe3+的盐溶液,先生成白色絮状沉淀,又迅速转变为灰绿色 ,最终变为红褐色的是Fe2+的盐溶液。 (4)KMnO4(或溴水)法:分别加入少量酸性KMnO4溶液 (或溴水),能使之褪色的是Fe2+的盐溶液,不能使之褪色 的是Fe3+的盐溶液。
2.“铁三角”的应用
(3)除杂方法(括号内为杂质)
①Fe2+(Fe3+):加过量铁粉过滤 ②FeCl3(FeCl2):加氯水或H2O2 ③FeCl2(CuCl2):加过量铁粉过滤 ④Fe(Al)、Fe2O3(Al2O3、SiO2):加过量强碱溶液过滤
铁及其化合物性质的综合考查 [考向分析]铁在生活生产中有广泛用途,是高考的命
1.“铁三角”中的转化关系
2.Fe3+有较强的氧化性,与还原剂反应生成 Fe2+ (1) Fe3+被 Fe 还原:_2_F_e_3_+_+__F_e_=_=_=__3_F_e_2+________________。 (2) Fe3+被 Cu 还原:2_F__e_3+__+__C_u_=_=_=_2_F__e_2+__+__C_u_2_+________。
【例】(2013年东北三校联考) 下列检验试剂选用正确的是( )。
A.用氯水、KSCN溶液检验FeCl3中是否有FeCl2 B.用酸性KMnO4溶液检验FeCl3中是否有FeCl2 C.用NaOH溶液检验MgCl2中是否有FeCl2 D.用硝酸检验某黄色固体是纯铜还是黄铜(铜和锌的合金) 解析:A组中的Fe3+产生的干扰无法消除;B组中酸性 KMnO4溶液还能氧化Cl-;C组中虽然Mg2+也能形成白色沉淀, 但若有Fe2+,则生成的白色沉淀颜色会发生变化,故C项正确;D 组中纯铜和黄铜均能溶解在硝酸中,不能达到目的。 答案:C
(3)FeCl3 中滴加氢硫酸,溶液变浑浊:________________ _________2_F_e_3+__+__H_2_S_=_=_=_2_F__e_2+__+__S_↓__+__2_H_+________________。
(4)Fe3+能使淀粉-KI 溶液变蓝:2_F__e3_+__+__2_I-__=_=_=_2_F_e_2_+_+_ 。I2
