内部审核计划表
年度内部质量体系审核计划表

年度第次审核
审核目的:
确定本公司按照GB/T19001:2000、YY/T0287:2003和《体外诊断试剂生产实施细则》建立的质量管理体系是否符合要求。
审核范围:
本公司生产与服务的全过程。
审核依据:
1)GB/T19001-2000;
2)YY/T0287-2003;
3)《体外诊断试剂生产实施细则》;
批准:日期:
4)其他相关的法律、法规;
5)质量管理体系文件;
6)产品审核计划:
日期
审核时间
部门
审核涉及的质量管理体系标准YY/T 0287-2003的要求
部门参加人员
审核员
首次会议
研发中心
采购部
财务部
行政人事部
生产部
仓储物流部
销售部
市场部
审核组会议
末次会议
编制:日期:
审核:日期:
CMA质量管理体系内部审核实施计划表
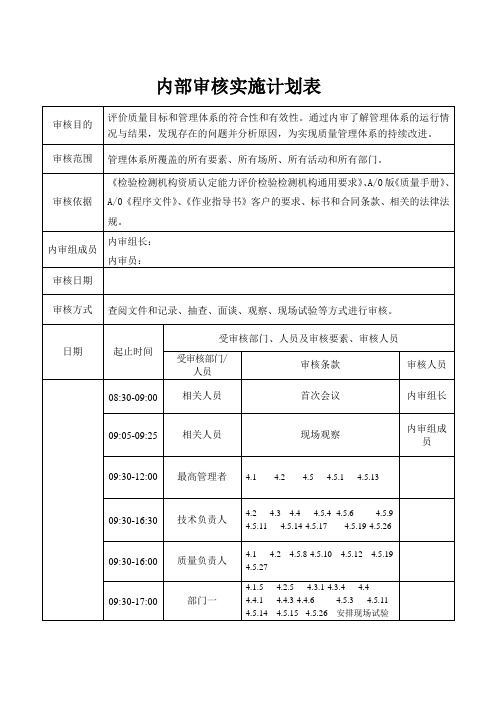
内审组长:
内审员:
审核日期
审核方式
查阅文件和记录、抽查、面谈、观察、现场试验等方式进行审核。
日期
起止时间
受审核部门、人员及审核要素、审核人员
受审核部门/
人员审核Biblioteka 款审核人员08:30-09:00
相关人员
首次会议
内审组长
09:05-09:25
相关人员
现场观察
内审组成员
09:30-12:00
最高管理者
4.14.24.54.5.1 4.5.13
09:30-16:30
技术负责人
4.24.3 4.44.5.4-4.5.64.5.94.5.114.5.14-4.5.17 4.5.19-4.5.26
09:30-16:00
质量负责人
4.14.24.5.8-4.5.104.5.12 4.5.19 4.5.27
内部审核实施计划表
审核目的
评价质量目标和管理体系的符合性和有效性。通过内审了解管理体系的运行情况与结果,发现存在的问题并分析原因,为实现质量管理体系的持续改进。
审核范围
管理体系所覆盖的所有要素、所有场所、所有活动和所有部门。
审核依据
《检验检测机构资质认定能力评价检验检测机构通用要求》、A/0版《质量手册》、A/0《程序文件》、《作业指导书》客户的要求、标书和合同条款、相关的法律法规。
09:30-10:30
与领导和受审部门交换意见
11:00-11:30
相关人员
末次会议
内审组长
编制: 审核: 批准: 日期:
(内审组组长) (质量负责人) (总经理)
09:30-17:00
部门一
4.1.54.2.54.3.1-4.3.44.44.4.1 4.4.3-4.4.64.5.34.5.114.5.144.5.15-4.5.26安排现场试验
ISO13485-2016内部审核计划表范例

ISO13485:2016内部审核计划表
审核目的对公司质量管理体系的符合性及实施的有效性进行检查,使公司质量管理体系符合规范要求,并获得ISO 13485认证证书
审核范围营业部、管理部、培训部、采购部、物料部、工艺部、研发部、品质部、生产部、计划部、体系部、设备部、客服部、工程部、研发部
依据文件《医疗器械生产质量管理规范》、ISO 9001:2015《质量管理体系要求》、ISO 13485:2016《医疗器械质量管理体系用于法规的要求》
审核组成员组长:组员:
审核安排
日期时间受审部门审核内容审核员
内审员及各部门负
责人
首次会议
管理层4.1、4.2.1、4.2.2、4.2.3、4.2.4、4.2.5、
5.1、5.2、5.3、5.4、5.5、
6.1
管理部 4.2.3、4.2.4
营业部5.2、7.2.1、7.2.2、7.2.3、7.5.4、7.5.10、8.2.1
培训部 6.2
设备部 6.3、6.4
生产部、计划部7.5.1、7.5.2、7.5.3、7.5.4、7.5.5、7.5.6、7.5.7、7.5.8、7.5.9
工艺部、研发部7.1、7.3
工程部7.2
采购部、物料部7.4.1、7.4.2、7.4.3、7.5.3、7.5.4
品质部、体系部7.4.3、7.6、8.2.3、8.2.4、8.3、8.4、8.5.2、
8.5.3
客服部7.2.3
内审员审核组内部总结
内审员及各部门负
末次会议
责人
编制人∕日期:批准人∕日期:。
内部审核实施计划表
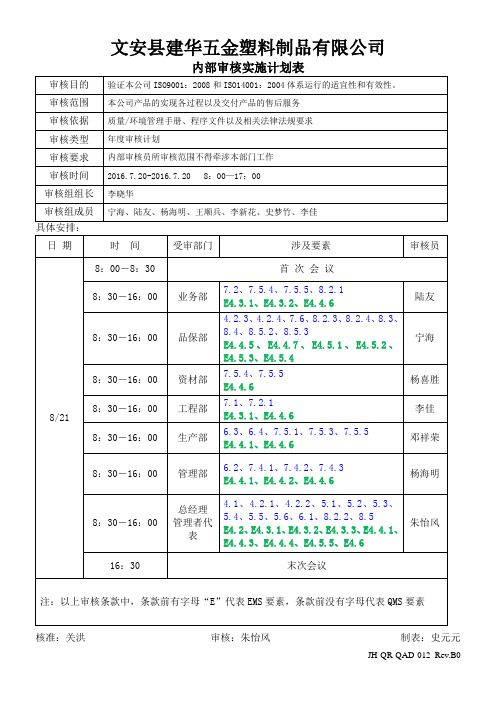
验证本公司ISO9001:2008和ISO14001:2004体系运行的适宜性和有效性。
审核范围
本公司产品的实现各过程以及交付产品的售后服务
审核依据
质量/环境管理手册、程序文件以及相关法律法规要求
审核类型
年度审核计划
审核要求
内部审核员所审核范围不得牵涉本部门工作
审核时间
2016.7.20-2016.7.208:00—17:00
E4.4.1、E4.4.6
邓祥荣
8:30-16:00
管理部
6.2、7.4.1、7.4.2、7.4.3
E4.4.1、E4.4.2、E4.4.6
杨海明
8:30-16:00
总经理
管理者代表
4.1、4.2.1、4.2.2、5.1、5.2、5.3、5.4、5.5、5.6、6.1、8.2.2、8.5
E4.2、E4.3.1、E4.3.2、E4.3.3、E4.4.1、E4.4.3、E4.4.4、E4.5.5、E4.6
E4.4.5、E4.4.7、E4.5.1、E4.5.2、E4.5.3、E4.5.4
宁海
8:30-16:00
资材部
7.5.4、7.5.5
E4.4.6
杨喜胜
8:30-16:00
工程部
7.1、7.2.1
E4.3.1、E4.4.6
李佳
8:30-16:00
生产部
6.3、6.4、7.5.1、7.5.3、7.5.5
朱怡风
16:30
末次会议
注:以上审核条款中,条款前有字母“E”代表EMS要素,条款前没有字母代表QMS要素
核准:关洪审核:朱怡风制表:史元元
审核组组长
李晓华
审核组成员
2内部审核实施计划表

南京汤峰机电有限公司
版本 A/0
内部审核实施计划表
一目的:
验证本公司的质量管理体系是否符合ISO9001:2015和本公司建立的质量管理体系要求、是否得到了正确的实施和保持,及时发现质量管理体系在执行中存在的问题,并采取必要的纠正与预防措施,以保持质量管理体系的有效性和符合性。
二范围:机电产品(手持式电动工具、园林工具)的设计、生产和销售(许可产品除外)三依据:
ISO9001:2015质量管理体系要求、相关法律法规、产品标准、本公司的质量手册、程序文件、作业指导书、合同等。
四日期安排:2016年9月8日
8日8:30-9:00 内审前会议 9:00-16:30 各部门审核其中12:00-13:00午餐休息16:00-16:30内审后会议
五审核组成人员名单:袁长城、仲春雨、程永辉审核组长:袁长城
注:9.3 (ISO9001:2015)管理评审于2016-9-20再查。
批准:卢国峰审核:袁长城制定:仲春雨日期:2016-9-1
表单编号TF4-37。
内部质量体系审核整改计划表

05年9月12日
75
样件检验报告(材料,尺寸,外观,性能)。
徐盛风
05年9月12日
76
OTS交样
徐盛风
05年9月12日
77
小组可行性承诺
徐盛风
05年9月12日
78
产品、过程质量体系评审
徐盛风
05年9月12日
79
过程流程图
徐盛风
05年9月12日
80
平面布置图
徐盛风
05年9月12日
81
特性矩阵图
徐盛风
67
材料规范
徐盛风
05年9月12日
68
设备清单
徐盛风
05年9月12日
69
工装、模具开发计划
徐盛风
05年9月12日
70
工装、模具清单
徐盛风
05年9月12日
71
量、检具实验设备清单
徐盛风
05年9月12日
72
产品/过程的特殊特性清单
徐盛风
05年9月12日
73
样件控制计划
徐盛风
05年9月12日
74
产品试验大岗
责任人
完成
期限
跟踪
验证人
日期
52
产品开发过程
第一阶段
无开发意向书或开发协议书
徐盛风
05年9月12日
53
无新开发建议书
徐盛风
05年9月12日
54
开新产品开发任务书
徐盛风
05年9月12日
55
无APQP项目小组职责表
徐盛风
05年9月12日
56
计划和确定项目
无新产品可行性分析报告
徐盛风
内部审核方案表
内部审核方案一、审核目的内部审核是公司自我检查和评估其管理体系有效性的过程,旨在发现潜在问题,及时采取纠正措施,确保管理体系持续改进,并符合相关法规和标准。
二、审核范围本次审核范围包括公司所有部门和业务,重点关注质量、环境、职业健康安全管理体系的有效性、合规性和实施情况。
三、审核人员本次审核由公司内部质量管理部门组织,审核人员包括质量主管、环境专员、安全专员等。
审核人员需经过培训并取得相应资格。
四、审核方法本次审核采用现场检查和文件审查相结合的方法,通过查看现场、询问员工、检查文件等方式,对管理体系的执行情况进行全面评估。
五、审核时间安排本次审核计划用时一周,分为两个阶段:第一阶段为各部门现场审核,第二阶段为汇总分析、提出整改意见并跟进整改情况。
六、审核内容1. 质量管理体系:检查质量管理体系文件的执行情况,包括质量计划、质量控制程序、问题处理程序等。
2. 环境管理体系:检查环境管理体系文件的执行情况,包括环境管理计划、环境监测程序、废物管理程序等。
3. 职业健康安全管理体系:检查职业健康安全管理体系文件的执行情况,包括安全操作规程、应急预案、安全培训等。
4. 管理体系的有效性评估:评估管理体系是否符合相关法规和标准,是否能够确保公司业务活动的合规性和有效性。
5. 管理体系的持续改进:检查管理体系的执行过程中是否存在问题,是否及时采取纠正措施并进行改进。
七、整改措施在审核过程中发现的问题和不足,将提出整改意见和建议,并要求相关部门和单位在规定时间内进行整改。
整改措施应包括改进方案、责任人、完成时间等,并需进行跟踪和验证,确保问题得到彻底解决。
八、总结报告审核结束后,将对审核结果进行汇总和分析,编写内部审核报告,包括审核范围、审核方法、审核内容、整改措施等。
报告将提交公司管理层,以便对管理体系进行持续改进和优化。
九、审核频次考虑到公司业务的复杂性和管理体系的动态性,建议每年至少进行一次内部审核,以确保管理体系的有效性和合规性。
年度内部审核计划表
填表说明:1.本表由质量管理部门填写;
2.管理者代表审核,总经理批准;
3.√表示计划时间,×审核已进行,□纠正措施已制定,★纠正措施已验证;
4.本表应在十二月份下发。
_2014年度内部审核计划表
XLWY/QR-8.2.2-01NO:
审核目的:
根据公司质量手册和程序文件要求,对正在运行的质量体系进行定期评价,检查质量体系运行是否持续有效,并为质量管理体系的改进提供依据。
审核范围:
质量管理工作各职能部门
审核依据:
1、SO9001:2008不适用条款:
2、公司质量管理体系文件、相关制度;
3、适用的法律、法规和相关方要求。
审核频次:
每两次内审时间不超过12个月
审核方式:
本年度的内部质量管理体系审核采用集中式的审核方法进行审核,审核过程中采取抽样抽样方法进行审核。
月份
部门
1
2
3
4
5
6
7
8
9
10
11
12
审核安排
综合部
√
工程部
√
安保部
√
保洁部
√
中烟大厦物管部பைடு நூலகம்
√
技术中心物管部
√
编制/日期:
审核/日期:
内部审核计划及日程表
■ 公司管理体Байду номын сангаас文件 ■ 相关法律法规
审核组名单
审核组长: 审核组员:
审核日期 2020年5月25日 至 2020年5月29日,共开展审核5个工作日
受审核部门 领导层(总经理&管理者代表)、综合部、生产部、质保部、安环部、市场部、财务部
审核方法
1、询问法:与被审核部门责任人面谈 2、书面审核:被审核部门文件规定 3、现场观察审核 4、抽样的方法
2020年5月30日至6 月6日
措施的实施和验证的要求。
纠正/预防措 施的验证
1.验证发现不符合项及建议项 部门的纠正/预防措施实施情 况。
第一次验证:2020 年6月10日; 第二次验证:2020 年6月15日
编制/日期: 审核/日期: 批准/日期:
体系组 体系组
体系管理员 体系管理员
xxx有限公司
内部审核计划表
HFQEHP-2201
Rev.:B/0
审核目的
审核公司质量、环境、职业健康安全管理体系的符合性,以确定体系是否得到有效实施与运 行,同时识别体系的薄弱环节和潜在的改进机会,不断改进体系运行的有效性和提高效率。
审核范围 xxx
审核依据
■ GB/T19001-2016/ISO9001:2015 《质量管理体系 要求》 ■ GB/T24001-2016/ISO14001:2015 《环境管理体系 要求及使用指南》 ■ GB/T45001-2020/ISO45001:2018 《职业健康和安全管理体系 要求及使用指南》 ■ 顾客要求和期望
现场审核
月29日
各部门办公室 生产现场
审核人员、 各部门负责人
末次会议
宣布审核的发现,提出不符合 项,并对不符合项进行确认。
内部审核计划表
内部审核计划
二、审核范围:
三、审核准则: 四、审核覆盖产品:
五、审核时间:
1.体系审核: 2.过程审核: 3.产品审核:
六、审核组成员:
七、内部审核行程安排:
审核日程
过程类型
过程名称
过程主要责任部门
内审员
陪审人员
备注
制造过程审核
产品审核
说明: 1.受审核部门负责人在审核本部门时,如时间有冲突请按排人员接待或陪同相关审核员; 2.COP表示顾客导向过程、MP表示管理过程、SP表示支持过程。
八、质量管理体系QMS、环境管理体系EMS、有害物质管理体系HSPM所涉及的全部过程及对应标准条款、审核 要素。
过程名称 审核部门
IATF16949:2016 ISO9001:2015
审核要素 ISO14001:2015
IECQ QC 080000:2012
九、首/末次会议:
核准APPROVED BY:
审核CHE
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2021年度内部审核方案
毕晓腾连志钢尹民贤
日期:2021/4/1 日期:2021/4/1 日期:2021/4/1
2021年度内部审核方案
毕晓腾审核: 连志钢尹民贤
日期:2021/4/10
审核报告
不合格报告
不合格项分布表
连志钢尹民贤
日期:2021-4-11 日期:2021-4-11
内审首(末)次会议签到表
会议记录
会议记录
关于质量管理体系内部审核的
通知
各部门:
为了检查公司质量管理体系运行以来的效果,确保公司质量方针和目标的实现,按照标准的要求以及公司贯标工作方案,经公司研究决定,成立审核组并进行公司质量管理体系内部审核,请做好准备工作。
一、审核组成员:
组长:唐翠华
组员:夏辛生邓斌熊波
二、审核时间:
2007年5月10日—11日
特此通知
江西贝思特科技 2007年5月1日
附:2007年度内部审核方案。
