九年级化学化学式
九年级化学常见化学式和化学方程式

九年级化学常见化学式和化学方程式一、常见单质氢气H2氮气N2氯气Cl2氧气O2臭氧O3氦气He氖气Ne氩气Ar碳 C 硅Si 硫S 磷P 碘I2钾K 钙Ca 钠Na镁Mg铝Al锌Zn铁Fe 铜Cu汞Hg银Ag金Au二、化合物1、氧化物水H2O 三氧化硫SO3 一氧化碳CO二氧化碳CO2 五氧化二磷白色P2O5过氧化氢H2O2二氧化氮红棕色NO2二氧化硫SO2 氧化钙白色CaO氧化亚铁FeO 氧化铁红色Fe2O3四氧化三铁黑色Fe3O4氧化镁MgO 氧化锌ZnO 二氧化锰黑色MnO2氧化汞HgO 氧化铝Al2O3 氧化铜CuO 2、其他化合物硝酸HNO3 硫酸H2SO4 盐酸HCl 碳酸H2CO3 硫化氢H2S氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙Ca(OH2 氢氧化镁Mg(OH2 氢氧化铝Al(OH3 氢氧化锌Zn(OH2氢氧化铁红褐色Fe(OH3氢氧化亚铁Fe(OH2 氢氧化铜蓝色Cu(OH2氢氧化钡Ba(OH2 氨水NH3·H2O氯化钠NaCl 氯化铜CuCl2 氯化铝AlCl3 氯化钾KCl 氯化亚铁FeCl2 氯化铁FeCl3 氯化银AgCl 氯化钙CaCl2 氯化镁MgCl2 氯化钡BaCl2 氯化锌ZnCl2 硫酸铜CuSO4高锰酸钾暗紫色KMnO4 锰酸钾K2MnO4 氯酸钾白色KClO3碳酸钙CaCO3 硝酸钾KNO3 硝酸钠NaNO3 硝酸铁Fe(NO33硝酸亚铁Fe(NO32硝酸铝Al(NO33 碳酸钠Na2CO3碳酸钙CaCO3碳酸铵(NH42CO3碳酸氢钠NaHCO3硫酸铁Fe2(SO43 硫酸亚铁FeSO4 硝酸银AgNO3 硝酸钡Ba(NO32 硝酸铵NH4NO3 硫酸钡BaSO43、常见有机化合物C2H5OH 葡萄糖C6H12O6 甲烷CH4 乙醇(酒精)写出下列反应的化学方程式(加下划线的方程式请掌握反应的现象)点燃一、化合反应1、红磷在空气(或氧气)中燃烧:4P+5O2 2P2O5点燃2、氢气在空气中燃烧生成水:2H2+O22H2O点燃3、硫磺在空气(或氧气)中燃烧:S + O2SO2点燃4、镁条在空气(或氧气)中燃烧:2Mg + O2 2MgO点燃5、铁丝在氧气中燃烧:3Fe + 2O2 Fe3O4点燃6、木炭在空气(或氧气)中完全燃烧:C + O2 CO2点燃7、木炭不充分燃烧:2C + O2 2CO点燃8、一氧化碳燃烧:2CO + O2 2CO29、二氧化碳、二氧化硫三氧化硫分别和水反应生成相应的酸: CO2+ H2O == H2CO3 SO2+ H2O == H2SO3(亚硫酸)SO3 + H2O == H2SO4高温10、二氧化碳通过灼热的炭层:CO2+ C 2CO11、生石灰与水反应:CaO + H2O == Ca(OH2△二、分解反应12、高锰酸钾制氧气:2KMnO4K2MnO4+ MnO2+ O2↑△13、氯酸钾制氧气:2KClO3 2KCl + 3O2↑MnO214、双氧水制氧气:2H2O2 2H2O + O2↑通电通电15、电解水:2H2O 2H2↑+ O2↑16、碳酸分解:H2CO3 H2O + CO2↑高温17、高温煅烧石灰石:CaCO3 CaO +CO2↑三、置换反应18、铜和硝酸银溶液反应:Cu + 2AgNO3 == 2Ag + Cu(NO3219、铁和硫酸铜溶液反应:Fe + CuSO4 == Cu + FeSO420、锌、铁、镁、铝分别和硫酸反应:Zn + H2SO4 == ZnSO4 + H2↑Fe + H2SO4 == FeSO4 + H2↑Mg + H2SO4 == MgSO4 + H2↑2Al + 3H2SO4 == Al2(SO43 + 3H2↑21、锌、铁、镁、铝分别和盐酸反应:Zn + 2HCl == ZnCl2 + H2↑Fe + 2HCl == FeCl2+ H2↑Mg + 2HCl == MgCl2 + H2↑2Al + 6 HCl == 2AlCl3 + 3H2↑高温22、木炭还原氧化铁:3C + 2Fe2O3 4Fe + 3CO2↑高温木炭还原氧化铜:C + 2CuO 2Cu + CO2↑四、复分解反应(一)酸 + 碱→ 盐 + 水23、氢氧化钠分别与盐酸、硫酸反应:NaOH + HCl == NaCl + H2O2NaOH + H2SO4 == Na2SO4 + 2H2O24、氢氧化铜分别与盐酸、硫酸反应:Cu(OH2 + 2HCl == CuCl2 + 2H2O Cu(OH2 + H2SO4 == CuSO4 + 2H2O25、氢氧化铝治疗胃酸过多:Al(OH3 + 3HCl == AlCl3 + 3H2O26、氢氧化镁分别与盐酸、硫酸反应:Mg(OH2 + 2HCl == MgCl2 + 2H2O Mg(OH2 + H2SO4 == MgSO4 + 2H2O27、氢氧化铁分别与盐酸、硫酸反应:Fe(OH3 + 3HCl == FeCl3 + 3H2O Fe(OH3 + 3 H2SO4 == Fe2(SO43 + 3H2O28、氢氧化钙分别与盐酸、硫酸反应:Ca(OH2 + 2HCl == CaCl2 + 2H2O Ca(OH2 + H2SO4 == CaSO4 + 2H2O(二)酸 + 盐→ 另一种酸 + 另一种盐29、盐酸与硝酸银溶液反应:HCl + AgNO3 == AgCl↓+ HNO330、氯化钡溶液与硫酸溶液反应:BaCl2 + H2SO4 == BaSO4↓+ 2HCl31、碳酸钠与稀盐酸:Na2CO3 + 2HCl == 2NaCl+ H2O + CO232、石灰石与稀盐酸反应制取二氧化碳:CaCO3+2HCl = CaCl2+H2O+CO233、碳酸氢钠用于治疗胃酸过多:NaHCO3 + HCl == NaCl+ H2O + CO234、碳酸钡与盐酸反应:BaCO3+2HCl = BaCl2+H2O+CO2(三)碱溶液 + 盐溶液→ 另一种碱 + 另一种盐35、硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2NaOH = Na2SO4+Cu(OH2↓36、氯化铁溶液和氢氧化钠溶液反应:FeCl3+3NaOH==Fe(OH3↓+3NaCl37、碳酸钠溶液和石灰水反应:Na2CO3+ Ca(OH2== CaCO3↓+2NaOH(四)盐溶液 + 盐溶液→ 两种新盐38、硝酸银溶液与氯化钠溶液反应:AgNO3 + NaCl == AgCl↓+ NaNO339、氯化钡溶液与碳酸钠溶液反应:BaCl2+ Na2CO3 = BaCO3↓+ 2NaCl40、氯化钡溶液与硫酸钠溶液反应:BaCl2+ Na2SO4 = BaSO4↓+ 2NaCl(五)金属氧化物 + 酸→ 盐 + 水41、稀盐酸或稀硫酸清洗铁锈:6HCl + Fe2O3 == 2FeCl3 + 3H2OFe2O3 + 3 H2SO4 == Fe2(SO43 + 3H2O42、氧化铜分别与稀硫酸、稀盐酸反应:CuO + H2SO4== CuSO4+ H2OCuO + 2HCl == CuCl2 + 2H2O五、其他反应类型43、二氧化碳通入澄清石灰水中:CO2 + Ca(OH2 == CaCO3↓+ H2O(验证二氧化碳)44、二氧化碳与氢氧化钡反应:CO2 + Ba(OH2 == BaCO3↓+ H2O45、氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3 + H2O(吸收二氧化碳)46、氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH ==Na2SO3+ H2O (用于吸收二氧化硫)(亚硫酸钠)47、氢氧化钠溶液吸收三氧化硫:SO3 + 2NaOH ==Na2SO4+ H2O48、三氧化硫与氢氧化钡反应:SO3+ Ba(OH2 == BaSO4↓+ H2O △49、一氧化碳还原氧化铜:CO + CuO Cu + CO2△50、一氧化碳还原氧化铁:3CO + Fe2O3 2Fe+3CO2点燃51、酒精燃烧:C2H5OH + 3O2 2CO2 + 3H2O52、甲烷燃烧:CH4 + 2O2 CO2 + 2H2O。
人教版九年级化学化学式汇总.doc
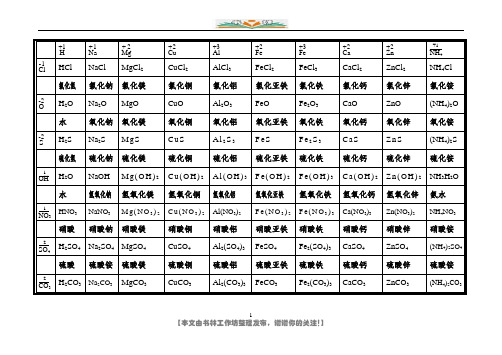
1H +1Na +1Mg +2Cu +2Al +3Fe +2Fe +3Ca +2Zn +2+1NH 4Cl -1HCl NaCl MgCl 2 CuCl 2 AlCl 3 FeCl 2 FeCl 3 CaCl 2 ZnCl 2 NH 4Cl氯化氢 氯化钠 氯化镁 氯化铜 氯化铝 氯化亚铁 氯化铁 氯化钙 氯化锌 氯化铵 O -2H 2O Na 2OMgOCuO Al 2O 3 FeO Fe 2O 3 CaO ZnO (NH 4)2O水 氧化钠 氧化镁 氧化铜 氧化铝 氧化亚铁 氧化铁 氧化钙 氧化锌 氧化铵 S -2H 2S Na 2SM gSC uS A l 2S 3 F e S F e 2S 3 C aS Zn S (NH 4)2S硫化氢 硫化钠 硫化镁 硫化铜硫化铝硫化亚铁硫化铁硫化钙硫化锌硫化铵-1OHH 2O NaOH M g(O H )2 C u (O H )2 A l (OH )3 F e (O H )2 F e (O H )3 C a (OH )2 Zn (O H )2 NH 3H 2O水氢氧化钠氢氧化镁氢氧化铜氢氧化铝氢氧化亚铁氢氧化铁氢氧化钙氢氧化锌氨水-1NO 3 HNO 3NaNO 3M g(N O 3)2 C u (N O 3)2 Al(NO 3)2 F e (N O 3)2 F e (N O 3)3 Ca(NO 3)3Zn(NO 3)2NH 4NO 3硝酸 硝酸钠 硝酸镁 硝酸铜 硝酸铝 硝酸亚铁 硝酸铁 硝酸钙 硝酸锌 硝酸铵-2SO 4 H 2SO 4 Na 2SO 4 MgSO 4CuSO 4 Al 2(SO 4)3 FeSO 4 Fe 2(SO 4)3 CaSO 4 ZnSO 4 (NH 4)2SO 4硫酸 硫酸铵 硫酸镁 硫酸铜 硫酸铝硫酸亚铁硫酸铁 硫酸钙 硫酸锌 硫酸铵-2CO 3 H 2CO 3 Na 2CO 3 MgCO 3CuCO 3Al 2(CO 3)3 FeCO 3Fe 2(CO 3)3CaCO 3ZnCO 3(NH 4)2CO 32碳酸碳酸钠 碳酸镁碳酸铜碳酸铝碳酸亚铁碳酸铁碳酸钙碳酸锌碳酸铵H +1Na +1Mg +2Cu +2Al +3Fe +2Fe +3Ca +2Zn +2+1NH 4Cl -1氯化氢 氯化钠 氯化镁 氯化铜 氯化铝 氯化亚铁 氯化铁 氯化钙 氯化锌 氯化铵 O -2水 氧化钠 氧化镁 氧化铜 氧化铝 氧化亚铁 氧化铁 氧化钙 氧化锌 氧化铵 S -2硫化氢 硫化钠 硫化镁 硫化铜 硫化铝 硫化亚铁 硫化铁 硫化钙 硫化锌 硫化铵 -1OH水氢氧化钠氢氧化镁氢氧化铜氢氧化铝氢氧化亚铁氢氧化铁氢氧化钙氢氧化锌氨水-1NO 3硝酸 硝酸钠 硝酸镁 硝酸铜 硝酸铝 硝酸亚铁 硝酸铁 硝酸钙 硝酸锌 硝酸铵-2SO 4硫酸 硫酸铵 硫酸镁 硫酸铜硫酸铝硫酸亚铁硫酸铁硫酸钙硫酸锌硫酸铵3-2CO 3碳酸碳酸钠 碳酸镁碳酸铜碳酸铝碳酸亚铁碳酸铁碳酸钙碳酸锌碳酸铵H +1Na +1Mg +2Cu +2Al +3Fe +2Fe +3Ca +2Zn +2+1NH 4Cl -1HCl NaCl MgCl 2 CuCl 2 AlCl 3 FeCl 2 FeCl 3 CaCl 2 ZnCl 2 NH 4ClO -2H 2O Na 2O MgO CuO Al 2O 3 FeO Fe 2O 3 CaO ZnO (NH 4)2OS -2H 2S Na 2S M gS C uS A l 2S 3 F e S F e 2S 3 C aS Zn S (NH 4)2S-1OHH 2O NaOH M g(O H )2 C u (O H )2 A l (OH )3 F e (O H )2 F e (O H )3 C a (OH )2 Zn (O H )2 NH 3H 2O-1NO 3 HNO 3NaNO 3M g(N O 3)2 C u (N O 3)2 Al(NO 3)2 F e (N O 3)2 F e (N O 3)3 Ca(NO 3)3Zn(NO 3)2NH 4NO 3-2SO 4 H 2SO 4 Na 2SO 4 MgSO 4CuSO 4Al 2(SO 4)3FeSO 4Fe 2(SO 4)3CaSO 4ZnSO 4(NH 4)2SO 4-2H2CO3Na2CO3MgCO3CuCO3Al2(CO3)3FeCO3Fe2(CO3)3CaCO3ZnCO3(NH4)2CO3 CO34。
九年级上册化学必须记住的化学式和化学方程式化合价

九年级上册化学必须记住的化学式一、单质的化学式:(24个)1、气态非金属单质:氧气O2、氮气N2、氢气H2、氯气Cl22、固态非金属单质:碳C 、磷P、硫S、硅Si3、稀有气体单质:氦He、氖Ne、氩Ar4、金属单质:铁Fe、铜Cu、锌Zn、铝Al、银Ag、镁Mg、钡Ba、金Au、汞Hg、钾K、钙Ca、锰Mn、钠Na二、化合物的化学式:(37个)1、氧化物:水H2O、二氧化碳CO2、过氧化氢H2O2、二氧化锰MnO2、一氧化碳CO、二氧化硫SO2、二氧化氮NO2、氧化铜CuO、氧化铁Fe2O3、四氧化三铁Fe3O4、氧化镁MgO、氧化钙CaO、一氧化碳CO、五氧化二磷P2O5、氧化铝Al2O3、二氧化硅SiO2、氧化汞HgO、特殊:氨气NH32、酸:硫酸H2SO4、碳酸H2CO3、盐酸HCl、硝酸HNO33、碱:氢氧化钠NaOH、氢氧化钙Ca(OH)2、氢氧化钾KOH4、盐:氯化钠NaCl、氯化钾KCl、硫酸铜CuSO4、碳酸钠Na2CO3、氯酸钾KClO3、高锰酸钾KMnO4、锰酸钾K2MnO4、碳酸钙CaCO3、硫酸亚铁FeSO4、硫酸铁Fe2(SO4)35、有机物:甲烷CH4、乙醇(俗名酒精)C2H5OH九年级上册化学必须记住的化学方程式(34个)1、镁燃烧:2Mg+O22MgO2、铁燃烧:3Fe+2O2Fe3O43、铝燃烧:4Al+3O22Al2O34、氢气燃烧:2H2+O22H2O(淡蓝色火焰)5、红磷燃烧:4P+5O22P2O56、硫粉燃烧: S+O2SO27、碳充分燃烧:C+O2CO2 8、碳不充分燃烧:2C+O22CO9、二氧化碳通过灼热碳层: C+CO22CO10、一氧化碳燃烧:2CO+O22CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO3(溶液变红)12、生石灰溶于水:CaO+H2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4·5H2O14、实验室用双氧水制氧气:2H2O2 2H2O+O2↑15、加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑16、水在直流电的作用下分解:2H2O 2H2↑+O2↑ 17、碳酸不稳定而分解:H2CO3==H2O+CO2↑18、高温煅烧石灰石(二氧化碳工业制法):CaCO3 CaO+CO2↑19、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu(湿法炼铜的反应原理)20、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑21、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑ 22、氢气还原氧化铜:H2+CuO Cu+H2O23、木炭还原氧化铜:C+2CuO 2Cu+CO2↑24、水蒸气通过灼热碳层:H2O+C H2+CO(水煤气)25、焦炭还原氧化铁:3C+2Fe2O34Fe+3CO2↑26、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO4(蓝色沉淀)27、甲烷在空气中燃烧:CH4+2O2 CO2+2H2O (蓝色火焰)28、酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O29、一氧化碳还原氧化铜:CO+CuO Cu+CO230、一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO231、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O(变浑浊)32、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O33、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO234、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+2HCl==2NaCl+H2O+CO2↑化合价正一钾钠和氢银,正二钙铜镁钡锌,铝三硅四氧负二,铁变二三碳二四,氟氯溴碘负一价, 单质零价永不变。
九年级化学全册 化学式和化学方程式汇总

九年级化学全册化学式和化学方程式汇总单质化合物酸盐有机物其他:氨气NH3常见物质的俗名常见的化学方程式说明:用楷体标示的内容不是重点。
化合反应•••••••••••••••红磷在空气中燃烧,产生白烟:4P+5O2—白磷自燃:4P+5O2=2P.O<木炭充分燃烧:C+O2—CO2木炭不充分燃烧:2C+O2堂暨2CO硫在空气(氧气)中燃烧:S+O o-SO2铁丝在氧气中燃烧:3Fe+2O o—Fe3O4铝在氧气中燃烧:4A1+3O2—2A12O3铝不易生锈的原因:4Al+3O.=2Al2O3镁在空气中燃烧:2Mg+O o—2MgO铜在空气中加热:2Cu+O2-2CuO氢气在氧气中燃烧:2H2+O詈2H2O将CO2变成CO:C+CO2-2CO氧化碳溶于水形成碳酸:CO2+H2O=H2CO32P2O5用生石灰制取熟石灰:CaO+H2O=Ca(OH)2一氧化碳燃烧:2CO+O2-2CO2向澄清的石灰水中通入过量的二氧化碳,变浑浊的石灰水又变澄清:CaCO3+CO2+H2O=Ca(HCO3)2氢气在氯气中燃烧:亘整占燃钠在氯气中燃烧:—镁在氮气中燃烧:工暨(注意氮元素的化合价)上面三个化学方程式给我们的启示是:燃烧不一定有氧气参与。
分解反应汞在空气中加热:2Hg+O.=^=2HgO氧化汞加强热:2HgO-2Hg+OJ分解过氧化氢制取氧气(实验室制取氧气的反应原理之一):2H2O2胆必2H2O+OJ加热高锰酸钾制取氧气(实验室制取氧气的反应原理之一):2KMnO^JLK2MnO4+MnO2+OJ加热氯酸钾制取氧气(实验室制取氧气的反应原理之一):2KClO3喽2KC1+302T••••••••分解过氧化氢制取氧气符合绿色化学的观念,是三种方案中最安全、最节约资源的一种。
电解水生成氢气和氧气:2H20—2HJ+OJ工业制取生石灰和C02的反应原理:CaC03—CaO+CO.T干粉灭火器的反应原理(碳酸氢钠受热分解):2NaHC03—Na2cO3+H2O+CO2T碱式碳酸铜受热分解:Cu2(0H)2C03—2CuO+H2O+COJ过氧化氢溶液不稳定,发生分解:2H2O2=2H2O+O2T碳酸不稳定,分解成水和二氧化碳:H2co3=H2O+CO2T碳铵(碳酸氢铵)“消失”并发出刺激性气味:NH4HCO3=NH3T+C02t+H20石笋、钟乳石的形成过程:CaCO3+CO2+H2O=Ca(HCO3)2Ca(HCO3)2=CaCOJ+CO2T+H2O置换反应氢气还原氧化铜:H2+CuO=^=Cu+H20木炭还原氧化铜:C+2CuO-2Cu+C02木炭还原氧化铁:3C+2Fe o O3-4Fe+3COJ水煤气的形成:C+H 2O —H 2+CO (注意没有气体生成符号实验室制取氢气的反应原理:Zn+H 2so 4=ZnSO 4+HJ 金属与稀盐酸的反应 ■ 2X +2HCl=2X Cl+H 2T(X 是+1价的金属,包括K 、Na )■ X +2HCl=X C12+H 2T (X 是+2价的金属,包括Ca 、Mg 、Zn 、Fe ) ■ 2Al+6HCl=2AlCl 3+3HJ •金属与稀硫酸的反应■ 2X +H 2SO 4=X 2sO 4+H 2t(X 是+1价的金属,包括K 、Na )■ X +H 2so 4=X SO 4+H 2T (X 是+2价的金属,包括Ca 、Mg 、Zn 、Fe ) ■ 2Al+3H 2so 4=Al 2(SO 4)3+3HJ •金属与盐溶液的反应■镁♦3Mg+2AlCl 3=3MgCl 2+2Al 3Mg+Al 2(so 4)3=3Mgso 4+2Al 3Mg+2Al(No 3)3=3Mg(No 3)2+2Al♦ Mg+X Cl2=MgCl 2+X (X 是+2价的金属,包括Zn 、Fe 、Cu ) ♦ Mg+X SO 4=MgSO 4+X (X 是+2价的金属,包括Zn 、Fe 、Cu )♦ Mg+X (NO 3)2=Mg(NO 3)2+X (X 是+2价的金属,包括Zn 、Fe 、Cu ) ♦ Mg+2AgNo 3=Mg(No 3)2+2Ag■铝 ♦ 2Al+3X Cl 2=2AlCl 3+3X (X 是+2价的金属,包括Zn 、Fe 、Cu ) ♦ 2Al+3X SO 4=Al 2(SO 4)3+3X (X 是+2价的金属,包括Zn 、Fe 、Cu ) ♦ 2Al+3X (NO 3)2=2Al(NO 3)3+3X (X 是+2价的金属,包括Zn 、Fe 、Cu ) ♦ Al+3AgNo 3=Al(No 3)3+3Ag■锌 ♦ Zn+X Cl2=ZnCl 2+X (X 是+2价的金属,包括Fe 、Cu ) ♦ Zn+X SO 4=ZnSO 4+X (X 是+2价的金属,包括Fe 、Cu )♦ Zn+X (NO 3)2=Zn(NO 3)2+X (X 是+2价的金属,包括Fe 、Cu ) ♦ Zn+2AgNo 3=Zn(No 3)2+2Ag■铁♦ Fe+CuCl 2=FeCl 2+Cu ♦ Fe+Cuso 4=Feso 4+Cu♦ Fe+Cu(No 3)3=Fe(No 3)3+Cu ♦ Fe+2AgNo 3=Fe(No 3)2+2Ag ■铜:Cu+2AgNO 3=Cu(NO 3)2+2Ag■K 、不遵循这样的置换反应,它们与盐溶液反应时,会先和水反应生成对应的碱,然后再和盐溶液反应。
九年级上册化学式

九年级上册化学式九年级上册化学式化学式是用元素符号表示纯净物组成及原子个数的式子。
分子晶体的化学式叫做分子式,可以表示这种物质的分子构成。
以下是九年级上册化学式,欢迎阅读。
1.元素符号:H He C N O F Ne Na Mg Al Si P S Cl 氢氦碳氮氧氟氖钠镁铝硅磷硫氯 Ar K Ca Mn Fe Cu Zn Ag Ba Pt Au Hg I 氩钾钙锰铁铜锌银钡铂金汞碘2.常见离子和化合物中元素的化合价:H+ Na+K+ Ag+ NH4++1价氢离子钠离子钾离子银离子铵根离子Ca2+ Mg2+ Cu2+Ba2+Zn2+Fe2+ +2价钙离子镁离子铜离子钡离子锌离子亚铁离子 Fe3+ Al3+ +3价铁离子铝离子Cl-OH- NO3--1价氯离子氢氧根离子硝酸根离子O2-SO42-CO32- -2价氧离子硫酸根离子碳酸根离子3.常见物质的化学式与名称:单质:C:碳S:硫P:磷 Fe:铁 Mg:镁 Al:铝Hg:汞 Zn:锌 Cu:铜 Ag:银 O2:氧气 H2:氧气 N2:氮气 O3:臭氧氧化物:CO:一氧化碳 CO2:二氧化碳 SO2:二氧化硫MnO2:二氧化锰SO3:三氧化硫 H2O2:过氧化氢 CuO:氧化铜 CaO:氧化钙 MgO:氧化镁HgO Fe2O3:氧化铁Al2O3:氧化铝H2O:水P2O5:五氧化二磷Fe3O4:四氧化三铁酸:HCl:盐酸H2SO4:硫酸HNO3:硝酸H2CO3:碳酸H2S亚硫酸CH3COOH:醋酸碱:NaOH:氢氧化钠 Ca(OH)2:氢氧化钙KOH:氢氧化钾Mg(OH)2:氢氧化镁Cu(OH)2:氢氧化铜NH3 .H2O氨水Fe(OH)3:氢氧化铁Al(OH)3:氢氧化铁盐酸盐:KCl:氯化钾NaCl:氯化钠KCl:氯化钾AgCl:氯化银CuCl2:氯化铜CaCl2:氯化钙MgCl2:氯化镁ZnCl2:氯化锌BaCl2:氯化钡FeCl2:氯化亚铁 AlCl3:氯化铝 FeCl3:氯化铁碳酸盐:CaCO3:碳酸钙 Na2CO3:碳酸钠 NaHCO3:碳酸氢钠 BaCO3:碳酸钡 K2CO3:碳酸钾NH4HCO3:碳酸氢铵硫酸盐:Na2SO4:硫酸钠ZnSO4:硫酸锌MgSO4:硫酸镁CaSO4:硫酸钙CuSO4:硫酸铜BaSO4:硫酸钡FeSO4:硫酸亚铁Fe2(SO4)3:硫酸铁Al2(SO4)3:硫酸铝 (NH4)2SO4:硫酸铵 Na2SO3:亚硫酸钠硝酸盐:AgNO3:硝酸银 NaNO3:硝酸钠 Cu(NO3)2:硝酸铜 KNO3:硝酸钾NH4NO3:硝酸铵 NaNO2:亚硝酸钠钾盐:KMnO4:高锰酸钾K2MnO4:锰酸钾 KClO3:氯酸钾有机化合物:C2H5OH:乙醇C6H12O6:葡萄糖 CH4:甲烷九年级化学方程式分类:1.碳充分燃烧: C+O22.碳不充分燃烧:2C+O3.一氧化碳燃烧:2CO+O24.产生一氧化碳:C+CO5.硫燃烧:S+O26.红磷燃烧: 4P+5O2O57.氢气燃烧: 2H2+O2点燃2O8.铁燃烧:3Fe+2O3O49.镁燃烧:2Mg+O10.铝燃烧: 4Al+3O2O311.甲烷燃烧:CH4+2O2+2H2O12.酒精燃烧:C2H5OH+3O2点燃2+3H2O13.呼吸原理:C6H12O6+6O26CO2+6H2O14.高锰酸钾制氧气: 2KMnO2MnO4+MnO2+O2↑15.氯酸钾制氧气: 2KClO3MnO2KCl+3O2↑△16.过氧化氢制氧气: 2H2O2 MnO2 2O +O2↑17.水通电分解: 2H2O2H2↑+O2↑19.实验室制氢气的原理:Zn+H2SO4=ZnSO4+H2↑20.镁或硫酸性质:Mg+H2SO4=MgSO4+H2↑21.铁或硫酸性质:Fe+H2SO4=FeSO4+H2↑22.铝或硫酸性质:2Al+3H2SO4=Al2(SO4)3+H2↑23.镁或盐酸性质:Mg+2HCl=MgCl2+H2↑24.锌或盐酸性质:Zn+2HCl=ZnCl2+H2↑25.铁或盐酸性质:Fe+2HCl=FeCl2+H2↑26.铝或盐酸性质:2Al+6HCl=2AlCl3+3H2↑27.酸或碱的性质:NaOH+HCl=NaCl+H2O28.酸或碱的性质:Ca(OH)2+2HCl=CaCl2+H2O29.酸或碱的性质:2NaOH+H2SO4=Na2SO4+2H2O30.酸或碱的性质:Ca(OH)2+H2SO4=CaSO4+2H2O31.制取CO2或CaCO3 作补钙药剂:CaCO3+2HCl=CaCl2+CO2↑+H2O32.碳酸盐或酸的性质:Na2CO3+2HCl=2NaCl+CO2↑+H2O33.治疗胃酸过多症的原理:NaHCO3 +HCl=NaCl+CO2↑+H2O34.氯化钠与硝酸银反应产生白色沉淀:NaCl+AgNO3=NaNO3+AgCl35.制取氢氧化钠的原理:Ca(OH)2+Na2CO3=CaCO3 +2NaOH36.氢氧化钠与硫酸铜反应产生蓝色沉淀:2NaOH+CuSO4=Na2SO4+Cu(OH)237.制取水煤气的'原理:C+H2O2+CO38.氢气还原氧化铜:H2+2O39.碳还原氧化铜:C+2CuO2↑40.一氧化碳还原氧化铜:241.氢气还原氧化铁:Fe2O3+3H2O42.碳还原氧化铁:2Fe2O3+3C2↑43.工业炼铁的原理:Fe2O3+3CO244.铁置换硫酸铜中的铜:Fe+CuSO4=Cu+FeSO445.铜置换硝酸银中的银:Cu+2AgNO3=2Ag+Cu(NO3)246.铝置换硫酸铜中的铜:2Al+3CuSO4=3Cu+Al2(SO4)347.生石灰制熟石灰:H2O+CaO=Ca(OH)2 48.碳酸不稳定:H2CO3=H2O+CO2↑49.工业制生石灰的原理:CaCO2↑50.检验CO2或澄清石灰水变浑浊原理:CO2+Ca(OH)2=CaCO3 +H2O51.烧碱变质的原理:CO2+2NaOH=Na2CO3+H2O52.碱与非金属氧化物的性质:SO2+2NaOH=Na2SO3+H2O SO3+2NaOH=Na2SO4+H2O53.非金属氧化物的性质:H2O+CO2 =H2CO3 H2O+SO2 =H2SO3 H2O+SO3 =H2SO454.除铁锈的原理或金属氧化物与酸的性质:Fe2O3+6HCl=2FeCl3+3H2O Fe2O3+3H2SO4=Fe2(SO4)3+3H2O【九年级上册化学式】。
九年级(上)化学式与化学方程式汇总

九年级(上)化学式与化学方程式汇总常见阳离子:钠离子Na+镁离子Mg2+铝离子Al3+氢离子H+(一般金属离子带正电)常见阴离子:氯离子Cl- 氧离子O2-硫离子S2- 氢氧根离子OH-硝酸根离子NO3-硫酸根离子SO42-碳酸根离子CO32-(一般非金属离子带负电)一、化学式1、单质(一)金属单质:铜:Cu铁:Fe铝:Al锌:Zn镁:Mg钙:Ca钠:Na钾:K(二)非金属固体单质:硫:S磷:P碳:C(三)稀有气体单质:氦气:He氖气:Ne氩气:Ar(四)非金属气体单质氧气:O2氢气:H2氮气:N2氯气:Cl22、化合物(一)氧化物:水:H2O一氧化碳:CO二氧化碳:CO2五氧化二磷:P2O5二氧化硫:SO2氧化铜:CuO二氧化锰:MnO2四氧化三铁:Fe3O4氧化铁:Fe2O3氧化亚铁:FeO 氧化铝:Al2O3氧化钠:Na2O氧化钾:K2O氧化钙:CaO(二)酸、碱和盐1.酸类:硫酸:H2SO4盐酸(氯化氢):HCl硝酸:HNO3碳酸:H2CO32.碱类:氢氧化钠:NaOH氢氧化钾:KOH氢氧化钙:Ca(OH)2氢氧化铁:Fe(OH)3氢氧化亚铁:Fe(OH)2氢氧化铜:Cu(OH)2氢氧化镁:Mg(OH)2氢氧化铝:Al(OH)3氨水:NH3·H2O 注:虽然氨水不含有OH,但是氨水是碱,比较特殊,记住即可。
3.盐类:氯化钠:NaCl氯化钾:KCl氯化镁:MgCl2氯化锌:ZnCl2氯化钙:CaCl2氯化铁:FeCl3氯化亚铁:FeCl2氯化铜:CuCl2氯化铝:AlCl3硫酸钠:Na2SO4硫酸钾:K2SO4硫酸镁:MgSO4硫酸锌:Zn SO4硫酸铁:Fe2(SO4)3硫酸亚铁:FeSO4硫酸铜:CuSO4硫酸铝:Al2(SO4)3硫酸钡:BaSO4硝酸钠:NaNO3硝酸钾:KNO3硝酸镁:Mg(NO3)2硝酸锌:Zn(NO3)2硝酸铁:Fe(NO3)3硝酸亚铁:Fe(NO3)2硝酸铜:Cu(NO3)2硝酸铝:Al(NO3)3硝酸银:AgNO3碳酸钠:Na2 CO3碳酸钾:K2CO3碳酸钙:CaCO3碳酸钡:Ba CO3碳酸镁:Mg CO3碳酸锌:Zn CO33、其他:氯酸钾:KClO3高锰酸钾:KMnO4锰酸钾:K2MnO4注:常见元素的化合价常见原子团的化合价K Na Ag H 正一价氢氧根OH:-1Ca Mg Ba Zn 正二价硝酸根NO3: -1Al正三价硫酸根SO4:-2F Cl Br I 负一价碳酸根CO3:-2O、S(写在最后)负二价铵根NH4: +1Fe(+2价亚铁,+3价铁)Cu(+1价亚铜,+2价铜):铜二价最常见二、化学方程式(1)单质与氧气的反应1、镁条在空气中燃烧:2Mg + O2点燃2MgO2、铁丝在氧气中燃烧:3Fe + 2O2点燃Fe3O43、铜在空气中受热:2Cu + O2Δ2CuO4、铝箔在氧气中燃烧:2点燃2Al2O35、氢气在空气中燃烧:2H2 + O2点燃2H2O6、红磷在空气中燃烧:4P + 5O2点燃2P2O57、硫在氧气中燃烧:S + O2点燃SO28、碳在氧气中燃烧:(充分燃烧)C + O2点燃CO29、碳在氧气中燃烧:(不充分燃烧)2C + O2点燃2CO(2)化合物与氧气的反应10、一氧化碳的燃烧:2CO + O2点燃2CO211、甲烷的燃烧:CH4 + 2O2点燃CO2 + 2H2O12、酒精在空气中燃烧:C2H5OH + 3O22CO2 + 3H2O(3)几个分解反应13、水在直流电的作用下分解:2H2O 2H2↑+ O2 ↑14、加热高锰酸钾:2KMnO4ΔK2MnO4 + MnO2 + O2↑15、分解过氧化氢:2H2O MnO22 H2O +O2↑16、加热氯酸钾:2KClO3MnO2Δ2KCl +3O2↑17、高温煅烧石灰石:CaCO3高温CaO + CO2↑18、碳酸不稳定而分解:H2CO3 === H2O + CO2↑(4)几个氧化还原反应19、焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑20、木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21、氢气还原氧化铜:H2 + CuO ΔCu + H2O22、一氧化碳还原四氧化三铁:3O4高温3Fe + 4CO223、一氧化碳还原氧化铜:CO+ CuO ΔCu + CO224、一氧化碳还原氧化铁:3CO+ Fe23高温2Fe + 3CO2(5)实验室制取氢气的反应:25、锌和稀硫酸:Zn + H2SO4 = ZnSO4 + H2↑26、锌和稀盐酸:Zn + 2HCl=== ZnCl2 + H2↑(6)实验室制取二氧化碳的反应:27、大理石与稀盐酸反应:CaCO3+ 2HCl === CaCl2+ H2O + CO2↑(7)其他28、铁和硫酸铜:Fe + CuSO4 ===Cu + FeSO4。
九年级化学化学式
(4)表示原子数的“小写数字”的书写部位
三:化学式的读法: 一般从右向左读作“某化某”有时还要 读出化学式中各种元素的原子个数
(1) 氧化物:如HgO . SO2 . Fe3O4 ,读作“氧化某”,. 有时还要读出化学式中各种元素的原子个数,如Fe3O4读作四 氧化三铁 “几氧化几某” 。
六. 化合价的运用
1. 根据元素 化合价推出实际存在的物质的化学式 (1). 排列元素 符号------正价在前负价在后 (2). 确定原子个数-------求两种元素正负化合价绝对值的最小公倍数 (3). 写出化学式----------把原子个数写在各元素 符号的右下方 (4). 检查化学式----------依据: 化合价代数和为0
例7. 关于S 和.S2-的叙述中错误的是(D )
A 具有相同的核电荷数
B 电层数相同
C 最外层电子数不相同
D 核外电子数相同
例8.燃放爆竹产生一种污染物,其元素的质量比为l:1,
该污染物 是( C )
A. H2S
B .CO C.S02
D. N02
例9.甲醛(化学式为CH2O)是室内装潢时的主要污染物之一,
化学式中各原子的相对原子质量的总和,就是相对分子质量
(符号为Mr)
求 O2. H2O. KMnO4 的相对分子质量 2.计算物质组成元素的质量 比
化学式中各元素之间的质量比=各原子的相对原子质量总和之比 求MnO2中锰元素和氧元素的质量比等于
3.求物质中某元素的质量 分数
化合物中某元素的质量分数=该元素相对原子质量×原子个数
九年级上册常见的化学式
非金属 单质
稀有气体 化合物 阴离 子 阳离子 H+ 氢离子 NH4
+
OH- 氢氧根 H 2O 水 NH3·H2O↑ 氨水 KOH 氢氧化钾 NaOH 氢氧化钠 Ba(OH)2 氢氧化钡 Ca(OH)2 氢氧化钙 Mg(OH)2↓ 氢氧化镁 Mn(OH)2↓ 氢氧化锰 Zn(OH)2↓ 氢氧化锌 Al(OH)3↓ 氢氧化铝 Cu(OH)2↓ 氢氧化铜 Fe(OH)2↓ 氢氧化亚 铁 Fe(OH)3↓
O2氧离子 H2O 水 _ _ K2O 氧化钾 Na2O 氧化钠 BaO 氧化钡 CaO 氧化钙 MgO 氧化镁 MnO 氧化锰 ZnO 氧化锌 Al2O3 氧化铝 CuO 氧化铜 FeO 氧化亚 铁 Fe2O3
铵根离 子 K+ 钾离子 Na Ba Ca Mg Mn
+
钠离子
2+
钡离子
2+
钙离子
2+
镁离子
CO32- 碳酸根 H2CO3、↑ 碳酸 (NH4)2CO3 碳酸铵 K2CO3 碳酸钾 Na2CO3 碳酸钠 BaCO3↓ 碳酸钡 CaCO3↓ 碳酸钙 MgCO3 微 碳酸镁 MnCO3↓ 碳酸锰 ZnCO3↓ 碳酸锌 _ _ CuCO3↓ 碳酸铜 FeCO3↓ 碳酸亚铁 _
分 类 → 酸 ↓ 盐
九年级上册常见化学式
金属单 质 单 质 K 钾 Pb 铅 H2 氢气 P 磷 Ca 钙 Cu 铜 O2 氧气 S 硫 He 氦 NO3- 硝酸根 HNO3、↑ 硝酸 NH4NO3 硝酸铵 KNO3 硝酸钾 NaNO3 硝酸钠 Ba(NO3)2 硝酸钡 Ca(NO3)2 硝酸钙 Mg(NO3)2 硝酸镁 Mn(NO3)2 硝酸锰 Zn(NO3)2 硝酸锌 Al(NO3)3 硝酸铝 Cu (NO3)2 硝酸铜 Fe(NO3)2 硝酸亚铁 Fe(NO3)3 Na 钠 Hg 汞 N2 氮气 C 碳 Ne 氖 Mg 镁 Ag 银 Cl2 氯气 Si 硅 Ar 氩 Cl- 氯离子 HCl、↑ 盐酸 NH4Cl 氯化铵 KCl 氯化钾 NaCl 氯化钠 BaCl2 氯化钡 CaCl2 氯化钙 MgCl2 氯化镁 MnCl2 氯化锰 ZnCl2 氯化锌 AlCl3 氯化铝 CuCl2 氯化铜 FeCl2 氯化亚 铁 FeCl3 Al 铝 Pt 铂 O3 臭氧 Zn 锌 Au 金 I2 碘 Fe 铁 Mn 锰 Sn 锡
九年级化学中考常见化学式和化学方程式
九年级化学中考常见化学式和化学方程式九年级化学常见化学式和化学方程式一、常见单质氢气:H2氖气:Ne碳:C钾:K铁:Fe氮气:N2氩气:Ar硅:Si钙:Ca铜:Cu氯气:Cl2硫:S钠:Na汞:Hg氧气:O2磷:P镁:Mg银:Ag臭氧:O3碘:I2铝:Al金:Au氦气:He锌:Zn二、化合物1、氧化物水:H2O二氧化碳:CO2 二氧化氮:NO2 氧化亚铁:FeO 氧化镁:MgO 氧化汞:HgO 硝酸:HNO3碳酸:CO3氢氧化钠:NaOH氢氧化镁:Mg(OH)2 氢氧化铁:Fe(OH)3 氢氧化钡:Ba(OH)2 氯化钠:NaCl氯化钾:KCl氯化银:AgCl氯化钡:BaCl2高锰酸钾:KMnO4 碳酸钙:CaCO3硝酸铁:Fe(NO3)2 碳酸钠:Na2CO3碳酸氢钠:NaHCO3 二氧化硫:SO2一氧化碳:CO过氧化氢:H2O2氧化钙:CaO五氧化二磷:P2O5 红色氧化铁:Fe2O3 氧化锌:ZnO氧化铝:Al2O3硫酸:H2SO4硫化氢:H2S氢氧化钾:XXX氢氧化铝:Al(OH)3 四氧化三铁:Fe3O4 二氧化锰:MnO2氧化铜:CuO盐酸:HCl氢氧化钙:Ca(OH)2 氢氧化锌:Zn(OH)2 氢氧化铜:Cu(OH)2 氯化铝:AlCl3氯化铁:FeCl3氯化镁:MgCl2硫酸铜:CuSO4氯酸钾:KClO3硝酸钠:NaNO3硝酸铝:Al(NO3)3 碳酸铵:NH4HCO3硫酸XXX:FeSO4黑色氧化锰:MnO2暗紫色高锰酸钾:KMnO42、其他化合物氢氧化亚铁:Fe(OH)2氨水:NH3·H2O氯化铜:CuCl2氯化亚铁:FeCl2氯化钙:CaCl2氯化锌:ZnCl2硝酸钾:KNO3硝酸亚铁:Fe(NO3)2甲烷:CH4化学式与化学方程式以下是常见的化学式和化学方程式,以及相关反应的现象。
1、化合反应1.1、点燃红磷4P + 5O2 → 2P2O5 (点燃)1.2、氢气燃烧生成水2H2 + O2 → 2H2O (点燃)1.3、硫磺燃烧S + O2 → SO2 (点燃)1.4、镁条燃烧2Mg + O2 → 2MgO (点燃)1.5、铁丝在氧气中燃烧3Fe + 2O2 → Fe3O4 (点燃)1.6、木炭完全燃烧C + O2 → CO2 (点燃)1.7、木炭不充分燃烧2C + O2 → 2CO (点燃)1.8、一氧化碳燃烧2CO + O2 → 2CO2 (点燃)1.9、二氧化碳、二氧化硫和三氧化硫与水反应生成相应的酸CO2 + H2O → H2CO3SO2 + H2O → H2SO3SO3 + H2O → H2SO4 (高温)1.10、二氧化碳通过灼热的炭层CO2 + C → 2CO (高温)1.11、生石灰与水反应CaO + H2O → Ca(OH)22、分解反应2.1、高锰酸钾制氧气2KMnO4 → K2MnO4 + MnO2 + O2↑ (加热)2.2、氯酸钾制氧气2KClO3 → 2KCl + 3O2↑ (加热)2.3、双氧水制氧气2H2O2 → 2H2O + O2↑ (通电)2.4、电解水2H2O → 2H2↑ + O2↑ (通电)2.5、碳酸分解H2CO3 → H2O + CO2↑ (高温)2.6、高温煅烧石灰石CaCO3 → CaO + CO2↑ (高温)3、置换反应3.1、铜和硝酸银溶液反应Cu + 2AgNO3 → 2Ag + Cu(NO3)23.2、铁和硫酸铜溶液反应Fe + CuSO4 → Cu + FeSO42CO2H2O四、化学反应1.金属与酸的反应当锌、铁、镁、铝与盐酸反应时,它们会产生相应的金属盐和氢气的反应。
人教版初三化学需要背诵的化学式
人教版初三化学需要背诵的化学式一、介绍化学式是化学元素或化合物的符号表示法,是化学中的基本概念之一。
在初中化学学习中,掌握化学式是非常重要的,不仅是理论学习的基础,也是实验操作的必备知识。
人教版初三化学需要背诵的化学式,涉及到元素的符号、化合物的组成以及化学反应等内容。
二、常见元素的化学式1. 氢:H2. 氦:He3. 铍:Be4. 碳:C5. 氮:N6. 氧:O7. 氟:F8. 钠:Na9. 镁:Mg10. 铝:Al11. 锌:Zn12. 铁:Fe13. 铜:Cu三、常见化合物的化学式1. 氨气:NH32. 氯化钠:NaCl3. 氧化铜:Cu2O4. 二氧化碳:CO25. 一氧化碳:CO6. 亚硝酸盐:NO2-7. 硫酸:H2SO48. 碳酸钠:Na2CO39. 铝矾:Al2(SO4)310. 硫化氢:H2S11. 过氧化氢:H2O212. 白砷:As2O3四、化学反应中的化学式1. 直接组成反应:例如氢气与氧气的反应生成水,化学式为2H2 + O2 → 2H2O2. 分解反应:例如过氧化氢分解成水和氧气,化学式为2H2O2 → 2H2O + O23. 单一置换反应:例如锌与盐酸生成氢气和氯化锌,化学式为Zn + 2HCl → ZnCl2 + H24. 双置换反应:例如氯化钠与硫酸反应生成盐酸和硫酸钠,化学式为NaCl + H2SO4 → HCl + Na2SO45. 酸碱中和反应:例如氢氧化钠与硫酸反应生成水和硫酸钠,化学式为2NaOH + H2SO4 → 2H2O + Na2SO4五、总结人教版初三化学需要背诵的化学式,包括常见元素的化学式、常见化合物的化学式以及化学反应中的化学式。
通过背诵这些化学式,可以帮助学生牢固掌握这些基本的化学知识,为进一步深入学习化学打下坚实的基础。
在日常的学习中,可以通过多种方式来背诵和巩固这些化学式,如制作化学式卡片、做化学式练习题等。
希望学生们能够重视化学式的背诵,从而在化学学习中取得更好的成绩。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
新2皇冠hg0088-官方版app下载
对高处作业场所有何要求? 教学与教育是部分与整体的关系。A.正确B.错误 变色硅胶干燥时为兰色,受潮后变粉红色,可以在℃下烘干反复使用,直至破碎不能使用为止。 有一砖围墙长30m,高1.5m,厚240cm,每隔5m有一个370mm×120mm的附墙砖跺。已知砌砖每立方米用0.522工日,用砂浆0.26m³。每立方米砂浆用水泥180kg,砂1600kg。计算应用多少工日,多少水泥,多少砂子?砂子用量为kg.A.4658B.4672C.4686D.4695 科学管理理论创始人是A.泰勒B.法约尔C.麦格雷戈D.韦伯E.梅奥 业务计算题:资料:某企业发生以下业务:(1)企业筹建期间发生下列费用:以支票支付注册登记费20000元;以支票购买办公用品80000元;应付职工工资180000元;以银行存款80000元支付借款利息,其中48000元为固定资产资产的借款利息。企业于当年正式投入运营,开办费分5年平均摊销, 患者男,48岁,因“发现双侧颈淋巴结肿大3个月”来诊。无发热、盗汗和体重减轻。否认高血压、心脏病和糖尿病病史。查体:ECOG=1;双侧颈部数枚肿大淋巴结,质韧、活动;余无阳性体征。实验室检查:血常规、肝功能、肾功能、电解质、凝血功能无异常;LDH128U/L;乙型肝炎5项:HBs 2010年4月1日A企业与B银行签订一份借款合同,借款期限为1年。如A企业在2011年4月1日借款期限届满时不能履行偿还借款,则以下可引起诉讼时效中断的事由有。A、2011年6月1日B银行对A企业提起诉讼B、2011年5月10日B银行向A企业提出偿还借款的要求C、2011年5月16日A企业同意偿还借款D 在学习与教学要素中,学生这一要素主要从哪些方面影响学与教的过程?()A.年龄差异B.群体差异C.智力水平D.个体差异 急性点滴型银屑病患者常需联合以下哪种药物A.免疫抑制剂B.糖皮质激素C.抗生素D.免疫调节剂 现一无症状的胆囊结石胆囊炎病人。B超示胆囊壁厚0.4cm,结石周围未见胆囊腔,胆囊肿胀,内回声不均匀,胆囊大于13cm×4cm,结石大于2.0cm,胆总管0.9cm。下一步选择应该是。A.内镜胆囊切除B.开腹手术胆囊切除C.腹腔镜胆囊切除,切除困难时中转开腹D.做MRCP或胆道造影检查E.保守治 高速公路紧急电话系统由安装在公路两侧的紧急电话亭(分机)和两部分组成。A、无线紧急电话系统B、高速公路管理中心紧急电话中心控制台C、车载紧急电话系统D、各高速支队紧急电话处理部门 汽车之底盘包括1.传动系2.转向系3.悬吊系4.制动系5.车轮系,以上何者影响行车安全最深?A.1.2B.2.3C.4.5D.2.4.5 人类淋巴细胞膜上富含HLA抗原,目前已检出约224个基因座位,其中下列哪组HLA可以用血清学方法检出。A,B,DQ和DRB.A,B和CC.A,B,C,DQ和DRD.A,B,C和DRE.A,B和DR 角膜A.色白半透明B.无屈光能力C.表面盖有一层球结膜D.富有感觉神经未梢E.富有淋巴管 针对《刑法》的适用范围,下列观点正确的是()A.凡是在中华人民共和国领域内犯罪的,都适用我国刑法B.凡是在中华人民共和国船舶或者航空器内犯罪的也适用我国刑法,但是在我国船舶或者航空器停靠的国家不认为是犯罪的除外C.我国《刑法》的适用范围采用的是以属地管辖为主,属人管辖 肾病综合征无下列哪种症状A.高脂血症B.蛋白尿C.类脂质尿D.尿钙排出多E.凹陷性水肿 多发性肌炎的临床特点下列哪项表述是不正确的A.四肢对称性近端肌无力B.首发症状多为站立、上下楼和梳头困难C.常伴肌肉酸痛和压痛D.血沉和血清肌酶CK等正常E.可伴颈肌无力,表现抬头困难 者建立了静脉通道并进行输血治疗。因时间紧迫,从血库取回血后,为了尽早将血输给患者,护士便将血袋放在热水中提温,5分钟后为患者输入。当输入15分钟左右,患者感到头部胀痛,出现恶心呕吐,腰背部剧痛。如患者出现以上情况,此反应的致死原因是()A.心力衰竭B.呼吸衰竭C.肾功 当终端发现激活集或候选集中的某个基站的导频信号强度小于时,就启动该基站对应的切换去掉计时器。A.T_TDROPB.T_COMPC.T_DROPD.T_ADD 临床上损伤机会最大的脊椎是A.颈椎B.下颈椎C.胸椎D.腰椎E.骶椎 邮政运营者的法律地位按照自主权可以划分为四种形式,下列国家中邮政运营者属私营公司的是。A.日本、西班牙、缅甸B.新西兰和德国C.荷兰和新加坡D.荷兰和西班牙 某市地铁工程施工作业面内,因大量水和流沙涌入,引起部分结构损坏及周边地区地面沉降,造成3栋建筑物严重倾斜,直接经济损失约合1.5亿元。根据《生产安全事故报告和调查处理条例》规定,该事故的等级属于。A.特别重大事故B.重大事故C.较大事故D.一般事故 补中益气汤的组方配伍特点主要是A.补气与健脾配用B.补气与养血配用C.补气与燥湿配用D.补气与升提配用E.补气与理气配用 属于地方性甲状腺肿的临床表现A.生长发育落后B.甲状腺肿大C.聋哑D.末梢神经炎E.智力低下 下列关于慢性病流行趋势叙述错误的是A.在国内慢性病发病率逐年上升B.发达国家的慢性病发病率及死亡率占疾病负担主要成分C.我国的慢性病主要由营养不良引起的D.在发达地区慢性病主要由不良习惯引起的E.在慢性病中,癌症、心脑血管病占很大比重 民用爆炸物品生产企业凭《民用爆炸物品生产许可证》,销售本企业生产的民用爆炸物品。A、可以B、不可以C、需当地公安部门审批 地方性斑疹伤寒的主要传染源是A.病人B.野鼠C.家鼠D.病原携带者E.隐性感染者 输尿管梗阻,在肾动态显像中的表现为()A.肾盂不显影B.肾盂影无扩大C.肾盂影消退快D.肾实质不显影E.肾盂影明显增浓 [问答题,案例分析题]作者B投给某出版社一部书稿。该社编辑A在审稿中发现,书稿中对某些少数民族沿用了旧时一些蔑称,还有丑化少数民族风俗习惯的内容。于是,就建议B对这些文字和内容进行修改。但是B不以为然,认为自己这样写是有史料根据的,故不愿意修改。为打消A的顾虑,B还立 鼻咽癌好发于A.梨状隐窝B.咽鼓管圆枕C.咽隐窝D.口咽部E.喉咽部 某大型电厂采用四回500kV线路并网,其中两回线路长度为80km,另外两回线路长度为100km,均采用4×LGJ-400导线(充电功率为1.1Mvar/km)。如在电厂母线上安装高压并联电抗器对线路充电功率进行补偿,则高抗的容量宜选为。A.356MvarB.396MvarC.200MvarD.180Mvar 术后疼痛对内分泌系统的影响,下列哪项是错误的ACTH升高B.皮质醇升高C.儿茶酚胺增多D.胰岛素增多E.抗利尿激素增多 《》共六卷,主要记述了周穆王巡游四海,见西王母的故事。 美国建筑师学会(AIA)的合同条件主要用于工程。A.铁路和公路B.房屋建筑C.石油化工D.大型基础设施 有机磷农药中毒A.双侧瞳孔缩小B.小脑幕裂孔疝早期C.双侧瞳孔散大D.瞳孔呈椭圆形并伴散大E.瞳孔对光反应消失 小鼠子宫为双子宫型,呈“Y”形,左右子宫角在膀胱背部汇合成子宫体,。A、其子宫体为一无分隔的完整腔体,后逐渐狭窄形成子宫颈。B、其子宫体为完全分隔的两个相对独立的腔体,后逐渐狭窄形成子宫颈。C、其前部以中隔分成两部,后部中隔消失,逐渐形成子宫颈。D、其前部为无中隔 [问答题,论述题]高中的统计与初中的统计有哪些区别? [问答题,案例分析题]某城市桥梁工程,采用钻孔灌注桩基础,承台最大尺寸为:长8m,宽6m,高3m,梁体为现浇预应力钢筋混凝土箱梁。跨越既有道路部分,梁跨度30m,支架高20m.其他段为预制梁。(1)桩身混凝土浇注前,项目技术负责人到场就施工方法对作业人员进行了交底,随后立即进行 下列哪一项不是关于无效婚姻的原因。A.同居B.重婚C.有禁止结婚的亲属关系D.未达到法定结婚年龄的
