临床检验定量测定项目的室内质量控制监测项目允许不精密度变异
临床检验定量测定项目的室内质量控制监测项目允许不精密度(变异系数)要求
临床检验定量测定项目的室内质量控制监测项目允许不精密度
变异系数)要求
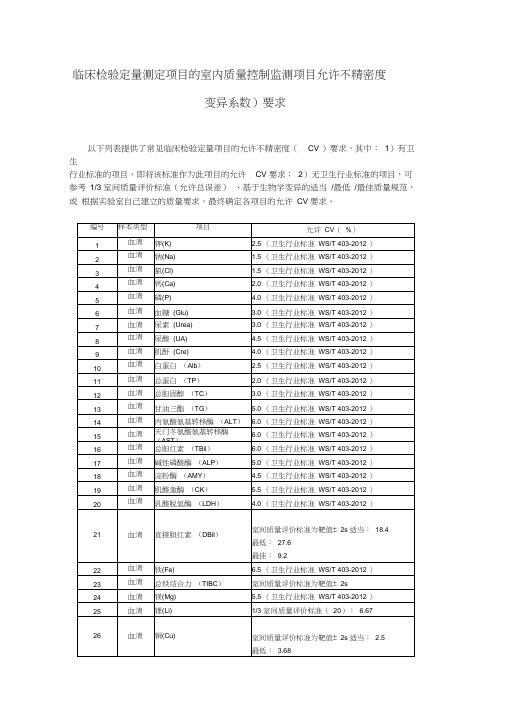
以下列表提供了常见临床检验定量项目的允许不精密度(CV )要求,其中:1)有卫生
行业标准的项目,即将该标准作为此项目的允许CV 要求;2)无卫生行业标准的项目,可参考1/3 室间质量评价标准(允许总误差)、基于生物学变异的适当/最低/最佳质量规范,或根据实验室自己建立的质量要求,最终确定各项目的允许CV 要求。
注:适当、最低和最佳评价标准来自根据生物学变异导出的不同层次允许变异系数。
临检室内质控不精密度
附件六临床检验定量测定项目的室内质量控制监测项目允许不
精密度(变异系数)要求
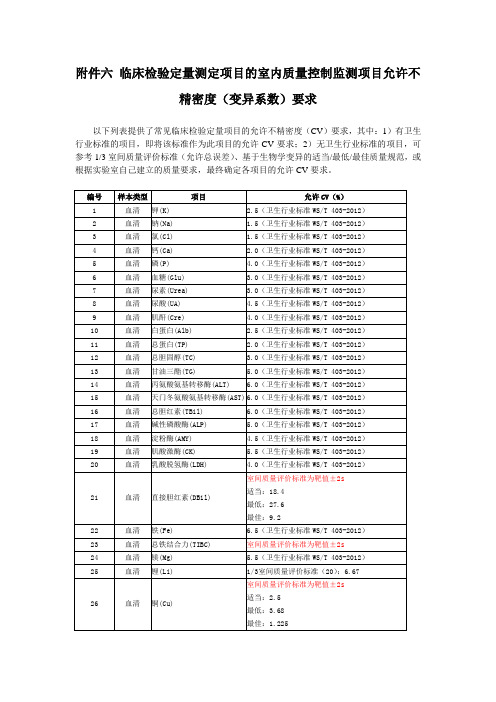
以下列表提供了常见临床检验定量项目的允许不精密度(CV)要求,其中:1)有卫生行业标准的项目,即将该标准作为此项目的允许CV要求;2)无卫生行业标准的项目,可参考1/3室间质量评价标准(允许总误差)、基于生物学变异的适当/最低/最佳质量规范,或根据实验室自己建立的质量要求,最终确定各项目的允许CV要求。
注:适当、最低和最佳评价标准来自根据生物学变异导出的不同层次允许变异系数。
临床检验定量测定室内质量控制

临床检验定量测定室内质量控制1 范围本标准规定了对临床检验定量测定项目室内质量控制的目的、室内质量控制方法的设计、室内质量控制的实际操作、室内质量控制数据的管理、基于患者数据质量控制方法以及室内质量控制数据实验室间比对。
本标准适用于开展临床检验服务的医疗卫生机构的临床实验室的定量测定。
2 术语与定义下列术语和定义适用于本文件。
2.1质量控制 quality control质量管理的一部分,致力于满足质量要求。
[GB/T 19000-2016,3.2.10]2.2室内质量控制 internal quality control检验人员按照一定的频度连续测定稳定样品中的特定组分,并采用一系列方法进行分析,按照统计学规律推断和评价本批次测量结果的可靠程度,以此判断检验报告是否可发出,及时发现并排除质量环节中的不满意因素。
2.3质量控制策略 quality control strategy质控品种类、每种检测频次、放置的位置,以及用于质控数据解释和确定分析批是在控还是失控的规则。
2.4测量偏倚 measurement bias [JJF 1001 5.5]简称偏倚(bias)系统测量误差的估计。
2.5测量精密度 measurement precision [JJF 1001 5.10]简称精密度(precision)在规定条件下,对同一或类似被测对象重复测量所得示值或测量得值间的一致程度。
2.6随机测量误差 random measurement error [JJF 1001 5.6]简称随机误差(random error)在重复测量中按不可预见方式变化的测量误差的分量。
2.7系统测量误差 systematic measurement error [JJF 1001 5.4]简称系统误差(systematic error)在重复测量中保持恒定不变或按可预见方式变化的测量误差的分量。
2.8实验标准差 experimental standard deviation[JJF 1001 5.17]对同一被测量进行n次测量,表征测量结果分散性的量。
临床检验专业医疗质量控制指标

一、标本类型错误率类型不符合要求的标本数占同期标本总数的比例。
标本类型错误率= ×100%反映所采集标本的类型是否符合要求,是检验前的重要质量指标。
标本类型符合要求是保证检验结果准确性的前提条件。
送检标本的类型与检验项目标本类型要求不相同,例如检验项目要求标本类型为血清,但送检标本为抗凝全血,检测时误采用血浆。
特别是一管多用时,分装后不易识别。
标本总数要求汇总该期间所有标本(血液、尿液、胸腹水等)的总数。
二、标本容器错误率采集容器不符合要求的标本数占同期标本总数的比例。
标本容器错误率= ×100%反映用于采集标本的容器是否符合要求,是检验前的重要质量指标。
送检标本的容器与要求标本送检容器类型不相同。
尤见于门诊患者,如 24h 尿液、晨尿等,从家里采集标本送检,未用无菌容器。
再如护士采血时使用 EDTA 抗凝管采集全血用于凝血检查,血培养采集两瓶都为需氧或者均为厌氧。
三、标本采集量错误率采集量不符合要求的标本数占同期标本总数的比例。
标本采集量错误率= ×100%反映标本采集量是否正确,是检验前的重要质量指标。
标本采集量不足或者过多都可能影响检验结果。
送检标本的量过多或者过少,不能满足要求标本量。
过少:如凝血功能检测,标本量过少会影响结果;胸腹水形态学检测,影响细胞计数、重要细胞的检出率。
过多:对于抗凝标本,标本量过多导致抗凝剂与标本量的比例不当,影响抗凝效果。
四、血培养污染率污染的血培养标本数占同期血培养标本总数的比例。
血培养污染率= ×100%反映血培养过程是否操作正确,是检验前的重要质量指标。
血培养污染标准:参考各单位规定的标准。
如:与临床确认患者是否有发烧、是否有导管,报阳时间、 CRP 结果等,综合考虑后判断。
注意计数的是瓶数,与患者数无关。
如:一个患者申请 2 瓶,则计数 2 瓶,而不是 1 瓶。
五、抗凝标本凝集率凝集的标本数占同期需抗凝的标本总数的比例。
临床检验15个质量控制指标

临床检验15个质量控制指标反映标本采集量就是否正确,就是检验前得重要质量指标。
标本采集量不足或过多都可能影响检验结果。
标本类型错误率中明确规定,是分析采集标本类型不符合要求的标本比例,其计算公式为:标本类型错误率=类型不符合要求的标本数/标本总数×100%。
标本容器错误率中明确规定,是分析采集容器不符合要求的标本比例,其计算公式为:标本容器错误率=采集容器错误的标本数/标本总数×100%。
单从字面意思不难理解这两个指标,但是在实际的操作过程中难免会心生疑问,如果一个大便杯里面装有尿液是归为标本类型错误还是标本容器错误?这就取决于申请的项目,如果申请的项目为大便常规,则归为标本类型错误。
如果申请项目为尿液培养,则归为标本容器错误。
那么我们再举几个例子:如果一个装有尿液的紫头管送检血常规,则归为标本类型错误;如果一个装有大便的无菌杯送检尿培养,则同样归为标本类型错误;如果一个装有血液的红头管送检血常规,则归为标本容器错误;如果一个装有尿液的常规尿杯送检尿培养,则归为标本容器错误。
在这里值得一提的是“标本总数”包括所有类型的标本总数,而不单指某一种类型的标本。
在临床实践过程中如果存在标本类型和检测项目不一致,且对检测结果没有影响的情况,则应视为标本合格。
例如,尿杯里面采集的大便送检大便常规则应视为标本合格。
通过以上的思考和分析对标本类型错误和标本容器错误这两个指标有了更清晰的认识。
探讨2:如何清晰界定标本采集量错误和抗凝标本凝集?标本采集量错误率是分析的标本体积,其计算公式为:标本采集量错误率=量不足或过多(抗凝标本)的标本数/标本总数×100%。
抗凝标本凝集率是分析需要抗凝标本的凝集情况,其计算公式为:抗凝标本凝集率=凝集的标本数/需抗凝标本总数×100%。
似乎这两个指标是完全独立的,当然在大多数情况下都可以明确界定。
假设一个送检红头管的生化项目,由于检测项目多,标本量采集不够,那么这肯定是标本采集量错误。
临床检验定量测定项目的室内质量控制监测项目允许不精密度(变异系数)要求
临床检验定量测定项目的室内质量控制监测项目允许不精密
度(变异系数)要求
(TC)
(FSH)
标准差(Standard Deviation),在概率统计中最常使用作为统计分布程度(statistical dispersion)上的测量。
标准差定义是总体各单位标准值与其平均数离差平方的算术平均数的平方根。
它反映组内个体间的离散程度。
简单来说,标准差是一组数据平均值分散程度的一种度量。
一个较大的标准差,代表大部分数值和其平均值之间差异较大;一个较小的标准差,代表这些数值较接近平均值。
变异系数 C·V =(标准偏差 SD÷平均值 MN )× 100%。
临床检验定量测定室内质量控制要求及室内质量控制实验室间比对
临床检验定量测定室内质量控制要求及室内质量控制实验室间比对临床检验定量测定室内质量控制是保障临床检验结果准确性和可靠性的重要措施。
室内质量控制要求是指在临床检验过程中,为保证结果的准确性,需要设置和实施的一系列质量控制措施和要求。
室内质量控制实验室间比对是指对不同实验室进行比对评估,确定不同实验室中检验结果的准确性和可靠性的比较。
室内质量控制要求主要包括以下几个方面:1.质量控制品的使用:临床检验仪器和试剂的厂家通常都提供质量控制品,实验室需要根据仪器的要求选用合适的质量控制品,并按厂家提供的说明书正确使用。
2.质量控制程序的建立:实验室需要制定质量控制的程序和标准,明确每个检测项目的质量控制要求,包括质控样品的制备、质控参数的设定、质控结果的判定等。
3.质控样品的制备:质控样品是实验室进行定量测定的参照,为确保结果的准确性和可靠性,质控样品的制备需要按照一定的规范和标准进行,如按照国家标准物质提供的浓度值或人工制备的稀释液进行制备。
4.质控参数的设定:根据仪器的精密度和准确度等性能要求,以及临床需求和实验室实际情况,设定每个检测项目的质控参数,如目标值、参考范围和允许偏差的范围等。
5.质控结果的判定:根据质控参数设定的标准,对每次质控的结果进行判定,判断结果是否在允许偏差范围内。
如果结果超出允许偏差范围,需要及时采取纠正措施,确认问题的原因并进行调整。
室内质量控制实验室间比对是保证临床检验结果准确性和可靠性的重要手段。
通过与其他实验室的比对评估,可以评估本实验室与其他实验室之间结果的准确性和可靠性。
室内质量控制实验室间比对的具体实施步骤如下:1.选择比对标本:选择一组标本进行质量控制比对,通常是实验室内部的质控样本和外部提供的质控样本。
2.进行测定:将所选质控标本分配给各个实验室进行测定,按各自实验室的常规程序进行质量控制测定。
此步骤要求各个实验室在同一时间内进行测定,以避免时间差对结果的影响。
检验项目允许不精密要求
临床检验定量测定项目的室内质量控制监测项目允许不精密度
(变异系数)要求
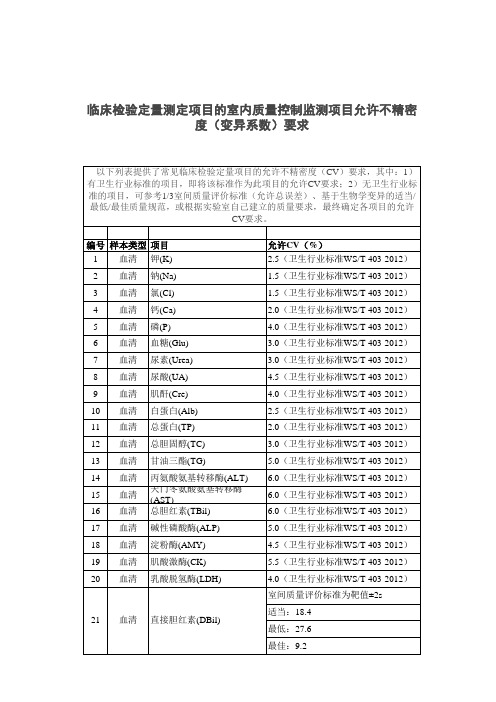
以下列表提供了常见临床检验定量项目的允许不精密度(CV)要求,其中:1)有卫生行业标准的项目,即将该标准作为此项目的允许CV要求;2)无卫生行业标准的项目,可参考1/3室间质量评价标准(允许总误差)、基于生物学变异的适当/最低/最佳质量规范,或根据实验室自己建立的质量要求,最终确定各项目的允许CV要求。
注:适当、最低和最佳评价标准来自根据生物学变异导出的不同层次允许变异系数。
临床检验定量测定室内质量控制要求及室内质量控制实验室间比对
8
10
13s控制规则
概率(P)
1-3s规则检出系统误差的功效函数图
00000.....156789 00..34 00..012
0
1
2
3
4
临界系统误差(△SEc)
1
2
4
6
8
10
12
20
13s/22s/R4s/41s/10x控制方 法
1-3s/2-2s/R-4s/4-1s/10-x规则检出系 统误差的功效函数图
5 Sigma精密度 6 Sigma精密度
4.00% 2.00% 6.00% 6.00% 0.08 mg/dL
4% 1 mm Hg 1.60% 0.008 0.2 mg/dL 1.00% 2.00% 6.00% 6.00% 0.06 mg/dL 3.00%
3.30% 1.70% 5.00% 5.00% 0.067 mg/dL
差
中等
良好
>10%
2-10%
<2%
13s/22s/R4s/41s/12X 13s/22s/R4s/41s/8X
13s/22s/R4s/41s
N=6
N=4
N=2
13s/22s/R4s/41s/8X N=4
13s/22s/R4s/41s N=2
13s/22s/R4s/(41sW) N=2
临床实验室定量测定室内质量控制-文档资料
对具体检测过程进行回顾分析 失控后,应对该批检测的全过程进行迅 速、仔细的回顾。分析有无特殊情况,如电 压波动、仪器不稳、试剂瓶标签脱落、试剂 放置位置不符合要求、质控品瓶盖松动、复 溶过程异常等。并应检查使用的容器、量器 是否正确、仪器有无变动、校准品或试剂有 无变更生产厂家、批号或接近失效期等,同 时复查计算结果。 对于认为上述“失控原因初步估计”中 可能性较大的方面,在回顾分析过程中应特 别加以注意。
重新测定质控品
失控
在控
进行标本测定
启用同一批号新的质控品
失控
在控
进行标本测定, 丢弃旧的质控品
更换另一批号质控品测定
失控
在控
进行标本测定, 丢弃全部旧批号的质控品
对仪器进行全面维护、检查 包括光路系统、试剂、试剂 针、样品针、清洗头、分配 器等。
没有发现问题
发现问题
正确处理后, 重新测定质控品, 在控,进行标本测定
通过选择性复查进一步分析判断失控原因和 决定处理.一般应进行选择性复测。 复查时,应包括下述样品,以便尽量一次找出原因,及 时发出患者标本的化验报告。①失控时使用的质控品;②重 新打开一瓶相同批号的质控品;③失控时使用的校准品;④ 重新打开一支相同批号的校准品;⑤少数几个患者标本,最 好包括已知病情、近期曾做过该项目检测的患者标本;⑥如 有条件,加测一瓶定值质控品。 多数情况下,通过上面的分析和复查可以查出原因,并能 对患者标本提出较妥善的处理措施。 难以处理的问题,及时与厂方联系!
13S和R4S规则反映的是随机误差。22S、41S和 10X反映的是系统误差,系统误差超出一定 的程度,也可从13S和R4S规则反映出来。
室内质控数据的周期性评价
质控失控处理流程图
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
临床检验定量测定项目的室内质量控制监测项目允许不精密度
(变异系数)要求
以下列表提供了常见临床检验定量项目的允许不精密度(CV)要求,其中:1)有卫生行业标准的项目,即将该标准作为此项目的允许CV要求;2)无卫生行业标准的项目,可参考1/3室间质量评价标准(允许总误差)、基于生物学变异的适当/最低/最佳质量规范,或根据实验室自己建立的质量要求,最终确定各项目的允许CV要求。
注:适当、最低和最佳评价标准来自根据生物学变异导出的不同层次允许变异系数。
