第五章 磺化反应
磺化反应相关知识
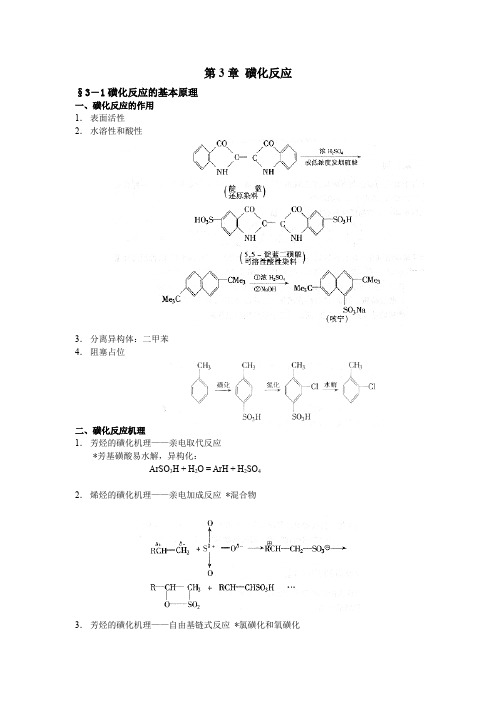
第3章磺化反应§3-1磺化反应的基本原理一、磺化反应的作用1.表面活性2.水溶性和酸性3.分离异构体:二甲苯4.阻塞占位二、磺化反应机理1.芳烃的磺化机理——亲电取代反应*芳基磺酸易水解,异构化:ArSO3H + H2O = ArH + H2SO42.烯烃的磺化机理——亲电加成反应*混合物3.芳烃的磺化机理——自由基链式反应*氯磺化和氧磺化三、影响磺化反应的主要因素1.被磺化物的性质(1)饱和烷烃较难磺化,芳烃较易磺化(2)芳烃取代基:电子效应:苯>氯苯>溴苯>对硝基苯甲醚>对硝基甲苯>硝基苯空间效应:邻二甲苯>甲苯>乙苯>异丙苯>叔丁苯2.反应温度(1)对反应速率的影响: T↑—r↑—t↓(低温长时)(2)对磺酸基引入位置的影响甲苯:低温——对位,邻位;升高温度——间位产物增多萘:低温——α位;高温——β位(动力学-热力学:水解-再磺化-异构化)(3)对多磺化的影响T↑——利于多磺化3.磺化催化剂和磺化助剂(1)促使反应易于进行——吡啶,邻氯苯甲醛(2)改变磺酸基引入位置(3)抑止副反应HAc、Na2SO4——抑止砜的生成硼酸(与羟基形成硼酸酯)——阻止氧化反应§3-2常用磺化剂及其磺化方法一、硫酸:稀硫酸、浓硫酸,发烟硫酸1.使用高浓度过量的酸∴ C ↑则X↓2.脱水物理脱水法:(1)共沸(2)高温β-萘磺酸:160℃,过量40%化学脱水法:BF3, SOCl2: H2O+ SOCl2→2HCl ↑+ SO2↑3.硫酸的浓度与其它物理性质的关系(熔点,密度,比热,溶解度,电阻)20~25%,60~65%4.操作方法:向被磺化物仲缓慢加入磺化剂优点:平稳,易于传质、传热,副反应少缺点:残渣,后处理困难二、三氧化硫——优点:不生成水,反应速度快,活性高,理论量即可完成反应缺点:物料粘度高,传质困难,副反应多1.SO3在室温下易聚合——γ型加稳定剂:0.1%硼酐,二苯砜,(CH3)2SO42.SO3具有强氧化性——控制温度,加入稀释剂SO3(气):N2, SO2; SO3(液): SO2(液),CCl4 (防止爆炸-强放热)三、氯磺酸ClSO3H (SO3·HCl )活性强,价格高,HCl腐蚀:制备芳磺酸或磺酰氯,N-磺化(甜蜜素)(1)分批加料:将有机物加入氯磺酸中(减少砜的生成)(2)稀释剂:二氯苯,四氯乙烷,硝基苯四、氯磺化和氧磺化氯磺化:Cl2+SO2氧磺化: O2+SO2注意:(1)仲碳磺酸盐(2)氯磺化:采用SO2过量(SO2:Cl2=3:1),低转化率(50~70%)的方法控制副反应(氯化,多磺化)五、烘焙磺化法。
关于磺化反应的介绍

❖ 特点:生成C-S+ 键H 2 S 。4 O
+ S3 O HH 2 O
+ 2 C lS3 H O
S2 C O l+ H 2 S4 + O H C l
硫酸化反响: 有机化合物分子中引入硫酸基〔-OSO3H〕的
化学过程。 特点:生成C-O-S键。 例:烯烃、脂肪醇等的硫酸化。
+ + RO HH 2 S4 O R O S3 H OH 2 O
五、烘焙磺化法
将等摩尔的芳伯、仲胺与浓硫酸成盐后,在高温下发生分 子内的脱水和重排反响,主要生成对氨基苯磺酸;假设对位 被占据,那么生成邻位产物。反响温度对异构体比例有影响。
NH2
NH2H2SO 4
NH2
H2N H2N
+ H2SO 4
H2O SO 3H
SO3H
+ 17O5C
OCH3 H2SO4
❖ 评价:
❖ 用发烟硫酸为磺化剂不好。
❖ 用稀硫酸为磺化剂采用共沸脱水磺化法或在有机溶剂中以氯 磺酸为磺化剂更好。
❖ 加料方式不对,即使低温反响也会有较多副反响,78%的低 收率正常。
评价: 〔1〕二甲苯的磺化是典型的低π磺化,较低浓度硫酸就可以进展磺化。采 用浓硫酸为磺化剂、142℃高温反响会发生二磺化副反响。 〔2〕加料方式不对。即使是采用浓硫酸,也应将浓硫酸滴加到二甲苯中。 〔3〕应在室温下向二甲苯中滴加稀硫酸,然后升温到沸腾,利用二甲苯与 水共沸除水,直到反响完全。
S3 O H
NaOH O H
O S3 O H HCl
O
O Cl O
利用磺酸基的水解性,完成特定的反响后,再将其水解。
二、硫酸的配制
❖ 硫酸和发烟硫酸:
第五章:磺化反应

沸点/℃
磺化速度 磺化转化率 磺化热效应 磺化物粘度 副反应 产生废酸量 反应器容积
需加热 低 少 大 大
十分粘稠 多,有时很高 无 很小
2013年7月29日3时45分
21
硫酸的浓度和用量
π值:用SO3质量百分数表示 “废酸”中所含 H2SO4的浓度。 计算:
2013年7月29日3时45分
OH
OH OH H2SO4 90℃ HO3S
雪佛酸
OH H2SO4 106~120℃ HO3S
R 酸
SO3H
SO3H OH H2SO4+2%SO3 70~80℃ HO3S
G 酸
SO3H
OH
HO3S
OH H2SO4+SO3
雪佛酸
OH
35~55℃ HO3S
2013年7月29日3时45分
34
磺化剂的配制
2013年7月29日3时45分
23
异构化
SO3H
磺化时发现,在一定条件下, 磺基会从原来的位置转移到其 他位置,这种现象称为“磺
+ H2SO4
160℃
SO3H
酸的异构化”
(1)多数情况是磺酸基 水解再磺化的过程。
(2)无水生成或无水参 与反应时,可以认为是分 子内重排。
HO 3S
CH3
CH3
H2SO4 200℃
2013年7月29日3时45分
4
5.1.2 磺化目的
可将-SO3H转化为其它基团: -OH, -NH2, -CN, -Cl, ……
Cl O Cl
OH
Cl
O
Cl
2013年7月29日3时45分
磺化反应知识点总结

磺化反应知识点总结一、磺化反应的机理磺化反应的机理主要包括三个步骤:磺酸酯或磺酰氯的亲核取代、醇解和亲核加成。
1. 磺酸酯或磺酰氯的亲核取代磺化反应通常以磺酸酯或磺酰氯作为试剂,它们在反应中起到亲核取代的作用。
当磺酸酯或磺酰氯与化合物中的氢原子发生交换时,产生磺化产物。
这个过程可以用下面的化学方程式表示:R-OH + R'-OSO2Cl → R-OSO2R' + HCl其中,R和R'分别是有机基团,可以是烷基、芳基等。
2. 醇解醇解是磺化反应中的一个重要步骤,它是指磺酸酯或磺酰氯与醇在碱性条件下发生反应,生成磺酸盐。
具体的化学方程式如下:R-OSO2R' + H2O → R-OH + R'-OSO3H3. 亲核加成在一些特殊的情况下,磺酸酯或磺酰氯也可以与烯烃或炔烃等化合物发生亲核加成反应,生成磺酸酯或磺酰氯。
这个过程可以用下面的化学方程式表示:R-OSO2R' + R"CH=CH2 → R'-OSO2R"CH-CH2SO2R'以上就是磺化反应的机理,通过以上三个步骤,磺化反应引起了有机物中的氢原子的取代,生成了磺化产物。
二、磺化反应的影响因素磺化反应的速率和选择性受到许多因素的影响,包括试剂的种类、反应条件、溶剂等。
下面具体介绍一下各种影响因素:1. 试剂的种类磺酸酯和磺酰氯是磺化反应中最常用的试剂,它们在反应中起到亲核取代的作用。
不同种类的试剂对反应速率和选择性具有不同的影响,通常情况下,磺酸酯的活性要比磺酰氯高,因此磺酸酯在磺化反应中的应用更为广泛。
2. 反应条件反应条件包括温度、pH值、反应物浓度等,这些条件对磺化反应的速率和选择性有着重要的影响。
通常情况下,较高的温度和碱性条件有利于加速磺化反应的进行,提高产物的产率。
3. 溶剂溶剂在磺化反应中起到溶解反应物和促进反应的作用,不同溶剂对反应速率和选择性也有着一定的影响。
第5章芳香烃2

A 从诱导效应分析对苯环的影响
B 从共轭效应分析对苯环的影响
31
5.6.2 取代基定位规律的理论解释
A 从诱导效应分析对苯环的影响
a 甲基碳上电子云密度比苯环碳大; b 甲基碳SP3杂化苯环碳SP2杂化,后者电负性强,
吸引甲基电子云偏向苯环,苯环电子云密度增大。 综合结果: 供电效应。
B 从共轭效应分析对苯环的影响 甲基的超共轭效应结果: 供电效应。
51
5.7.1 稠环的结构
0.142nm
0.136nm
0.139 0.140nm
α 位:1,4,5,8 β :2,3,6,7 γ 位:9,10 稳定性:两个单独苯的共振(离域)能之和:301.2kJ/mol;
萘的离域(共振)能:255kJ/mol,因此萘比苯活泼。
α位电子云密度最高:活性最高; β位电子云密度低于α位:活性低于α位; γ9,10位电子云密度最低:活性最低。
CH3
CH3
COO H
Cl
SO 3H
NO 2
44
5.6.3 二取代苯的定位规律
5.6.3.2 环上原有的两个取代基定位作用不一致
(1)如两个取代基属于同一类,但定位作用不一致则第三个 取代基进入苯 环的位置主要由定位效应强色定位基决 定;如两个取代基定位作用强弱相差不大,则得混合物。
C OO H
OC H 3
17
5.5 单环芳烃的化学性质
5.5.1.2 加成反应
苯及同系物与氢、卤素加成,生成脂环烃或其 衍生物的反应。
Ni
+3H2 △
紫外线Cl H
Cl H
+ 3Cl2
△
H Cl
Cl H
HCl HCl
磺化反应的特点

磺化反应的特点磺化反应是一种重要的有机合成反应,在药物、染料、橡胶、塑料等化工领域中广泛应用。
本文将从磺化反应的概念、反应机理、反应条件、应用等方面进行详细阐述,希望对读者有所启发。
一、概念和分类磺化反应是将有机物中的活泼亲核试剂和亚硫酸或其衍生物进行反应,生成含有磺基的化合物的反应过程。
磺化反应可分为直接磺化和间接磺化两种。
间接磺化又分为偶联磺化和氧化磺化。
偶联磺化是指使用碱性条件下的偶联试剂反应,将两个不同的有机化合物偶联生成磺化产物。
氧化磺化则是使用氧化剂将有机化合物氧化成相应的酸,然后与亚硫酸或其衍生物反应生成磺化产物。
二、反应机理磺化反应的机理非常复杂,与反应条件、试剂选择等因素有很大关系。
下面简要介绍一下直接磺化的机理。
对于亚硫酸盐的磺化反应,其机理主要分为两个步骤:首先是有机物中的活泼亲核试剂把亚硫酸盐中的硫酸酯基取代,生成新的硫酸酯,并过渡态消失;生成的新硫酸酯参与亚硫酸盐酯化反应,生成磺化产物和硫酸酯。
总的反应方程式为:(1)ROH+HSO3R'→ROSOR'+H2O三、反应条件溶剂:磺化反应使用的溶剂从极性溶剂到非极性溶剂不一,一般根据反应物和试剂的特性选择合适的溶剂。
如催化剂催化的磺化反应,通常使用极性溶剂如N,N-二甲基甲酰胺(DMF),N-甲基吡咯烷酮(NMP)等。
而直接间接氧化磺化反应需要使用的溶剂则较多,如乙腈、丙酮、二氯甲烷、甲醇等。
反应时间:磺化反应的反应时间与温度、反应物的浓度和反应条件等因素有关。
反应时间一般在几小时到一天左右。
四、应用由于磺化反应的反应条件较为宽松,且反应的产物具有良好的物理化学性质,因此磺化反应在诸多领域有广泛应用。
例如在染料和颜料合成中,一些有机染料和颜料通过磺化反应可以改善其溶解性、抗光、耐污染等物理化学性质。
在医药领域,一些药物和激素也可以通过磺化反应进行改性,提高其生物利用度和药效等方面的性能。
在橡胶和塑料工业中,磺化反应可以增加其抗氧化、抗切断、化学稳定性等方面的性能,使其更有耐久性。
有机化学 第五章 芳烃

Ⅰ 贡献大
Ⅱ
Ⅲ
Ⅳ 贡献小 键长、键角不等 的不等价结构
Ⅴ
键长,键角完全 相等的等价结构
H
H
H
H
H
H
苯的结构小结
(1)苯是一个正六边形的平面分子,键长、键角平均化; )苯是一个正六边形的平面分子,键长、键角平均化; (2)电子云分布在苯环的上方和下方; )电子云分布在苯环的上方和下方; 电子高度离域, 个 电子在基态下都在成键轨道 (3)π电子高度离域,6个π电子在基态下都在成键轨道 ) 电子高度离域 内,故体系的能量降低,而使苯环稳定。 故体系的能量降低,而使苯环稳定。
(3)具有平面和接近平面的环状结构。 (3)具有平面和接近平面的环状结构。 具有平面和接近平面的环状结构 (4) 易发生亲电取代反应 不易发生加成反应。 易发生亲电取代反应,不易发生加成反应 不易发生加成反应。
单环芳烃 联苯和联多苯 苯系芳烃 如:
联苯
芳烃
多环芳烃
本文由duan490513584贡献
ppt文档可能在WAP端浏览体验不佳。建议您优先选择TXT,或下载源文件到本机查看。
第五章
芳烃—— 芳香族碳氢化合物 芳烃
(1)碳氢比高 如: C:H=1:1 C : H = 10 : 8
特点
碳碳键长介于C—C与C=C之间 (2) 碳碳键长介于C—C与C=C之间 如: 0.139nm C— C 0.154nm C=C 0.133nm
三苯甲烷 2,3-二甲基 苯基己烷 二甲基-1-苯基己烷 二甲基
苯基: 苯基: -Ph 、 芳基: -Ar 芳基: R CH2H3C-CH3
m-二甲苯 二甲苯 1,3-二甲苯 二甲苯
第5章 磺化-1

被磺化物
甲苯
787
苯
155
硝基苯
2.4
k×105(g•mol•s)
(2)空间位阻效应的影响
表
R
磺化异构产物的比例(25℃,89.1% H2SO4)
随着空间位阻效应的增强,邻位磺化产物越来越少,对位磺 化产物增多
(3)萘系芳烃的磺化
萘环亲电取代反应比苯环活泼,萘酚比萘容易磺化。
2H2SO4
K1
SO3 + H3O+ + HSO4[SO3] =
K1[H2SO4]2
K1 =
[H3O+][HSO4-] [SO3]
[H2SO4]2
[H3O+][HSO4-]
(II)
v(SO )=k(SO )[ArH]
3 3
K1[H2SO4]2
[H3O+][HSO4-]
(III)
H2O + H2SO4
HO 3S SO3H
4)磺化的温度和时间的影响
(1)反应温度影响磺酸基进入芳环的位置和异构磺 CH 酸生成的比例。 CH
3
3
H2SO4
200℃
SO3H
100 α -位产物 β -位产物
90 80 70 60
SO3H
o-位产物 m-位产物 p-位产物
80
Yield/%
Yield/%
60
50 40 30
磺化铜酞菁 酞菁化合物以其独特的色光、低廉的生产成本、较好的稳定性及着色性 而受到人们的关注,并被广泛用作染料和颜料。尤其作为直接类染料, 因其染色工艺简单、染色成本低而具有广阔的市场。磺化的铜钛菁染料 粉末和液态产品已经商品化。
纤维
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
发烟硫酸(SO3•H2SO4) 氯磺酸(ClSO3H) 其它:氨基磺酸(NH2SO3H)、亚硫酸盐(Na2SO3)
5.1.4 磺化方法
过量硫酸磺化法(液相磺化法,H2SO4) 共沸去水磺化法(气相磺化法, H2SO4) 亲电取代 三氧化硫磺化(SO3) 氯磺酸磺化(ClSO3H) 芳香族 芳伯胺烘焙磺化法 化合物
K1[H2SO4]2 [H3O+][HSO4-]
v(SO )=k(SO )[ArH]
3 3
H2O + H2SO4
K
H3O+ + HSO4-
[H3O+]=[HSO4-]≈[H2O]=1-[H2SO4] v(SO )=k(SO )[ArH]
3 3
K1[1-[H2O]]2 [H2O]2 1 [H2O]2
(5)萃取法
5.2.4.2 共沸去水磺化
工艺过程 将被磺化物以气体形式通入硫酸中,反应 生成的水与过量芳烃形成共沸物一起蒸出。
适用范围: 低沸点芳烃,如苯、甲苯等。
5.2.4.2 共沸去水磺化
特点 (1)利用有机蒸气带走水份; (2)磺化剂用量较少,利用率超过91~92%。
设备: 间歇釜式或多锅串联的生产工艺 工艺条件 磺化剂:98.5%H2SO4 配比:苯:磺化剂=6~8:1 反应温度:170~190℃ 苯单程转化率:12~17% 苯磺酸收率:96~98%
CH(CH3)2 0.057
C(CH3)3 0
萘系芳烃的磺化
SO3H HO3S
SO3H
(1)产物与磺化剂的种类、浓度和反应温度有关。
SO3H
+ H2SO4
SO3H
SO3H
SO3H SO3H
+
SO3H
(2)多磺化产物的制备往往需要进行多步磺化。
SO3H
SO3H
H2SO4 60℃
SO3•H2SO4 35~55℃
置换磺化(亚硫酸盐法) 氧磺化(SO2+O2) 游离基反应 氯磺化(SO +Cl ) 2 2 加成磺化(NaHSO3) 置换磺化
脂肪族 化合物
5.2 芳香族化合物的磺化
磺化反应历程 磺化反应动力学 磺化反应影响因素 磺化生产工艺
5.2.1 磺化反应历程
H2SO4中电离平衡:
2H2SO4 2H2SO4 3H2SO4 3H2SO4 SO3 + H3O+ + HSO4H3SO4+ + HSO4H2S2O7 + H3O+ + 2HSO4HSO3+ + H3O+ + 2HSO4-
k1 k-1
H SO 3SO3SO3H
+ SO3
.+ . . . .. .
K2,-H+
+H+
5.2.2 磺化反应动力学
ArH + SO3
3 3
k
ArSO3H
v(SO )=k(SO )[ArH][SO3] 2H2SO4
K1
SO3 + H3O+ + HSO4K1[H2SO4]2
[SO3] =
[H3O+][HSO4-]
+ Na2SO 3
磺化产物的分离
(1)稀释析出法
(2)稀释盐析法
OH
SO3H
磺化
HO 3S
OH
OH
+
HO3S
SO3K OH
SO3H
OH
KCl
↓+
KO3S
KO3S
SO3K
OH
NaCl
↓
NaO3S SO3Na
(3)中和盐析法
(4)脱硫酸钙法
2ArSO3H + Ca(OH)2 → (ArSO3)2Ca + H2O H2SO4 + Ca(OH)2 → CaSO4↓+2H2O (ArSO3)2Ca + Na2CO3 → 2ArSO3Na +CaCO3↓
C12H25
H2O
SO3Na
C12H25
SO3
-
胶束
阴离子表面活性剂
可将-SO3H转化为其它基团,如-OH,-NH2, -CN,-Cl等。
SO3H
Cl
碱性水解
OH
O
Cl
Cl
O
Cl
利用-SO3H的可水解性,辅助定位或提高反 应活性。
OH OH
OH
OH
磺化
HO 3S
溴化
HO 3S
Br
水解 H+
Br
5.2.3.5 催化剂及添加剂的影响
O SO3H
催化剂可以影响磺酸基进入的位置。
O O SO3H
磺化
O
磺化 HgSO4催化
O
O
添加剂可以抑制副反应的发生
ArSO3H + SO3 ArSO3H + 2H2SO4 ArSO2+ + HSO4ArSO2+ + H3O+ + HSO4-
5.2.3.6 搅拌的影响
(4)有机络合物法
5.2.4.5 氯磺酸磺化
活性: S3;
O OH HO S O OH
O
特点:(1)易水解; (2)价格贵,应用少; (3)产品纯度高。
5.2.4.5 氯磺酸磺化
用量:n(ArH):n(ClSO3H)=1:4~5 主要应用:制备磺酰胺类化合物
慢
较快
较完全 一般 一般 少
较快
较完全 一般 一般 少
瞬间完成
定量转化
放热量大,需冷 却
磺化转化率 达到平衡,不完全 磺化热效应 磺化物粘度 副反应 需加热 低 少
十分粘稠 多,有时很高
产生废酸量
反应器容积
大
大
较少
大
较少
一般
无
很小
5.2.3.3 磺化物的水解及异构化作用
水解作用
ArH + H2SO4
磺化
+
SO3H
H2O
5.1.2 磺化目的
赋予有机物酸性、水溶性、表面活性及对 纤维的亲和力等。
N N N N N Cu N N N (SO3H)2-4
磺化铜酞菁
HOOC-Wool-NH2
H+
HOOC-Wool-NH3+
Dye-SO3-
HOOC-W ool-NH 3+. -O3S-Dye
酸性染料对蛋白质纤维上染
+ MgCl2 + H2O
NO 2 O
SO3Na
+ NaSO 3 100~102℃ 水介质
SO3H
SO3H
SO3H
SO3•H2SO4
50~90℃
SO3H SO3H
SO3•H2SO4 150~250℃
HO 3S SO3H SO3H
5.2.3.2 磺化剂的影响
表 不同磺化剂对反应的影响
项目 磺化剂
H2SO4 290~317
ClSO3H 151~150
SO3•H2SO4
SO3 46
沸点,℃
磺化速度
加快物料在酸相中的溶解. 强化传热、传质,提高反应速度,防止局部过 热和副产物的生成。
5.2.4 磺化生产工艺
过量硫酸磺化 共沸去水磺化 芳伯胺的烘焙磺化 三氧化硫磺化 氯磺酸磺化 置换磺化
5.2.4.1 过量硫酸磺化
ArH + H2SO4 ArSO3H + H2O
特点: (1)以硫酸为反应介质,在液相中进行; (2)磺化试剂硫酸过量很多倍; (3)应用范围很广; (4)反应可逆; (5)有大量废酸生成。
5.2.3.1 被磺化物结构的影响
取代基的影响
表 有机芳烃磺化速度的比较
被磺化物
甲苯
苯
硝基苯
0.24
k×106(g•mol•s)
78.7 15.5
5.2.3.1 被磺化物结构的影响
空间效应的影响
表
R
一磺化异构产物的比例(25℃,89.1%H2SO4)
R o/p
CH3 0.88
C2H5 0.39
200℃
SO3H
SO3H
SO3H
H2SO4 155℃
HO 3S SO3H
5.2.3.4 反应温度的影响
反应温度高,反应速度快,反应时间短。
反应温度高,副反应速度加快。
SO3H +
>170℃
SO2
5.2.3.4 反应温度的影响
影响异构体比例。
o-位产物 m-位产物 p-位产物
100 α -位产物 β -位产物
(3)带有-OH,-OCH3,-NO2和多卤基化合物 不宜采用。
工艺操作 早期:炒盘、炒锅、烘焙盘; 后期:球磨机式固相反应器 新方法:溶剂法(采用二氯苯、三氯苯、 二苯砜等高沸点溶剂,在180~220℃反 应)
5.2.4.4 三氧化硫磺化
优点 (1)不生成水、无废酸; (2)磺化能力强、反应速度快; (3)磺化剂用量省,接近理论量; (4)避免分离产品质量高,杂质少; (5)生产效率高。 缺点 反应剧烈,不易控制。
100%H2SO4 145℃
SO3H
65%SO3•H2SO4
60~80℃
HO 3S
SO3H
SO3H
异构化
155℃
HO 3S SO3H
65%SO3•H2SO4 155℃
HO 3S SO3H
生产实例——β -萘磺酸钠的生产和应用 磺化 SO H
3
