药物化学基础03 化学结构与药理活性
合集下载
化学结构与药理活性
pH
非解离%
解离%
2.0
100.0
0.00
4.0
99.96
0.04
6.0
96.17
3.83
7.0
71.53
28.47
8.0
20.02
79.93
10.0
0.25
99.75
12.0
0.00
100.0
第二章 化学结构与药理活性 第一节败涂地 化学结构与理化性质(Structure Activity Relationship Pharmacokinetic Phase)
3、胎盘屏障和药物分布
第二章 化学结构与药理活性 二、影响药物到达作用部位的因素 (三) 药物的蛋白结合
药物进入血液后与血浆蛋白的结合是影响药物分布、代谢和排泄的重要因素。 药物与血浆蛋白的结合特点:
1、可逆的结合(多数是以氢键、范德华力、疏水键、离子键结合的); 2、结合物不能通透生物膜(药物-蛋白结合物分子量大); 3、药物-蛋白结合物没有药理活性;
药物大多数为有机弱酸和弱碱(见P10,表2-3),在体液中存在着解离平衡。 只有未解离型的药物才能通透脂质的生物膜。 即有机弱酸、弱碱药物的吸收与它们的解离度有关。 那么解离度又与什么有关呢?
二、药物的解离度
解离度与什么有关?
药物的解离度与它的解离常数pKa有关,与药物所处的体内介质的pH有关。 对于酸性药物有: pKa:药物的解离常数; pH:介质的pH。 酸性药物在pH小的介质中,解离度小,未解离型药物浓度高。
04
03
01
02
第一节 化学结构与理化性质
药物的脂水分配系数对药物吸收的影响
疏水常数л具有加和性,即化合物分子的分配系数
非解离%
解离%
2.0
100.0
0.00
4.0
99.96
0.04
6.0
96.17
3.83
7.0
71.53
28.47
8.0
20.02
79.93
10.0
0.25
99.75
12.0
0.00
100.0
第二章 化学结构与药理活性 第一节败涂地 化学结构与理化性质(Structure Activity Relationship Pharmacokinetic Phase)
3、胎盘屏障和药物分布
第二章 化学结构与药理活性 二、影响药物到达作用部位的因素 (三) 药物的蛋白结合
药物进入血液后与血浆蛋白的结合是影响药物分布、代谢和排泄的重要因素。 药物与血浆蛋白的结合特点:
1、可逆的结合(多数是以氢键、范德华力、疏水键、离子键结合的); 2、结合物不能通透生物膜(药物-蛋白结合物分子量大); 3、药物-蛋白结合物没有药理活性;
药物大多数为有机弱酸和弱碱(见P10,表2-3),在体液中存在着解离平衡。 只有未解离型的药物才能通透脂质的生物膜。 即有机弱酸、弱碱药物的吸收与它们的解离度有关。 那么解离度又与什么有关呢?
二、药物的解离度
解离度与什么有关?
药物的解离度与它的解离常数pKa有关,与药物所处的体内介质的pH有关。 对于酸性药物有: pKa:药物的解离常数; pH:介质的pH。 酸性药物在pH小的介质中,解离度小,未解离型药物浓度高。
04
03
01
02
第一节 化学结构与理化性质
药物的脂水分配系数对药物吸收的影响
疏水常数л具有加和性,即化合物分子的分配系数
药物化学第三章 药物的结构与生物活性

HN S
(S)-(-)- 四咪唑 (左旋咪唑)
• 广谱、高效驱虫药,并有增强免疫能力的作用 • ( S ) - ( - ) - 异构体:驱虫作用 • ( R ) - ( + ) - 异构体:呕吐等副作用
沙利度胺(反应停)
O H
N
OO
N H
O
( R) - 异构体
O H
N
COOH
OR (a) R = CONH2
择性
维拉帕米( verapamil )
H3C CH3 N
CH3 CN
OCH3
H3CO OCH3
OCH3
(S)- 维拉帕米: Ca++ 拮抗剂; (R)- 异构体: Ca++ 拮抗活性是 (S) 一体的 1/10 ; (S)- 体和 (R)- 体具有相似的逆转多药耐药性作用
。 (R)- 体能明显提高许多抗肿瘤药物的抗肿瘤活性
结构非特异性药物
药物的药理作用与化学结构类型的关 系不大,主要受药物各种理化性质的影 响。如全身麻醉药,从其化学结构上看 ,有气体,低分子量的卤烃,醇,醚, 烯烃等,其作用主要受药物的脂水 ( 气 ) 分配系数的影响。
结构特异性药物
• 药物的药理作用依赖于药物分子的特异的化 学结构,及其按某种特异的空间相互关系排 列。
依托唑啉( etozoline )
N HS N
COOCH2CH3
O
CH3
(S) - ( - ) - 依托唑啉
• (S)-(-)- 依托唑啉:利尿作用
• (R)-(+)- 依托唑啉:抗利尿作用,能抵消另一 对映体的部分药效。
③ 对映体之一有毒或具有严重的副作 用
四咪唑( tetramisole )
(S)-(-)- 四咪唑 (左旋咪唑)
• 广谱、高效驱虫药,并有增强免疫能力的作用 • ( S ) - ( - ) - 异构体:驱虫作用 • ( R ) - ( + ) - 异构体:呕吐等副作用
沙利度胺(反应停)
O H
N
OO
N H
O
( R) - 异构体
O H
N
COOH
OR (a) R = CONH2
择性
维拉帕米( verapamil )
H3C CH3 N
CH3 CN
OCH3
H3CO OCH3
OCH3
(S)- 维拉帕米: Ca++ 拮抗剂; (R)- 异构体: Ca++ 拮抗活性是 (S) 一体的 1/10 ; (S)- 体和 (R)- 体具有相似的逆转多药耐药性作用
。 (R)- 体能明显提高许多抗肿瘤药物的抗肿瘤活性
结构非特异性药物
药物的药理作用与化学结构类型的关 系不大,主要受药物各种理化性质的影 响。如全身麻醉药,从其化学结构上看 ,有气体,低分子量的卤烃,醇,醚, 烯烃等,其作用主要受药物的脂水 ( 气 ) 分配系数的影响。
结构特异性药物
• 药物的药理作用依赖于药物分子的特异的化 学结构,及其按某种特异的空间相互关系排 列。
依托唑啉( etozoline )
N HS N
COOCH2CH3
O
CH3
(S) - ( - ) - 依托唑啉
• (S)-(-)- 依托唑啉:利尿作用
• (R)-(+)- 依托唑啉:抗利尿作用,能抵消另一 对映体的部分药效。
③ 对映体之一有毒或具有严重的副作 用
四咪唑( tetramisole )
药物化学第三章 药物的结构与生物活性 PPT课件

药物与受体的结合方式主要分为可逆和不可逆两种。 不可逆结合:共价键 可逆结合:非共价键
离子键 氢键 离子-偶极键及偶极-偶极键(定向力) 范德华力(色散力) 疏水键 电荷转移复合物 金属离子络合物
1.药物和受体之间主要的相互键合作用
作用类型
键能(KJ/mol) 有效半径(nm)
发生构象变化,柔性药物分子也会呈现各种构象, 受体只能与药物多种构象中的一种结合,此时的 药物构象成为药效构象,只有能为受体识别并与 受体结构互补的构象。
构型、构象有何区别? 优势构象=药效构象?
相同一种结构,因具有不同构象,可作用于 不同受体,产生不同性质的活性。
只有特异性的优势构象才能产生最大活性: 构象不同,产生生物活性的的强弱不同。
中枢神经系统药物需要需要穿过血脑屏障, 适当增强药物亲脂性,有利于吸收,增强活 性,巴比妥药物lgP在2.0左右。
麻醉药物活性与结构没有明显关系,一般 lgP值越大,麻醉作用越强
药物水溶性与药物形成氢键的数目以及离子 化程度有关。容易离子化的药物可增加其水 溶性。
2.酸碱性和解离度对药物的影响
受体学说
药物 + 受体
药物受体复合物
受体构象改变
药理效应
受体:位于细胞膜或细胞内能识别相应化学信使 并与之结合,产生某些生物学效应的一类物质。
影响药物与受体相互作用的因素有很多 药物受体的结合方式 药物结构中的各官能团 药物分子的电荷分布 药物分子的构型、构象等立体因素
1.药物和受体之间主要的相互键合作用
铂金属络合物 抗肿瘤药物
使肿瘤细胞 DNA的复制
停止。
药物与受体往往是以多种键合方式结合,一般作 用部位越多,作用力越强而药物活性较好。
2.药物结构中的各官能团对药效的影响
离子键 氢键 离子-偶极键及偶极-偶极键(定向力) 范德华力(色散力) 疏水键 电荷转移复合物 金属离子络合物
1.药物和受体之间主要的相互键合作用
作用类型
键能(KJ/mol) 有效半径(nm)
发生构象变化,柔性药物分子也会呈现各种构象, 受体只能与药物多种构象中的一种结合,此时的 药物构象成为药效构象,只有能为受体识别并与 受体结构互补的构象。
构型、构象有何区别? 优势构象=药效构象?
相同一种结构,因具有不同构象,可作用于 不同受体,产生不同性质的活性。
只有特异性的优势构象才能产生最大活性: 构象不同,产生生物活性的的强弱不同。
中枢神经系统药物需要需要穿过血脑屏障, 适当增强药物亲脂性,有利于吸收,增强活 性,巴比妥药物lgP在2.0左右。
麻醉药物活性与结构没有明显关系,一般 lgP值越大,麻醉作用越强
药物水溶性与药物形成氢键的数目以及离子 化程度有关。容易离子化的药物可增加其水 溶性。
2.酸碱性和解离度对药物的影响
受体学说
药物 + 受体
药物受体复合物
受体构象改变
药理效应
受体:位于细胞膜或细胞内能识别相应化学信使 并与之结合,产生某些生物学效应的一类物质。
影响药物与受体相互作用的因素有很多 药物受体的结合方式 药物结构中的各官能团 药物分子的电荷分布 药物分子的构型、构象等立体因素
1.药物和受体之间主要的相互键合作用
铂金属络合物 抗肿瘤药物
使肿瘤细胞 DNA的复制
停止。
药物与受体往往是以多种键合方式结合,一般作 用部位越多,作用力越强而药物活性较好。
2.药物结构中的各官能团对药效的影响
药物化学结构与药理活性

选定适宜的给药途径和恰当的药物剂型,并确保制 剂的质量,是药剂相的决定因素。
概论
药代动力相:包括药物进入血液循环的吸收、 向各组织和器官的分布、与血浆蛋白或体内成 分的非特异性结合、生物转化以及排泄途径等 过程。
生物利用度:一定剂量药物进入机体后,吸收入血 液中的药量和速率。
药效相:是药代动力相的续发,表征药物对机 体的作用。 这一时相是药物在作用部位与生物靶标发生相 互作用,直接引发生物化学或生物物理变化或 通过放大作用(如第二信号系统)或级联反应, 导致人们在宏观上可以观测的生理效应。
因此,有机酸或有机碱类药物的吸收并不取决于它们的总浓度, 而和它们的解离度有关。解离度和药物的pKa值及吸收部位的 pH值有关。即与药物本身的酸碱性有关,与药物吸收时所处 环境的pH值有关。 其关系如下:
①酸性药物的解离:HA+H2O←→A-+H3O+
解离常数Ka为:Ka=([H3O+][A-])/[HA]
二、影响药物到达作用部位的因素
1、药物分子因素。即药物的化学结构与由结构所决定的理化 性质。它包括溶解度、分配系数、电解度、分子间力、氧化还 原电位、电子等排、官能团之间的距离和立体化学。
药物动力相的构效关系
(structure-activity relationship in the pharmacokinetic phase)
2、药物在其中运行的生物学因素。药物分子与细胞间及细胞 内体液,与生物聚合物等相互作用,这种相互作用决定了药物 的吸收、分布和消除特征,决定了药物的生物利用度。 1、药物的分配系数 分配系数P的定义: P=C生物相/C水相
药物化学结构与药理活性PPT课件

药物分子的立体构型
对映异构
对映异构体是具有相同化学组成但空 间结构不同的分子形式,其对药物的 生物活性具有重要影响。
手性分子
手性分子是指不能与其镜像重合的分 子,许多药物分子具有手性,其对药 物的吸收、分布、代谢和排泄过程具 有重要影响。
02
药理活性与化学结构的关 系
药物的作用靶点
药物靶点是指药物在体内的作用 结合位点,包括酶、受体、离子
基于片段的药物设计
片段
指具有特定三维构象和药理活性的小分子基团。基于片段的药物设计是从大量的 化合物库中筛选出与靶点结合的片段,再通过拼接和优化这些片段来发现新药物 。
总结
基于片段的药物设计利用已知活性片段作为药物发现的起点,通过拼接和优化这 些片段,发现具有潜在药理活性的新药物。
计算机辅助药物设计
抗生素的药理活性
抗生素主要用于治疗由细菌引起 的感染。
抗生素通过抑制或杀死细菌的生 长来发挥作用,从而减轻感染症
状,治愈疾病。
不同种类的抗生素具有不同的抗 菌谱和作用机制,它们的化学结 构也各具特点,但都具备抗菌的
药理活性。
镇痛药的药理活性
镇痛药主要用于缓解疼痛。
镇痛药主要通过抑制疼痛信号的传递或抑制前列腺素的合成来发挥作用,达到缓解疼痛的目 的。
药物化学结构与药理活性的跨学科研究
总结词
结合化学、生物学、药理学等多学科知识,研究药物化学结构与药理活性之间的关系。
详细描述
药物化学结构与药理活性之间的关系是复杂而多变的,需要结合化学、生物学、药理学 等多学科知识进行研究。通过跨学科的合作,可以深入了解药物的化学结构与药理活性 之间的关系,为新药的研发提供理论支持和实践指导。同时,这种跨学科的研究也有助
化学结构与药理活性

分子结构的变化
吸收的速度和级数 分布容积 代谢的速度和类型 血清蛋白等的亲和常数、 血清蛋白等的亲和常数、解离常数 消除的速率类型和消除率
二、药效相
作用方式: 作用方式: 1. 结构非特异性药物:生物活性通常不依赖于 结构非特异性药物: 化学结构 2. 结构特异性药物:依赖于药物分子内化学基 结构特异性药物: 团的一种精确结合与空间排列 亲和力 内在活性 药物- 药物-受体的相互作用 受体: 受体:生物体的细胞膜上或细胞以内的一种 特异性大分子结构。 特异性大分子结构。包括激素和神经递质的 受体、 受体、酶、其它的蛋白质和核酸等生物大分 子。 化学结构与药理活性
1)反映药物作用的特异性 (2)有助于解析,认识药物的作用机理
(mechanism of action)和作用方式(mode of action)
(3)由于靶点及药物-靶点三维结构难于确 证,所以通过构效关系可间接阐明,解析 药效和毒性. (4)助于新药设计及合成
• (1)反映药物作用的特异性 反映药物作用的特异性 • 药效的产生:药物同机体的作用部位,即靶点发生 • 相互作用,产生药效 • 药物特异性:是指药物对疾病的某一生理,生化过 • 程有特定的作用,即要求药物仅与疾病治疗相关 • 的靶点产生结合 • 药物选择性:即要求药物对某种病理状态产生稳 • 定的功效.
生理情况下,细胞内外液 稍有差别 细胞内液pH 7.0, 稍有差别, 生理情况下,细胞内外液pH稍有差别,细胞内液 , 细胞外液pH 7.4,因此弱酸性药物在细胞外液解离增多, 细胞外液 ,因此弱酸性药物在细胞外液解离增多, 易导致自胞内向胞外转运。弱碱性药物则相反。 易导致自胞内向胞外转运。弱碱性药物则相反。临床上 有利用此性质促使某些弱酸性药物加速排泄。 有利用此性质促使某些弱酸性药物加速排泄。如巴比妥 类药物中毒,可口服NaHCO3 使血液和体液碱化,可加 使血液和体液碱化, 类药物中毒,可口服 速巴比妥类由脑细胞向血浆转运,进而自尿液排泄。 速巴比妥类由脑细胞向血浆转运,进而自尿液排泄。
药物化学化学结构和药理活性
(四) 药物从体内的消除
资料仅供参考,不当之处,请联系改正。
二、影响药物到达作用部位的因素
• 主要受两大因素的制约. • 一是药物分子因素,即药物的化学结构及由化学结
构所决定的理化性质,如溶解度、分配系数、电离 度、分子间力、氧化还原电位、电子等排、官能 团之间的距离和立体化学. • 二是药物在其中运行的生物学因素,包括药物分子 与细胞间及细胞内体液和与生物聚合物等的相互 作用,这种相互作用决定了药物的吸收,分布和消除 特征,决定了药物的生物利用度.
资料仅供参考,不当之处,请联系改正。
资料仅供参考,不当之处,请联系改正。
三 药物的水溶性
1 氢键 羟基和亚胺基团;可生成的氢键越多,分子的水溶性
越大。
2 解离 离子-偶极键
3水溶性的预测 (1)经验法 有机功能基的碳增溶势
(2)分配系数分析法
分配系数也能预测药物的水溶性。药典关于水溶度的定义,溶解度 大于3.3%为溶解,相当于lgP指0.5。因此以0.5为基准,小于0.5的为 水溶性,大于0.5的为水不溶性的。
第一节
资料仅供参考,不当之处,请联系改正。
化学结构与理化性质
• 一、药物的分配系数
C org
P=
Cw
Corg表示药物在生物非水相或正辛醇中的浓度 Cw表示药物在水相的浓度
• 是评价药物亲脂性或亲水性大小的标准, 即药物在生物非水相中物质的量浓度Corg与 在水相中物质浓度Cw之比。
• 常用其对数lgP表示
• 药物蛋白结合分为可逆和不可逆。在不可逆反 应中,药物通过共价键和蛋白结合。大多数药 物与蛋白的结合时可逆过程,药物以氢键,范 德华力,疏水键和离子键与蛋白结合。
资料仅供参考,不当之处,请联系改正。
资料仅供参考,不当之处,请联系改正。
二、影响药物到达作用部位的因素
• 主要受两大因素的制约. • 一是药物分子因素,即药物的化学结构及由化学结
构所决定的理化性质,如溶解度、分配系数、电离 度、分子间力、氧化还原电位、电子等排、官能 团之间的距离和立体化学. • 二是药物在其中运行的生物学因素,包括药物分子 与细胞间及细胞内体液和与生物聚合物等的相互 作用,这种相互作用决定了药物的吸收,分布和消除 特征,决定了药物的生物利用度.
资料仅供参考,不当之处,请联系改正。
资料仅供参考,不当之处,请联系改正。
三 药物的水溶性
1 氢键 羟基和亚胺基团;可生成的氢键越多,分子的水溶性
越大。
2 解离 离子-偶极键
3水溶性的预测 (1)经验法 有机功能基的碳增溶势
(2)分配系数分析法
分配系数也能预测药物的水溶性。药典关于水溶度的定义,溶解度 大于3.3%为溶解,相当于lgP指0.5。因此以0.5为基准,小于0.5的为 水溶性,大于0.5的为水不溶性的。
第一节
资料仅供参考,不当之处,请联系改正。
化学结构与理化性质
• 一、药物的分配系数
C org
P=
Cw
Corg表示药物在生物非水相或正辛醇中的浓度 Cw表示药物在水相的浓度
• 是评价药物亲脂性或亲水性大小的标准, 即药物在生物非水相中物质的量浓度Corg与 在水相中物质浓度Cw之比。
• 常用其对数lgP表示
• 药物蛋白结合分为可逆和不可逆。在不可逆反 应中,药物通过共价键和蛋白结合。大多数药 物与蛋白的结合时可逆过程,药物以氢键,范 德华力,疏水键和离子键与蛋白结合。
资料仅供参考,不当之处,请联系改正。
第3章 药物的化学结构与生物活性的关系(1,2节)
药物的解离度对活性的影响最经典的例子是 巴比妥药物,下表列出巴比妥类药物在体 液(pH7.4)中分子型(未解离形式)的百分 率。
巴比妥酸和苯巴比妥酸为强酸,在体液 (pH7.4)中,几乎百分之百的解离,不能 透过血脑屏障,所以无活性。苯巴比妥、 海索比妥等巴比妥类药物为弱酸,在 体液 (pH7.4)中,有近50%或更多以分子型存 在,能透过血脑屏障,到达中枢,因此具 有活性。海索比妥有近90以分子型存在, 透膜快所以显效最快。
• 作用于中枢神经系统的药物,需通过血脑 屏障,应具有相对较大的脂溶性。例如全 身麻醉药中的吸入麻醉药,麻醉作用与log P相关,lgP在一定范围 内越大,麻醉作 用越强。巴比妥类药物,logP在0.5~2.0之 间作用最好。因此,适度的亲脂性(lgP 在一定范围内)有最佳药效。
(二)酸碱性与解离度对药效的影响
• 3、药物分子的电荷分布对药效的影响 受体是大分子蛋白结构,其电荷分布不均 匀,而药物的电子云密度分布也不均匀。 药物的电性性质使其与受体可产生电性结 合,与生物活性有密切关系。如果电荷密 度分布正好和其特定受体相匹配,会使受 体和药物相互接近,相互作用增强,药物 与受体容易形成复合物而增加活性。
• 疏水性参数(Lipophilicity parameters ) • 电性参数(Electronic parameters) • 立体参数(Steric parameters )
Hansch方法的一般操作过程
• 从先导化合物出发,设计并合成首批化合物。 • 用可靠的定量方法测活性。 • 确定及计算化合物及取代基的各种理化参数或常 数。 • 用计算机程序计算Hansch方程,求出一个或几个 显著相关的方程。 • 用所得方程,定量地设计第二批新的化合物,并 预测活性。Hansch方程除了研究定量构效关系外, 还能用来解释药物作用机理,推测和描述可能的 受体模型,研究除活性以外的其它药代动力学定 量关系。
化学结构与药理活性关系PPT
99.91 99.01 90.91 50.0 9.09 0.99 0.09
[A -]%or[B]%
0.09 0.99 9.09 50.0 90.91 99.01 99.91
弱酸
外界pH低于pKa 2个单位, 该药99%为分子态,沉淀 完全;
外界pH高于pKa 2个单位, 该药99%为离子态,溶解 完全;
结构非特异性药物
活性主要和理化性质有关
结构特异性药物
活性与化学结构和特定受体作用有关
21
结构非特异性药物
01
在体内具备某种相同的
物理化学性质,就能产
02
生相同的生物活性,与
化学结构的差异关系小
03
全身吸入麻醉药、
04
巴比妥类等
药理活性主要取决于分子的 物理化学性质,而对化学结构 或化学性质的要求无特异性
弱碱
外界pH低于pKa 2个单位, 该药99%为离子态,溶解完 全
外界pH高于pKa 2个单位,
该药99%为分子态,沉淀完
全
10
由Handerson公式得出的经验规律
01
2.肠道pH为7~8,故多数弱碱
性药物(pKa=7.5 ~ 10)在肠 02 道吸收。如可待因( pKa=8.0
),胃中多以离子态存在而不
03 离子型----分子型 04 脂溶性:分子型>离子型…… 05 分子/离子:
药物的酸碱强度 药物吸收时所处环境的pH值
——pH分配学说
8
pH分配学说(Handerson公式)
实际意义何在?
9
不同pH值时分子态、离子态占比
pKa– pH
3 2 1 0 -1 -2 -3
[HA环境pH的关系
[A -]%or[B]%
0.09 0.99 9.09 50.0 90.91 99.01 99.91
弱酸
外界pH低于pKa 2个单位, 该药99%为分子态,沉淀 完全;
外界pH高于pKa 2个单位, 该药99%为离子态,溶解 完全;
结构非特异性药物
活性主要和理化性质有关
结构特异性药物
活性与化学结构和特定受体作用有关
21
结构非特异性药物
01
在体内具备某种相同的
物理化学性质,就能产
02
生相同的生物活性,与
化学结构的差异关系小
03
全身吸入麻醉药、
04
巴比妥类等
药理活性主要取决于分子的 物理化学性质,而对化学结构 或化学性质的要求无特异性
弱碱
外界pH低于pKa 2个单位, 该药99%为离子态,溶解完 全
外界pH高于pKa 2个单位,
该药99%为分子态,沉淀完
全
10
由Handerson公式得出的经验规律
01
2.肠道pH为7~8,故多数弱碱
性药物(pKa=7.5 ~ 10)在肠 02 道吸收。如可待因( pKa=8.0
),胃中多以离子态存在而不
03 离子型----分子型 04 脂溶性:分子型>离子型…… 05 分子/离子:
药物的酸碱强度 药物吸收时所处环境的pH值
——pH分配学说
8
pH分配学说(Handerson公式)
实际意义何在?
9
不同pH值时分子态、离子态占比
pKa– pH
3 2 1 0 -1 -2 -3
[HA环境pH的关系
药物化学第三章-药物的结构与生物活性
范德华力 (Van der Waals force, VDW)
指一个原子的原子核对另一个原子的外围电子的吸 引作用,非极性分子中电子运动产生的暂时偶极间 的极弱引力,也称为色散力。
疏水键 (Hydrophobic bond)
当药物非极性部分不溶于水,水分子在药物非极性分子结构 的外周有序的排列
很多药物是弱有机酸和弱有机碱,这些药物在体液中 可部分解离 解离形式存在[离子型,水溶性的]——易于转运 非解离形式[分子型,脂溶性的]——易于吸收
解离度由化合物解离常数pKa和溶液介质的pH决定 药物发挥作用应有适当的解离度
药物的解离度增加,会使药物的离子浓度上升,未 解离的分子型减少,可减少在亲脂性组织中的吸收
4
抗菌药环丙沙星
斯帕沙星(活性增加16倍)
4、立体因素对药效的影响
药物的立体因素对药效有较大影响 主要包括:
药物分子中官能团的距离对活性的影响 由于药物构型和构象不同而形成的几何异构 光学异构和构象异构对药物活性的影响
(1)药物分子中官能团的距离对活性的影响
药物与受体作用时,一些药效团的特征原子需 要与受体的相关位置相匹配,这些原子间的距 离对它们之间的作用会产生距离上的互补性。
两个对映异构体产生 相同和相等的生物活 性和强度(氯喹)
(3) 对映异构对活性的影响 两种对映异构体产生相反的作用(多巴酚丁
胺)
多巴酚丁胺的左旋体可以激动α1受体,产生血管收缩副作用 其右旋体却拮抗α1受体
(4)构象异构体对活性的影响
药物的能量最低构象称为优势构象 受体和酶的作用部位有高度立体专一性,受体会
当药物和受体的非极性基团(亲脂部分)相互接近,在两个非极 性区之间的水分子有秩序状态减少,导致系统的能量降低, 使两个非极性部分的结合更稳定,这种结合成为疏水键或疏 水作用.
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
米帕明
去甲米帕明
吸烟时吸入烟草中的烟碱,即可脱去氮上的甲基,也可使吡咯 烷环破坏氧化,最终形成亚硝基化合物而诱发肺癌。
(三) 醇的氧化
雌二醇分子中引入17位炔乙基取代,增加空间位阻,使羟基代 谢氧化减慢,因而17α-炔乙基雌二醇是强效雌激素作用药物
甲醇和乙醇的毒性
CH3OH CH2O
与体内有关生命活动的氨基化合物 缩合,因而有高毒性,致命或致盲
One recent study based on GlaxoSmithKline compounds, suggests that the key factors controlling bioavailability are polar surface area and molecular flexibility (number of rotatable bonds), and it was suggested, perhaps controversially, 10 that drug molecular weight might be increased if these properties are kept under control. J. Med. Chem. 2004, 47, 6338-6348
不同给药方式的吸收
吸收是指药物从用药部位进入血液循环的过程 静脉给药没有吸收问题 (1)消化道吸收:药物从肠胃道粘膜吸收,主要通过被 动转运;
(2)注射部位吸收:皮下或肌内注射药物先沿结缔组织 扩散,后经毛细血管和淋巴内皮细 胞进入血液循环;
(3)呼吸道吸收:小分子酯溶性挥发性的药物或气体可 从肺泡上皮细胞迅速吸收;
红霉素 Erythromycin
克拉红霉素 clarithromycin
药物的亲脂性
戊巴比妥的氧换成硫,成为硫巴比妥。由于硫的原子半径比 氧大,形成氢键的趋向减低,亲脂性增加,起效快
戊巴比妥
硫喷妥
改变药物的亲水性
喜树碱不溶于水,引入碱性基团,可形成水溶性的三氟乙酸盐, 抗癌作用增强
irinotecan
药物在体内的过程
药物的ADMET
ADMET (药物的吸收, 分配, 代谢, 排泄和毒性)药物 动力学方法是当代药物设计和药物筛选中十分重要的方 法。药物早期ADME/T性质评价方法可显著地提高药物 研发的成功率,降低药物的开发成本,减少药物毒性和 副作用的发生,并能指导临床合理用药。
A:Absorption :药物从作用部位进入体循环的过程 D:Distribution :药物吸收后通过细胞膜屏障向各组织、器官或者体液进行转运的过程 M:Metabolism(Biotransformation):药物在体内受酶系统或者肠道菌丛的作用而发 生结构转化的过程 E :Excretion:药物以原型或者代谢产物的形式排出体外的过程 T:Toxcity:药物对机体的毒性 ADMET就是对药物的吸收、分布、代谢、排泄和毒性进行全面的研究。 其中ADME是药物代谢动力学(Pharmacokinetics, PK)的研究内容
水杨酸和对氨基水杨酸的缩合
抗爱滋病药齐多夫定的代谢转化和缩合
谷胱苷肽带有巯基,可加成至药物的亲电中心:
降血压药氯倍特
药物代谢在药物研究中的作用
结构修饰改变代谢转化的速率
肾上腺素β受体拮抗剂美托洛尔有降低血压、减慢心率等效应, 但因甲氧基的甲基在代谢转化时很易脱除,药物作用持续不长。 增加位阻后,代谢大为减缓,药理作用便延长。
水解反应常用来设计前药
(八) 乙酰化反应
磺胺、肼、对氨基苯甲酸等在体内都可在氨基上进行乙酰化
(九) 甲基化反应
儿茶酚胺通过儿茶酚胺转甲基酶的作用,环上间位羟基进行甲 基化而代谢转化。利用这性质,将儿茶酚胺的间位羟基改造为 羟甲基,甲基化反应受阻,药物的作用时间变长。
代谢转化的最终目的是将外来物质变为水溶性,以利 于排泄,药物经上述第I相转化后便和葡萄糖醛酸、硫 酸、氨基酸等缩合。
临床应用丙磺舒抑制penicillin和indomethacin等的主动分泌而提高血浓度和效应; 而依他尼酸用药时因其抑制尿酸的主动分泌,导致尿酸增多产生痛风
四、药物的代谢转化
药物或毒物进入体内,大多经酶的催化进行化学变化,成为水 溶性化合物排出体外。在一系列的化学转化中,有的代谢产物 具有高度活性(包括毒性),有的产物不具有活性,有毒化合物 转化为无活性的化合物,便产生解毒效果。
CH3CH2OH
CH3CHO
可与儿茶酚胺等氨基化合物缩合
工业酒精
兑成劣质白酒
(四) 含氮化合物的氧化
氨基或杂环上的氮代谢氧化可生成氮氧化物、羟胺、羟胺酸 RCONHOH等化合物,这类产物毒性较高,可导致溶血、致畸、 致癌等作用,或导致变性血红蛋白的产生。
醋氨酚、非那西丁等药物的氨基都可在体内羟化,醋氨酚的肝脏毒性由于氧化, 非那西丁的羟氨化产物对大鼠有致癌作用,利多卡因环上有两个邻位甲基产生位 阻,氨基难以氧化,因而没有致癌性。
阻滞代谢转化,消炎镇痛效果更好
加速药物的代谢转化,缩短药效果
胺碘酮对肝脏、肾脏、肺脏有毒性,改进后成为短效药物
药物的理化性质
任何药物均需及时抵达作用部位,并维持一定的浓度和时间, 才能与受体结合,产生一定的药理作用,从而发挥预期的治疗 作用。 血管外给药,必须先被吸收,才能输送到全身:首先,药物必 须有一定的水溶性,才能通过体液转运;另一方面,药物必须 通过生物膜,才能进入细胞以内,这个过程称为转运。 生物膜的主要成分是脂质,药物必须有一定的脂溶性,才能透 过生物膜。 主动转运:通过膜上的特异性载体蛋白,摄取氨基酸、糖类、 嘌呤、嘧啶等生命必需物质; 被动转运:药物分子等外源性物质由高浓度一侧扩散到低浓度一侧
除了电离度以外,氢键形成的趋势也是支配药物水溶性的一个因素: COOH, CO, OH, NH2, NHR, NR2, NR3等增加水溶性;醚,硫醚, 卤素等增加亲脂性。 油水分配系数P定义:药物在正辛醇和水中浓度的比值
脂相药物浓度
P= 水相药物浓度
cLogP: calculated logP aLogP: analyzed logP
ADME与药效关系
药效产生依赖于吸收(A)和分布(D);
代谢(M)和排泄(E)则控制了药物的作用过程和持效时间;
药物的ADME与药物的化学结构和理化性质密切相关。
一、药物吸收
药物的吸收除受肠胃道pH值、食物中的脂肪量和药物在胃肠道 的代谢生理因素影响外,其化学结构、酸碱性解离度脂水分配 系数晶形及颗粒大小等均有显著影响。 静脉或皮下注射100%吸收
(二) 脱烷基反应
氨基上的取代基也以同样的机理脱去
RNHCH3 RNHCH2OH RNH2 + CH2O
氧上脱除甲基后,抗心律失常作用变强, 氮上再脱除甲基后,活性与原药相当。
抗抑郁药米帕明(imipromine)代谢转化脱去氨基上的甲基, 成为去甲米帕明(desipramine),活性更有增强,也可环上 第二位氧化为羟基。
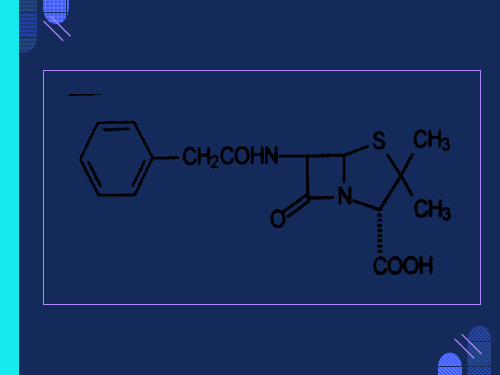
第三章化学结构与药理活性
药物的化学结构与生物活性间的关系,通常称为构效 关系(Structure-activity relationships, SAR),是药物 化学研究的主要内容之一。药物在体内与特定的受体 部位发生相互作用,引发出生物活性,药物的化学结 构必须与受体大分子的结构相互匹配。药物化学结构 改变会引起药理活性发生变化,药物的化学结构还决 定其理化性质,影响药物在体内的吸收、分布和代谢 等。因此药物的药理活性与药物的理化性质有关,与 药物结构中电子云密度有关,与药物的立体化学结构 有关。
(一) 羟化反应
氧化是代谢转化中常见的反应,其中羟化反应为将碳所连接 的氢原子氧化为羟基 烯丙位羟化
脂肪链的羟化:
末端或靠近末端位置羟化
甲磺丁尿环上的甲基可代谢转化为羟甲基,于是就失去活性。 如将甲基改成氯,就可增加代谢的稳定性,从而延长对糖尿病 的治疗作用:
芳环在代谢过程中,先成环氧化合物,再裂环成酚。给电子 基团加快反应速度,吸电子基团基团,代谢速度变慢。
topotecan
改变药物的亲水性
降低青光眼患者眼压,但是有中枢神经副作用,引入氨基,脂溶 性降低,无中枢神经副作用
可乐定
氨基可乐定
Drug Likeness
Only 11% of drugs enteringclinical development reach the market place, being withdrawn for reasons associated with efficacy (25%), toxicology (24%), clinical safety (12%), drug metabolism and pharmacokinetics (DMPK, 8%), formulation (1%), and portfolio and other reasons (30%).2 Thus, of 70% of failures caused by specific effects, 45% can be ascribed to DMPK, safety, and formulation properties related to the physicochemical nature, or druglikeness, of the drug candidate itself. The proportion may even be higher, since some reported “efficacy” failures might be due to poor DMPK. For oral drug
药物研发早期ADMET性质研究主要以人源性或人源化组 织功能性蛋白质为“药靶”,体外研究技术与计算机模拟等 方法相结合,研究药物与体内生物物理和生物化学屏障 因素间的相互作用。
