九年级化学上册第二部分期末复习攻略综合专题六化学方程式课件新版新人教版
合集下载
新人教化学九上课件: 化学方程式

课件目录
首页
末页
第五单元 课题1 第2课时 化学方程式
7.[2018·玉林]洁厕灵、84 消毒液是两种常见的清洁、消毒用品,混合 使用时会发生如下反应:
下列说法正确的是( B ) A.该反应是分解反应 B.有毒气体是 Cl2 C.反应前后元素化合价不变 D.84 消毒液、洁厕灵能混合使用
课件目录
首页
第五单元 课题1 第2课时 化学方程式
第五单元 化学方程式
课题1 质量守恒定律 第2课时 化学方程式
学习指南
知识管理
归类探究 当堂测评
分层作业
课件目录
首页
末页
第五单元 课题1 第2课时 化学方程式
学习指南
知识管理
归类探究 当堂测评 分层作业
化学方程式的意义
例1
1 题 1、2、5~7 题
化学方程式的读法
首页
末页
第五单元 课题1 第2课时 化学方程式
分层作业
点击进入word链接
课件目录
首页
末页
第五单元 课题1 第2课时 化学方程式
参考答案
点击进入答案PPT链接
点击进入答案word链接
课件目录
首页
末页
课件目录
首页
末页
第五单元 课题1 第2课时 化学方程式
点燃 下列关于化学方程式 4P+5O2=====2P2O5 的读法,错误的是( B ) A.磷和氧气在点燃的条件下反应生成五氧化二磷 B.在点燃的条件下,每 4 体积的磷和 5 体积的氧气完全反应,生成五氧 化二磷 C.在点燃的条件下,每 4 个磷原子和 5 个氧分子结合生成 2 个五氧化二 磷分子 D.在点燃的条件下,每 124 份质量的磷和 160 份质量的氧气完全反应, 生成 284 份质量的五氧化二磷 【解析】 化学式前的系数表示参加反应的微粒个数比,且 P 是固体,不 能表示体积比。
人教九年级化学(上)化学方程式(PPT复习课件)

知识点四
化学方程式的意义和读法
【典型例题4】
(
2020年北京市朝阳区中考一模)下列关于2CO+O2
点燃
===
2CO2的理解
【答案】C
知识点一
质量守恒定律
【变式训练1】 (2020年云南省中考)建立“宏观-微观-符号”之间的联系是学习化学的 思维方法。下图是汽车尾气中某些有害气体在催化剂作用下转化为空气中的无毒成分 的微观示意图。下列有关说法不正确的是( ) A .反应前后原子的种类和数目都没有发生改变 B .参加反应的两种物质的分子个数比为2 : 3 C .化学反应前后氮元素的化合价发生了改变 D .在化学反应中,分子可以再分,原子不可再分
应用
(2)计算化学反应中某些物质的质量; (3)确定组成物质的元素或物质的化学式;
(4)解释化学反应前后质量增加或减少的原因并进行相关的计算。
知识点一
质量守恒定律
【重难点1】化学反应过程中的变与不变
化学反应
种类
应用
六个
物质的总质量、 解释化学反应前后质量变化或确定某一物质的质量;
宏观 元素 种类、
元素 质量 。
确定生成物或反应物的元素组成;
不变
原子 种类 、
微观 原子 个数 、 确定未知物质的化学式或化学计量数;
原子 质量 。
两个 宏观 物质 种类 一定变 微观 分子 种类
化学方程式的书写或判断;
两个 宏观 元素化合价 氧化反应和还原反应的判断;
可能变 微观 分子个数
化学反应基本类型的判断。
化学方程式
考试说明
第五单元 化学方程式
1、 认识质量守恒定律,能说明化学反应中的质量关系;
2、 能正确书写简单的化学反应方程式; 考纲要求
人教版初中化学《化学方程式》复习专题课件(共29张PPT)

加入黄铜样品质量
20g
24g
20g
充分反应后,烧杯+剩余物质质量 158.8g 152.8g 148.8g
(1) 丙同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质
量是
0。.2g
Zn + 2HCl = ZnCl2 + H2↑
(2)计算黄铜样品中锌的质量分数。
(2)解:设黄铜样品中参加反应锌的质量为x
S+O2
点燃
SO2
32 32
64
1.下列关于S+O2 点燃 SO2的理解不正确的是( B )
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2∶1 1∶1
C.反应前后硫原子、氧原子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为1∶1
2.根据化学方程式2H2O 通电 2H2↑+O2↑,无法获取的信息是( D ) A.反应所需条件 B.生成物的状态 C.参加反应的反应物与生成物之间的质量比 D.氧气可助燃
所得KCl溶液中溶质的质量分数为
答:(1)混合物样品中KCl的质量分数为50%。 (2)当恰好完全反应时,所得溶液中溶质的质量分数为10%。
58
149
5.8 g
y
样品中KCl的质量分数为 所得KCl溶液中溶质的质量分数为
答:当恰好完全反应时,所得溶液中溶质的质量分数为10%。
解:设混合物样品中MgCl2的质量为x,反应生成KCl的质量为y。
MgCl2+2KOH
Mg(OH)2↓+2KCl
95
58
149
x
5.8 g
y
样品中KCl的质量分数为
九年级化学复习专题
化学方程式 复习 课件 初中化学人教版九年级上册(2021-2022学年)

3NaHCO3 + C6H8O7
C6H5O7Na3 +3H2O +3CO2 ↑
3×84 192
1.5 g x
x =1.1 g
3×84 192
=
1.5 g x
答:通过计算判断柠檬酸有剩余, 符合气泡水微酸的口感。
7
实际应用
7-6 动手操作
准备:矿泉水、白糖或蜂蜜、果汁、食品级柠檬酸、 碳酸氢钠、500 mL塑料瓶
1. 实验过程中你观察到了什么现象? 2. 甲烷充分燃烧生成了什么物质? 3. 你能找到影响甲烷充分燃烧或不充分
燃烧的关键物质吗?
初中化学
3 寻找关键物质
初中化学
蓝色火焰
生成无色液滴 澄清石灰水变浑浊
甲烷充分燃烧生成H2O和CO2
3 寻找关键物质
CH4
H2O + CO2
?
初中化学
3 寻找关键物质
初中化学
3 寻找关键物质
CH4 + O2
物质种类 元素种类 关键物质
H2O + CO2
变化前
CH4 CHO
O2
变化后 H2O + CO2 CHO
初中化学
4 书写化学方程式 ① ② ③ ④
初中化学
?
✔
4 书写化学方程式
初中化学
蓝色火焰 ①
生成无色液滴 澄清石灰水变浑浊
点燃
✘
4 书写化学方程式
②
初中化学
7
实际应用
7-2 查阅资料
初中化学
7
实际应用
7-3 寻找关键物质
配料:水、赤藓糖醇、二氧化碳、碳酸氢钠、柠檬酸、 三氯蔗糖、山梨酸钾、食用香精
人教版九年级化学上册《化学方程式》ppt
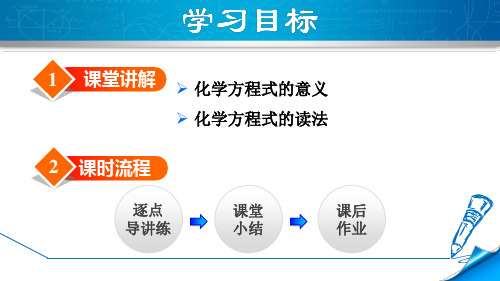
程 意义 量的意义:①表示反应物和生成物间的质量比
式
②表示参加反应和生成的各粒子 的数量关系
表示反应条件
化
宏观读法
学 方
读法
微观读法
程
质量读法
式
点燃
C+O2======CO2 1 2 : 1 6×2 : 12+16×2
12 : 32 : 44
2 易错小结
7.关于化学方程式CH4+2O2=点==燃=CO2+2H2O的描述 正确的是( )
2)微观读法:1个碳原子和1个氧原子反应生成1个二氧化 碳分子。
3)量的读法:每12份质量的碳和32份质量的氧气 完全反应生成 44份质量的二氧化碳。
归纳
知2-导
①“+”不能读成“加”,应读“和”、“与”、“跟”。 ②“=”不能读成“等于”,应读“生成”。 ③化学式应读成物质的名称。 ④反应条件也应读出。
(1)铜粉在空气中加热,是铜和氧气发生了化学反应。 根据质量守恒定律,反应后生成物的质量,一定等 于参加反应的铜粉和氧气的质量总和,所以生成物 的质量比原来铜粉的质量大。
(2)由于纸中的碳、氢元素与氧气反应生成二氧化碳、 水蒸气等气体后逸出,故灰烬的质量比纸的质量小。
(3)高锰酸钾受热分解后,生成锰酸钾、二氧化锰和氧气。 根据质量守恒定律,参加反应的高锰酸钾的质量一定 等于生成的锰酸钾、二氧化锰和氧气的总质量,由于 氧气的逸出,所以,反应剩余固体的质量必然小于原 反应物的质量。
是化合反应
各物质的分子 个数比为2:1:2
各物质的质量 比为1:8:9
点燃
A.S+O2=====SO2
知1-讲
点燃
B.2CO+O2=====2CO2
5.2化学方程式 课件-人教版九年级化学上册
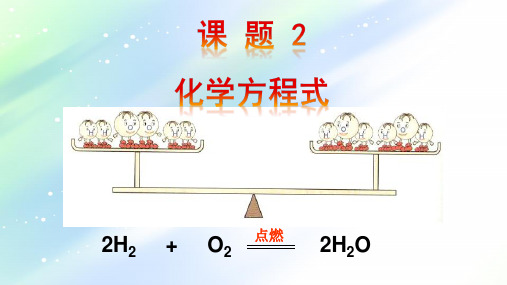
化学方程式: C +
氧气 点燃 二氧化碳
反应条件 生成
O2 点燃
CO2
如: 3Fe + 2O2 点燃 Fe3O4
2KMnO4
K2MnO4 + MnO2 + O2
质这的是含什义么:式碳子和?氧它气可在以点提燃供条件下
化 哪些信息?反它应怎生么成读二呢氧? 化碳
学
方 程
C + O2 点燃 CO2
微观含义; 每一个
C + O2点燃 CO2 反应物:C、O2。生成 物:CO2。条件:点燃
C + O2点燃 CO2
12 :16×2 :12+16×2
12 : 32 : 44
C + O2点燃 CO2
1 :1 : 1
1、所有的化学反应必须遵守 质量守恒 定律? 为什么质量会守恒呢? 在化学反应中,反应前后原子的种类没有改变, 数目没有增减,原子的质量也没有改变。
生成物的化学 式书写错误
2. H2O 通电 H2↑ + O2↑
没有配平
3. Fe+CuSO4
Cu↓+ FeSO4
不应该标生 成物的状态
4. 2KMnO4 Δ K2MnO4+ MnO2+ O2
未标明气 体的状态
点燃
5. Mg+ O2 Mg2O
不应该在化学 式中间配平
6. 4H2O2 MnO2 4H2O+2O2
③ 化学计量数1可以省略不写,各化学式前的计量数 必须是最简整数比。
课堂练习:配平铁在氧气中燃烧生成四氧化三铁的
化学方程式。
点燃
3 Fe +2 O2
Fe3O4
(1)观察法
氧气 点燃 二氧化碳
反应条件 生成
O2 点燃
CO2
如: 3Fe + 2O2 点燃 Fe3O4
2KMnO4
K2MnO4 + MnO2 + O2
质这的是含什义么:式碳子和?氧它气可在以点提燃供条件下
化 哪些信息?反它应怎生么成读二呢氧? 化碳
学
方 程
C + O2 点燃 CO2
微观含义; 每一个
C + O2点燃 CO2 反应物:C、O2。生成 物:CO2。条件:点燃
C + O2点燃 CO2
12 :16×2 :12+16×2
12 : 32 : 44
C + O2点燃 CO2
1 :1 : 1
1、所有的化学反应必须遵守 质量守恒 定律? 为什么质量会守恒呢? 在化学反应中,反应前后原子的种类没有改变, 数目没有增减,原子的质量也没有改变。
生成物的化学 式书写错误
2. H2O 通电 H2↑ + O2↑
没有配平
3. Fe+CuSO4
Cu↓+ FeSO4
不应该标生 成物的状态
4. 2KMnO4 Δ K2MnO4+ MnO2+ O2
未标明气 体的状态
点燃
5. Mg+ O2 Mg2O
不应该在化学 式中间配平
6. 4H2O2 MnO2 4H2O+2O2
③ 化学计量数1可以省略不写,各化学式前的计量数 必须是最简整数比。
课堂练习:配平铁在氧气中燃烧生成四氧化三铁的
化学方程式。
点燃
3 Fe +2 O2
Fe3O4
(1)观察法
化学方程式 初中九年级化学上册课件
A.X3Y2 B.X2Y3 C.X3Y4
D.XY2
5. a g白磷在b g氧气中燃烧,生成五氧化二磷的质量~~~( D )
A.一定是(a+b)g B.一定不足(a+b)gC.大于(a+b)g来自D.小于或等于(a+b)g
6.某种物质R发生反应的化学方程式为:
2R+2H2O+7O2=2FeSO4+2H2SO4,则R的化学式为 ~~~( D )
Fe + CuSO4 = FeSO4+Cu
56
160
152 64
在加热条件下氢气与氧化铜反应
CuO + H2 △ Cu + H2O
80
2
64 18
2.现将10克A和足量B混合加热,A与B发生化学 反应,10克A完全反应后生成8克C和4克D,则 参加反应的A与B的质量比为~~~~~( D )
A.1︰1 B.2︰1 C.4︰1 D.5︰1
第五单元 化学方程式
1
复习提问:
1.什么叫质量守恒定律? 参加化学反应的各物质的质量总和等
于反应后生成的各物质的质量总和。 2.为什么化学反应前后各物质的质量总和相
等? 答:因为在化学反应前后,各种原子的种
类、数目、质量都没有发生变化。
2
学习目标:
1.了解化学方程式的概念。 2.理解化学方程式的意义。 3.知道化学方程式的读法。 重难点:
下列说法中不正确的是~~~~~~~~~~~( A )
物质
X
Y
Z
Q
反应前的质量
4
10
1
25
反应后的质量
待测
21
10
9
A.该反应为分解反应 B.该反应遵守质量守恒定律 C.X中待测值为零 D.若Q为氧气,则该反应为氧化反应
人教版九年级上册化学《化学方程式》课件
下列说法中,不正确的是( C ) A.物质甲是单质 B.丙分子中A、B原子个数比为3∶1 C.反应前后原子的个数没有改变,分子的个数 也没有改变 D.根据质量守恒定律可推知,乙的化学式为A2
微观
原子种类 原子质量 原子数目
物质的种类 改变 分子的种类 元素的化合价 可能 改变 分子数目
化 学 方 程 式
思考:
怎样用一个式子来表示化学反应呢?
如:木炭在氧气中燃烧生成二氧化碳
碳 + 氧气
点燃
二氧化碳
该式子确实能表示反应物、生成物及反应条件; 但书写不方便、国际上也不通用且不能体现质量守 恒定律。
课题1
第二课时 化学方程式
学习目标
• 记住化学方程式能提供的相关信息
旧知回顾 1、质量守恒定律:
参加化学反应的各物质质量总和,
2、化学反应前后总质量守恒的实质
等于反应后生成的各物质质量总和。
反也没有改变。
宏观
元素种类 不 元素质量 物质的总质量 变
2、化学方程式表示的意义:
(1)表明了反应物、生成物及反应条件; (2)表明了反应物和生成物各物质的粒子 个数之比; (3)表明了反应物和生成物各物质的质量 之比(即各物质的相对分子质量与化 学式前的计量数的乘积之比);
点燃
2H2 + O2
2× 2 4
32 : 32
2H2O
:
18×2 36
3、化学方程式的读法:
1、化学方程式 用化学式来表示化学反应的式子。
化 学 方 程 式
文字表达式:
碳
+ 和
氧气 二氧化碳 反应条件 生成
点燃
化学方程式:
C
+
