急性髓细胞白血病M2亚型细胞形态学及细胞遗传学分析
儿童白血病诊疗规范

儿童白血病诊疗规范【总论】急性白血病是造血系统的恶性疾病,居儿童恶性肿瘤发病率的首位,亦是儿童时期的主要死亡原因之一。
儿童白血病发病率约34/100万,每年新发生的白血病患儿为15000 - 20000名。
其中90%以上为急性白血病,急性淋巴细胞白血病(ALL)约占2/3。
急性髓性细胞白血病( AML)占1/3。
近20年来,儿童白血病的疗效有了很大进步,目前国内外先进治疗组用化疗方法已使ALL的5年无病生存率达70%-80%。
AML化疗及造血干细胞移植的效果可达40% -50%。
(一)定义白血病是造血系统的恶性疾病,主要是造血器官内白血病细胞恶性增生和非造血器官内的白血病细胞浸润。
白血病细胞分别由造血系统的粒、红、巨核、淋巴及单桉系细胞恶性转化而来。
根据白血病发病的单克隆学说,白血病是由一个最先突变的白细胞经过不断增殖和发展而形成。
它具有异常形态、代谢及功能,它呈无限制的生长,失去分化成熟的功能。
(二)病因和发病机制病因尚未明确,但可能和遗传和环境因素都有关系。
1. 遗传学研究发现,Down综合征患者患急性非淋巴细胞白血病的概率比非Down综合征患者高出4倍。
神经纤维瘤、先天性中性粒细胞减少症都与肿瘤的高发有关。
如果家庭中有一个成员发生白血病,其近亲患病率比普通人群3-5倍。
2.环境:危险因素包括电离辐射,烷化剂,拓扑异构酶Ⅱ抑制剂的应用等。
有证据表明接触拓普异构酶Ⅱ抑制荆能导致儿童期患急性白血病。
(三)临床表现1.症状(1)起病多较急,发热常为首发症状,热型不定。
贫血为进行性加重,常见乏力、气促等,皮肤出血点或瘀斑,口腔黏膜出血,鼻出血,消化道出血等。
贫血严重者可听到心脏杂音。
(2)白血病细胞浸润表现:①患者常有不同程度的肝、脾、淋巴结肿大。
②白血病细胞浸润皮肤可有结节、肿块及斑丘疹等。
③骨浸润可以有骨痛,病理性骨折。
④中枢神经系统白血病:早期通常通过脑脊液检查发现白血病细胞,晚期可见颅神经麻痹,末梢神经炎等症状。
细胞遗传学分析

六、骨髓异常增生综合症(MDS)
1 、 异常检出率:30-50%,以缺失(整个 或部分缺失)多见,获得(额外未知起 源的物质)其次,易位少见 2 、 缺失:del(5q)最常见,del(20q), del(11q),del(7q)其次,del(13q) 少见
七、白血病染色体畸变的临床和生物学意义
其余患者则涉及3条或更多染色体其中必 定包括9和22号染色体在内的复杂易位
加图2(示ph)120
产生BCR/ABL融合基因 9q34 的 ABL 原癌基因易位到 22q11 上 和 BCR 基因部分融合产生 BCR/ABL 融合 基因 BCR/ABL融合蛋白具激酶活性
2、CML慢性期的染色体改变 Ph见于95%的CML患者( Ph(+)CML )
• 144
3、inv(16)(p13q22) AML-M4
inv(16)(p13q22)见于25%AML-M4 形成CBFB- MYH11融合基因 构成M4EO亚型 M4EO亚型放化疗效果好,CR近100%,MS达5 年
• 图57
• 153
五、急性淋巴细胞白血病(ALL)
大约60%-85%的ALL患者可检的检出有助于白血病的诊 断和鉴别诊断 克隆性染色体异常的发现是诊断MDS或白血 病的主要依据,据此可与其他非恶性血液病进 行鉴别
2 、特异性染色体重排的发现不但有助于 AML 和 ALL 的鉴别,而且有助于进一步识别它们中的各 自亚型 MICM(morphologic , immunologic , cytogenetic and molecular biologic) 将特异性染 色体重排和细胞形态学特征、免疫学表型和分 子生物学特性等一起列为白血病诊断分型的重 要指标
急性髓细胞白血病
急性髓细胞白血病要点1:分类M1(急性粒细胞白血病微分化型)、M2(急性粒细胞白血病部分分化型)、M3(急性早幼粒细胞白血病)、M4(急性粒-单核细胞白血病)、M5(急性单核细胞白血病)、M6(急性红白血病)和M7(急性巨核细胞白血病)。
要点2:急性粒细胞白血病外周血基本特点:贫血、部分白血病可见幼红细胞,例如M1、M6和M7;白细胞数多数增高,但有的病例可以正常,甚至减少,减少多见于M6和M7;出现大量幼稚细胞,特别是原始细胞是主要的特征,原始和幼稚细胞应超过30%;M3以异常早幼粒细胞为主,可高达90%;M4原单和幼单细胞可占30%~40%,M5原单和幼单可占30%~45%。
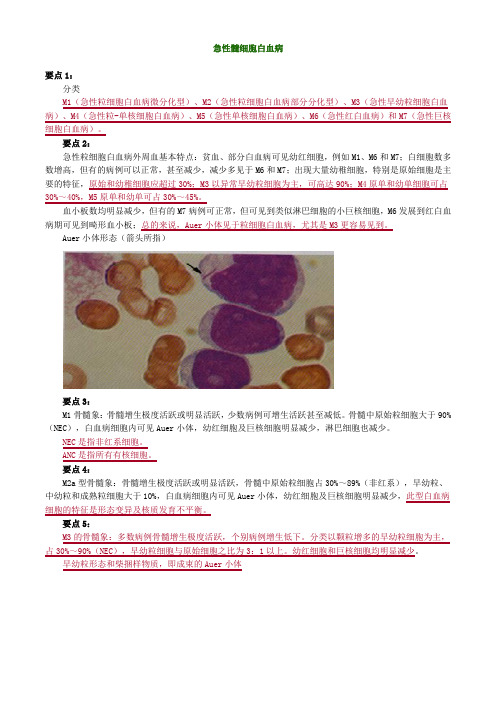
血小板数均明显减少,但有的M7病例可正常,但可见到类似淋巴细胞的小巨核细胞,M6发展到红白血病期可见到畸形血小板;总的来说,Auer小体见于粒细胞白血病,尤其是M3更容易见到。
Auer小体形态(箭头所指)要点3:M1骨髓象:骨髓增生极度活跃或明显活跃,少数病例可增生活跃甚至减低。
骨髓中原始粒细胞大于90%(NEC),白血病细胞内可见Auer小体,幼红细胞及巨核细胞明显减少,淋巴细胞也减少。
NEC是指非红系细胞。
ANC是指所有有核细胞。
要点4:M2a型骨髓象:骨髓增生极度活跃或明显活跃,骨髓中原始粒细胞占30%~89%(非红系),早幼粒、中幼粒和成熟粒细胞大于10%,白血病细胞内可见Auer小体,幼红细胞及巨核细胞明显减少,此型白血病细胞的特征是形态变异及核质发育不平衡。
要点5:M3的骨髓象:多数病例骨髓增生极度活跃,个别病例增生低下。
分类以颗粒增多的早幼粒细胞为主,占30%~90%(NEC),早幼粒细胞与原始细胞之比为3:1以上。
幼红细胞和巨核细胞均明显减少。
早幼粒形态和柴捆样物质,即成束的Auer小体早幼粒形态和柴捆样物质,即成束的Auer小体要点6:M4型骨髓象:骨髓增生极度活跃或明显活跃。
粒、单核两系同时增生,红系、巨核系受抑制。
急性髓细胞白血病M2型的护理措施

住环境,避免交叉感染 加强个人卫生:勤洗手,戴口罩, 02 避免接触感染源 合理使用抗生素:根据医生建议, 03 合理使用抗生素,避免滥用 监测体温:定期监测患者体温,
04
及时发现感染迹象,及时处理
饮食护理
STEP1
STEP2
STEP3
STEP4
饮食清淡,易消 化,避免油腻、 辛辣、刺激性食 物
贫血:注意观察患者血红蛋白、红细胞计数 等指标,及时采取输血等措施。
神经系统并发症:注意观察患者意识、精 神状态等,及时采取对症处理措施。
感谢您的观看
制作人:刀客特万
观察患者的药物 反应、治疗效果
等
治疗配合
01 02 03 04
01
患者教育:向患者及家属解释治疗 方案、副作用及注意事项
02
心理支持:鼓励患者保持积极心 态,减轻焦虑和恐惧
03
药物管理:确保患者按时按量服用 药物,避免漏服或过量
04
监测病情:密切观察患者病情变化, 及时报告医生并采取相应措施
心理支持
急性髓细胞白血病M2 型的护理措施
刀客特万
目录
01 急性髓细胞白血病M2型的概述 02 护理措施 03 护理注意事项
急性髓细胞白血病2型的 概述
疾病定义
急性髓细胞白血 病M2型是一种 急性白血病,属 于髓系白血病
01
主要表现为贫 血、出血、感 染等症状
03
02
发病率较高, 占所有白血病 的10%-15%
01 倾听患者:耐心倾听患者 的感受和需求,给予关心 和支持
02 鼓励患者:鼓励患者积极 面对疾病,增强信心和勇 气
03 提供信息:提供有关疾病 和治疗的信息,帮助患者 了解病情和治疗方案
aml病理诊断标准

aml病理诊断标准急性髓性白血病(AML)是一种原发于骨髓幼稚细胞的异质性疾病,通常表现为骨髓、外周血和组织器官中的白血病细胞增生和浸润。
尽管AML的确切发病机制尚不完全清楚,但研究人员已经确定了多种可能与AML发病相关的因素,包括基因突变、染色体异常、环境暴露和遗传风险。
这些因素的综合作用可能导致幼稚造血细胞失去正常的分化和成熟过程,从而导致AML的发生。
在诊断AML时,病理学家通常需要考虑一系列临床、组织学和分子生物学特征。
虽然某些标准诊断标志在不同的实验室和研究中可能有所不同,但一般而言,AML病理诊断标准包括细胞形态学、免疫表型、细胞遗传学和分子生物学标志。
在细胞形态学方面,AML的诊断常常要求对骨髓、外周血或组织病理标本进行细胞学检查。
AML细胞通常表现为高度异型增生、异形核、细胞浆异常和核分裂不良等特征。
标本的染色质形态学特征也可能对AML的诊断和分型提供重要线索。
此外,免疫表型分析也是AML病理诊断的重要一环。
通过检测AML细胞表面和细胞内的特异标志物,包括CD系列标志和其他免疫亚型标志,可以帮助病理学家确定AML的类型和亚型。
例如,CD34阳性和CD117(c-kit)阳性表型通常与AML的幼稚细胞相关,而MPO(过氧化物酶)或CD33阳性表型常见于AML的粒细胞亚型。
此外,细胞遗传学分析是AML病理诊断中不可或缺的一部分。
常见的染色体异常,如t(8;21),t(15;17)和inv(16),以及各种其他染色体改变,如NPM1、FLT3等基因突变,可以帮助确定AML的亚型和预后。
分子生物学技术的进展也为AML的病理诊断提供了新的机会,例如通过检测AML相关基因或染色体异常的特定融合基因来帮助确定AML的亚型和预后。
让我们总结一下本文的重点,我们可以发现,AML的病理诊断需要综合考虑多种临床、组织学和分子生物学特征。
虽然现有的AML病理诊断标准已经相对完善,但仍需要进一步深入研究和探讨,以提高AML的早期诊断率和治疗效果。
形态学及免疫分型倾向AML-M2的急性早幼粒细胞白血病1例报道

doi:10.3971/j.issn.1000-8578.2023.22.1212形态学及免疫分型倾向AML-M 2的急性早幼粒细胞白血病1例报道彭惜茹1,赵翔宇1,成娟1,2Morphological and Immunophenotypic Tendency of AML-M 2 in Acute Promyelocytic Leukemia: A Case ReportPENG Xiru 1, ZHAO Xiangyu 1, CHENG Juan 1,21.The First Clinical Medical College of Lanzhou University, Lanzhou 730000, China;2. Department of Hematology, First Hospital of Lanzhou University, Lanzhou 730000, China CorrespondingAuthor:CHENGJuan,E-mail:******************Funding: Gansu Natural Science Foundation Program(No.21JR1RA114); Lanzhou Science and Technology Bureau Project(No.2021-1-110)Competing interests: The authors declare that they have no competing interests.关键词:白血病;形态学;免疫表型;add(21)(q22)中图分类号:R733.71 开放科学(资源服务)标识码(OSID):收稿日期:2022-10-17;修回日期:2022-11-12基金项目:甘肃省自然科学基金(21JR1RA114),兰州市科技局项目(2021-1-110)作者单位:1. 730000 兰州,兰州大学第一临床医学院;2. 730000 兰州,兰州大学第一医院血液科通信作者:成娟(1980-),女,博士,主任医师,主要从事白血病多药耐药机制研究与临床诊疗,E-mail: ******************,ORCID: 0000-0002-1196-9066作者简介:彭惜茹(1998-),女,硕士在读,主要从事血液病的诊断与治疗,ORCID: 0009-0005-2894-7962·病例报道·0 引言急性早幼粒细胞白血病(acute promyelocytic leukemia, APL )是以t (15;17)(q24;q21)或PML-RARα融合基因阳性为特征的特殊类型急性髓系白血病(acute myeloid leukemia, AML )。
白血病细胞遗传学分类

白血病细胞遗传学分类
白血病细胞遗传学分类是根据白血病细胞的染色体异常进行分类的一种方法。
这种分类方法对于白血病的诊断、治疗和预后评估具有重要意义。
根据白血病细胞遗传学分类,白血病可以分为以下几类:
1. 急性髓细胞白血病(AML):约 50%的 AML 患者存在染色体异常,其中最常见的是t(8;21)(q22;q22)和 t(15;17)(q22;q12)。
2. 急性淋巴细胞白血病(ALL):约 80%的 ALL 患者存在染色体异常,其中最常见的是 t(9;22)(q34;q11)。
3. 慢性粒细胞白血病(CML):约 95%的 CML 患者存在费城染色体(Ph),即t(9;22)(q34;q11)。
4. 慢性淋巴细胞白血病(CLL):约 50%的 CLL 患者存在染色体异常,其中最常见的是 13q14 缺失和 11q23 缺失。
白血病细胞遗传学分类对于白血病的治疗具有重要指导意义。
例如,对于t(9;22)(q34;q11)阳性的慢性粒细胞白血病患者,伊马替尼等酪氨酸激酶抑制剂可以显著提高治疗效果。
对于 t(8;21)(q22;q22)阳性的急性髓细胞白血病患者,化疗联合全反式维甲酸等治疗可以提高生存率。
总之,白血病细胞遗传学分类是白血病诊断和治疗的重要依据,对于提高白血病的治疗效果和生存率具有重要意义。
急性白血病MICM分型

急性白血病MICM分型:白血病MICM分型,是指形态学(morphology)、免疫学(immunology)、细胞遗传学(cytogenetics)、分子特征(molecular)分型形态学分型(FAB)分型1.急性非淋巴细胞性白血病(ANLL)或急性髓系白血病(AML):M1型:急性原粒细胞性白血病未分化型,骨髓中原粒细胞≥90%,POX染色阳性率>3%。
M2型:急性原粒细胞性白血病部分分化型,以原幼粒细胞为主,早幼粒细胞>3%,中、晚幼及成熟粒细胞>10%为M2a型。
M3型:急怀多颗粒早幼粒细胞性白血病,以颗粒增多的异常早幼粒细胞为主,>30%。
其又分为粗颗粒型(M3a)和细颗粒型(M3b)。
M4型:急性粒-单核细胞性白病,粒系及单核细胞均增生。
M5型:急性单核细胞性白血病,M5a为原单核细胞型,原单核>80%;M5b为部分分化型,以幼单核细胞为主,原单核<80%。
M6型:急性红白血病,原幼红细胞≥50%,非红系细胞中原始细胞>30%。
M7型:急性巨核细胞性白血病,原巨核细胞>30%,并经电镜、血小板过氧化物酶检查、血小板免疫标志物或血小板膜糖蛋白Ⅱb/Ⅲa检查等证实。
M0型:近年确定,为髓系最早阶段的白血病,形态学上极少髓系分化,不能鉴别,必须用免疫标志物确定。
2.急性淋巴细胞性白血病(ALL):L1:以小原淋巴细胞为主,大小较一致。
L2:以大原淋巴细胞为主,大小不一致。
L3:以大原淋巴细胞为主,胞质内含大量空泡。
3.急性白血病的主要化学染色特点:免疫学分型-基本免疫表型1.急性非淋巴细胞白血病(ANLL)FAB分型与免疫标志:2.急性T淋巴细胞白血病(T-ALL)FAB分型与免疫学标志:3.急性非T淋巴细胞白血病(non-T-ALL)FAB分型与免疫学标志:4. 混合细胞性白血病:有极少部分病人白血病细胞为淋巴系和髓系细胞双克隆或同一细胞系免疫标志双表型,即混合细胞性白血病。
此型白血病用形态方法极难诊断,必须结合多参数流式细胞术分析才能确诊。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
急性髓细胞白血病M2亚型细胞形态学及细胞遗传学分析作者:谢守军,王娜,彭兴荣,郝长来【摘要】目的:了解急性粒细胞白血病AML-M2亚型的细胞形态学及细胞遗传学特征。
方法:对23例以FAB分类标准确诊的AML-M2初发患者的细胞形态学及细胞遗传学资料进行回顾性分析;应用骨髓细胞短期培养法制备染色体标本,以R显带技术进行核型分析。
结果:34%M2a、92%M2b患者白血病细胞内可见Auer小体,Auer小体在M2b 患者细胞中检出率明显高于M2a患者;M2患者白血病细胞POX染色呈强阳性反应,在M2a细胞表达多为弥散细颗粒状,而在M2b呈局灶团块状。
23例患者中18例有克隆性染色体异常,异常核型检出率78.3%(18/23)。
16例M2a患者无一致性的染色体异常。
7例M2b患者均有特异性的t(8;21)异常,其中3例伴有y染色体丢失。
结论:M2白血病组内异质性较大,M2a和M2b似乎具有各自独特的细胞形态学及细胞遗传学特性。
【关键词】急性粒细胞白血病; AML-M2;细胞形态学;细胞遗传学急性粒细胞部分分化型白血病(acute myelomonocytic leukemia, AML-M2) 是一组异质性较大的髓细胞白血病,常伴有特殊的染色体异常。
其诊断标准由FAB协作组于1976年提出,在FAB分型的基础上,国内又将其分为M2a和M2b,后者由我国首先提出,1980年被列入国内急性非淋巴细胞白血病分型标准中的一种特殊亚型。
2001年WHO分型中特别提出4种有再现性遗传学异常的急性髓细胞白血病,其中t(8;21)(q22,q22)与M2b密切相关。
细胞形态学和细胞遗传学对AML-M2白血病的诊断、治疗和预后判断具有重要意义。
为了解AML-M2的细胞形态学及细胞遗传学特点,报告57例研究资料。
1 资料与方法1.1 研究对象:57例均为2003年至2006年12月在我院血液室按FAB标准确诊的M2初诊治患者,其中23例进行了染色体核型分析。
M2的诊断标准按文献[1]。
1.2 试剂:瑞氏-姬姆萨(Wright-Gimsa)染液:珠海贝索生物技术有限公司。
α-NAE,PAS和POX试剂盒购自中国医学科学院血研所科技公司。
1.3 形态学检查:骨髓及血涂片经瑞氏-姬姆萨染色后分类计数,常规进行POX、α-NAE(NaF)和PAS组化染色。
1.4 染色体核型分析:取患者初诊治疗前的骨髓,经24~48h 培养后,收集细胞常规制片,应用R显带技术进行核型分析。
分析中期细胞数16~42个,根据细胞遗传学国际命名体制(ISCN,1995)[2]对核型进行描述。
至少2个细胞有同样的染色体增加或结构重排,或者3个细胞有同样的染色体丢失方可确认为一个异常可隆。
1.5 统计学处理:两均数比较应用t检验,统计数据采用SPSS10.0分析软件处理。
2 结果2.1 临床特征:57例患者中男32例,女25例,中位年龄40岁(3~73)。
其中13例为M2b亚型,余均为M2a亚型。
乏力、面色苍白为常见临床表现,肝、脾、淋巴结肿大例数分别为12、7、11例,16例有胸骨压痛,21例有皮肤紫癜、瘀斑。
2.2 血液学特征:本组57例患者白细胞中位数20.08×109/L,(0.66~450.01)×109/L,血红蛋白中位数70g/L,(36~168)g/L,血小板中位数40×1012/L,(6~658)×1012/L。
其中M2a患者44例,白细胞中位数27.84×109/L,(0.66~450.01)×109/L ,血红蛋白中位数75g/L(38~168)g/L,血小板中位数44×1012/L,(6~658)×1012/L。
M2b患者13例,白细胞中位数10.43×109/L(1.91~77.0)×109/L ,血红蛋白中位数60g/L(36~95)g/L,血小板中位数29×1012/L,(11~241)×1012/L。
M2b患者白细胞、血红蛋白和血小板减少较M2a更为明显(p<0.05)。
49例患者外周血涂片可见原粒。
M2患者骨髓增生多为明显活跃或极度活跃,2例(3.5%)M2a 患者为低增生性急性白血病。
约34%(15/44)M2a、92% (12/13)M2b 患者白血病细胞内可见Auer小体。
Auer小体在M2b发生频率较M2b 明显增高,有显著性差异(P<0.01)。
M2b患者骨髓细胞异常中性中幼粒明显增多:胞核与胞质发育极不平衡,胞质丰富,易见空泡,内外浆明显,内浆含多量细小粉红色中性颗粒,亦常见粗大橙红色朝阳红颗粒,染色质细致疏松,核仁大而明显,该特点有助于M2a与M2b 的鉴别诊断。
M2患者白血病细胞POX染色呈强阳性反应,在M2a细胞表达多呈弥散细颗粒状分布,而在M2b多表达于异常中幼粒细胞胞核凹陷处(高尔基富含区)呈局灶团块状,此点亦有助于鉴别诊断。
2.3 细胞遗传学特征:57例M2患者中23例进行了染色体核型分析,第1~16例为M2a亚型白血病,第17~23例为M2b白血病。
23例M2患者异常核型检出率78.3%(18/23),18例染色体异常患者中,单纯数目异常1例,结构异常12例,5例同时伴有数目和结构异常。
分别占异常核型总数的5.5%、66.7%和27.8%。
9例患者为异常核型与正常核型的嵌合体。
t(8;21)易位8例,占M2亚型的34.8%,其中1例为罕见的伴t(8;21)(q22,q22)的复杂易位,核型为46,xy,t(8;21;8)(q22,q22,q24)。
7例M2b患者均有t(8;21)异常,其中3例伴有y染色体丢失。
16例M2a患者无特异性的染色体重排,除2、10、13、16和19号染色体未见受累外,其余染色体均被累及。
详细资料见表1。
3 讨论AML-M2白血病的年发病率较高,约为0.66/10万,占急性粒细胞白血病的35.5%[3]。
M2b多为全血细胞减少,血红蛋白、血小板减少较M2a更为明显,与慢性再生障碍性贫血相似。
本组47.4% (27/57)M2患者骨髓白血病细胞内可见Auer小体,该小体在M2b更为易见,约占92%(12/13)。
异常中性中幼粒细胞在M2b明显增多:胞核与胞质发育极不均衡,内外浆明显,内浆含细小粉红色中性颗粒,胞核凹陷折叠,呈肾形、马蹄形,染色质细致疏松,核仁大而明显。
M2细胞POX呈强阳性,在M2a细胞表达多为弥散细颗粒状分布,而在M2b呈局灶团块状。
从免疫表型看,胞核、胞质的多种蛋白形成紊乱远较核浆发育不平衡复杂得多,有以下特点:①代表不同发育阶段的蛋白共存(CD34和CD33共存);②代表不同细胞系列的蛋白共存(CD33和CD19共存,CD19和CD56共存);③该共存的同细胞系列的蛋白却不同时表达(M2b细胞表达CD19却不表达CD10、 CD20、 CD22)。
AML1/ETO融合基因有助于探明这些紊乱现象的发生机制,最近发现AML1/ETO对在正常髓细胞分化中起重要作用的转录因子PU.1和粒细胞分化因子C/EBPα发挥关键调节作用[4,5]。
表1 23例M2患者细胞遗传学检测结果(略)大约20%~40%的AML-M2患者有t(8;21),本组资料t(8;21)占M2的34.8%,与文献相符[6]。
在分子水平上该易位导致原位于21号染色体长臂2区2带的AML1基因易位到8号染色体长臂2区2带上,与该处的ETO基因融合,形成AML1/ETO融合基因转录本,在M2白血病发病中起重要作用[7]。
本组7例M2b患者均有t(8;21)异常,提示M2b与t(8;21)存在高度特异性,t(8;21)可作为M2b诊断分型的标志。
M2b患者t(8;21)可以单独发生,也可伴有其它染色体异常,-y 是M2b最常见的伴随改变,本组42.9%(3/7)M2b患者伴有性染色体y丢失。
第六届国际白血病染色体会议对103例复发的AML进行分析[8],发生多次复发的病例大多在t(8;21)组,t(8;21)复发时常伴随出现9q-非随机性异常或复杂易位。
这可能与AML1/ETO在长期缓解的M2b患者骨髓细胞中持久表达而不能剔除有关[9]。
本组中4例有t(8;21)的M2b患者经HA(高三尖杉酯碱、阿糖胞苷)方案治疗获完全缓解8~13个月后复发,1例染色体核型为t(8;21;8)复杂变异易位,另1例为t(8;21)易位伴9q-附加异常,支持上述结论。
具有单纯t(8;21)者预后较佳,完全缓解率高,伴有附加复杂异常预后相对较差,尤其-y和9q-的t(8;21)者CR率低。
16例M2a患者进行了染色体核型分析,异常核型检出率68.8%(11/16),无一致性的染色体异常。
可见较有特异性的异常染色体,包括del(5),-7,t(8;21),del(11),del(12)(p12)等。
11q23(MLL)异常主要见于AML-M5患者,该异常为高度异质性,可以是缺失或易位,后者中涉及的伙伴染色体不定,以t(9;11)(p21,q23)为最常见,患者预后差。
有文献报道,del(12)(p12)异常较少见,患者多为M2型,本组2例患者有12p-,并不少见,可能与样本量偏少有关。
3例(例5、13、15)患者有MDS前驱病史,涉及der(3)(3;6), del(5q), -11,del(11), del(12p), der(14)(5;14), del(15),-18异常,有MDS 前驱病史患者的CR率明显低于无MDS前驱病史的AML患者。
值得一提的是本文发现1例嗜酸细胞明显增高的病例,嗜酸细胞占骨髓有核细胞总数的19.5%,其染色体核型为46,xy,inv(1)(p22q44)。
嗜酸细胞增多与该染色体异常是否具有内在关联,需要进一步研究阐明。
M2患者组内异质性较大,特别是M2b和M2a似乎具有各自独特的临床表现和和生物学特性。
概而言之有6点区别:①M2b患者白细胞、血红蛋白、血小板减少较M2a更为明显。
②M2b患者骨髓异常中性中幼粒细胞较M2a明显增多。
③M2b患者POX染色呈局灶团块状分布于异常中幼粒细胞胞核凹陷处,而M2a多为弥散细颗粒状分布。
④Auer小体在M2b更为多见。
⑤M2b患者有特征性的t(8;21)异常和AML1/ETO融合基因,而M2a多表现为非特异性的基因重排,无一致性的染色体异常。
⑥M2b具有单纯t(8;21)异常患者易多次复发,但预后较佳,完全缓解率高,中位生存时间长。
有鉴于此,WHO在对恶性血液系统疾病分类时,把AML伴t(8;21)(q22,q22)/AML1-ETO作为独立亚型应用于临床诊断。
