聚乳酸乙醇酸/RNAⅢ抑制肽缓释微球的血液相容性
【国家自然科学基金】_载药率_基金支持热词逐年推荐_【万方软件创新助手】_20140730
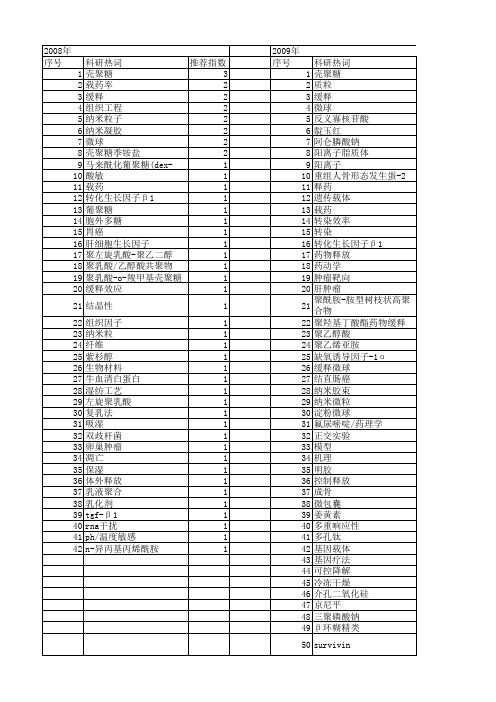
2012年 序号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52
科研热词 药物载体 缓释 聚乙二醇 琥珀酰化壳聚糖 氧化石墨烯 偶联药物 5-氟尿嘧啶 高效液相色谱法 靶向 载药率 表阿霉素 葛根素 药物传输 胶束 肿瘤 肠溶缓释 肝癌 肝星状细胞 聚苹果酸苄基酯 聚合物前药 细胞存活率 纳米载体 纳米壳聚糖 空间稳定脂质体 磁共振分子影像 盐酸降解 白蛋白纳米粒 海藻酸钠 氯化钙 氧氟沙星 毛萼乙素 控制释放 抗肿瘤 微球 微丸 大黄酸 多柔比星 多壁碳纳米管 复乳-固化法 壳聚糖微球 噬菌体 去溶剂-化学交联法 功能化 刺激响应 冬凌草甲素 万古霉素 sio2 plga微球 mir-29b go
科研热词 推荐指数 壳聚糖 3 缓释 2 纳米颗粒 2 牛血清白蛋白 2 黄芩苷明胶微球 1 顺铂 1 靶向化疗 1 静电喷射 1 镀层修饰 1 量子点 1 酸性矿山废水 1 表面活性剂 1 表征 1 药物递送 1 药物缓释 1 药物传递体系 1 肝靶向 1 聚乳酸羟基乙酸 1 聚n-异丙基丙烯酰胺 1 缓释杀菌 1 细胞毒性 1 纳米载体 1 纳米粒子 1 纳米粒 1 紫杉醇 1 硫化物矿山尾矿 1 盐酸四环素 1 生物材料 1 琼脂糖醋酸酯 1 溶胀 1 海藻酸钙微球 1 氧化亚铁硫杆菌 1 杂化水凝胶 1 抗癌活性 1 抑菌 1 快速膜乳化 1 微乳液 1 影响因素 1 平阳霉素 1 姜黄素 1 多面体低聚倍半硅氧烷 1 复合胶束 1 壳聚糖温敏凝胶 1 壳聚糖季铵盐 1 双乳化-凝胶法 1 单分散 1 体外释放 1 乳糖酰基壳聚糖 1 乙醇脂质体 1 γ -聚谷氨酸-柠檬酸-顺铂复合物 1 γ -聚谷氨酸 1 plga微球 1
一次性使用去白细胞塑料血袋标准

一次性使用去白细胞塑料血袋标准YZB医疗器械注册产品标准YZB/国BDST 004,2007一次性使用去白细胞塑料血袋2007-08-28发布 2007-09-18实施北京博德桑特输采血器材科技开发中心发布IYZB/国 BDST 004 — 2007前言一次性使用去白细胞塑料血袋是本中心投入市场使用近四年的产品,该产品主要用于采血后去除全血或成份血(悬浮红细胞)中的白细胞,该类产品在市场上应用一直采用YY 0329 —2002《一次性使用去白细胞滤器》标准和GB 14232.1,2004《人体血液及血液成分分袋式塑料容器第一部份:传统型血袋》双标准进行监控。
血袋和去白细胞滤板连为一体的整体标准目前尚无国家标准和行业标准,此次重新注册特制定本企业标准,以作为该产品注册、生产、交付以及质量监督检查的技术依据。
本标准的结构、要素和表述规则,按照国家标准GB/T1系列《标准化工作导则》的要求进行编写。
本标准由北京博德桑特输采血器材科技开发中心提出并负责起草。
本标准主要起草人:王海荣、牛志瑞、张秉鑫、孙洁本标准于2007年8月首次发布,自发布之日起实施II目次前言1 范围…………………………………………………………………………………………………………12 引用标准……………………………………………………………………………………………………13 分类与命名………………………………………………………………………………………………… 14 材料………………………………………………………………………………………………………… 25 要求………………………………………………………………………………………………………… 26 检验规则…………………………………………………………………………………………………… 67 标志………………………………………………………………………………………………………8 8 包装……………………………………………………………………………………………………… 8 附录A(规范性附录)微粒含量测定方法………………………………………………………………… 8 A.1 方法提要……………………………………………………………………………………………… 8 A.2 试验条件与仪器……………………………………………………………………………………… 8 A.3 操作步骤……………………………………………………………………………………………… 8 A.4 结果计算……………………………………………………………………………………………… 8 附录B(规范性附录)微粒含量测定方法,显微镜计数法(仲裁法)………………………………9 B.1 方法提要……………………………………………………………………………………………… 9 B.2 试验条件与器具……………………………………………………………………………………… 9 B.3 操作步骤……………………………………………………………………………………………… 9 B.4 结果计算……………………………………………………………………………………………… 9 附录C(规范性附录)化学性能检验液制备…………………………………………………………… … 10 C.1 去白细胞塑料血袋滤板部分化学试验液制备方法………………………………………………… 10 C.2 去白细胞塑料血袋血袋部分化学试验液制备方法………………………………………………… 10 C.3 结果判断…………………………………………………………………………………………… 10 C.4 环氧乙烷残留量................................................................................................... 10 附录D(规范性附录)化学性能检验方法........................................................................ 11 D.1 去白细胞塑料血袋滤板部分化学性能试验方法............................................................ 11 D.2 去白细胞塑料血袋的血袋部分化学性能试验方法......................................................... 11 附录E(规范性附录)不含血液保存液的去白细胞血袋无菌试验液制备方法........................... 12 附录F(规范性附录)剩余白细胞数测定方法,普通光学显微镜计数法................................. 13 F.1 方法提要............................................................................................................ 13 F.2 试验仪器、试剂与器具.......................................................................................... 13 F.3 操作步骤............................................................................................................ 13 F.4 结果计算............................................................................................................ 13 附录G(规范性附录)剩余白细胞数测定方法,荧光显微镜计数法(仲裁法)........................... 14 G.1 方法提要...............................................................................................................14 G.2 试验仪器、试剂与材料.............................................................................................14 G.3 操作步骤...............................................................................................................14 G.4 结果计算...............................................................................................................14 附录H(规范性附录)游离血红蛋白测定方法,四甲基联苯胺法................................................ 15 H.1 方法提要 (15)IIIH.2 试验仪器与试剂…………………………………………………………………………………………15 H.3 操作步骤…………………………………………………………………………………………………15 H.4 结果计算…………………………………………………………………………………………………15 附录I(规范性附录)游离血红蛋白测定方法,邻联甲苯胺法(仲裁法)………………………… 17 I.1 方法提要…………………………………………………………………………………………………17 I.2 试验仪器与试剂…………………………………………………………………………………………17 I.3 操作步骤...............................................................................................................17 I.4 结果计算............................................................................................................ 17 附录J(规范性附录)红细胞、血小板回收率测定方法...................................................... 18 J.1 方法提要............................................................................................................18 J.2 试验仪器与器具...................................................................................................18 J.3 血液样品与测定步骤.............................................................................................18 J.4 红细胞、血小板回收率计算....................................................................................18 附录K(规范性附录)血小板低渗休克相对变化率试验...................................................... 20 K.1 方法提要............................................................................................................20 K.2 试验仪器与器具...................................................................................................20 K.3 样品准备............................................................................................................20 K.4 操作步骤............................................................................................................20 K.5 结果计算............................................................................................................20 附录L(规范性附录)溶血试验.......................................................................................22 L.1 方法提要............................................................................................................ 22 L.2 试验仪器与试剂................................................................................................... 22 L.3 操作步骤............................................................................................................ 22 L.4 结果计算............................................................................................................ 22 附录M(资料性附录)去白细胞塑料血袋应用示例.................................................................. 23 参考标准 (24)IVYZB/国 BDST 004 — 2007一次性使用去白细胞塑料血袋1 范围本标准规定了一次性使用去白细胞塑料血袋的分类与命名、材料、要求、检验规则、标志和包装。
负载骨髓干细胞来源外泌体负载骨髓干细胞来源外泌体的3D水凝胶通过调节免疫促进损伤软骨的修复

由于缺乏血管、神经和淋巴组织,关节软骨自我修复的能力受到限制[1]。
一旦受损,就会导致关节肿胀和疼痛,加速骨关节炎的进展。
迄今为止,尽管目前已取得很多进展,但是完全再生透明软骨以及恢复其原有的A 3D hydrogel loaded with exosomes derived from bone marrow stem cells promotes cartilage repair in rats by modulating immunological microenvironmentGUAN Pengfei 1,CUI Ruiwen 2,WANG Qiyou 3,SUN Yongjian 41Department of Spine Surgery,Third Affiliated Hospital of Sun Yat-sen University,Guangzhou 510630,China;2Department of Organ Transplantation,Second Affiliated Hospital of Guangzhou University of Chinese Medicine,Guangzhou 510006,China;3Department of Spine Surgery,4Department of Pediatric Orthopedics,Center for Orthopedic Surgery,Third Affiliated Hospital of Southern Medical University,Guangzhou 510515,China摘要:目的分探究负载骨髓干细胞来源外泌体的GelMA 水凝胶对软骨损伤的修复情况。
方法首先利用超速离心法分离提取出骨髓干细胞上清液中的外泌体,并通过外泌体透射电镜、粒径分析以及Western blot 检测外泌体表面marker 。
交联PMMA@玻尿酸微胶囊的制备及其释放性能

交联PMMA@玻尿酸微胶囊的制备及其释放性能王建平,王凡,王喜睿,王学晨,李伟,张兴祥(天津工业大学天津市先进纤维与储能技术重点实验室,天津300387)摘要:为成功制备玻尿酸微胶囊,在水/油(W/O )反相乳液体系中通过自由基聚合制备了以玻尿酸水溶液为芯材、季戊四醇四丙烯酸酯(PET4A )交联甲基丙烯酸甲酯(MMA )聚合物为壁材的微胶囊。
采用扫描电子显微镜(SEM )、透射电子显微镜(TEM )、傅里叶红外光谱仪(FTIR )、激光散射粒度分布分析仪(LSPSDA )、紫外分光光度计(UV )对微胶囊的形貌、结构、粒径分布、包覆率及释放性能进行了表征。
结果表明:微胶囊具有不规则球形及核壳结构形貌。
当油水比为10颐1、芯壁比为1颐1、玻尿酸用量为1.5mg/mL 、交联剂添加量为0.67%(相对于壁材)时,微胶囊包覆率与载药率分别达到极大值81.40%和1.221%,表面形貌最好,其粒径在1.4~2.0滋m 之间。
微胶囊累计释放量随交联剂用量的升高而下降,同时微胶囊具有pH 响应性,pH =5.5时累计释放量最大。
关键词:W/O 反相乳液;玻尿酸;季戊四醇四丙烯酸酯;甲基丙烯酸甲酯;微胶囊;释放性能;自由基聚合中图分类号:TB34文献标志码:A文章编号:员远苑员原园圆源载(圆园23)园6原园园17原06Preparation and release properties of crosslinked PMMA@hyaluronic acid microcapsulesWANG Jianping ,WANG Fan ,WANG Xirui ,WANG Xuechen ,LI Wei ,ZHANG Xingxiang(Tianjin Key Laboratory of Advanced Fibers and Energy Storage Technology ,Tiangong University ,Tianjin 300387,China )Abstract :In order to prepare hyaluronic acid microcopsule袁microcapsules with hyaluronic acid aqueous solution as thecore and pentaerythritol tetraacrylate 渊PET4A冤cross-linked methyl methacrylate 渊MMA冤polymer as the wall were prepared by a free radical polymerization in a W/O inverse emulsion system.The morphology袁structure袁particle size distribution袁coating ratio and release property of the microcapsules were characterized by scanning electron microscopy 渊SEM冤袁transmission electron microscopy 渊TEM冤袁Fourier transform infrared spectroscopy渊FTIR冤袁laser scattering particle size distribution analyzer 渊LSPSDA冤and ultraviolet spectrophotometer 渊UV冤.The results showed that the microcapsules had irregular spherical shape and core-shell structure.When the oil/water ratio was 10颐1袁the core/wall ratio was 1颐1袁the dosage of hyaluronic acid was 1.5mg/mL袁and the addition of crosslinking agent was 0.67%渊relative to the wall material冤袁the encapsulation efficiency and drug loading rate of the microcapsules reached the maximum of 81.40%and 1.221%袁respectively.The surface morphology was the best袁and the particle size was within 1.4-2.0滋m.The cumulative release of microcapsules decreased withthe increase of the amount of crosslinking agent.At the same time袁the microcapsules were pH-responsive袁andthe cumulative release was the most when pH =5.5.Key words :W/O inverse emulsion曰hyaluronic acid曰pentaerythritol tetraacrylate曰methyl methacrylate曰microcapsule曰re鄄lease property曰free radical polymerization玻尿酸学名“透明质酸”,是一种天然安全、可降解的生物材料,其质地粘稠透明像玻璃一样,因此命名为“hyaluronic acid ”,简称为“HA ”[1]。
LID_PLGA缓释纳米微球的含量测定及其释放度分析方法的研究

西南国防医药 2009 年第 19卷第 2 期
# 167#
# 论著 #
LID 2 PLGA 缓释纳米微球的含量测定及其释放度分析方法的研究
赵先英 , 刘毅敏, 肖 湘, 贺 建
400038) ( 第三军医大学药学院化学教研室 , 重庆 摘要
目的 : 建立简便、 快捷的利多卡因载药微球含量的测 定方法。 方法 : 以 262 nm 为 测定波 长 , 用 紫外分 光光度 法对
- 1 - 1 - 1 - 1 - 1
# 168#
西南国防医药 2009 年第 19 卷第 2 期
图 1 PLGA 吸收曲线 表 1
利多卡因加入量 ( L g) 1250 2500 3750 实验测得量 ( L g) 1233 . 6? 7 .5 2412 . 5? 2 . 66 3592 . 5? 3 . 22
利多卡因载药微球的活性成分进行测定。 结果 : 利多卡因在 50~ 300 L g# m l- 1 范围具有良好 的线性关 系 , r = 0. 9998, 平 均回收率 ( 96. 99 ? 0 . 19)% , RSD= 0. 35 。 24 h 微球累积释药率为 30. 1% 。 结论 : 紫外分光光 度法测定 利多卡因载 药微 球含量的方法具有快捷、 简便 、 重现性好等特点。 关键词 利多卡因 ; 乙交酯丙 交酯共聚物微球 ; 含量 ; 测定 中图分类号 R 971. 2 文献标识码 A 文章编号 1004 2 0188( 2009) 02 2 0167 2 03 D eterm ina tion of lidoca in e conten t in L ID 2 PLGA nanospher es and study of a na lyt ica l m ethod s of its su sta in ed re lea se
【国家自然科学基金】_载药微球_基金支持热词逐年推荐_【万方软件创新助手】_20140801
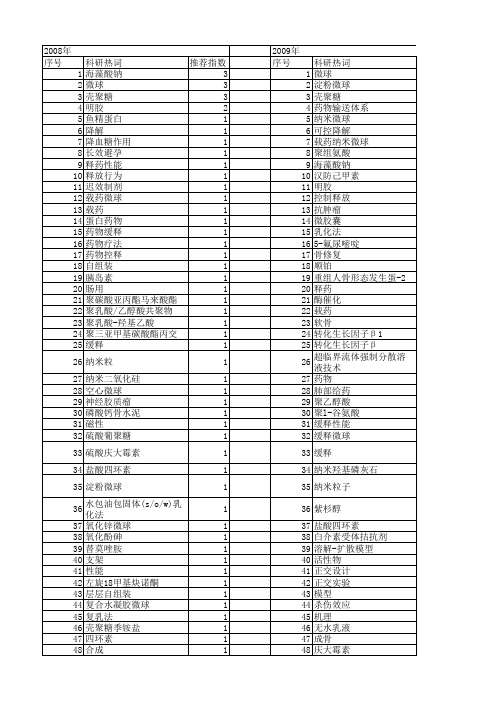
科研热词 推荐指数 海藻酸钠 3 微球 3 壳聚糖 3 明胶 2 鱼精蛋白 1 降解 1 降血糖作用 1 长效避孕 1 释药性能 1 释放行为 1 迟效制剂 1 载药微球 1 载药 1 蛋白药物 1 药物缓释 1 药物疗法 1 药物控释 1 自组装 1 胰岛素 1 肠用 1 聚碳酸亚丙酯马来酸酯 1 聚乳酸/乙醇酸共聚物 1 聚乳酸-羟基乙酸 1 聚三亚甲基碳酸酯丙交酯 1 缓释 1 纳米粒 1 纳米二氧化硅 1 空心微球 1 神经胶质瘤 1 磷酸钙骨水泥 1 磁性 1 硫酸葡聚糖 1 硫酸庆大霉素 1 盐酸四环素 1 淀粉微球 1 水包油包固体(s/o/w)乳化法 1 氧化锌微球 1 氧化酚砷 1 替莫唑胺 1 支架 1 性能 1 左旋18甲基炔诺酮 1 层层自组装 1 复合水凝胶微球 1 复乳法 1 壳聚糖季铵盐 1 四环素 1 合成 1 可降解 1 口服 1 原位制备 1 分子量 1
2011年 序号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52
53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91
2011年 科研热词 推荐指数 微球 9 壳聚糖 7 载药微球 3 淀粉微球 3 体外释药 3 骨髓基质细胞 2 骨形态发生蛋白 2 药物缓释 2 缓释 2 氟苯尼考 2 响应曲面法 2 包封率 2 包埋载药 2 骨缺损修复 1 静电自组装 1 静电吸附 1 降解 1 阿霉素 1 释放曲线 1 酸性问题 1 造影剂 1 载药量 1 载药纳米微球 1 载体材料 1 转铁蛋白靶向 1 角质细胞生长因子 1 蛋白酶k 1 药物释放 1 药物稳定性 1 药物控制释放 1 药剂学 1 荧光标记 1 荧光微球 1 茶碱 1 膜强度 1 胶束 1 聚磷酸钙 1 聚氰基丙烯酸正丁酯 1 聚己内酯 1 聚乳酸-羟基乙酸共聚物 1 缓释微球 1 组织工程化皮肤 1 纳米羟基磷灰石 1 纳米微球 1 纳米微囊 1 纤维蛋白胶 1 盐酸环丙沙星 1 电场 1 甲硝唑 1 生长因子 1 生物相容性 1 淀粉 1
3D打印脑出血尼龙材料导板生物相容性研究罗伟1刘震洋2
3D打印脑出血尼龙材料导板生物相容性研究罗伟1 刘震洋2*发布时间:2023-07-06T05:03:22.838Z 来源:《医师在线》2023年7期作者:罗伟1 刘震洋2*[导读] 3D打印神经脑出血导板在临床其精准性、有效性均在临床得到验证,但其材料生物学性能并未深入研究。
研究以3D打印导板最适宜尼龙材料为对象,分别对体外细胞毒性、皮肤致敏性和皮内刺激性进行检测与验证。
结果显示,试验样品的极性与非极性浸提液均未引起皮肤致敏反应与皮内反应,无潜在细胞毒性。
PA材料是一种适合3D打印脑出血导板材料,满足国标对器械生物安全性的要求。
山西雅韵雕医疗科技有限公司1 山西白求恩医院2摘要:3D打印神经脑出血导板在临床其精准性、有效性均在临床得到验证,但其材料生物学性能并未深入研究。
研究以3D打印导板最适宜尼龙材料为对象,分别对体外细胞毒性、皮肤致敏性和皮内刺激性进行检测与验证。
结果显示,试验样品的极性与非极性浸提液均未引起皮肤致敏反应与皮内反应,无潜在细胞毒性。
PA材料是一种适合3D打印脑出血导板材料,满足国标对器械生物安全性的要求。
关键词:3D打印脑出血导板、尼龙、皮肤致敏性、细胞毒性、皮内反应0.引言目前3D打印在神经外科脑出血得到广泛应用,其精准性、有效性均已得到验证,但其材料性能并未在临床得到验证。
FDA发布了一个《某些接触完整皮肤器械生物相容性选择的更新》指导原则草案中高分子聚合物ABS、环氧树脂系胶结剂,PTFE、ePTFE、PVDF、FEP、HIPS、尼龙、PBT、PC、PEEK、PEI、聚乙烯(包括LDPE和HDPE)、PET、PMMA、POM、PPSU、PP、PU以及硅胶材料可被豁免生物相容性测试。
但由于3D打印导板属于材料的再加工一次性器械,或接触破损皮肤产品,被列为豁免排除在外的医疗器械。
3D打印导板治疗脑出血在临床应用精准度高,操作简单,在临床取得较为广泛科研应用,但实际材料生物相容性并未得到验证。
中医大药剂学
中医大药剂学药剂学单选题1.“轻握成团,轻压即散”是指片剂制备工艺中什么的标准(B )粉末混合制软材干燥压片包衣2.《中国药典》将灰黄霉素原料药的粒度限度规定为5μm以下的粒子不得少于85%,其原因是(D )减小粒径有利于制剂均匀性减小粒径有利于制剂的成型减小粒径有利于制剂稳定减小粒径有利于药物的吸收此项规定不合理3.《中华人民共和国药典》是由(B )国家药典委员会制定的药物手册国家药典委员会编写的药品规格标准的法典国家颁布的药品集国家食品药品监督管理局制定的药品标准国家食品药品监督管理局实施的法典4.1982年,第一个上市的基因工程药物是(B )乙肝疫苗重组人胰岛素白细胞介素-2PO尿激酶5.5%葡萄糖注射液,请选择适宜的灭菌法(B )干燥灭菌(160℃,2h)热压灭菌流通蒸汽灭菌紫外线灭菌过滤除菌6.HLB值在哪个范围的表面活性剂适合作O/W型乳化剂(D )HLB值在1~3HLB值在3~6HLB值在7~9HLB值在8~18HLB 值在13~187.PEG为基质的滴丸宜采用的冷凝剂是(C )水50%乙醇二甲基硅油无水乙醇稀硫酸8.阿司匹林包衣片,使用哪种包衣液吸收最慢(C )1%乙基纤维素3%乙基纤维素5%乙基纤维素3%羟丙甲基纤维素5%羟丙甲基纤维素9.被FDA批准,可用于制备缓释微球注射剂的生物降解骨架材料是(A )PLGA壳聚糖淀粉乙基纤维素HPMC10.崩解剂(C )糊精淀粉羧甲基淀粉钠硬脂酸镁微晶纤维素11.表面活性剂HLB值适合作W/O型乳化剂的是(B )8~183~613~187~91~312.表面活性剂的溶解度急剧增大时的温度是(A )Krafft点昙点HLB值MC杀菌与消毒13.表面活性剂溶解度下降,出现混浊时的温度是(B )Krafft点昙点HLB值MC杀菌与消毒14.不能够避免药物首关效应的给药途径是(E )皮下注射给药舌下给药鼻黏膜给药皮吸收给药口服给药15.不能用作复方阿司匹林片润滑剂的是(A )硬脂酸镁微粉硅胶滑石粉PEG均不是16.不溶性骨架片的材料(E )PVA HPMC蜡类醋酸纤维素聚乙烯17.常用空胶囊的型号有几种?(D )最小型号是几号(A )56781B18.代谢和排泄过程(C )吸收分布消除排泄代谢19.单凝聚法制备微囊时,加入硫酸钠水溶液的目的是(A )凝聚剂稳定剂阻滞剂增塑剂稀释剂20.低温粉碎适于何种性质药物的粉碎(E )易氧化、刺激性较强的药物比重较小不溶于水而又对粉碎粒度有较高要求的药物熔点低或对热敏感的药物软性纤维状药物温度敏感、黏性大韧性强的药物21.滴丸的非水溶性基质(D )PEG-6000 水液状石蜡硬脂酸石油醚22.非离子型表面活性剂(D )泊洛沙姆苯扎氯铵卵磷脂肥皂类乙醇23.分散相以离子或分子状态分散的是(A )溶液剂溶胶剂乳剂混悬剂乳化剂24.高分子物质组成的基质骨架型固体胶体粒子(B )抗体修饰纳米粒微球前体药物25.固体分散体中药物溶出快慢顺序正确的是(A )无定型>微晶态>分子态分子态>微晶态>无定型微晶态>分子态>无定型分子态>无定型>微晶态微晶态>无定型>分子态26.关于表面活性剂的叙述中正确的是(D )能使溶液表面张力降低的物质能使溶液表面张力增加的物质能使溶液表面张力不改变的物质能使溶液表面张力急剧下降的物质能使溶液表面张力急剧上升的物质27.关于蛋白质多肽类药物的理化性质错误的叙述是(E )蛋白质大分子是一种两性电解质蛋白质大分子在水中表现出亲水胶体的性质蛋白质大分子具有旋光性蛋白质大分子具有紫外吸收保证蛋白质大分子生物活性的高级结构主要是由强相互作用,如肽键来维持的28.关于散剂的特点叙述错误的是(B )外用散覆盖面积大,可以同时发挥保护和收敛等作用粉碎程度大,比表面积大,较其他固体制剂稳定制备工艺简单,剂量易控制,便于婴幼儿服用贮存、运输、携带方便既可内服,也可外用,贮存时需防潮29.关于药物制剂配伍变化的错误叙述为(D )配伍变化包括物理、化学与药理学方面的变化药理学方面的配伍变化又称为疗效配伍变化药物配伍后在体内相互作用,产生不利于治疗的变化,属于疗效配伍禁忌物理配伍变化往往导致制剂出现产气现象易产生物理配伍变化的药物制剂若改变制备条件可防止配伍变化的发生30.加入KMnO4(E )180℃3~4h时被破坏能溶于水中不具挥发性易被吸附能被强氧化剂破坏31.浸出方法中的单渗漉法一般包括六个步骤,正确者为(A )药材粉碎、润湿、装筒、排气、浸渍、渗漉药材粉碎、装筒、润湿、排气、浸渍、渗漉药材粉碎、装筒、润湿、浸渍、排气、渗漉药材粉碎、润湿、排气、装筒、浸渍、渗漉药材粉碎、润湿、排气、浸渍、装筒、渗漉32.浸提药材时(D )粉碎度越大越好温度越高越好时间越长越好浓度差越大越好速度越快越好33.经皮吸收制剂中加入氮酮的目的是(B )增加贴剂的柔韧性促进药物经皮吸收增加药物分散均匀使皮肤保持湿润增加药物溶解度34.具有“一步制粒机”之称的是(D )搅拌制粒机转动制粒机高速搅拌制粒机流化床制粒机喷雾制粒机35.颗粒剂的分类不包括(C )可溶性混悬性乳浊性泡腾性肠溶性36.颗粒剂需检查、散剂不需检查的项目(A )溶化性崩解度外观均匀度融变时限粒度37.可使物料瞬间干燥的是(C )冷冻干燥沸腾干燥喷雾干燥减压干燥常压干燥38.可以避免复方药物之间的配伍反应(D )肠溶片糖衣片口含片双层片舌下片39.可用固体分散技术制备,具有疗效迅速、生物利用度高等特点的是(C )微丸微球滴丸软胶囊脂质体40.可用于膜控片的致孔剂(B )单棕榈酸甘油脂PE-G6000甲基纤维素甘油乙基纤维素41.可作为缓释型薄膜衣的材料是(B )HPMC EC邻苯二甲酸羟丙基甲基纤维素丙烯酸树脂Ⅱ号丙烯酸树脂Ⅳ号42.可做经皮吸收制剂中背衬层的为(D )丙烯酸树脂月桂氮酮乙烯-醋酸乙烯共聚物铝箔聚乙烯醇43.可做经皮吸收制剂中控释膜的为(C )丙烯酸树脂月桂氮酮乙烯-醋酸乙烯共聚物铝箔聚乙烯醇44.控释小丸或膜孔中加入的致孔剂是( E )硬脂酸聚氯乙烯聚乙烯醇蔗糖聚乙二醇-40045.利用两种带有相反电荷的高分子作囊材(B )单凝聚法复凝聚法喷雾干燥法界面缩聚法46.明胶(A )成型材料增塑剂增稠剂遮光剂溶剂47.片剂中的助流剂(D )山梨酸硬脂酸甘油酯乙基纤维素滑石粉聚乙二醇-40048.气雾剂常用的抛射剂是(D )氮气二氧化碳丙二醇氟里昂一氧化碳49.气雾剂中抛射药物的动力是(D )阀门杆弹簧推动钮抛射剂雾化室50.亲水亲油平衡值是(C )Krafft点昙点HLB值MC 杀菌与消毒51.乳剂制备中,属于W/O型乳化剂有(B )阿拉伯胶脂肪酸山梨坦聚山梨酯西黄蓍胶泊洛沙姆52.散剂的吸湿性取决于原、辅料的CRH值,如A、B两种水溶性药物粉末的CRH值分别分30%和70%,当两者等比例混合时,混合物的CRH值为( C )100%50% 21%40% 45%53.设计缓释、控释制剂时对药物溶解度要求一般是(B )大于0.01mg/ml 大于0.1mg/ml大于1.0mg/ml大于10mg/ml 大于20mg/ml54.肾上腺素变成棕红色物质的原因是(B )水解氧化聚合脱羧晶型转变55.渗透泵型片剂控释的基本原理是(D )减小溶出减慢扩散片外渗透压大于片内,将片内药物压出片剂膜内渗透压大于片剂膜外,将药物从细孔压出溶蚀作用56.生物转化(E )吸收分布消除排泄代谢57.什么是研究药物制剂工业生产的基本理论、工艺技术、生产设备和质量管理的科学,也是药剂学重要的分支学科( B )生物药剂学工业药剂学物理药剂学药代动力学临床药剂学58.适合作O/W型乳化剂的HLB值是(E )HLB值1~5 HLB值3~8 HLB值7~9 HLB值8~18 HLB值13~1859.水溶性软膏基质(E )山梨酸硬脂酸甘油酯乙基纤维素滑石粉聚乙二醇-40060.为增加片剂的体积和重量,应加入(A )稀释剂崩解剂润湿剂润滑剂黏合剂61.维生素C注射液,请选择适宜的灭菌法(C )干燥灭菌(160℃,2h) 热压灭菌流通蒸汽灭菌紫外线灭菌过滤除菌62.细胞膜变形而将某物质液体颗粒摄入细胞内时称为(E )被动扩散促进扩散主动转运吞噬胞饮63.下列表面活性剂的阳离子部分有表面活性的为(C )肥皂类聚山梨酯类溴苄烷铵十二烷硫酸钠司盘类64.下列表面活性剂有起昙现象的主要是哪一类(E )一价皂类聚氧乙烯聚氧丙烯共聚物类磺酸化物季铵化物聚山梨酯类65.下列不能作气雾剂抛射剂的是(C )三氯一氟甲烷丙烷丙二醇压缩二氧化碳正丁烷66.下列不属于表面活性剂类别的是(E )脱水山梨醇脂肪酸酯类聚氧乙烯去水山梨醇脂肪酸酯类聚氧乙烯脂肪醇醚类聚氧乙烯脂肪酸酯类聚氯乙烯类67.下列不属于浸出药剂特点的是(D )符合中医辨证施治的要求减少服用剂量常以水或不同浓度的乙醇为溶剂制剂稳定性好可达到增强疗效,缓和药性的目的68.下列关于胶囊剂的叙述哪一条不正确(C )吸收好,生物利用度高可提高药物的稳定性可避免肝的首关效应可掩盖药物的不良臭味可使液体药物固体化69.下列关于乳膏剂的正确表述为(A,B,C,D )乳膏剂分为O/W型与W/O型两类表面活性剂常作为乳膏剂的乳化剂O/W型乳膏基质中药物释放与穿透皮肤较其他基质快W/O型乳膏具反向吸收作用,忌用于溃疡创面W/O型乳膏剂需加入保湿剂、防腐剂70.下列关于药典叙述错误的是(C )药典是一个国家记载药品规格和标准的法典药典由国家药典委员会编写药典由政府颁布施行,具有法律约束力药典中收载已经上市销售的全部药物和制剂一个国家的药典在一定程度上反映这个国家药品生产、医疗和科技水平71.下列关于药物微囊化的特点的叙述,错误的是(E )缓释或控释药物防止药物在胃内失活或减少对胃的刺激性使药物浓集于靶区掩盖药物的不良气味或味道提高药物的释放速率72.下列关于脂质体相变温度的叙述错误的是(A )在相变温度以上,升高温度脂质体膜的流动性变小在一定条件下,由不同磷脂组成的脂质体有可能存在不同的相与磷脂的种类有关在相变温度以上,升高温度脂质双分子层中疏水链可以从有序排列变为无序排列在相变温度以上,升高温度脂质体膜的厚度减小73.下列过程中一般不存在竞争抑制的是(A )肾小球过滤胆汁排泄肾小管分泌肾小管重吸收药物从血液透析74.下列哪一种措施不能增加浓度梯度(C )不断搅拌更换新鲜溶剂高压提取动态提取采用渗漉提取法75.下列哪种方法不能增加药物溶解度(E )加入助溶剂加入非离子型表面活性剂制成盐类加入潜溶剂加入助悬剂76.下列哪种现象不属于化学配伍变化(B )溴化铵与利尿药物配伍产生氨气麝香草酚与薄荷脑形成低共熔混合物水杨酸钠在酸性药液中析出生物碱盐溶液与鞣酸产生沉淀维生素B12与维生素C制成溶液,维生素B12效价下降77.下列有关气雾剂的叙述,不正确的是(D )气雾剂稳定,吸收和奏效迅速气雾剂剂量准确、使用方便喷雾给药可减少创面涂药的机械刺激药物存在胃肠道内破坏和首关效应78.下列有关气雾剂的正确表述是(B )气雾剂是由药物与抛射剂、附加剂、阀门系统三部分组成的按分散系统分类,气雾剂可分为溶液型、混悬型和乳浊液型只能吸入给药现在压缩气体已经完全能作为氟里昂的替代品采用冷灌法填充抛射剂,具有速度快的优点,常用于制备含水溶液的气雾剂79.下列有关气雾剂特点的叙述,不正确的是(B )杜绝了与空气、水分和光线接触,稳定性强剂量不准确给药刺激小不易被微生物污染生产成本较高80.现代生物技术是(E )以细胞工程为核心的基因工程以发酵工程和酶工程为核心的基因工程以细胞工程为核心发酵工程和酶工程以基因工程为核心的细胞工程以基因工程为核心以及具备基因工程和细胞工程内涵的发酵工程和酶工程81.向以硬脂酸钠为乳化剂制备的O/W型乳剂中,加入大量氯化钙后,乳剂可出现(C )分层絮凝转相合并破裂82.硝酸甘油应制成(E )肠溶片糖衣片口含片双层片舌下片83.性质稳定,受湿遇热不起变化的药物(D )结晶压片法干法制粒压片粉末直接压片湿法制粒压片空白颗粒法84.药品的稳定性受到多种因素的影响,下列哪一项为影响药品稳定性的非处方因素(D )药物的化学结构剂型辅料湿度药物的结晶形态85.药物从用药部位进入体循环的过程(A )吸收分布消除排泄代谢86.药物的可压性不好,在湿热条件下不稳定者(B )结晶压片法干法制粒压片粉末直接压片湿法制粒压片空白颗粒法87.药物的脂溶性是影响下列哪一步骤的最重要因素(C )肾小球过滤肾小管分泌肾小管重吸收尿量尿液酸碱性88.药物在体内发生代谢的主要部位是(D )胃肠道肺脏血脑屏障肝脏肾脏89.以下不能用于制备脂质体的方法是(A )复凝聚法逆向蒸发法冷冻干燥法注入法薄膜分散法90.以下不是药剂学配伍变化实验与处理方法的是(C )可见的配伍变化试验和变化点的pH测定稳定性实验临床用药人群的调整改变调配次序或调整溶剂改变剂型或改变药物91.以下不属于减压浓缩装置的是(D )减压蒸馏器真空浓缩罐刮板式薄膜蒸发器夹层锅旋转蒸发仪92.以下不属于纳米粒的制备方法的是(E )乳化聚合法天然高分子凝聚法液中干燥法自动乳化法干膜超声法93.以下不属于生物技术药物特点的是(C )相对分子质量大,不易吸收结构复杂易被消化道内酶及胃酸等降解从血中消除慢在酸碱环境不适宜的情况下容易失活94.以下方法中,不是微囊的制备方法的是(E )凝聚法液中干燥法界面缩聚法改变温度法薄膜分散法95.以下关于固体分散体的叙述,错误的是(B )固体分散体存在老化的缺点共沉淀物中药物以稳定型存在固态溶液中药物以分子状态分散固体分散体可促进药物的溶出简单低共熔混合物中药物以微晶存在96.以下关于环糊精的叙述,错误的是(A )环糊精是由环糊精葡萄糖转位酶作用与淀粉后形成的产物是水溶性、还原性白色结晶粉末结构为中空圆筒形其中以β-环糊精溶解度最小环糊精的中空圆筒处为疏水性97.以下关于判断微粒是否为脂质体的说法正确的是(C )具有微型囊泡球状小体具有类脂质双分子层结构的微型囊泡具有磷脂双分子结构的微型囊泡由表面活性剂构成的胶团98.以下哪一湿度较适宜胶囊贮存(A )20% 40% 60% 80%100%99.以下哪种材料制备固体分散体具有缓释作用(A )PEG PVP EC 胆酸泊洛沙姆-188100.以延缓溶出速率为原理的缓、控释制剂(A )溶蚀性骨架片膜控释小丸渗透泵片微球纳米球101.引起乳剂破裂的是(E )ζ电位降低油水两相密度差不同造成光、热、空气及微生物等的作用乳化剂类型改变乳化剂失去作用102.引起乳剂转相的是(D )ζ电位降低油水两相密度差不同造成光、热、空气及微生物等的作用乳化剂类型改变乳化剂失去作用103.用β-环糊精包裹挥发油制备的固体粉末为(B )固体分散体包合物脂质体微球微囊104.用包括粉体本身孔隙及粒子间孔隙在内的体积计算的密度为(A )堆密度真密度粒密度振实密度振动密度105.油脂类软膏基质,请选择适宜的灭菌法(A )干燥灭菌(160℃,2h)热压灭菌流通蒸汽灭菌紫外线灭菌过滤除菌106.油脂性基质的灭菌方法可选用(B )热压灭菌干热灭菌气体灭菌紫外线灭菌湿热灭菌107.在注射剂中加入焦亚硫酸钠作为(D )金属离子络合剂抑菌剂pH调节剂抗氧剂渗透压调节剂108.在注射剂中具有局部止痛和抑菌双重作用的附加剂是(D )盐酸普鲁卡因盐酸利多卡因苯酚苯甲醇硫柳汞109.这种分类方法,便于应用物理化学的原理来阐明各类制剂特征(B )按给药途径分类按分散系统分类按制法分类按形态分类按药物种类分类110.正确浸出过程是(C )浸润、溶解浸润、渗透、解吸、溶解浸润、渗透、解吸、溶解、扩散浸润、溶解、过滤、浓缩、干燥浸润、溶解、解吸、扩散111.直接影响气雾剂给药剂量准确性的是(D )附加剂的种类抛射剂的种类抛射剂的用量阀门系统的精密程度药液的黏度112.制备固体分散体时,若药物溶解于熔融的载体中呈分子状态分散着则为(B )低共熔混合物固态溶液玻璃溶液共沉淀物无定形物113.制备过程需调节溶液的pH为3.5~5.0及加入适量氯化钠(C )0.5%盐酸普鲁卡因注射液10%维生素C注射液5%葡萄糖注射液静脉注射用脂肪乳丹参注射液114.制备过程需用醇去杂质,调节溶液的pH及加抗氧剂(E )0.5%盐酸普鲁卡因注射液10%维生素C注射液5%葡萄糖注射液静脉注射用脂肪乳丹参注射液115.制备过程需用碳酸氢钠调节溶液的pH及加入抗氧剂,并通二氧化碳(B )0.5%盐酸普鲁卡因注射液10%维生素C注射液5%葡萄糖注射液静脉注射用脂肪乳丹参注射液116.制备脂质体的方法(A )逆向蒸发法熔融法单凝聚法饱和水溶液法117.主要用于杀菌和防腐的阳离子型表面活性剂是(D )聚山梨酯类司盘类卵磷脂季铵化物肥皂类118.注射剂溶剂(E )山梨酸硬脂酸甘油酯乙基纤维素滑石粉聚乙二醇-400119.最适合作为增溶剂的HLB值是(E )HLB值1~5 HLB值3~8 HLB值7~9 HLB值8~18 HLB值13~18120.作为助悬剂的是(A )沉降硫黄30g硫酸锌30g羧甲基纤维素钠5g甘油100ml纯化水加至1000ml名词解释121.D值:是在一定的处理环境中和在一定的热力致死温度条件下某细菌数群中每杀死90%原有残存活菌数时所需要的时间。
药剂学第新剂型历年试题
药剂学第新剂型历年试题南昌大学药学院历年药剂学试题(新剂型部分)04级A卷一、单项选择题1、下列属于控制扩散为原理的缓控释制剂的方法为A、控制粒子大小B、采用不溶性高分子材料为阻滞剂制备的骨架片D、制成溶解度小的盐C、用蜡质类为基质制成溶蚀性骨架片2、在pH-速度曲线图最低点所对应的横坐标,即为A、药物最稳定的pHB、药物最不稳定的pHC、反应速度的最高点D、反应速度的最低点。
3、15g水溶性物质A与20g水溶性物质B(CRH值分别为78%和60%),两者混合物的CRH值为A、26.2%B、46.8%C、66%D、52.5%4、下列哪一辅料不能用作初级渗透泵控释片的半透膜材料?A、醋酸纤维素B、乙基纤维素C、羟丙甲纤维素D、丙烯酸树脂(EudragitRL100,EudragitRS100)5、下列制剂技术(或剂型)静脉注射没有靶向性的是A、纳米粒B、乳剂C、小分子溶液型注射剂D、脂质体6、下列叙述不属于结肠定位释药系统优点的是A、避免首过效应B、有利于多肽、蛋白质类大分子药物的吸收C、固体制剂在结肠中的转运时间很长,可达20~30h,因此OCDDS的研究对缓、控释制剂,特别是日服一次制剂的开发具有指导意义D、治疗小肠局部病变7、以明胶、阿拉伯胶为囊材,采用复凝聚法制备微囊时,其中一个步骤是将pH调到3.7,其目的是A、使阿拉伯胶荷正电B、使明胶荷正电C、使阿拉伯胶荷负电D、使明胶荷负电二、填空题1、滴丸本质上是一种采用熔融法制备的2、对口服缓控释制剂进行体外评价时,一般需要进行试验,测定不同取样时间点的药物释放百分数。
3、药物的靶向从到达的部位讲可以分为三级,第一级指到达特定的4、将一些难溶性药物研制为环糊精或环糊精衍生物的包合物的主要目的是5、纳米乳属于稳定系统,制备纳米乳时,只要处方合适,纳米乳可以自发形成或通过轻微搅拌形成,不需要高速搅拌,基于此性质,发展出了自乳化给药系统。
6、微粒分散体系由于高度分散具有一些特殊的性能,其中之一是:微粒分散体系是多相体系,分散相和分散介质之间存在着相界面,因而会出现大量的现象。
二甲双胍通过miR-194-5pRBM6通路抑制肝细
展
,但是 miR194
5p 是否与二甲双胍的 抗 癌 作
[
5-6]
用有关 系,尚 未 可 知。 本 研 究 拟 以 HepG2 细 胞 为
研究对象,观察二 甲 双 胍、miR194
5p 对 2 细
胞增殖、凋亡的调控,揭 示 二 甲 双 胍 与 miR194
i
nomac
e
l
l
st
hr
oughmiR194
5p/RBM6pa
t
hwa
y
1
WANG Yi
ng2 ,WANGJun
zhou1 ,
gang ,HUANG Ti
TANG Rong
x
i
ng1 ,LISu1 ,XIONG Yong1*
(
1.
Depar
tmentof Hepa
t
obi
l
i
arySurge
ry,Panzh
i
huaCent
ra
lHo
spi
t
a
l,Si
chuanPr
ov
i
nc
e,Panzh
i
hua
617000,Ch
i
na;2.
Depar
tmentof Endo
c
r
i
no
l
ogy,Panzh
i
huaCent
ra
lHo
spi
t
a
l,
Si
chuanPr
ov
i
nc
e,Panzh
i
hua 617000,Ch
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
基础医学 中国组织工程研究与临床康复第 2眷第6期2008—02—05出版 Journal ofClinical Rehabilitative T ̄ssue Engineering Research February 2008 Vo1.12.No.6
聚乳酸乙醇 ̄/RNAIII}[P¥=J肽缓释微球的血液相容性★☆ 张小斌,郝立波,王继芳,姚 琦,梁茂华 Blood compatibility of polyaiticglycolic acid/RNA 171 inhibiting peptide microspheres Zhang Xiao-bin,Hao Li-bo,Wang Ji・fang,Yao Qi。Liang Mao-hua
Deparm ̄nt of Orthopaedics,General Hospital of Chinese PLA. Be@rig 100853.China
Zhang Xiao-bin☆, Smdymg for doctorate,Attending physician,Department 0f OtShopaedics. General Hospital of Chinese PL Beijing 1O0853.China xitubin2@163 com
Correspondenee to: Hao Li—bo, M.D., Associate chief physician,Department of Orthopaedics, General Hospital 0f Chinese PLA.Bering 1O0853.Cllina libo hao@hotmaiLc( ̄a
Supported by:the Nadonal Natlwal Science Foundation of China No 30640088*
Received:2007—10-24 Accepted:2007--11--23
解放军总医院骨 科, 北京市
l00853
张小斌☆,男, l972年生,陕西 省汉中市人,汉 族,解放军总医院 骨科在读博士,主 治医师,主要从事 关节外科疾病的 研究。 Xitubin2@163.tom
通讯作者:郝立 波,博士,副主任 医师,解放军总医 院骨科,北京市 l00853 libohao@hotmail_
国家自然科学基 金资助项目 (3O640088)
中图分类号:R31808 文献标识码:A 文章编号:1673—8225 (2008)06-01022—05
收稿日期:2007.10.24 修回日期:2007—11-23 f07-50-l0-58OI/Y Y)
1022
Abstract AIM:Studies reveal that RNAIII inhibiting peptide(PdP1 is an effective suppressant for staphylococci and the mechanism obviously differs from traditional antibiotic drug,indicating its potential application.This study evaluated blood compatibility of polyaiticglycolic acid(PLGA1瓜IP microspheres. METH0DS:The experiment was performed in the Pharmacological Research Institute and Animal Experimental Center at the General Hospital of Chinese PLA from October 2005 to October 2007.Thirty healthy adult New Zealand white rabbits were grouped randomly,witl1 6 animals ln each group.Drugs and reagents:PLGA,dimethyl sulphoxide,MTT,DMEM,dinitoflruorobenzene.(1) Preparation of PLGA/RIP microspheres:Fmoc method was used to synthesize RIP from C end to N end,then the synthesized crude peptide sample was purified by the reverse phase high performance liquid chromatography,and composition was collected by means of ultraviolet absorption Deal【.111e purified PIR was obtained from freezing and drying.Afterwards liquid.phase multiple emulsion method was used to synthesize PLGA,RIP microspheres of 50—7O nltn diameter.( Preparation of eluent:l ,L PLGA,RIP microsphere was eluted sterily with saline at 37℃for 72 hours to harvest stock solution.then equal volume of stroke.physiological saline solution was added to obtain 0.5 dilution.⑨Haemolysis test:With distilled water and stroke.physiological saline solution as positive and negative controls respectively,the rate of haemolysis of 100%and 50%eluent of PLGA爪IP were studied.( Hemagglutinatin test and PLGA/RIP effect on prothrombin time(PT1 and activated partial thromboplastin time(APTT):With stroke.physiological saline solution as negative contro1.the effects of l00%and 50%eluent of PLG删P on PT and APr丌were observed.⑨The effects of 100%and 50%eluent of PLGA爪IP on the leucocyte,erythrocyte,thrombocyte and platelet aggregation were detected. RESULTS:Totally 30 rabbits were involved in the result analysis.(1)Haemolysis test showed that.the haemolysis rates of l00%and 50%eluent of PLGA,RIP were 3.24%and 2.67%.They were in coincidence with the criteria of biomaterials(<5%1. Hemagglutinatin test showed that the 1 00%and 50%eluent of PLGA/RIP had no significant effect on hemagglutinatin. ( PLGA,RIP showed no significant effect on PT and APTT.( PLGA/RIP also showed no significant effect on leucocyte. erythrocyte and thrombocyte.⑨PLGA/RIP showed no significant effect on platelet aggregation. C0NCLUS10N:PLGA爪IP microspheres have good blood compatibUity.
Zhang XB,Hao LB,Wang JF,Yao Q,Liang MH.Blood compatibility of polyaiticglycolic acid/RNA III inhibiting peptide microspheres.Zhongguo Zuzhi Gongcheng Yanjiu yu Linchuang Kangfu 2008;l2(6):1022—1026(China) [WWW.zglckf.condzglckf/ejourual/upfilesd08—6,6k一1022(ps).pdf]
摘要 目的:研究表明RNA III抑制肽(RNA III inhibiting peptide,RIP)是葡萄球菌一种有效的全面抑制剂,作用机制与传统抗 菌素明显不同,有着良好的应用前景。通过实验评价聚乳酸乙醇酸(polyaitlcglycolic acid,PLGA)/RIP缓释微球的血液相 容性。 方法:实验于2005—10/2007—10在解放军总医院临床药理研究所及医学动物实验中心完成。选择成年健康新西兰大白兔3O只, 按随机数字表法分组,每组6只。药品及试剂:PLGA,二甲基亚砜、MTT,DMEM,二硝基氟苯。实验方法:( ̄)PLGA/RIP 微球制备:采用Fmoc法由c端至N端先合成粗品肽:采用反相液相色谱法对RIP粗品进行纯化分析,按紫外吸收峰收集组分, 冷冻干燥,得到RIP纯品。再采用液相复乳法制备直径50 ̄70 nlln的PLGA/RIP微球。②洗提液制备:PLGA/RIP微球粉末按 l g,L在37℃无菌条件下用生理盐水洗提72 h,制得洗提液原液;加入同体积的无菌生理盐水制得0.5 g,L的稀释液。③溶 血实验:以蒸馏水和生理盐水分别为阳性、阴性对照,观察PLGA/RIP洗提液原液和0.5 g,L洗提液的溶血率。④凝血实验及 PLGA/RIP对凝血酶原时间和活化部分凝血酶时间的影响实验:以生理盐水为阴性对照,观察PLGA/RIP洗提液原液和0.5 g,L 洗提液对兔凝血时间的影响和凝血酶原时间和活化部分凝血酶时间的影响。⑤PLGA/RIP对兔白细胞、红细胞和血小板及血 小板聚集的影响实验:观察PLGA/RIP洗提液原液和0.5 g,L洗提液对兔白细胞、红细胞和血小板及血小板聚集的影响。 结果:纳入动物3O只。均进入结果分析。①溶血实验结果显示PLGA/RIP洗提液原液和0.5 g/L洗提液的溶血率 分别为3.24%和2.67%,两者的溶血率均<5%,符合医用生物材料的溶血实验要求。②凝血实验结果表明 PLGA/RIP洗提液原液和O.5 g/L洗提液对兔凝血时间无明显影响。③PLGA/RIP对各时间点兔凝血酶原时间和活 化部分凝血酶时间均无明显作用。④PLGA/RIP对兔白细胞、红细胞和血小板无明显影响。⑤PLGA/RIP对兔血小 板聚集无明显影响。 结论:PLGA/RIP缓释微球具有良好的血液相容性。 关键词:PLGA/RIP微球;血液相容性;生物材料
