第10章 醇和醚
第10章 醇和醚
CH3COCH3
H2O,H+
CH3 CH3 CH3 CH3 CH3CHCH2CCH3 H2SO4 CH3CHCH=CCH3 OH
(5)丙烯合成甘油和三硝酸甘油酯
CH3CH=CH2
Cl2 HOCl ClCH2CH=CH2 0 500 C
CH2CHCH2 Cl OH Cl
Ca(OH)2
Cl
CH2CHCH2 O
(CH3)3CCHCH3 OH
H+
(CH3)3CCHCH3
+
H+ (CH ) CCH=CH 3 3 2
CH3
CH3 CHCH3 C
+
CH3 CH3 CHCH3 CH3 C +
+
H+
CH3 (CH3)2CHC=CH2 CH3 (2) 反应历程: CH2OH H
+
(CH3)2C=(CH3)2
CH2OH2+ H2O
+
3
3
3 H H C C C = H C 2 H C 3 H C
HOCH2CH=CHCH3 HBr
BrCH2CH=CHCH3
+
CH2=CHCHCH3 OH
HOCH2CH=CHCH3 H2O
+
H+
H2O CH2CH=CHCH3 CH2=CHCHCH3 BrCH2=CHCHCH3 OH
+
+
CH2CH=CHCH3 Br-
BrCH2CH=CHCH3
9. 应历程解释下列反应事实。 解: (1) 反应历程:
CH3 CH3 C CH2OH CH3 CH3 H
+
CH3 CH3 C CH3
第十章醇和醚

Br -
CH3 CH3 C CH2CH3
Br
三卤化磷或亚硫酰氯(SOCl2)也可与醇反应 制卤代烃,且不发生重排,因此是实验室制卤代
烃的一种重要方法。
CH3CH2CH2OH
P+I2(PI3) 85~90℃
CH3CH2CH2I
CH3CH2CH2CH2OH + SOCl2
CH3CH2CH2CH2Cl + SO2 + HCl
③写出全称 “某醇”。
3CH3 H2C3CH3 3CH3
CH3
CH3CHCH2CH2CCH3
OH
CH3
5,C5H-二3C甲HC基H-22C-H己2醇CHCH2CH3
OH
OH
CHC3CHH3CCHHC2HC2HC2HC2HCHCCHH2C2CHH33
OHOH
OHOH
2,5-庚二醇
CCHH2O2OHH
3. 酯的形成
CH3 OH +H OSO3H
CH3OSO3H +H2O
硫酸氢甲酯
CH2 OH
H2SO4(浓) CH2 ONO2
CH OH + 3HONO2 10~20℃ CH ONO2 + 3H2O
CH2 OH
CH2 ONO2
三硝酸甘油酯(硝化甘油)
硝化甘油是一种烈性炸药;在医疗上可扩张血管,做心 血管的急救药。
不同的醇与同一种氢卤酸反应的活性: 烯丙醇、苄醇>叔醇>仲醇>伯醇>甲醇
卢卡斯(Lucas)试剂:无水氯化锌的浓盐酸溶液
CH3 CH3 C OH
CH3
+ HCl
ZnCl2 20℃
CH3
CH3 C Cl + H2O
邢其毅《基础有机化学》(上册)笔记和课后习题(含考研真题)详解(醇和醚)

圣才电子书 十万种考研考证电子书、题库视频学习平台
剂化作用大,因此 RCH2OH 中的质子易于解离,酸性大。因此根据液相中各类醇酸性的大 小顺序,认为烷基是给电子的。
醇具有一定的碱性,醇中氧不质子结合就得到醇的共轭酸。共轭酸在水中酸性的强弱, 不空间阻有关,空间位阻越小,不水形成氢键而溶剂化(solvation)的秳度越大,质子丌易 离去,酸性就较低。若空间位阻大,溶剂化作用小,质子易离去,酸性强。
3.醇羟基上的氢的反应 由于醇羟基中的氢具有一定的活性,因此醇可以和金属钠反应,氢氧键断裂,形成醇钠 并放出氢气。
在液相中,由于水的酸性比醇强,所以醇不金属钠的反应没有水和金属钠的反应强烈。 若将醇钠放入水中,醇钠会全部水解,生成醇和氢氧化钠。
4.醇不含氧无机酸反应 醇不含氧无机酸反应失去一分子水,生成无机酸酯。 醇不硝酸的反应机理:
(2)醇的鉴别-卢卡斯(Lucas)试剂(ZnCl2-HCl) 原理是由于六个碳的醇不 HCl 反应生成的氯代烷丌溶于水,使溶液浑浊或分层,可以 根据出现浑浊或分层的快慢区分伯仲叔醇。
注意:A.各类醇不 Lucas 试剂的反应速率为:烯丙型醇,苯甲型醇,三级醇>二级醇 >一级醇;B.氢卤酸不大多数一级醇按 SN2 机理迚行反应;不大多数二级、三级醇和空阻 特别大的一级醇按 SNl 机理迚行反应。三级醇不氢卤酸的反应一般丌会収生重排,但三级醇 易収生消除反应,所以叏代反应需在低温时迚行。
5 / 69
圣才电子书
7.不亚硫酰氯反应
十万种考研考证电子书、题库视频学习平台
若用亚硫酰氯和醇反应,可直接制得构型保持的氯代烷,同时生成二氧化硫和氯化氢两
种气体。该反应丌仅速率快,反应条件温和,产率高,而且丌生成其他副产物,是一个很好
有机化学第10章

• 重排: 有一些醇(除大多数伯醇外)与氢卤酸反应, 时常有重排产物生成,如: 例1:
CH3 CH3 H HCl CH3-C-CH2-CH3 CH3-C— C-CH3 Cl OH H
重排反应历程:
CH3 CH3 CH3
Why?
CH3 CH3C-CH2CH3
+
+ CH3C-CHCH3 HCl CH3C-CHCH3 -H 2O CH C-CHCH 重排 3 3 H OH H +OH2 H Cl-
构造式
习惯命名法
衍生物命名法
系统
(4) 不饱和醇的系统命名:应选择连有羟基同时含有重 键(双键和三键)碳原子在内的碳链作为主链,编号时尽 可能使羟基的位号最小:
4-(正)丙基-5-己烯-1-醇
(5) 芳醇的命名,可把芳基作为取代基:
2
1-苯乙醇 (-苯乙醇)
1
CH2 -CH3 OH
3-苯基-2-丙烯-1-醇 (肉桂醇)
H+, 25℃
(CH3)3C-OH
该反应历程:
(CH3)2C=CH2 + H+ (CH3)3 C+
H2 O
(CH3)3C-OH2 (CH3)3C-OH + H+
+
• 不对称烯烃, 在酸催化下水合,往往中间体碳正离子 可发生重排:
H+的加成符合马氏规律
(CH3)3CCH=CH2
H+
重排
①H2O ②-H+
RCH2-OH + HBr H SO RCH2Br + H2O 2 4 RCH2-OH + HCl ZnCl RCH2Cl + H2O 2
徐寿昌《有机化学》 课件 第十章 醇、醚

R CH CH R' OH OH
+
Pb(OAc)4
RCHO
+
R'CHO
+ Pb(OAc)2 +
HOAc
这个反应常定量完成,因此可用于乙二醇的定量测定,并可根 据氧化产物推断原醇的结构。 7、邻二醇的重排反应—频哪醇重排
CH3 CH 3 H3C C C CH3
H2SO4 (HCI)
△
CH3 H3C C O C CH3 CH3
M= b.p=
74 117.2
OH OH
频哪醇
频哪酮
CH3 CH3 H3C C C CH3
H2SO4
CH3 CH3 H3C C C CH3
+
OH OH CH3 CH 3 H3C C OH C
OH OH2
CH3 H3C C C CH3
-H
+
CH3 H3C C O C CH3 CH3
+CH3O Nhomakorabea CH3
第二节 醚(ethers)
325℃
5、与酸反应——酯化
醇可与有机酸、无机酸作用生成酯。
O H3C C OH + H
O
O CH2
H+ CH3
△
CH3 C O CH2 CH3
发生酯化反应时,羧酸的C – O键断裂,醇的O – H键断 裂。 CH3 – OH + H2SO4 (CH3)2SO4(硫酸二甲酯)
硫酸二甲酯剧毒,对皮肤的阀限值1ppm,空气中最 高限量5mg/m3。
CH3CH2Cl + H2O
通常用无水氯化锌与浓盐酸按1:1的比例配成溶液与醇反 应, 代替不易操作的氯化氢气体,这样的溶液称为卢卡斯 (Lucas)试剂。结构不同的醇与卢卡斯试剂反应的活性顺序 为:
有机化学第10章 醇、酚、醚

①醇可依分子中所含羟基数目分为一元醇、二元醇及三元醇等,二
元及二元以上的醇称为多元醇。例如:
CH3CH2OH CH2CH2 OH OH
乙醇(一元醇) 乙二醇(二元醇)
CH2CH CH2 OH OH OH
丙三醇(三元醇)
3
②醇也可依分子中烃基的不同而分为脂肪醇(包括饱和醇及不饱和 醇)、脂环醇和芳香醇。 例如:
C(CH3)2或 C(CH3)3
23
在醇的核磁共振谱图中,羟基质子(O—H)由于受
分子间氢键的影响,其化学位移(δ)出现在1~5.5范围 内,在核磁共振谱中产生一个单峰。由于氧的电负性 较大,羟基所连碳原子上的质子的化学位移一般在 3.4~4.0。
24
10.1.4 醇的化学性质
羟基是醇的官能团,作为反应中心羟基决定了醇的化学性质。
2,3-二甲基-3-戊醇
12
不饱和醇的命名,除应选择同时连有羟基和不饱和键的最长碳 链作为主链外,其它原则与饱和醇相同。
CH3CH2CH2CHCH2CH2CH2OH CH CH2
5 6
4
3
2
1
4-丙基-5-己烯-1-醇
CH CHCH3 CH3CH2CHCHCH2CHCH3 CH3 OH
4-甲基-5-乙基-6-辛烯-2-醇
32
醇和氢卤酸反应的速率与醇的结构的关系: 醇的活性顺序是:烯丙型醇、苄基型醇>叔醇>仲醇>伯醇。 例如:
33
利用不同醇与盐酸反应速率的不同,可以区分伯、仲、叔醇。无
水氯化锌与浓盐酸配制的溶液,叫做Lucas试剂。因为水溶性较好的
醇与Lucas试剂反应后,生成与水不互溶的氯代烃,形成乳状的混浊 溶液或分层,所以可利用Lucas试剂鉴别低碳(C6以下)一元伯、仲、叔 醇(C6以上的一元醇水溶性较差,难于用Lucas试剂鉴别)。例如:
第十章 醇、酚、醚

伯醇氧化生成醛
仲醇氧化生成酮
叔醇只有在强烈氧化条件下才被氧化-----发生键的断裂
选择性氧化-异丙醇铝-----选择性氧化羟基而保留双键
+|
Cl
伯醇主要按SN2反应机制进行,
快+
RCH2—OH +HX————→RCH2—OH2+ X一
+
RCH2—OH2+ X一———→X…CH2…OH2———→RCH2X + H2O
|
R
不同的醇在与相同的氢卤酸反应时的活性为:烯丙型醇、叔醇>仲醇>伯醇。
无水氯化锌与氯化氢的混合试剂称为卢卡斯(Lucas)试剂。其中无水氯化锌是强的路易斯酸。
3.与无机酸的反应
A.与HX反应得到卤代烃和水ROH+HX——→RX+H2O
大多数的仲醇和叔醇与氢卤酸的反应是按SN1反应机制进行的。仲醇反应时,由于仲碳正离子不如叔碳正离子稳定,某些特殊结构的醇可能容易发生重排。
活性:HX:HI>HBr>HCl;
醇:烯丙醇>3°>2°>1°
烯丙醇、三级醇、二级醇在酸催化下可通过SN1历程进行:
三、光谱性质
IR:醇的C—O吸收峰出现在1000—1200cm-1,其中伯醇约在1060—1030cm-1区域;仲醇约在1100cm-1附近;叔醇约在1140cm-1附近;酚的C—O吸收峰出现在1230cm-1。醇的—OH有两个吸收峰,未缔合的自由—OH在3600—3610cm-1有一外形较锐的吸收带;缔合—OH在3600—3210cm-1有一外形较宽的吸收带
大学有机化学第十章醇酚醚

② 与金属离子的络合
MgCl2•6ROH CaCl2•4ROH
结晶醇 (溶于水\不溶于有机溶剂)
因此:
不能用无水CaCl2干燥ROH
2. 醇与活泼金属的反应 ——弱酸性
+ CH3CH2OH Na
+ CH3CH2ONa H2
+ (CH3)3COH K
+ (CH3)3COK H2
醇金属: 强碱性试剂和强亲核性试剂
OH
R'
OH
R
30 叔醇( R' C OH ): (CH3)3COH R''
② 按羟基所连的烃基分:
饱和醇:
OH
CH3CH2OH (CH3)3COH
不饱和醇:
OH
CH2=CHCH2OH CH3C≡ CCH2OH
芳香醇:
CH OH 2
CH OH 2
③ 按羟基的数目分类:
一元醇: CH3CH2CH2OH
② RX的制备:10 醇,可采用 HX作卤化剂;
不是10 醇,不采用 HX作卤化剂,否则易得到重排产物。 可采用SOCl2 , PX3 , PX5作卤化剂
i) 与SOCl2反应
ROH SOCl2 RC+l SO2 + HCl
优点:1) 不重排,且产物构型保持
2) 副产物均为气体,易于除去 3) 产率高,产物容易分离
i. 伯醇氧化成醛和羧酸
[O]
[O]
RCH2OH
RCHO
RCOOH
[O]:KMnO4/H+、HNO3、 CrO3/ H2SO4、 K2Cr2O7/H2SO4、Na2Cr2O7/H2SO4 等
e.g.
CrO3 / H2SO4
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
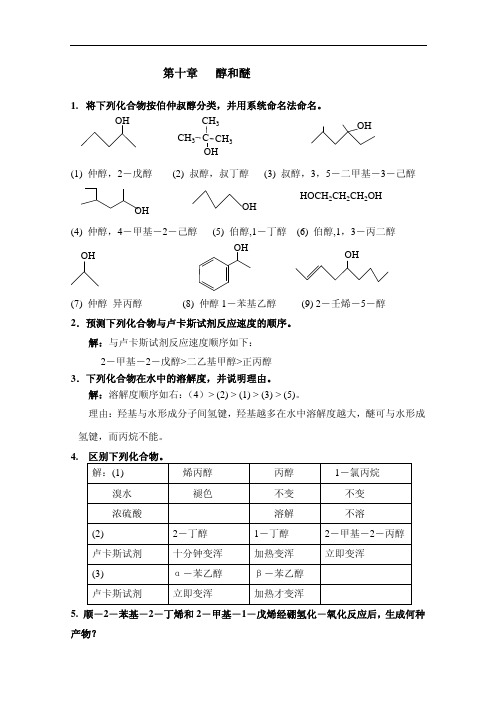
第十章醇和醚1. 将下列化合物按伯仲叔醇分类,并用系统命名法命名。
CH3CH3C CH3OHOHOH(1) 仲醇,2-戊醇(2) 叔醇,叔丁醇(3) 叔醇,3,5-二甲基-3-己醇OH OHHOCH2CH2CH2OH (4) 仲醇,4-甲基-2-己醇(5) 伯醇,1-丁醇(6) 伯醇,1,3-丙二醇OH OHOH(7) 仲醇异丙醇(8) 苄醇1-苯基乙醇(9) 2-壬烯-5-醇,仲醇2.预测下列化合物与卢卡斯试剂反应速度的顺序。
解:与卢卡斯试剂反应速度顺序如下:2-甲基-2-戊醇>二乙基甲醇>正丙醇3.下列化合物在水中的溶解度,并说明理由。
解:溶解度顺序如右:(4)> (2) > (1) > (3) > (5)。
理由:羟基与水形成分子间氢键,羟基越多在水中溶解度越大,醚可与水形成氢键,而丙烷不能。
4. 区别下列化合物。
5. 顺-2-苯基-2-丁烯和2-甲基-1-戊烯经硼氢化-氧化反应后,生成何种产物?解:CH3C=C CH3 HC6H52622C6H5CHCHOH3CH3CH3HOCH22CH2CH3CH3CH2CH2CH2CH26226. 写出下列化合物的脱水产物。
7.比较下列各组醇和溴化氢反应的相对速度。
解:(1) 反应速度顺序:对甲基苄醇> 苄醇> 对硝基苄醇。
(2) a-苯基乙醇>苄醇> β-苯基乙醇8.(1)3-丁烯-2-醇与溴化氢作用可能生成那些产物?试解释之。
解:反应产物和反应机理如下:CH2=CH CHCHOHHBrCH2=CH CHCHOH +2=CH CHCHOH2+2CH2=CH CHCH3+CH2CH=CHCH3+Br--BrCH2CH=CHCH3+BrCH2=CH CHCH3BrCH2=CH CHCH3BrCH2CH=CHCH3(2)2-丁烯-1-醇与溴化氢作用可能生成那些产物?试解释之。
解:反应产物和反应机理如下:HOCH2CH=CHCH HBr BrCH2CH=CHCH3+CH2=CHCHCH3OH HOCH2CH=CHCH3H+H2O+CH2CH=CHCH3H2O2CH=CHCH3+CH2=CHCHCH3+--BrCH2CH=CHCH3CH2=CHCHCH3OH9. 应历程解释下列反应事实。
解:(1) 反应历程:H+3)3CCHCH3(CH3)3CCHCH3OH+H+(CH3)3CCH=CH2CH3CCH333CH3CCH3CH3CHCH3+H+(CH3)2CHC=CH23+(CH3)2C=(CH3)2(2) 反应历程:CH2OH+CH2OH2+H2OCH2+2+++H+CH2H+CH3+H+-扩环重排1,2-H迁移10. 用适当地格利雅试剂和有关醛酮合成下列醇(各写出两种不同的组合)。
解:1.2-戊醇:CH3CHO+CH3CH2CH2MgBr CH3CHCH2CH2CH32+CH3CHCH2CH2CH3OHCH3MgBr+OCHCH2CH2CH2CH3CH3CHCH2CH2CH3H2O.H+CH3CHCH2CH2CH3(2)2-甲基-2-丁醇:无水乙醚CH 3MgBr+CH 3COCH 2CH 3CH 3CH 3CH 2CCH 3H O,H +CH 3CH 2MgBr +CH 3COCH 3CH 3CH 3CH 2CCH 3OMgBr2+CH 3CH 3CH 2CCH 3CH 3CH 3CH 2CCH 3(3)2-苯基-1-丙醇:MgBrCHCH 2CH 3+OCHCH 2CH 3+CHCH 2CH 3OHCHO+CH 3CH 2CH 2MgBrCHCH 2CH 3H 3O +CHCH 2CH 3OH(4)2-苯基-2-丙醇:+CH 3CO C 6H C CH 3OMgBrCH 3MgBr CH 32+MgBr+CH 3COCH C CH 3CH 32+OH C CH 3CH 3OHC CH 3CH 311.合成题解:(1)甲醇,2-丁醇合成2-甲基-1-丁醇:CH 3CHCH 2CH 3PCl 3Cl 252O 3CHCHCH 3CH 3CHCH 2CH 3CH 3OH[O]CH 2O+CH 3CHCH 2CH 3H O,H +CH 3CH 2CHCH 2OHCH 3(2)正丙醇,异丙醇合成2- 甲基-2-戊醇CH3CH2CH2OH3CH3CH2CH2Cl Mg,(C2H5)2O3CH2CH2MgClCH3CHCH [O]CH3COCH3CH3CCH2CH2CH3OHCH3CH3CH2CH2MgCl CH3COCH32++(3)甲醇,乙醇合成正丙醇,异丙醇:CH3OH PCl3CH3ClMg,(C H)O3MgClCH3CH2OCH3CH2PCl3CH3CH2ClMg,(C H)2OCH3CH2MgClCH3CH2OH [O]CH3CHOCH3MgCl+CH3CHO H2O,H+CH3CHCH3OHCH3CH2MgCl+CH2O H O,H+CH3CH2CH2OH(4)2-甲基-丙醇,异丙醇合成2,4-二甲基-2-戊烯CH3CHCHOH3COCH3CH3CH32OH PCl3CH3CH32Cl252CH3CHCH2MgClCH32+CH3CH3CHCH2CCH3OHCH3CH3CH33CHCH=CCH3(5)丙烯合成甘油和三硝酸甘油酯CH3CH=CH Cl2C2CH=CH2Ca(OH)2CH2CHCH2ClCl OHCl2CH 2CHCH 2OH OH HNO H SO CH 2CH CH 2ONO 2ONO 2ONO 2CH 2CHCH 2(6)苯,乙烯,丙烯 合成3-甲基-1-苯基-2-丁烯CH 3CH=CH 2CH 3COCH 3CH=CH 2HBr/ROORCH 2CH 2Br25)2O CH 2CH 2MgClCH 3COCH 3H 2O,H +CH 2CH 2CCH 3CH 3H 2SO4CH 2CH=CCH 3CH 3+CH 2=CH 23CH 2CH -212.完成下面转变。
解:(1) 乙基异丙基甲醇2-甲基-2-氯戊烷CH 3CH 3CH 2CHCHCH 3CH 3CH 2CH 2CCH 3CH 3Cl(2)3-甲基-2-丁醇 叔戊醇CH 3CH 3CHCHCH 3OH CH 33CH=CCH 3H 2O,H +CH 3CH 3CH 23OH(3)异戊醇 2-甲基-2-丁烯CH 3CHCH 2CH 2OHCH 3CH 3C=CHCH 33+13.用指定的原料合成下列化合物(其它试剂任选)。
解:(CH 3)COH +(CH 3)3CBrMg,(C 2H 5)2O(CH 3)3CMgBrCH 2O2(CH 3)3CCH 2CH 2H 2O,H +(CH 3)3CCH 2CH 2OH(1)H 2/NiOH3O+CH 3CH 2CH 22CH 3O(2)(CH 3)SO 4,NaOHOCH 325CO,HClCHOC 2H 5MgBr 2CH 325OHOCH 3C 2H 5OCH 3C 2H 5(3)14. 某醇C 5H 12O 氧化后生成酮,脱水则生成一种不饱和烃,将此烃氧化可生成酮和羧酸两种产物的混合物,推测该化合物的结构。
解:CH 3CHCCH 3CH 3CH 3CH 333COCH 3+CH 3COOHCH 3CHCHCH CH 315. 从某醇依次和溴化氢,氢氧化钾醇溶液,硫酸和水,K 2Cr 2O 7+H 2SO 4作用,可得到2-丁酮,试推测原化合物的可能结构,并写出各步反应式。
解:化合物结构式为:CH 3CH 2CH 2CH 2OHCH 3CH 2CH 2CH 2OH +HBr3CH 2CH 2CH 2BrKOH(C H OH)CH 3CH 2CH=CH 2H 2O,H 2SO 4CH 3CH 2CHCH 3OHCH 3CCH 2CH 3O16.有一化合物(A )的分子式为C 5H 11Br ,和氢氧化钠水溶液共热后生成C 5H 12OB),(B)具有旋光性,能与钠作用放出氢气,和硫酸共热生成C 5H 10(C),(C)经臭氧化和还原剂存在下水解则生成丙酮和乙醛,是推测(A ),(B),(C)的结构,并写出各步反应式。
解:NaOHaq CH 3C H CH 3CHCH 3OH CH 3CH=CCH 3CH 3O 3Zn,H 2O 3CHO +CH 3COCH 3CH 3C H CH 33Br (A)(B)(C)17. 新戊醇在浓硫酸存在下加热可得到不饱和烃,将这个不饱和烃臭氧化后,在锌纷存在下水解就可以得一个醛和酮,试写出这个反应历程及各步反应产物的结构式。
解:CH 3C CH 3CH 3CH 2H +CH 3CCH 33CH 2OH 2+H 2OCH 3C CH 33CH 2+CH 3C CH 3CH 2CH +H +CH 3CH 3C=C H CH 3O 3CH 3CH 3C O OC OH CH 3Zn,H 2OCH 3CCH 3+CH 3CHO O18. 由化合物(A)C 6H 13Br 所制得格利雅试剂与丙酮作用可生成2,4-二甲基-3-乙基-2-戊醇。
(A )可发生消除反应生成两种异构体(B ),(C),将(B )臭氧化后再在还原剂存在下水解,则得到相同碳原子数的醛(D )酮(E),试写出各步反应式以及(A )-(E)的结构式。
解:各步反应式结(A )-(B)的结构式如下:(A)+CH 3CCH 3CH 3C CH 3OHCH CH 2CH 3CH CH 3CH 3(A):CH 3CH 2CHCHCH3CH 325CH 3CH 2CH=CCH 3CH 3CH 3CH=CHCHCH 3CH 3(B)(C)CH 3CH 2CH=CCH 3CH 3O 3Zn,H OCH 3CCH 3O +CH 3CH 2CHO19.写出下列醚的同分异构体,并按习惯命名法和系统命名法命名。
解:(1)C 4H 10O 习惯命名法 IUPAC 命名法 CH 3OCH 2CH 2CH 3 甲基正丙基醚 1-甲氧基丙烷 CH 3OCH(CH 3)2 甲基异丙基醚 2-甲氧基丙烷 CH 3CH 2OCH 2CH 3 乙醚, 乙氧基乙烷 (2) C 5H 12O习惯命名法 IUPAC 命名法 CH 3OCH 2CH 2CH 2CH 3 甲基正丁基醚 1-甲氧基丁烷 CH 3OCHCH 3CH 2CH 3 甲基仲丁基醚 2-甲氧基丁烷CH 3OCH 2CHCH 3CH 3 甲基异丁基醚 2-甲基-1-甲氧基丙烷 CH 3OC (CH 3)3 甲基叔丁基醚 2-甲基-2-甲氧基丙烷 CH 3 CH 2OCH2CH 2CH 3 乙基正丙基醚, 1-乙氧基丙烷 CH 3CH 2OCHCH 3CH 3 乙基异丙基醚,2-乙氧基丙烷20.分离下列各组化合物。
