(完整版)南京大学物理化学选择题答案完整版
南京大学物理化学选择题完整版教材

第一章热力学第一定律及其应用物化试卷(一)1.物质的量为n的纯理想气体,该气体在如下的哪一组物理量确定之后,其它状态函数方有定值。
( )(A) p (B) V (C) T,U (D) T, p2. 下述说法哪一个正确? ( )(A) 热是体系中微观粒子平均平动能的量度(B) 温度是体系所储存热量的量度(C) 温度是体系中微观粒子平均能量的量度(D) 温度是体系中微观粒子平均平动能的量度3. 有一高压钢筒,打开活塞后气体喷出筒外,当筒内压力与筒外压力相等时关闭活塞,此时筒内温度将: ( )(A)不变 (B)升高 (C)降低 (D)无法判定4. 1 mol 373 K,标准压力下的水经下列两个不同过程变成373 K,标准压力下的水气, (1) 等温等压可逆蒸发,(2) 真空蒸发这两个过程中功和热的关系为: ( )(A) |W1|> |W2| Q1> Q2 (B)|W1|< |W2| Q1< Q2(C) |W1|= |W2| Q1= Q2 (D)|W1|> |W2| Q1< Q25. 恒容下,一定量的理想气体,当温度升高时热力学能将:( )(A)降低 (B)增加 (C)不变 (D)增加、减少不能确定6. 在体系温度恒定的变化中,体系与环境之间: ( )(A) 一定产生热交换 (B) 一定不产生热交换(C) 不一定产生热交换 (D) 温度恒定与热交换无关7. 一可逆热机与另一不可逆热机在其他条件都相同时,燃烧等量的燃料,则可逆热机拖动的列车运行的速度:( )(A) 较快 (B) 较慢 (C) 一样 (D) 不一定8. 始态完全相同(p1,V1,T1)的一个理想气体体系,和另一个范德华气体体系,分别进行绝热恒外压(p0)膨胀。
当膨胀相同体积之后,下述哪一种说法正确?( )(A) 范德华气体的热力学能减少量比理想气体多(B) 范德华气体的终态温度比理想气体低(C) 范德华气体所做的功比理想气体少(D) 范德华气体的焓变与理想气体的焓变相等9.ΔH =Q p , 此式适用于下列哪个过程:( )(A) 理想气体从106 Pa反抗恒外压105 Pa膨胀到105 Pa(B) 0℃ , 105 Pa 下冰融化成水(C) 电解 CuSO4水溶液(D) 气体从(298 K, 105 Pa)可逆变化到(373 K, 104 Pa) 10.在100℃和25℃之间工作的热机,其最大效率为: ( ) (A) 100 % (B) 75 % (C) 25 % (D) 20 % 11.对于封闭体系,在指定始终态间的绝热可逆途径可以有:( )(A) 一条 (B) 二条 (C) 三条 (D) 三条以上12.某理想气体的γ =C p/C v=1.40,则该气体为几原子分子气体? ( ) (A) 单原子分子气体 (B) 双原子分子气体(C) 三原子分子气体 (D) 四原子分子气体13.实际气体绝热恒外压膨胀时,其温度将: ( )(A) 升高 (B) 降低 (C) 不变 (D) 不确定14.当以5 mol H2气与4 mol Cl2气混合,最后生成2 mol HCl气。
(完整版)南京大学物理化学下册(第五版傅献彩)复习题及解答

第八章电解质溶液第九章1.可逆电极有哪些主要类型?每种类型试举一例,并写出该电极的还原反应。
对于气体电极和氧化还原电极在书写电极表示式时应注意什么问题?答:可逆电极有三种类型:(1)金属气体电极如Zn(s)|Zn2+ (m) Zn2+(m) +2e- = Zn(s)(2)金属难溶盐和金属难溶氧化物电极如Ag(s)|AgCl(s)|Cl-(m), AgCl(s)+ e- = Ag(s)+Cl-(m)(3)氧化还原电极如:Pt|Fe3+(m1),Fe2+(m2) Fe3+(m1) +e- = Fe2+(m2)对于气体电极和氧化还原电极,在书写时要标明电极反应所依附的惰性金属。
2.什么叫电池的电动势?用伏特表侧得的电池的端电压与电池的电动势是否相同?为何在测电动势时要用对消法?答:正、负两端的电势差叫电动势。
不同。
当把伏特计与电池接通后,必须有适量的电流通过才能使伏特计显示,这样电池中发生化学反应,溶液浓度发生改变,同时电池有内阻,也会有电压降,所以只能在没有电流通过的情况下才能测量电池的电动势。
3.为什么Weslon标准电池的负极采用含有Cd的质量分数约为0.04~0.12的Cd一Hg齐时,标准电池都有稳定的电动势值?试用Cd一Hg的二元相图说明。
标准电池的电动势会随温度而变化吗?答:在Cd一Hg的二元相图上,Cd的质量分数约为0.04~0.12的Cd一Hg齐落在与Cd一Hg固溶体的两相平衡区,在一定温度下Cd一Hg齐的活度有定值。
因为标准电池的电动势在定温下只与Cd一Hg齐的活度有关,所以电动势也有定值,但电动势会随温度而改变。
4.用书面表示电池时有哪些通用符号?为什么电极电势有正、有负?用实验能测到负的电动势吗?答:用“|”表示不同界面,用“||”表示盐桥。
电极电势有正有负是相对于标准氢电极而言的。
不能测到负电势。
5.电极电势是否就是电极表面与电解质溶液之间的电势差?单个电极的电势能否测量?如何用Nernst方程计算电极的还原电势?5.电极电势是否就是电极表面与电解质溶液之间的电势差?单个电极的电势能否测量?如何用Nernst 方程计算电极的还原电势?答:电极电势不是电极表面与电解质溶液之间的电势差。
南大班物化复习题答案

南大班物化复习题答案南京大学物理化学课程复习题答案一、选择题1. 物理化学中的“物理”一词主要指的是()A. 物理现象B. 物理过程C. 物理性质D. 物理量答案:C2. 根据热力学第一定律,下列哪个选项是正确的?A. 能量可以被创造B. 能量可以被消灭C. 能量守恒D. 能量可以无限制地转化为其他形式答案:C3. 化学平衡常数K与温度T的关系,由哪个方程描述?A. 范特霍夫方程B. 吉布斯自由能方程C. 克劳修斯-克拉佩龙方程D. 牛顿冷却定律答案:A二、填空题1. 热力学第二定律的开尔文表述是:不可能从单一热源吸热使之完全转化为________而不产生其他效果。
答案:功2. 理想气体状态方程为 PV = nRT,其中P代表________,V代表体积,n代表摩尔数,R是________,T是温度。
答案:压强;理想气体常数三、简答题1. 简述吉布斯自由能和化学平衡的关系。
答案:吉布斯自由能(G)是衡量一个化学反应在恒温恒压下自发进行方向的物理量。
当吉布斯自由能变化(ΔG)小于零时,反应是自发的;当ΔG大于零时,反应是非自发的;当ΔG等于零时,反应处于平衡状态。
2. 描述熵的概念及其在热力学中的重要性。
答案:熵是热力学系统中无序度的量度,通常用来描述系统的能量分布。
在热力学中,熵的变化是衡量系统从有序向无序转变的指标,也是热力学第二定律的体现,即自然界的自发过程总是向着熵增的方向进行。
四、计算题1. 给定一个理想气体在等压过程中,其体积从V1变化到V2,温度从T1变化到T2,求该过程中气体所做的功。
答案:在等压过程中,气体所做的功W可以通过公式W = P(V2 - V1)计算,其中P是恒定的压力。
2. 已知某化学反应的焓变ΔH和熵变ΔS,以及反应的初始和最终温度T1和T2,求该反应在T2温度下的吉布斯自由能变化ΔG2。
答案:吉布斯自由能变化可以通过公式ΔG = ΔH - TΔS计算。
在给定的T2温度下,将T1替换为T2,即可得到ΔG2的值。
南京大学物理化学考研真题(含结构化学)
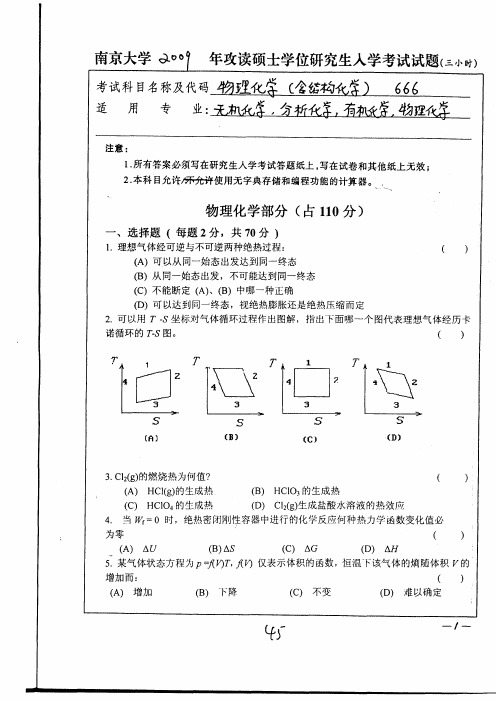
体经历卡
( )
quz
3
S (D9
3,Clzl⒆ 的燃烧 热 为何值 ? m) HCl(g)的 G) HClO4的 4.当 9/f=0时 为零 生成热 生成热 ⒀ ) HClO3的 rD) c12(⒄ 生成 热 生成 盐酸水溶 液 的热效应
(
)
,绝 热密 闭刚性容器 中进行的化学反应何种热力学 函数变化值 必
30.如 图在 毛细管 内装 入 润湿性液体,当 在毛细管 内左端加热 时,则管 内液体将 :( )
, (
↑ 加热
′
右 移 动 c)不 左 移动 (B)向 移动 (D)因 失 去平衡 而 左右 来 冂移动 m)向 I,其 2m的 31.半 径 为 I×10ˉ 球形 肥皂泡 的表 面张力 为 0.⒆ 5N・ mˉ 附加 压 力 为 : ( ) (c) 2.5N.m-2 (e) 5 N'm-2 (A) 0.025 (D) l0 N.m-2 N.m'' 一 毛细 管端插 入 水 中 ,毛 细管中水面上升 5cm,若 将毛细管 向下移动 ,留 了 3cm 32.将 在水 面 ,试 问水 在 毛 细 管 上 端 的行 为是 : m)水 (C)毛 从 毛细 管上端 溢 出 细 管 上端 水面 呈 凹形 弯 月面 (B)毛 (D)毛 ( 细 管 上端 水 面 呈 凸形弯 月面 细 管 上 端 水 面 早水平 面 )
南 京 大 学 aoo丨
刂 年 攻 读 硕 士 学 位研 究 生 入 学 考试 试题 (三 咐) 羔 , 6“
考试科 目名称及代码 毡 饧哩倪苄 c兮 獭
适 用
专
注意 : 1.所 有答案必须写在研究生人学考试答题纸上 ,写在试卷和其他纸上无效 ; 2.本 科 目允许秘 使用无字典存 储和编程功能的计算器 。
南京大学物理化学选择题问题详解完整版

第一章热力学第一定律及其应用物化试卷(一)1.物质的量为n的纯理想气体,该气体在如下的哪一组物理量确定之后,其它状态函数方有定值。
( )(A) p (B) V (C) T,U (D) T, p2. 下述说法哪一个正确? ( )(A) 热是体系中微观粒子平均平动能的量度 (B) 温度是体系所储存热量的量度(C) 温度是体系中微观粒子平均能量的量度 (D) 温度是体系中微观粒子平均平动能的量度3. 有一高压钢筒,打开活塞后气体喷出筒外,当筒内压力与筒外压力相等时关闭活塞,此时筒内温度将: ( )(A)不变 (B)升高 (C)降低 (D)无法判定4. 1 mol 373 K,标准压力下的水经下列两个不同过程变成373 K,标准压力下的水气, (1) 等温等压可逆蒸发, (2) 真空蒸发这两个过程中功和热的关系为: ( )(A) |W1|> |W2| Q1> Q2 (B)|W1|< |W2| Q1< Q2(C) |W1|= |W2| Q1= Q2 (D)|W1|> |W2| Q1< Q25. 恒容下,一定量的理想气体,当温度升高时热力学能将:( )(A)降低 (B)增加 (C)不变 (D)增加、减少不能确定6. 在体系温度恒定的变化中,体系与环境之间: ( )(A) 一定产生热交换 (B) 一定不产生热交换(C) 不一定产生热交换 (D) 温度恒定与热交换无关7. 一可逆热机与另一不可逆热机在其他条件都相同时,燃烧等量的燃料,则可逆热机拖动的列车运行的速度:( )(A) 较快 (B) 较慢 (C) 一样 (D) 不一定8. 始态完全相同(p1,V1,T1)的一个理想气体体系,和另一个范德华气体体系,分别进行绝热恒外压(p0)膨胀。
当膨胀相同体积之后,下述哪一种说法正确?( )(A) 范德华气体的热力学能减少量比理想气体多 (B) 范德华气体的终态温度比理想气体低(C) 范德华气体所做的功比理想气体少 (D) 范德华气体的焓变与理想气体的焓变相等9.ΔH =Qp , 此式适用于下列哪个过程:( )(A) 理想气体从106 Pa反抗恒外压105 Pa膨胀到105 Pa (B) 0℃ , 105 Pa 下冰融化成水(C) 电解 CuSO4水溶液 (D) 气体从(298 K, 105 Pa)可逆变化到(373 K, 104 Pa)10.在100℃和25℃之间工作的热机,其最大效率为: ( )(A) 100 % (B) 75 % (C) 25 % (D) 20 %11.对于封闭体系,在指定始终态间的绝热可逆途径可以有:( )(A) 一条 (B) 二条 (C) 三条 (D) 三条以上12.某理想气体的γ =Cp/Cv =1.40,则该气体为几原子分子气体? ( )(A) 单原子分子气体 (B) 双原子分子气体(C) 三原子分子气体 (D) 四原子分子气体13.实际气体绝热恒外压膨胀时,其温度将: ( )(A) 升高 (B) 降低 (C) 不变 (D) 不确定14.当以5 mol H2气与4 mol Cl2气混合,最后生成2 mol HCl气。
南大物化课本复习题答案

南大物化课本复习题答案1. 请解释物质的三态变化及其热力学基础。
答案:物质的三态变化包括固态、液态和气态之间的相互转化。
固态物质分子排列紧密,分子间作用力强;液态物质分子间作用力较弱,分子可以自由流动;气态物质分子间作用力最弱,分子运动自由度最高。
热力学基础涉及相变过程中的热力学参数变化,如焓变、熵变和自由能变等。
2. 简述布朗运动的物理意义及其对分子运动理论的验证。
答案:布朗运动是指悬浮在液体中的微小颗粒由于液体分子的无规则碰撞而产生的随机运动。
这一现象的物理意义在于,它提供了分子运动理论的实验证据,证实了液体分子的无规则热运动。
3. 描述理想气体状态方程及其适用范围。
答案:理想气体状态方程为PV=nRT,其中P表示压强,V表示体积,n 表示摩尔数,R是理想气体常数,T是绝对温度。
该方程适用于气体分子间相互作用力可以忽略不计,分子体积与容器体积相比可以忽略的情况。
4. 阐述热力学第一定律及其在能量守恒中的应用。
答案:热力学第一定律表明能量守恒,即系统内能的变化等于系统吸收的热量与对外做的功之和。
数学表达式为ΔU=Q+W。
这一定律在能量转换和守恒的分析中具有重要应用,如热机效率的计算。
5. 讨论熵的概念及其在热力学过程中的意义。
答案:熵是一个热力学状态函数,用于描述系统的无序度。
熵的增加表示系统无序度的增加,而熵的减少则表示系统无序度的减少。
在热力学过程中,熵的概念用于判断过程的自发性,即自然过程总是倾向于熵增的方向。
6. 简述化学势的定义及其在相平衡中的应用。
答案:化学势是描述在恒温恒压下,系统增加一个粒子时系统吉布斯自由能变化的物理量。
在相平衡中,化学势用于判断不同相之间的物质转移方向,即物质总是从化学势高的相转移到化学势低的相。
7. 描述范德华方程及其对实际气体的近似描述。
答案:范德华方程是实际气体状态方程的一种,考虑了分子体积和分子间相互作用力的影响。
方程形式为(P+a/V^2)(V-nb)=RT,其中a和b 是与气体种类有关的常数。
南京大学物理化学复习题答案
南京大学物理化学复习题答案一、选择题1. 热力学第一定律的数学表达式是:A. ΔU = Q + WB. ΔH = Q - WC. ΔG = ΔH - TΔSD. ΔS = Q/T答案:A2. 在等压条件下,一个理想气体的内能变化只与温度有关,这是因为:A. 理想气体分子间无作用力B. 理想气体分子的平动能与温度成正比C. 理想气体分子的转动能与温度无关D. 理想气体的体积不变答案:B3. 根据范特霍夫方程,当温度升高时,化学平衡常数K的变化趋势是:A. 增大B. 减小C. 保持不变D. 无法确定答案:D二、简答题1. 简述热力学第二定律的两种表述方式。
答:热力学第二定律有两种表述方式。
克劳修斯表述:不可能从单一热源吸热使之完全转化为功而不产生其他影响。
开尔文-普朗克表述:不可能制造一种循环过程,其唯一结果就是将热量从冷源转移到热源。
2. 解释什么是吉布斯自由能,并说明其在化学反应中的应用。
答:吉布斯自由能(Gibbs free energy)是描述系统在恒温恒压条件下进行自发过程的能力的物理量,定义为G = H - TS。
在化学反应中,吉布斯自由能的变化量(ΔG)可以用来判断反应的自发性:ΔG < 0时反应自发进行,ΔG > 0时反应非自发进行,ΔG = 0时反应处于平衡状态。
三、计算题1. 已知某理想气体在298K时的摩尔热容Cp = 35.2 J/(mol·K),求该气体在100K至298K温度范围内的焓变ΔH。
解:由于理想气体的焓变等于其热容与温度差的乘积,即ΔH =CpΔT。
将已知数值代入公式得:ΔH = 35.2 J/(mol·K) × (298K - 100K) = 35.2 J/(mol·K)× 198K = 6963.6 J/mol。
2. 某化学反应在298K时的平衡常数K = 10^3,求在相同温度下,该反应的吉布斯自由能变化ΔG。
(完整版)南京大学物理化学下册(第五版傅献彩)复习题及解答
答:对电解质瀋液来说电导G 是其呆电的能力,以1 1型电解质洛腋为例.第八章电解质溶液L Faraday 电解定律的基本内容是什么?这定律在电牝学中有何用魁?答:拉第电解定律的基本内容込:通电于电解质溶液之后,(1)在电楼上(聘相界面八发生化学窘化的物质的駅勻通入电荷成正比.(2)若 将几亍电解池申联■通人一定的电荷議后•衽各个电解池的电极卜.发生化学变比的物质的帚祁相等.Qf-i> —z^-eL —z± F根据Faraday 定律,通过分析电解过程中反应物在电极上物质的址的变化,就可求出电的址的数值•在 电化学的定駁研究和电解工业上有車要的应用.2. 电池中正极、负极、阴极、阳极的定义分别晶什么?为什么盘煤电池中负极是阳极而正极是阴极? 笞:给出陀了•到外电路的电极叫做电池的负极,在外砲路中电勢*低. 从外电路接受电子的电极叫做电池的止槻•在外电路中电势较高.发生氧化柞用的电极称为阳极■发生还原作用的一极称为阴极•原电池杓阳扱发生麵化作用•阴橈发生 还甌作用.内电路的电子由阳极运动到阴极.所械电池的阴彊是正彊,阳极是负极.3*电解质涪液的电导車和摩尔电导率与电解质溶液浓度的关采有何不同。
为什么?答匕蹑电解质漳液的电导率随若浓度的增大而升高(导电粒子数但大到一定程度以后,由于 正、负禹子之间的相f 作用增大•因而使离子的运动速率降低.电导率反而下降•弱电解质的电导率随故度 的变化不显蒼•浓度增加电离度减少.离子数目变化不天•摩尔电导率随灌廈的变化与电导率不同•浓度降 低,粒子之闾相互作用减弱・正、负薦子的运动速率因而增加•故摩爼电导率增加*4. 怎样分别求强电解嵐和弱电解质的无限稱降摩尔电錚率?为什么翌用车同的方袪?答:庄低威度尸,强电解陪液的摩尔电导率*枚线性关慕.Am*銘(1 一0Q在一定温度下,一定电解质溶液来说甲是定偵.通过作阳•宜线勺纵坐标的交点即为无限稀秫时落液 的辱尔电导率AS 1,即外推袪.弱电解质的无限廉释摩尔电导率A ;・跟据离了独立移动迄律•可由强电解质溶薇的无限稀释摩尔电 导率A 計设计求算,不能由外惟陆求出,由于购电解质的幡涪液在很低报度F ,Am 与丘不垦总线关系.并且 浓度的変化对的值影响很大.实验的谋差很大•由实验值直接求弱电解质的厲:很困难.5. 离子的摩尔电导率、离子的迁移速率、离子的电迁移率和离P 迁移数之间有哪些建址关系式?答,定図关系式*j uit* dE/dl r- = — dE/'dl牛t r_离子迁移連率*+川一厲产的电迁移率*A ;=(«7+u-)E6・在某电解质落液中•若丫门种离『疗在’则溶液的总电导应该用下列哪牛公式表示’(1) G =臣 +臣 + …*〔2〉G■无限稀释强电解质溶液十A :,G=M A// te —Am • c稀电解质溶液 Am =At + A 二(Am 4-Am )c = /lm * c+Am • CC4- ~Am * C 则 G+ =K+A// ・•・G 厂G+G 亠盒+斤…=》越7.电解质与非电解质的化学势表示形式冇何不同?活度因子的表示式有何不同? 答:非电解质的化学势的表示形式.阿=閔(T ) +RHny“・B 箫=山(T ) +RTlnu*R 电解质 抄=必(丁)+尺力皿8=川(7。
南大物理化学复习题答案
南大物理化学复习题答案1. 简述物理化学中的热力学第一定律。
答案:物理化学中的热力学第一定律,也称为能量守恒定律,表述为在一个封闭系统中,能量不能被创造或消灭,只能从一种形式转化为另一种形式,或者从一个物体转移到另一个物体。
在热力学过程中,系统吸收的热量(Q)等于系统内能的增加(ΔU)加上系统对外做的功(W),即Q = ΔU + W。
2. 描述理想气体状态方程。
答案:理想气体状态方程是 PV = nRT,其中P代表压强,V代表体积,n代表气体的摩尔数,R是理想气体常数,T是绝对温度。
该方程描述了理想气体在不同状态下的压强、体积、温度和摩尔数之间的关系。
3. 什么是化学平衡?答案:化学平衡是指在一个封闭系统中,正向反应和逆向反应以相同的速率进行,使得所有反应物和产物的浓度保持不变的状态。
在平衡状态下,虽然反应仍在进行,但宏观上观察不到任何变化。
4. 解释勒夏特列原理。
答案:勒夏特列原理指出,如果一个处于平衡状态的化学反应系统受到外部条件的改变(如浓度、温度或压强的变化),系统会自动调整以抵消这种改变,使得新的平衡状态能够重新建立。
例如,如果一个放热反应的系统温度升高,系统会倾向于向吸热的方向移动,以减少温度的增加。
5. 什么是电化学电池?答案:电化学电池是一种将化学能直接转化为电能的装置。
它由两个半电池组成,每个半电池包含一个电极和一个电解质溶液。
在电池的两极之间发生氧化还原反应,电子通过外部电路流动,产生电流。
6. 简述表面张力的概念。
答案:表面张力是液体表面分子之间相互吸引力的表现,这种力使得液体表面尽可能地缩小。
表面张力的存在使得液体能够抵抗外部力量,如水滴能够保持球形而不扩散。
7. 描述相变过程中的潜热。
答案:潜热是指在物质相变过程中(如熔化、凝固、蒸发、凝结)吸收或释放的热量,而在此过程中物质的温度保持不变。
例如,在水的沸腾过程中,水分子从液态转变为气态时需要吸收大量的热量,但温度保持在沸点不变,这部分吸收的热量就是潜热。
(完整版)南京大学物理化学下册(第五版傅献彩)复习题及解答
第八章电解质溶液第九章1.可逆电极有哪些主要类型?每种类型试举一例,并写出该电极的还原反应。
对于气体电极和氧化还原电极在书写电极表示式时应注意什么问题?答:可逆电极有三种类型:(1)金属气体电极如Zn(s)|Zn2+ (m) Zn2+(m) +2e- = Zn(s)(2)金属难溶盐和金属难溶氧化物电极如Ag(s)|AgCl(s)|Cl-(m), AgCl(s)+ e- = Ag(s)+Cl-(m)(3)氧化还原电极如:Pt|Fe3+(m1),Fe2+(m2) Fe3+(m1) +e- = Fe2+(m2)对于气体电极和氧化还原电极,在书写时要标明电极反应所依附的惰性金属。
2.什么叫电池的电动势?用伏特表侧得的电池的端电压与电池的电动势是否相同?为何在测电动势时要用对消法?答:正、负两端的电势差叫电动势。
不同。
当把伏特计与电池接通后,必须有适量的电流通过才能使伏特计显示,这样电池中发生化学反应,溶液浓度发生改变,同时电池有内阻,也会有电压降,所以只能在没有电流通过的情况下才能测量电池的电动势。
3.为什么Weslon标准电池的负极采用含有Cd的质量分数约为0.04~0.12的Cd一Hg齐时,标准电池都有稳定的电动势值?试用Cd一Hg的二元相图说明。
标准电池的电动势会随温度而变化吗?答:在Cd一Hg的二元相图上,Cd的质量分数约为0.04~0.12的Cd一Hg齐落在与Cd一Hg固溶体的两相平衡区,在一定温度下Cd一Hg齐的活度有定值。
因为标准电池的电动势在定温下只与Cd一Hg齐的活度有关,所以电动势也有定值,但电动势会随温度而改变。
4.用书面表示电池时有哪些通用符号?为什么电极电势有正、有负?用实验能测到负的电动势吗?答:用“|”表示不同界面,用“||”表示盐桥。
电极电势有正有负是相对于标准氢电极而言的。
不能测到负电势。
5.电极电势是否就是电极表面与电解质溶液之间的电势差?单个电极的电势能否测量?如何用Nernst方程计算电极的还原电势?5.电极电势是否就是电极表面与电解质溶液之间的电势差?单个电极的电势能否测量?如何用Nernst 方程计算电极的还原电势?答:电极电势不是电极表面与电解质溶液之间的电势差。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章热力学第一定律及其应用物化试卷(一)1.物质的量为n的纯理想气体,该气体在如下的哪一组物理量确定之后,其它状态函数方有定值。
( )(A) p (B) V (C) T,U (D) T, p2. 下述说法哪一个正确? ( )(A) 热是体系中微观粒子平均平动能的量度 (B) 温度是体系所储存热量的量度(C) 温度是体系中微观粒子平均能量的量度 (D) 温度是体系中微观粒子平均平动能的量度3. 有一高压钢筒,打开活塞后气体喷出筒外,当筒内压力与筒外压力相等时关闭活塞,此时筒内温度将: ( )(A)不变 (B)升高 (C)降低 (D)无法判定4. 1 mol 373 K,标准压力下的水经下列两个不同过程变成373 K,标准压力下的水气, (1) 等温等压可逆蒸发, (2) 真空蒸发这两个过程中功和热的关系为: ( )(A) |W1|> |W2| Q1> Q2 (B)|W1|< |W2| Q1< Q2(C) |W1|= |W2| Q1= Q2 (D)|W1|> |W2| Q1< Q25. 恒容下,一定量的理想气体,当温度升高时热力学能将:( )(A)降低 (B)增加 (C)不变 (D)增加、减少不能确定6. 在体系温度恒定的变化中,体系与环境之间: ( )(A) 一定产生热交换 (B) 一定不产生热交换(C) 不一定产生热交换 (D) 温度恒定与热交换无关7. 一可逆热机与另一不可逆热机在其他条件都相同时,燃烧等量的燃料,则可逆热机拖动的列车运行的速度:( )(A) 较快 (B) 较慢 (C) 一样 (D) 不一定8. 始态完全相同(p1,V1,T1)的一个理想气体体系,和另一个范德华气体体系,分别进行绝热恒外压(p0)膨胀。
当膨胀相同体积之后,下述哪一种说法正确?( )(A) 范德华气体的热力学能减少量比理想气体多 (B) 范德华气体的终态温度比理想气体低(C) 范德华气体所做的功比理想气体少 (D) 范德华气体的焓变与理想气体的焓变相等9.ΔH =Qp , 此式适用于下列哪个过程:( )(A) 理想气体从106 Pa反抗恒外压105 Pa膨胀到105 Pa (B) 0℃ , 105 Pa 下冰融化成水(C) 电解 CuSO4水溶液 (D) 气体从(298 K, 105 Pa)可逆变化到(373 K, 104 Pa)10.在100℃和25℃之间工作的热机,其最大效率为: ( )(A) 100 % (B) 75 % (C) 25 % (D) 20 %11.对于封闭体系,在指定始终态间的绝热可逆途径可以有:( )(A) 一条 (B) 二条 (C) 三条 (D) 三条以上12.某理想气体的γ =C p/Cv =1.40,则该气体为几原子分子气体? ( )(A) 单原子分子气体 (B) 双原子分子气体(C) 三原子分子气体 (D) 四原子分子气体13.实际气体绝热恒外压膨胀时,其温度将: ( )(A) 升高 (B) 降低 (C) 不变 (D) 不确定14.当以5 mol H2气与4 mol Cl2气混合,最后生成2 mol HCl气。
若以下式为基本单元,H2(g) + Cl2(g) ----> 2HCl(g),则反应进度ξ应是: ( )(A) 1 mol (B) 2 mol (C) 4 mol (D) 5 mol15.欲测定有机物燃烧热Qp,一般使反应在氧弹中进行,实测得热效应为Qv。
公式 Qp=Qv+Δn RT 中的Δn为:( )(A) 生成物与反应物总物质的量之差 (B) 生成物与反应物中气相物质的量之差(C) 生成物与反应物中凝聚相物质的量之差 (D) 生成物与反应物的总热容差16.凝固热在数值上与下列哪一种热相等: ( )(A) 升华热 (B) 溶解热 (C) 汽化热 (D) 熔化热17.已知 1mol HCl的无限稀释溶液与 1mol NaOH 的无限稀释溶液在恒温恒压下完全反应,热效应ΔrH =-55.9 kJ/mol,则 1mol HNO3的无限稀释溶液与 1mol KOH的无限稀释溶液在恒温恒压下完全反应的热效应ΔrH 为:( )(A) > -55.9 kJ/mol (B) < -55.9 kJ/mol (C) = -55.9 kJ/mol (D) 不能确定18.在标准压力下,1mol石墨与氧气反应生成1mol二氧化碳的反应热为ΔrH ,下列哪种说法是错误的? ( )(A) ΔH 是CO2(g)的标准生成热(B) ΔH =ΔU(C) ΔH 是石墨的燃烧热(D) ΔU <ΔH19.计算化学反应的热效应,下述说法哪些是正确的? ( )(1) 在同一算式中必须用同一参比态的热效应数据(2) 在同一算式中可用不同参比态的热效应数据(3) 在不同算式中可用不同参比态的热效应数据(4) 在不同算式中必须用同一参比态的热效应数(A) 1,3 (B) 2,4 (C) 1,4 (D) 2,320. Cl2(g)的燃烧热为何值? ( )(A)HCl(g)的生成热 (B)HClO3的生成热(C)HClO4的生成热 (D)Cl2(g)生成盐酸水溶液的热效应第一章热力学第一定律及其应用物化试卷(二)1. 1mol 单原子分子理想气体从 298 K,200.0 kPa 经历:① 等温, ② 绝热, ③ 等压三条途径可逆膨胀,使体积增加到原来的2倍,所作的功分别为W1,W2,W3,三者的关系是: ( )(A) |W1|>|W2|>|W3| (B) |W2|>|W1|>|W3|(C) |W3|>|W2|>|W1| (D) |W3|>|W1|>|W2|2. 下述说法哪一个是错误的? ( )(A) 封闭体系的状态与其状态图上的点一一对应(B) 封闭体系的状态即是其平衡态(C) 封闭体系的任一变化与其状态图上的实线一一对应(D) 封闭体系的任一可逆变化途径都可在其状态图上表示为实线3. 凡是在孤立体系中进行的变化,其ΔU和ΔH的值一定是: ( )(A) ΔU > 0 , ΔH > 0(B) ΔU = 0 , ΔH = 0(C) ΔU < 0 , ΔH < 0(D) ΔU = 0 , ΔH不确定4. " 封闭体系恒压过程中体系吸收的热量Qp等于其焓的增量ΔH ",这种说法: ( )(A) 正确 (B) 需增加无非体积功的条件(C) 需加可逆过程的条件 (D) 需加可逆过程与无非体积功的条件5. 非理想气体进行绝热自由膨胀时,下述答案中哪一个是错误的? ( )(A) Q=0 (B) W=0 (C) ΔU=0(D) ΔH=06. 当体系将热量传递给环境之后,体系的焓: ( )(A) 必定减少 (B) 必定增加 (C) 必定不变 (D) 不一定改变7. 一定量的理想气体从同一始态出发,分别经 (1) 等温压缩,(2) 绝热压缩到具有相同压力的终态,以H1,H2分别表示两个终态的焓值,则有:( )(A)H1> H2 (B)H1= H2 (C)H1< H2 (D)H1>=H28. 下列诸过程可应用公式 dU = (Cp- nR)dT进行计算的是:( )(A)实际气体等压可逆冷却 (C)理想气体绝热可逆膨胀(B)恒容搅拌某液体以升高温度 (D)量热弹中的燃烧过程9. 1mol单原子分子理想气体,从273 K,202.65 kPa, 经 pT=常数的可逆途径压缩到405.3 kPa 的终态,该气体的ΔU为: ( )(A)1702 J (B)-406.8 J (C)406.8 J (D)-1702 J10. 一定量的理想气体从同一初态分别经历等温可逆膨胀、绝热可逆膨胀到具有相同压力的终态,终态体积分别为V1,V2,则: ( )(A) V1> V2 (B)V1< V2 (C) V1= V2 (D) 无法确定11. 一容器的容积为V1=162.4 立方米,内有压力为94430 Pa,温度为288.65 K的空气。
当把容器加热至Tx时,从容器中逸出气体在压力为92834 Pa,温度为289.15K下,占体积114.3 m3;则Tx 的值为:()(A)1038.15 K (B)948.15 K (C)849.15 K (D)840.15 K12. 石墨的燃烧热: ( )(A) 等于CO生成热 (B) 等于CO2生成热(C) 等于金刚石燃烧热 (D) 等于零13. 298 K时,石墨的标准摩尔生成焓ΔfH : ( )(A) 大于零 (B) 小于零 (C) 等于零 (D) 不能确定14. 人在室内休息时,大约每天要吃 0.2 kg 的酐酪(摄取的能量约为 4000 kJ)。
假定这些能量全部不储存在体内,为了维持体温不变,这些能量全部变为热使汗水蒸发。
已知水的汽化热为 44 kJ/mol,则每天需喝水: ( )(A) 0.5 kg (B) 1.0 kg (C) 1.6 kg (D) 3.0 kg15. 高温下臭氧的摩尔等压热容C(p,m) 为: ( )(A) 6R (B) 6.5R (C) 7R (D) 7.5R16. 从统计热力学的观点看,对理想气体封闭体系在Wf =0、体积不变的情况下吸热时体系中粒子:( )(A) 能级提高,且各能级上的粒子分布数发生变化(B) 能级提高,但各能级上的粒子分布数不变(C) 能级不变,但能级上的粒子分布数发生变化(D) 能级不变,且各能级上的粒子分布数不变17. 若以B代表化学反应中任一组分,和 n(B)分别表示任一组分 B 在ξ= 0 及反应进度为ξ时的物质的量,则定义反应进度为: ( )(A)ξ=n(B,0) - n(B) (C)ξ=[n(B)-n(B,0)]/ν(B)(B)ξ= n(B)-n(B,0) (D)ξ=[n(B,0)-n(B)]/ν(B)18. 已知:Zn(s)+(1/2)O2 —> ZnO,ΔcHm=351.5 kJ/molHg(l)+(1/2)O2 ---> HgO,ΔcHm= 90.8 kJ/mol因此 Zn+HgO ---> ZnO+Hg 的ΔrHm是: ( )(A) 442.2 kJ/mol (B) 260.7 kJ/mol(C) -62.3 kJ/mol (D) -442.2 kJ/mol19. 下述说法正确的是: ( )(A) 水的生成热即是氧气的燃烧热 (B) 水蒸气的生成热即是氧气的燃烧热(C) 水的生成热即是氢气的燃烧热 (D) 水蒸气的生成热即是氢气的燃烧热20. 完全燃烧 8 dm3乙炔,需空气的体积为: ( )(A) 20 dm3 (B) 120 dm3 (C) 100 dm3 (D) 4 dm3第二章热力学第二定律物化试卷(一)1.理想气体绝热向真空膨胀,则:( )(A) ΔS = 0 , W = 0 (B) ΔH = 0,ΔU = 0(C) ΔG = 0,ΔH = 0(D) ΔU = 0,ΔG =02.熵变ΔS是: (1) 不可逆过程热温商之和 (2) 可逆过程热温商之和 (3) 与过程无关的状态函数 (4) 与过程有关的状态函数以上说法正确的是:( )(A) 1,2 (B) 2,3 (C) 2 (D) 43.理想气体经可逆与不可逆两种绝热过程:( )(A) 可以从同一始态出发达到同一终态(B) 从同一始态出发,不可能达到同一终态(C) 不能断定 (A)、(B) 中哪一种正确(D) 可以达到同一终态,视绝热膨胀还是绝热压缩而定4.在标准压力,273.15 K下水凝结为冰,判断体系的下列热力学量中何者一定为零?( ) (A) ΔU(B) ΔH(C) ΔS(D) ΔG5. 水在 100℃,标准压力下沸腾时,下列各量何者增加?( )(A) 熵 (B) 汽化热 (C) 吉布斯自由能 (D) 蒸气压6. 在 N2和 O2混合气体的绝热可逆压缩过程中,体系的热力学函数变化值在下列结论中正确的是:( )(A)ΔU=0 (B)ΔF=0 (C)ΔS=0 (D)ΔG=07. 在 270 K,101.325 kPa 下,1 mol 过冷水经等温等压过程凝结为同样条件下的冰,则体系及环境的熵变应为:( )(A) ΔS(体系)< 0 , ΔS(环境)< 0 (B) ΔS(体系)< 0 , ΔS(环境)> 0(C) ΔS(体系)> 0 , ΔS(环境)< 0 (D) ΔS(体系)> 0 , ΔS(环境)> 08. 理想气体在等温条件下,经恒外压压缩至稳定, 此变化中的体系熵变ΔS(体)及环境熵变ΔS(环)应为:( )(A)ΔS(体)>0,ΔS (环)<0 (B)ΔS(体)<0,ΔS(环)>0(C)ΔS(体)>0,ΔS(环)=0 (D)ΔS(体)<0,ΔS(环)=09.一个由气相变为凝聚相的化学反应,在恒温恒容下自发进行,问下列各组答案中,哪一个是正确的?( )(A)ΔS(体)>0,ΔS(环)<0 (B)ΔS(体)<0,ΔS(环)>0(C)ΔS(体)<0,ΔS(环)=0 (D)ΔS(体)>0,ΔS(环)=010. 在一简单的(单组分,单相,各向同性)封闭体系中,恒压只做膨胀功的条件下,吉布斯自由能值随温度升高如何变化? ( )(A)p T G )/(∂∂ > 0 (B) p T G )/(∂∂ < 0 (C) p T G )/(∂∂ = 0 (D) 视具体体系而定11. 某气体的状态方程为pV(m)= RT +αp ,其中α为大于零的常数,该气体经恒温膨胀,其热力学能:( )(A) 不变 (B) 增大 (C) 减少 (D) 不能确定12. 下列四个关系式中,哪一个不是麦克斯韦关系式? ( )(A)p s V T V T )/()/(∂∂=∂∂ (B)p s V T V T )/()/(∂∂=∂∂ (C)V T V T V T )/()/(∂∂=∂∂ (D)pT V T V T )/()/(∂∂-=∂∂ 13. 下列各式中哪个是化学势? ( )(A) (?T H/?T n(B))T,S, (B) (?T F/?T n(B))T,p,(C) (?T G/?T n(B))T,V, (D) (?T U/?T n(B))S,V,14. 298 K,标准压力下,有两瓶萘的苯溶液,第一瓶为 2 dm3(溶有 0.5 mol 萘),第二瓶为 1 dm3(溶有 0.25 mol 萘),若以μ1,μ2分别表示两瓶中萘的化学势,则: ( )(A)μ1 = 10μ2 (B)μ2= 2μ2(c)μ1 =μ2 (D)μ1= 0.5μ215.重结晶制取纯盐的过程中,析出的 NaCl 固体的化学势与母液中 NaCl 的化学势比较,高低如何? ( )(A) 高 (B) 低 (C) 相等 (D) 不可比较16.热力学第三定律可以表示为: ( )(A) 在0 K时,任何晶体的熵等于零 (B) 在0 K时,任何完整晶体的熵等于零(C) 在0 ℃时,任何晶体的熵等于零 (D) 在0 ℃时,任何完整晶体的熵等于零17.下列四种表述:(1) 等温等压下的可逆相变过程中,体系的熵变ΔS =ΔH相变/T相变(2) 体系经历一自发过程总有ΔS > 0(3) 自发过程的方向就是混乱度增加的方向(4) 在绝热可逆过程中,体系的熵变为零两者都不正确者为: ( )(A) 1,2 (B) 3,4 (C) 2,3 (D) 1,418.在绝热条件下,用大于气筒内的压力迅速推动活塞压缩气体,此过程的熵变为: ( ) (A) 大于零 (B) 等于零 (C) 小于零 (D) 不能确定19.在263 K的过冷水凝结成263 K的冰,则: ( )(A) ΔS<0(B) ΔS>0(C) ΔS=0 (D) 无法确定20.在标准压力和268.15 K下,冰变为水,体系的熵变ΔS体应: ( )(A)大于零 (B)小于零 (C)等于零 (D)无法确定第二章热力学第二定律物化试卷(二)1. 2 mol H2和 2 mol Cl2在绝热钢筒内反应生成 HCl 气体,起始时为常温常压。
