氧气,二氧化碳和空气的密度
0.7mpa空气密度

0.7mpa空气密度0.7mpa(兆帕)下的空气密度计算涉及到多个因素,包括温度、压力、气体成分等。
以下是一些详细信息:1.首先,我们需要知道空气的组成成分。
一般来说,空气主要由氮气(N2)、氧气(O2)、氩气(Ar)、二氧化碳(CO2)和水蒸气(H2O)等组成。
其中,氮气和氧气的体积分数最大,所以它们对空气密度的贡献也最大。
2.其次,我们需要考虑温度的影响。
在一定的压力下,气体的密度会随着温度的变化而变化。
这主要是因为温度会影响气体分子的平均速度和分布。
在较高的温度下,气体分子的平均速度会增加,导致气体分子的活动范围更广,从而使得气体的密度减小。
反之,在较低的温度下,气体分子的平均速度会减小,导致气体分子的活动范围缩小,使得气体的密度增加。
3.另外,我们还需要考虑气体成分的影响。
不同气体的分子量和分子体积不同,因此它们对气体密度的贡献也不同。
例如,二氧化碳的分子量比氮气和氧气大,所以它的密度比氮气和氧气大。
而水蒸气的分子量比氮气和氧气小,所以它的密度比氮气和氧气小。
根据以上信息,我们可以得出以下结论:在0.7mpa的压力下,空气的密度会受到温度、气体成分等多种因素的影响。
为了获得准确的空气密度值,我们需要知道这些参数的具体数值。
一般来说,在标准大气条件下(温度为25℃,压力为101325pa),干燥空气的密度约为1.29kg/m³。
但是,在0.7mpa的压力下,干燥空气的密度可能会略有不同。
如果需要更精确的数值,可以通过实验方法获得。
最后,需要注意的是,空气密度对于很多工程应用都非常重要。
例如,在气体压缩机的设计和操作中,需要知道不同压力下的空气密度值。
此外,空气密度也是计算空气动力学性能和能量转换效率的重要参数之一。
因此,了解如何计算和测量空气密度对于这些应用非常重要。
空气比重的单位

空气比重的单位1. 简介空气比重是指空气相对于某种参考物质的密度比值。
它是衡量空气中各种气体成分相对含量的重要指标。
空气比重的单位是国际单位制中的千克每立方米(kg/m³)。
2. 空气的组成空气主要由氮气(N₂)、氧气(O₂)、水蒸气(H₂O)、二氧化碳(CO₂)等气体组成。
其中,氮气占空气体积的约78%,氧气占约21%,其他气体占约1%。
3. 空气比重的计算方法空气比重的计算方法是将空气的密度与参考物质的密度进行比较。
空气的密度可以通过测量空气的质量和体积来确定,而参考物质的密度通常是已知的。
根据定义,空气比重可以用以下公式表示:空气比重 = 空气的密度 / 参考物质的密度4. 空气比重的影响因素空气比重受到多种因素的影响,包括温度、压力和湿度等。
下面分别介绍这些因素对空气比重的影响:4.1 温度温度对空气比重的影响很大。
在相同压力和湿度条件下,温度升高会导致空气密度减小,从而使空气比重减小;反之,温度降低会导致空气密度增大,空气比重增大。
4.2 压力压力对空气比重的影响也很显著。
在相同温度和湿度条件下,压力增大会使空气密度增大,空气比重增大;反之,压力减小会导致空气密度减小,空气比重减小。
4.3 湿度湿度对空气比重的影响相对较小。
在相同温度和压力条件下,湿度增加会导致空气中水蒸气的含量增加,从而使空气密度减小,空气比重减小;反之,湿度减小会导致空气密度增大,空气比重增大。
5. 空气比重的应用空气比重在工程和科学研究中有着广泛的应用。
以下是一些常见的应用领域:5.1 空气污染控制空气比重可以用于评估和监测大气中的污染物浓度。
不同污染物的比重不同,通过测量空气比重可以判断污染物的分布和浓度情况,从而采取相应的控制措施。
5.2 气象预测气象学中常用空气比重来预测天气变化。
通过测量和分析空气比重的变化,可以判断气压系统的演变和气象现象的发生,从而提前预测天气变化,为人们的生活和工作提供便利。
氧气的性质量

NH4HCO3 H2SO4
CO2 Fe3O4 P2O5 H2O
氧化物: 由两种元 素组成, 其中一种 元素是氧 元素的化 合物。
从“化学视角”认识身边的氧气——畅谈收获
知识
方法
无色无味的气体
观察法
物 理
资料链接:通过实验测得,20℃时,气体压
不易溶于水
强为1.013×105Pa时,一升水可以溶解气体 的体积是:氨气为702L,氢气为0.01819L,
缜密的实验设计 巧妙的实验改进 规范的实验操作
从“化学视角”认识身边的氧气——铁丝燃烧
民间绝活“打树花”
至今已有500余年历史 河北省非物质文化遗产
铁匠从打铁时四溅的火花 中得到灵感 勇敢者的游戏
从“化学视角”认识身边的氧气——铁丝燃烧
二、氧气的化学性质
氧气还可以与许多金属单质反应:比如钠、镁、铜等 镁 条 在 空 气 中 燃 烧
从“化学视角”认识身边的氧气——我来总结 二、氧气的化学性质
氧气
非金属单质
金属单质
化合物
获得结论:氧气的化学性质
A但这非通是常常为活情什泼么况√呢下B?,比有较些活物泼质却C比能较和稳氧定气“和D平非共常处稳”定,
从“化学视角”认识身边的氧气——我能发现
从氧反化应反这物应些来和反看化应,合属这反于三应哪个之种反间反应是应有什类什么型么样?共的同关点系?呢?
二、氧气的化学性质
实验前
在空气中点燃
木炭为黑色
在氧气中点燃
实验中 发红发热
发出白光,放出热量
实验后
产生的气体能 使澄清的石灰 水变浑浊
文字表达式:
碳 + 氧气 点燃
C O2
二氧化碳
氩气、二氧化碳、氧气、丙烷安全周知卡(危化品)
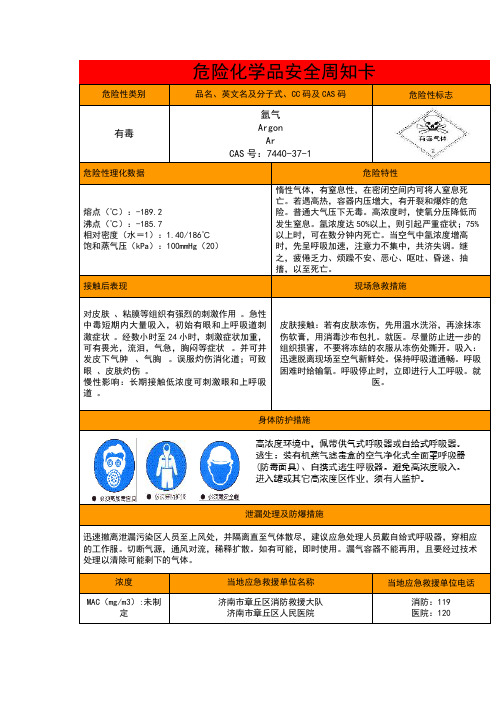
危险性类别品名、英文名及分子式、CC码及CAS码危险性标志有毒氩气ArgonArCAS号:7440-37-1危险性理化数据危险特性熔点(℃):-189.2沸点(℃):-185.7相对密度(水=1):1.40/186℃饱和蒸气压(kPa):100mmHg(20)惰性气体,有窒息性,在密闭空间内可将人窒息死亡。
若遇高热,容器内压增大,有开裂和爆炸的危险。
普通大气压下无毒。
高浓度时,使氧分压降低而发生窒息。
氩浓度达50%以上,则引起严重症状;75%以上时,可在数分钟内死亡。
当空气中氩浓度增高时,先呈呼吸加速,注意力不集中,共济失调。
继之,疲倦乏力、烦躁不安、恶心、呕吐、昏迷、抽搐,以至死亡。
接触后表现现场急救措施对皮肤、粘膜等组织有强烈的刺激作用。
急性中毒短期内大量吸入,初始有眼和上呼吸道刺激症状。
经数小时至24小时,刺激症状加重,可有畏光,流泪,气急,胸闷等症状。
并可并发皮下气肿、气胸。
误服灼伤消化道;可致眼、皮肤灼伤。
慢性影响:长期接触低浓度可刺激眼和上呼吸道。
皮肤接触:若有皮肤冻伤,先用温水洗浴,再涂抹冻伤软膏,用消毒沙布包扎。
就医。
尽量防止进一步的组织损害,不要将冻结的衣服从冻伤处撕开。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
呼吸困难时给输氧。
呼吸停止时,立即进行人工呼吸。
就医。
身体防护措施泄漏处理及防爆措施迅速撤离泄漏污染区人员至上风处,并隔离直至气体散尽,建议应急处理人员戴自给式呼吸器,穿相应的工作服。
切断气源,通风对流,稀释扩散。
如有可能,即时使用。
漏气容器不能再用,且要经过技术处理以清除可能剩下的气体。
浓度当地应急救援单位名称当地应急救援单位电话MAC(mg/m3):未制定济南市章丘区消防救援大队济南市章丘区人民医院消防:119医院:120危险性类别品名、英文名及分子式、CC码及CAS码危险性标志不燃窒息性二氧化碳carbon dioxideCO2CAS号:124-38-9危险性理化数据危险特性熔点(℃):-56.6沸点(℃):-78.5相对密度(空气=1):1.53饱和蒸气压(kPa):1013.25(-39℃) 若遇高热,容器内压增大,有开裂和爆炸的危险。
人教版2023初中化学九年级化学上册第二单元我们周围的空气考点总结

人教版2023初中化学九年级化学上册第二单元我们周围的空气考点总结单选题1、空气是一种宝贵的自然资源。
下列有关空气中各成分的说法错误的是A.液氮可用作制冷剂B.稀有气体可用于制造多种用途的电光源C.CO2属于空气污染物D.空气中的O2主要来源于植物的光合作用答案:CA、液氮汽化吸收热量,可用作制冷剂,故选项正确;B、稀有气体通电后发出不同颜色的光,可制造多种用途的电光源,故选项正确;C、二氧化碳本身没有毒性,不属于空气污染物,故选项错误;D、空气中的氧气主要来源于植物的光合作用,故选项正确;故选:C。
2、化学与生活息息相关。
下列生活中常见的物质属于纯净物的是A.矿泉水B.河水C.苏打水D.蒸馏水答案:D分析:根据纯净物由同种物质组成进行分析。
A、矿泉水中含有矿物质和水等,属于混合物,不符合题意;B、河水中含有泥沙、水等多种物质,属于混合物,不符合题意;C、苏打水中含有碳酸钠和水等多种物质,属于混合物,不符合题意;D、蒸馏水是净化程度最高的水,属于纯净物,符合题意。
故选D。
3、实验室用氯酸钾固体(二氧化锰作催化剂)制取氧气,下列装置组合正确的是A.①③B.①⑤C.②③D.②④答案:A实验室用氯酸钾固体(二氧化锰作催化剂)制取氧气,属于固体混合需加热型,发生装置是①,氧气密度比空气大、不易溶于水,可用向上排空法(装置④)或排水法(装置③)收集,故装置组合正确的是①③或①④,观察选项,只有A选项正确。
故选:A。
4、以下是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是A.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②B.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管a进入D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放答案:BA. 装置②是固液常温反应制取气体的装置,实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②,正确;B. 氧气和二氧化碳的密度都比空气的密度大,均可使用装置③,气体从导管a进入占据下方空间,空气则被赶到上方空间而从b排出,错误;C. 浓硫酸具有吸水性,能干燥不与其反应的气体,装置④是洗气装置,导气管是长进短出,实验室干燥氧气和二氧化碳均可使用装置④,气体从导管a进入,正确;D. 氧气和二氧化碳的密度比空气的密度大,对于密度比空气大的气体,集气瓶正放,实验室收集的氧气和二氧化碳,均可如图⑤临时存放,正确。
氧气理化性质表

相对密度(空气=1): 1.43
临界温度(℃): -118.4
燃烧热(kJ/mol):无意义
临界压力(MPa):5.08
辛醇/水分配系数:无资料
溶解性:微溶于水和乙醇燃Leabharlann 爆炸危险性危险类别:第2.2类
有害燃烧产物:无
爆炸极限(体积分数%):无意义
稳定性:稳定。
引燃温度(℃):无意义
包装类别:053
禁忌物:易燃或可燃物、活性金属粉末、乙炔。
危险特性:是易燃物、可燃物燃烧爆炸的基本要素之一,能氧化大多数活性物质。与易燃物(如乙炔、甲烷等)形成有爆炸性的混合物。
燃爆危险:本品助燃。
灭火方法:用水保持容器冷却,以防受热爆炸,急剧助长火势。迅速切断气源,用水喷淋保护切断气源的人员,然后根据着火原因选择适当灭火剂灭火。
氧气理化性质表
标识
中文名:氧气
英文名:liquid oxygen
分子式:O2
CAS号:7782-44-7
危规编号:22002
UN号:1073
理化性质
外观及性态:天蓝色透明而易流动的液体。
熔点(℃): -218.8
闪点(℃):无意义
沸点(℃): -183.1
相对密度(水=1 ): 1.14(-183℃)
灭火剂:水、二氧化碳、砂土。
毒性
最高允许浓度:中国MAC(mg/m3):未制定标准
健康危害
常压下,当氧的浓度超过40%时,有可能发生氧中毒。吸入40%~60%的氧时,出现胸骨后不适感、轻咳,进而胸闷,胸骨后烧灼感和呼吸困难,咳嗽加剧;严重时可发生肺水肿、窒息。吸入的氧浓度在80%以上时,出现面部肌肉抽动、面色苍白、眩晕、心动过速、虚脱,继而全身强直性抽搐、昏迷、呼吸衰竭而死亡。长期处于氧分压为60~100kpa(相当于吸入氧浓度40%左右)的条件下可发生眼损害,严重者可失明。
二氧化碳物理性质

-56.6
-60
-65
-70
1512
1522
1535
1546
-75
-80
-85
-90
1557
1566
1575
1782
表8二氧化碳的粘度(0.101325MPa,u×106)[4]
温度℃
粘度Pa·s
温度℃
粘度Pa·s
-100
-75
-50
-25
0
20
25
8.86
10.07
11.26
12.47
13.67
14.63
通用气体常数(R),MPa·m3/(kmol·K)
1330.5
0.35~0.51
22.26
-394.6
0.008314
二、物理性质、热力学性质
(一)特性参数[1-3]见表2
表2
性质பைடு நூலகம்
数值
性质
数值
熔点,℃
沸点,℃
相对密度(空气=1)
比容,m3/kg
绝热系数(K)
-56.6(527Kpa)
-78.5(升华)
22.3
23.4
24.6
27.6
27.7
区别氧气和二氧化碳的方法

区别氧气和二氧化碳的方法
1. 化学式:氧气的化学式为O2,而二氧化碳的化学式为CO2,从化学式上可以区分两者。
2. 气味:氧气是无色、无味的气体,而二氧化碳具有刺鼻的气味,通常被描述为与苏打水相似的气味。
3. 反应性:氧气是一种氧化剂,它能助燃;而二氧化碳则是一种灭火剂,它会扼杀火焰。
4. 密度:氧气比空气轻,而二氧化碳比空气重,因此可以通过密度的不同来区分两者。
5. 用途:氧气是支撑生命的气体,也被用于医疗、工业等领域;而二氧化碳则主要用于工业中去除金属表面氧化物、用于制造干冰等。
