药品菌落控制基本原理 PPT课件
放线菌ppt课件
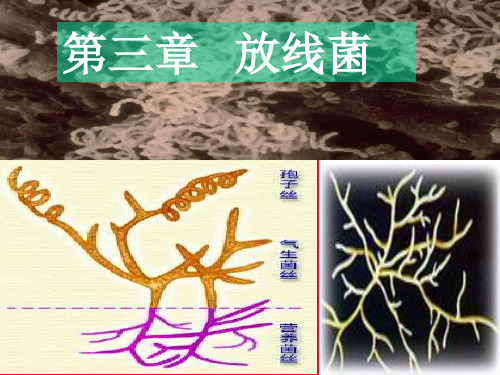
原核细胞型微生物 细胞壁的主要成分是肽聚糖 呈分枝状
最适生长PH相近,一般呈微碱性
对抗生素的敏感性与细菌相同
完整编辑ppt
5
孢子丝 气生菌丝
培养基表面 基内菌丝
完整编辑ppt
6
一、放线菌的形态结构
菌丝 组成:
孢子
完整编辑ppt
7
气生菌丝
分生孢子 孢子丝
固体基质 基内菌丝
放线菌的形态结构(模式图)
完整编辑ppt
42
病灶组织和瘘管的脓汁中,肉眼可见硫磺样颗粒 硫磺样颗粒压片,在镜下可见放射状排列的菌丝, 形似菊花状
硫磺样颗粒的镜下形态
完整编辑ppt
43
二、致病性
完整编辑ppt
44
放线菌正常寄居在口腔、上呼吸道、胃 肠道和泌尿生殖道,为人体的正常菌群。当 机体抵抗力下降,口腔卫生不良、拔牙或口 腔粘膜受损时,可致内源性感染,引起放线 菌病。
35
4、 链孢囊菌属(Streptosporangium)
最显著特点: 能形成孢子囊和孢囊孢子或形成螺旋孢子丝
可产生广谱抗生素
粉红链孢囊菌
多霉素
抑制革兰氏阳性细菌、阴性细菌、 病毒甚至肿瘤
绿色链孢囊菌 绿菌素 抑制细菌、霉菌、酵母菌
完整编辑ppt
36
5、游动放线菌属(Actinoplanes)
形态: 营养菌丝 没有或极少气生菌丝体 隔膜有或无 以孢子囊孢子繁殖,孢囊形成于营养菌丝体上或孢囊梗上
A.气生菌丝
B.基内菌丝
C.螺旋孢子丝
D.轮生孢子丝
E.孢子梗
完整编辑ppt
51
5.最适宜放线菌生长的温度为 ()
A.28-32℃ B.22-28℃ C.30-35℃ D.32-37℃ E.40℃
真菌培养ppt 课件

02 真菌培养的基本原理
真菌的营养需求
01
02
03
04
碳源
真菌通过摄取碳源获取能量, 常见的碳源包括葡萄糖、蔗糖
、麦芽糖等。
氮源
真菌需要氮源合成蛋白质和核 酸,常见的氮源包括氨基酸、
尿素、硝酸盐等。
无机盐
无机盐对真菌的生长至关重要 ,如镁、磷、硫等元素。
维生素和生长因子
某些维生素和生长因子是真菌 生长所必需的,如生物素、泛
详细描述
将真菌接种在含有碳源、氮源和其他 必要营养物质的液体培养基中,通过 控制温度、pH和通气量等条件,使真 菌进行代谢产生有用产物。
04 真菌培养的过程和步骤
菌种选择与保存
菌种选择
选择具有代表性的真菌种类,考 虑其经济价值、生态意义和研究 价值。
菌种保存
采用低温、干燥、真空等手段, 以及定期更换培养基等方法,确 保菌种不发生变异和死亡。
详细描述
将真菌接种在固体培养基表面,通过控制温度、湿度和气体环境等 条件,使真菌在固体培养基上生长繁殖。
特点
操作简单,成本低,适用于一般实验室和工业生产。
液体培养法
总结词
在液体培养基中悬浮生长 的方法
详细描述
将真菌接种在液体培养基 中,通过搅拌或振荡使真 菌在液体培养基中悬浮生 长。
特点
生长速度快,可实现大规 模生产,但设备要求较高 。
和培养基。
实验后需彻底清洗双手和实验 器具,确保无菌操作。
对于有毒或具有强烈气味的真 菌,应在通风橱中进行操作, 并佩戴化学防护眼镜和化学防
护服。
实验废弃物处理
01
废弃的培养基和真菌样品需进行 灭菌处理,确保无菌后才能丢弃 。
临床微生物室质量控制讲解课件

抗生素敏感性试验的质控菌株
细菌名称 金黄色葡萄球菌 金黄色葡萄球菌 大肠杆菌 绿脓假单胞菌 粪肠球菌 淋病奈瑟菌 流感嗜血杆菌 肺炎克雷伯菌
菌号
用途
ATCC 25923 纸片扩散质控
ATCC 29213 MIC测定质控
ATCC 25922 纸片和MIC
ATCC 27853 纸片和MIC
内容提要
• 目的 • 涉及内容
室内质控 室间质评 • 建立方法及步骤(室内质控) • 纠控方法 • 范例 • 注意事项
细菌室质控工作目的及重要性
• 保证临床细菌检验技术更好地发挥 • 服务于临床 • 耐药监测
小结:临床细菌室(实验室〕的质量控制和方法 标准化是一对相互制约的矛盾,实验室只有建 立标准化方法学才可能进行质量控制才能获得 好的结果。而连续地质量控制可维护方法学的稳 定性和正确性,随时发现问题,解决问题。
纠控
仪器 • 硬件设备的维护与检修 • 软件程序的更新升级
注意事项
• 临时改变方法学,必须有文字记录, 并通知临床各科
谢谢
鉴定标准 生长 生长,蓝色菌落 生长,无色菌落 生长,无色菌落 生长,无色菌落 生长被抑制 部分被抑制 生长 生长,产气 生长 部分或完全抑制
培养基的质量控制
例: • 血琼脂:哥伦比亚琼脂或胰大豆胨琼脂、5%
羊血、软琼脂或加适量抑制剂有利于肺炎链球 菌生长 • 巧克力琼脂:脑心浸液、5%兔血、5mg/100ml 去(操作程序) • 标本的采集、运输 • 培养鉴定培养基的选择 • 鉴定方法流程(包括涂片染色) • 培养条件 • 仪器法的注意事项
纠控
药物敏感性试验从以下几个方面进行: • 培养基的制备(配方、厚度) • 抗生素的选择(效期、剂量) • 接种及贴纸片的过程 • 培养条件 • 判读
梯度稀释涂平板制单菌落ppt课件

数据处理
涂布平板及培养
CFU概 念13
5
-8
-8
-8
-8
-7
-7
-7
-7
-6
-6
-6
-6
-5
-5
-5
-5
6
-8
-8
-8
-8
-7
-7
-7
-7
倒-置6 培养-6 -6经常-观6
察
-5
-5
-5
-5
7
M01=1-08×( -8
-8
)
M02=10-7×( -7
-7
-6M03=10×-6(
-6
-M5 04=10×(-5
-5
-8
×
-7
-6
-5
8
M02=10×M(03=10×(
M04=10×(
M0=(M02+M03+M04)÷3 =(1.5+1.0+1.1)
÷3×108 =1.2×108
10 接入平板的菌液是0.1ml, 对应的浓度就要乘以10
9
M0=(M02+M03+M04)÷3
=(1.5+1.0+1.1)
÷3×108
(
=1.2×108(C单F位U?/m)l
-1 -2 -3 -4 -5 -6 -7 -8
M0 M0 M0 M0 M0 M0 M0 M0
无菌 水
4
菌液接入平板
-8765
-8765
-8765
-8765
初始菌
液 菌液浓
度=M0
10 10 10 10 10 10 10 10
-1 -2 -3 -4 -5 -6 -7 -8
食品微生物实验ppt课件.ppt

紫外线灭菌法: 一般30W灯管,9m3空间,距地面2m每次打开紫外线 照射0.5h,就使室内空气灭菌。若照射紫外线时先喷 洒石炭酸等化学消毒剂,可增强灭菌效果。紫外线虽 有较强的杀菌力,但穿透力弱,即使一薄层玻璃或水 层就能将大部分紫外线滤除,因此只适用于空气及表 面杀菌。
化学药剂消毒灭菌: 微生物实验室中常用的化学杀菌剂有升汞、甲醛、高 锰酸钾、酒精、碘酒、龙胆紫、石炭酸、漂白粉、新 洁尔灭、煤酚皂溶液,它们有的是杀菌剂,有的是抑 菌剂。
实验器材
1. 药品和试剂 牛肉膏、蛋白胨、NaCl、 10% NaOH 溶液、10%盐酸溶液。
2. 器材 天平、药匙、瓷缸、玻璃棒、电炉、 PH试 纸、试管、三角瓶、分装漏斗、牛皮纸、棉 花、线绳、干燥箱、高压锅。
实验步骤
• 培养基的配制 • 分离培养微生物常用器皿的准备 • 培养基和玻璃器材的灭菌
在平板的表面(根霉点一点,曲霉、酵母可 点3-4点)。 2) 平板接斜面:一般是将经平板分散培养得到 的单菌落接种到斜面,以便作鉴定或扩大培 养、保存之用。
实验方法
平板划线
三点接种
实验方法
挑孢子: 将灭过菌的接种针在菌种管斜面上端冷却并湿润后,再
用针尖挑少量孢子。当移出接种针前,须将针柄在管口轻轻 碰几下,以抖落未粘牢的孢子。然后移出接种针,塞上棉塞, 将菌种管插回试管。 点接:
实验方法
培养基的制备过程 配方及配量---称取药品----加热溶解----调 节pH ----过滤----分装----加棉塞----包扎---
-灭菌----搁斜面----贮存
1. 称量 按照培养基配方与配量分别称取各药品。
取少量的水于烧杯中,将各培养基成分(琼脂 除外)逐一加入水中待溶。
药物制剂的微生物学检查ppt课件

❖ 1、油剂性药物的检测 ❖ 油剂性药物因难于和培养基充分混合,往往影
响检出结果。如果加入吐温-80,与油剂性药物混 合乳化,再用培养基稀释,可以使药品均匀分布在 培养基中。 ❖ 对照:吐温-80 。
资金是运动的价值,资金的价值是随 时间变 化而变 化的, 是时间 的函数 ,随时 间的推 移而增 值,其 增值的 这部分 资金就 是原有 资金的 时间价 值
资金是运动的价值,资金的价值是随 时间变 化而变 化的, 是时间 的函数 ,随时 间的推 移而增 值,其 增值的 这部分 资金就 是原有 资金的 时间价 值
❖ 检测时先把一定量药均经增菌后转种到选 择鉴别培养基——麦康凯平板或伊红美兰平 板(EMB平板)。
❖ 培养后挑取可疑菌落作革兰染色及生化反应。 生化反应包括 IMViC试验和乳糖发酵试验。 大肠杆菌IMViC试验结果为+、+、—、—
一般注射剂的无菌检查
❖ 直接接种法
资金是运动的价值,资金的价值是随 时间变 化而变 化的, 是时间 的函数 ,随时 间的推 移而增 值,其 增值的 这部分 资金就 是原有 资金的 时间价 值
❖ 需氧菌和厌氧菌的培养已全部采用硫乙醇酸 钠培养基检查。在同一培养基中,需氧菌在 培养基表面生长,而厌氧菌在培养基内生长。
资金是运动的价值,资金的价值是随 时间变 化而变 化的, 是时间 的函数 ,随时 间的推 移而增 值,其 增值的 这部分 资金就 是原有 资金的 时间价 值
❖ 如检测结果为革兰阴性杆菌,乳糖发酵 阳性及IMViC试验符合,则可判断每克 时间变 化而变 化的, 是时间 的函数 ,随时 间的推 移而增 值,其 增值的 这部分 资金就 是原有 资金的 时间价 值
❖ 一般选取菌落数在30-300之间的平板计数。
药物制剂的微生物污染与控制技术
药物制剂的微生物污染与控制技术药物制剂的微生物污染以及控制技术一直是制药行业关注的重点问题之一。
微生物污染可能会导致药物的质量下降、疗效不佳乃至严重的安全隐患。
因此,科学有效地控制药物制剂的微生物污染至关重要。
本文将从控制措施、检测方法和相关技术三个方面阐述药物制剂微生物污染及其控制技术。
一、控制措施1. 环境控制合理管理药物制剂生产环境是控制微生物污染的首要步骤。
保持无菌操作空间的洁净度和恰当的温湿度对控制微生物污染至关重要。
定期清洁和消毒工作台、无菌室和供气系统,使用合格的消毒剂,是有效控制环境微生物污染的基本措施。
2. 原辅材料控制药物制剂中的原辅材料可能是微生物污染的主要来源之一。
因此,药品生产企业应该对采购的原辅材料进行严格的质量控制,确保其符合相关的国家药典标准,确保药物的质量安全。
3. 人员培训与操作规范操作人员的素质和操作规范是控制微生物污染的关键。
通过合理的岗前培训和定期的职业技能培训,提高操作人员的专业素质和意识,降低人为错误带来的微生物污染风险。
二、检测方法1. 基本原理微生物的检测主要利用微生物生长特性,在特定培养基上培养目标微生物,并通过观察菌落形态和生长情况等进行判定。
常用的检测方法包括菌落计数法、刺激法、共济法等。
2. 检测设备为了提高微生物的检测准确性和效率,现代药品生产企业通常采用自动化微生物检测设备,如菌落计数仪、微生物培养仪等。
这些设备通过精确的测量和数据处理,能够大大提高微生物的检测效率和结果可靠性。
三、相关技术1. 无菌技术无菌技术是控制药物制剂微生物污染的核心技术之一。
通过合理的操作流程、严格的操作规范和无菌过滤装置等,可以有效地防止微生物的侵入和繁殖,保证药物制剂的无菌状态。
2. 消毒技术消毒技术是控制微生物污染的另一重要手段。
常用的消毒方法包括热湿热法、紫外线辐照法、化学消毒法等。
不同的消毒方法适用于不同的场合,经过科学合理的选择和使用,可有效地控制微生物的污染。
教学课件第一节食品中菌落总数的测定
一、菌落总数
是指食品检样经过处理,在一定条 件下培养后,所得1mL(g)或1cm2面积检 样中所含菌落的总数。
二、菌落总数测定的意义
1、判定食品被细菌污染的程度及卫生质量。 2、预测食品存用的期限长短。 3、了解细菌在食品中的繁殖动态。
三、菌落总数测定的方法
※ 平板倾注法# 平板表面涂布法 平板表面点滴法
或中心深紫色,圆形,稍凸起,边缘整齐,表面光 滑,常有金属光泽; 在麦康凯琼脂上的典型菌落:呈桃红色或中心桃红、 圆形,扁平,光滑湿润。
EMB平板照片及原理
麦康凯琼脂平板 Age of culture is 24 h
大肠杆菌、大肠菌群选择性显色培养基--COLI ID 用于在37℃下对食品中大肠菌群和大肠杆菌进行检测、计数及大肠杆菌的鉴定
湿润纸片后,立即贴于食具内侧表面,30秒后取 下,置于原塑料袋内。筷子以5只为一份样品,用 吸管吸取生理盐水湿润纸片后,立即将筷子进口 端(约5cm)抹拭两张,放入原塑料袋内。
2.将已采样的纸样置于37°C培养15小时.
纸片在黄色背景上出现红色斑点为阳性,纸片在紫 兰色背景上呈现红色斑点,但周围没有黄晕均为 大肠菌群阴性。同一份样品两张纸片均是阴性为 合格。
MPN 个/100 g/ml
0
0
0
<30
0
0
1
30
0
0
2
60
0
0
3
90
0
1
0
30
0
1
1
60
0
1
2
90
0
1
3
120
0
2
0
60
0
项目5微生物生长现象及常见控制菌的生长特征ppt(精)
6.2 阳性对照试验的操作环境
阳性对照试验是检查供试品是否有抑菌作 用及培养条件是否适宜。阳性对照菌液的 制备、计数及加入含供试品的培养基中等 操作,不能在检测供试品的无菌室或净化 台上进行,必须在单独的隔离间或净化台 操作,以免污染供试品及操作环境
6.3 关于复验
在各类供试品中检测大肠杆菌及其他控 制菌,按一次检出结果为准,不再抽样 复验。检出的大肠杆菌及其他控制菌培 养物须保留1个月,备查
1.1 药物对沙门菌的影响
此外,由于药品在生产过程中,常受到加热、 干燥等加工步骤的影响,药品中污染的沙门菌 可受到损伤或呈休眠状态,故须在增菌培养前 先进行预增菌。然后再进行增菌及分离、三糖 铁琼脂初步鉴别、生化试验、血清学试验等步 骤。其他控制菌也可能存在相同状况
2 对照用菌液
乙型副伤寒沙门菌〔CMCC(B)50094〕的营养琼 脂 斜面培养物少许,接种至5ml营养肉汤培养基内 。36±1℃培养18~24h后,用0.9%无菌氯化钠 溶液释至1:106,浓度相当于50-100个 cfu/0.1ml
5 结果判断-不能直接得出结论
5.4 当阴性对照有菌生长或阳性对照未生长 或生长菌落不是大肠杆菌,不能作出检验报 告。
试验操作应当严格按照相关要求进行
6.1 IMViC试验的顺序
以灭菌接种针沾取菌苔,首先接种于枸橼酸盐 琼脂斜面上,然后接种于蛋白胨水培养基、磷 酸盐葡萄糖胨水培养基中。切勿将培养基带入 枸橼酸盐琼脂斜面上,以免产生假阳性结果
除大肠埃希菌外,尚有部分志贺菌属、沙门 菌属的菌株;以及少数革兰阳性球菌、杆菌 和芽孢菌,其MUG为阳性 在MUG培养基成分中增加了去氧胆酸钠,可排 除革兰阳性菌的干扰 志贺菌、沙门菌在胆盐乳糖培养基中较难生 长,即使有生长,本法能检出。并且既然药 品中不得检出大肠杆菌,更不允许检出志贺
菌种的传代、保藏及菌液ppt课件
菌种保藏标签的规范与要求
菌种保藏标签必须规范、清晰,所有保藏 的菌种容器表面均应贴有相应的标签,标 签必须字迹清晰可见,应注明:菌种的名 称,系列号,传代次数,接种时间等。一 旦新一代菌种制备成功,上一代菌种务必 处理掉处理过程应记录。
2019
-
10
严格菌种的质量控制,确保菌种的质量 菌种的质量对检验至关重要,对实验式储 备的菌种而言,除了在起始阶段要对菌种 进行纯度和属性确认外,还应对每一次传 代都进行确认的质量控制系统。因为微生 物菌种从上一代传到下一代时,很可能发 生污染或变异,因此每次传代中至少要对 菌种进行形态学观察和革蓝染色检查,必 要时应做菌种鉴定试验,所有被确认受到 污染的菌种应及时销毁,不得用于常规实 2019 验。
和培养条件、保藏方法、储存条件及保存 库址等。 2019 -
12
3.在操作过程中,必须严格遵守实验室安 全防护措施规程,采取有效预防措施进行 自我保护。 4.为了防止菌种污染或将污染传播到别处, 其他部门的人员未经允许不得进微生物实 验室。所有的意外情况,都必须立即向主 管部门报告以便得到及时解决。 5相关记录 在菌种的使用制备与保藏过程 中,应建立菌种制备、保藏和使用的记录 格式。
2019 7
严格控制菌种的传代
避免频繁购买菌种及复壮等费时、耗力的工作。 1.复溶菌种并转种 按菌种说明书要求复溶所转 菌种并转接于适当的增菌培养基内(为第一代) 2.鉴定菌种后制甘油冷冻管 经菌种特性鉴定后, 挑取纯菌落制成浓菌悬液用于制备甘油冷冻管 , 保存管(为第二代)同时挑取纯菌落接斜面,工 作用菌种(为第三代) 3.将第二代保存,第三代以适当温度培养后用于 试验
分离培养:伊红美兰培养基(EMB平板)
