核磁共振1H化学位移图表
核磁共振氢谱(化学位移)(共17张PPT)

不同质子的化学位移
不同质子的化学位移
LOGO
•TMS化学性质不活泼,与样品之间不发生化学反响和分子间缔合;
•TMS是一个对称结构,四个甲基的化学环境完全相同,不管在氢谱还 是碳谱都只产生一个吸收峰; •Si的电负性小(1.9),TMS中氢核与碳核周围的电子云密度高,屏蔽效应大, 产生NMR信号所需的磁场强度比一般有机物中的氢核和碳核产生NMR信号 所需的磁场强度大得多,处于较高场,与绝大局部样品信号不发生重叠和干 扰;
不同质子的化学位移
核外电子的影响,屏蔽效应,化学位移 核磁共振氢谱(1H-NMR) ——化学位移(chemical shifts) 测定和计算方法——标准物质(通常用TMS,即四甲基硅)对照法: 四甲基硅(TMS)作为标准物质的优点: 核外电子的影响,屏蔽效应,化学位移 Produced by Jiwu Wen 核外电子的影响,屏蔽效应,化学位移 由于屏蔽效应不同导致化学环境不同的原子核共振频率不同,因而在不同的位置上出现吸收峰,这种现象称为化学位移。 TMS沸点低(27℃),容易去除,有利于回收样品。 诱导效应:吸电子诱导效应降低原子核周围的电子云密度,化学位移向低场移动, 增大。 氢键:分子形成氢键后,氢核周围的电子云密度降低,产生去屏蔽作用,化学位移向低场移动, 增大。 (3)叁键的磁各向异性效应 核磁共振条件及面临的问题 TMS是一个对称结构,四个甲基的化学环境完全相同,不管在氢谱还是碳谱都只产生一个吸收峰; Produced by Jiwu Wen
h
h
2
B0(1
)
核共振频率不同,因而在不同的位置上出现 吸收峰,这种现象称为化学位移。
1
2
B0(1
)
化学位移的表示方法与测定
核磁化学位移对照表

核磁化学位移对照表
核磁化学位移是核磁共振(NMR)的一个指标,与核磁共振信号的位置有关。
不同化学环境下的原子有不同的核磁化学位移值,其值可以与参考化合物进行比较,来确定分子结构。
下面是一些常见分子结构的核磁化学位移取值范围:
1. 甲基/氢(CH3/H):0-1.5 ppm
2. 亚甲基/氢(CH2/H):1.5-2.5 ppm
3. 亚甲基/氮(CH2/N):2.5-3.5 ppm
4. 烷基/烃基(R/H):0.5-1.5 ppm
5. 乙烷(C2H6):1.25 ppm
6. 对二甲苯(p-xylene):
7.0-7.5 ppm
7. 醛卡宾(carbene):200-400 ppm
8. 羟基(OH):4.5-5.5 ppm
9. 胺基(NH):0-4.5 ppm
10. 脱氧核糖(dioxgenated ribose):3.5 ppm
需要注意的是,不同的溶剂和温度条件下,核磁化学位移值也会有所变化。
因此,在核磁共振实验中,需要使用相同的溶剂和温度条件来进行比较。
高中有机化学H核磁共振图谱简析(比教材上面多讲一些)

高中有机化学H核磁共振图谱简析(比教材上面多讲一些)这是教材上乙醇的核磁共振上面的图啊,其实是个假的乙醇的核磁共振的氢谱图下面这个是丙醇的氢谱图,这才是真实的核磁共振氢谱图用电磁波照射有机化合物样品,有机化合物分子中1H氢原子核,在外加磁场中能分裂称两个能级。
当受到电磁波照射时,如果电磁波的能量正好等于两个能级差,1H氢原子核可以吸收一定能量,从低能级跃迁到高能级,发生1H核磁共振。
用核磁共振仪可以记录到样品的共振吸收电磁波有关信号(吸收峰),得到样品的1H核磁共振图谱。
分析1H核磁共振图谱,通过化学位移,吸收峰的峰面积和积分值、吸收峰的分裂情况,可以推测含氢原子的基团在碳骨架上的位置和数目。
我们可以用乙醇的核磁共振图谱为例作粗浅分析。
(1)若有机化合物分子中氢原子所处的化学环境不同,这些氢原子产生共振时吸收电磁波的频率不同,吸收峰在图谱上出现的位置也不同(这种差异称为化学位移),因而形成一定数目的特征吸收峰。
一般采用(CH3)4Si(四甲基硅烷TMS)为标准化合物,把它的化学位移值定为0 ppm,来判断带测化合物样品中不同化学环境的氢原子产生共振时吸收形成的吸收峰的化学位移。
化合物中质子周围的电子云密度越小,化学位移越大。
吸收峰的数目反映了有机分子中氢原子化学环境的种类。
特征峰的高度越高,处于相同环境的氢原子数目越多,该吸收峰的强度(也称为面积)之比代表不同环境H的数目比。
“峰裂”——这个很重要啊~~~(2)分子中相邻碳原子上所连接的质子,存在相互影响,能引起吸收峰的分裂,形成多重峰。
当只有一个相邻碳或相邻碳上的H原子数相同时,核磁共振谱中信号分裂成多重峰的数目和相邻碳上所连接的H原子的数目n相关数目为n+1。
例如,CH3CH2OH中,-CH3应该分裂成3重峰,-CH2应该分裂成4重峰。
当某个氢核邻近碳上的H原子不相同时,峰的裂分数目为(n+1)(n'+1)(n''+1)。
核磁共振(1HNMR)

以氢核为例,实受磁 场强度: HN=H0(1-σ) σ为屏蔽常数,表示 电子屏蔽效应的大小。
E=2μHo(1 - ) =2μHo(1 - ) /h
-0.05
-0.04 0.08 1.13 1.01 1.35 0.97 1.15 1.02
-0.23
-0.21 -0.01 0.81 0.95 0.74 0.39 0.58 0.33
1.18
1.35 1.00 1.04 0.69
-1.06
0.37 0.19 0.40 -1.19
−N
R: conj(2)
取代基 供电基团 -OH -0.50 -0.14 -0.40
o
m
p
-OCH3
-CH3 吸电基团 -COCH3
-0.43
-0.17 +0.64
-0.09
-0.09 +0.09
-0.37
-0.18 +0.30
取代基
o
-0.5 -0.2 +0.6
m
-0.1 -0.1 +0.1
p
-0.4 -0.2 +0.3
无磁共振现象
μ≠0
p≠0
核显磁性
磁共振现象
13C
1H等
原子核的自旋量子数(I)与质量数(A)及原子序数(Z)的关系
质量数 原子序数 (A) (Z) 自旋量子数 (I) 半整数 (1/2, 3/2, 5/2,…)
例
13C,1H,19F, 31P,15N 17O,35Cl,
CNMR核磁共振碳谱化学位移总览表课件

根据碳碳耦合和耦合常数,确定邻近碳原子 的类型和它们之间的关系。
峰形和强度
通过峰形和相对强度,确定化合物的结构和 它们在分子中的位置。
峰的位置和积分峰面积
通过峰的相对位置和积分峰面积,计算化合 物中各类碳原子的数量。
化学位移的基本概念和计算方法
1 化学位移
化学位移是一种定量指标,描述碳原子的磁场感受性,通常表示为δ值。
CNMR核磁共振碳谱化学 位移总览表课件
CNMR核磁共振碳谱化学位移总览表课件。
什么是核磁共振碳谱
核磁共振碳谱(CNMR)是一种分析化学的技术,用于确定和解释有机化合 物中碳原子的化学环境。
CNMR谱图的读取与解读方法
峰高与化学位移
测量CNMR谱图中峰的高度,根据化学位移 数值判断化合物中的碳原子类型。
2 计算方法
化学位移可以通过将每个峰位置相对于标准物质(如三甲基硅烷)进行测定和计算得到。
常见化合物的谱图和化学位移数值对照 表
谱图解读
通过解读常见化合物的CNMR谱图,学习化学位 移数值在不同类型化合物中的变化规律。
数值对照表
提供一张常见化合物的CNMR化学位移数值对照 表,帮助快速确定未知化合物的结构。
影响化学位移的因素及其解释
电子效应
电子的吸引或排斥会改变碳 原子的化学位移。
取代基效应
取代基的种类和位置会对化 学位移产生影响。
溶剂效应
溶剂分子的影响会改变化学 位移数值。
核磁共振碳谱在有机化学和药物研发中 的应用
1
结构确认
核磁共振碳谱帮助鉴组分定量
通过测量峰面积,核磁共振碳谱可以用于定量分析。
3
改进合成路径
通过核磁共振碳谱的结果,调整合成路径以获得更理想的产物。
1H-NMR图谱解析

B: Cl2CHCH(OCH2CH3)2
正确结构:
O CH2CH3 HC O CH2CH3
O CH2CH3
图谱解析与结构确定(5) : 某化合物的分子式为C6H10O3,其P-NMR核磁 共振谱图见下图,试确定该化合物的结构
O
O
H 3C C CH 2 C O CH 2CH 3
2
2
3
3
图: C6H10O3核磁共振谱图
图谱解析与结构确定(6) :
3H 2H
δ7.3 δ5.21
δ2.3 δ1.2
图谱解析与结构确定(3) :
化合物 C8H8O2,推断其结构
10 9 8 7 6 5 4 3
• =1+8+1/2(-8)=5
• δ=7-8芳环上氢,dd峰(对位取代)
O • δ= 9.87—醛基上氢, C H
• 低δ= 3.87 CH3上氢,低场移动,与电负性强 的元素相连: —O—CH3
• 正确结构:
O
H3CO
CH
图谱解析与结构确定(4) :
C7H16O3,推断其结构
9
δ 5.30 1
δ 3.38 δ 1.37 6
C7H16O3, =1+7+1/2(-16)=0
a. δ3.38和δ 1.37 四重峰和三重峰
—CH2CH3相互偶合峰 b. δ3.38含有—O—CH2 —结构 结构中有三个氧原子,可能具有(—O—CH2 —)3 c. δ5.3CH上氢吸收峰,低场与电负性基团相连
化合物 C3H7Cl,推断其结构
a bc CH3CH2CH2Cl
图谱解析与结构确定(7) :
核磁共振氢谱(1H-NMR)
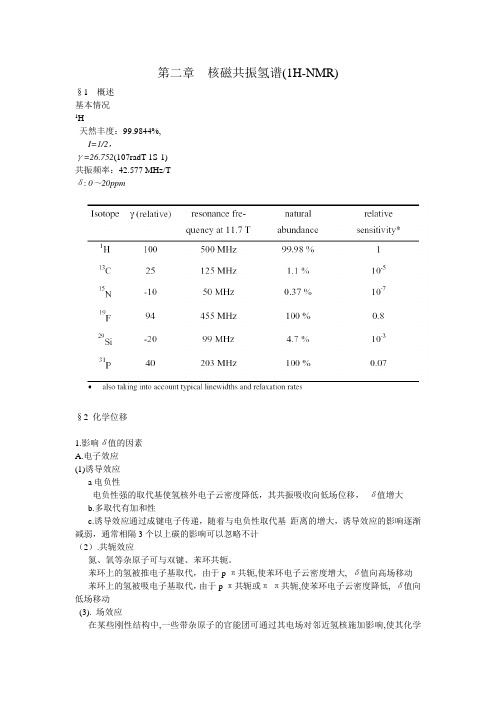
第二章核磁共振氢谱(1H-NMR)§1 概述基本情况1H天然丰度:99.9844%,I=1/2,γ=26.752(107radT-1S-1)共振频率:42.577 MHz/Tδ: 0~20ppm§2 化学位移1.影响δ值的因素A.电子效应(1)诱导效应a电负性电负性强的取代基使氢核外电子云密度降低,其共振吸收向低场位移,δ值增大b.多取代有加和性c.诱导效应通过成键电子传递,随着与电负性取代基距离的增大,诱导效应的影响逐渐减弱,通常相隔3个以上碳的影响可以忽略不计(2).共轭效应氮、氧等杂原子可与双键、苯环共轭。
苯环上的氢被推电子基取代,由于p-π共轭,使苯环电子云密度增大, δ值向高场移动苯环上的氢被吸电子基取代,由于p-π共轭或π-π共轭,使苯环电子云密度降低, δ值向低场移动(3). 场效应在某些刚性结构中,一些带杂原子的官能团可通过其电场对邻近氢核施加影响,使其化学位移发生变化.这些通过电场发挥的作用称为场效应(4). 范德华(Van der Waals)效应在某些刚性结构中,当两个氢核在空间上非常接近,其外层电子云互相排斥使核外电子云不能很好地包围氢核,相当于核外电子云密度降低,δ值向低场移动B.邻近基团的磁各向异性某些化学键和基团可对空间不同空间位置上的质子施加不同的影响,即它们的屏蔽作用是有方向性的。
磁各向异性产生的屏蔽作用通过空间传递,是远程的。
(1)芳环在苯环的外周区域感应磁场的方向与外加磁场的方向相同(顺磁屏蔽),苯环质子处于此去屏蔽区,其所受磁场强度为外加磁场和感应磁场之和,δ值向低场移动。
(2)双键>C=O, >C=C<的屏蔽作用与苯环类似。
在其平面的上、下方各有一个锥形屏蔽区(“+”),其它区域为去屏蔽区。
(3)三键互相垂直的两个π键轨道电子绕σ键产生环电流,在外加磁场作用下产生与三键平行但方向与外加磁场相反的感应磁场。
三键的两端位于屏蔽区(“+”),上、下方为去锥形屏蔽区(“-”)δ值比烯氢小。
2-1HNMR-化学位移

4.2.2.各类1H的化学位移
1~2:相邻没有电负性基团的饱和碳上的氢(CCHn)、烯烃或炔烃α-H 2~4.5:相邻有电负性基团(如:C=O、O、N、S、Cl、Br等)的饱和碳上的氢 (XCHn)、苯环α-H 其它氢核:炔氢:2~3 烯氢:4.5~8 芳氢(ArH): 6.0~9.0
O 2.0~3.0 HCCCH
O
2.0~3.0
HCCH
酮
O
2.0~3.0
HO C C H
9.0-10.0
醛
O
2.0~3.0
HCOCCH
10.0~12.0 (单峰)
3.4~4.5
羧酸
酯
注:相邻有两个及两个以上电负性基团取代时, δ 值会超过上述范围。
注意:上述范围只是在相邻只有一个电负性基团的情况,若多个电负性基团存在或是多种因素影 响时,化学位移可以发生较大的变化. 例:
-CH3 ,δ = 1.8,出现在高场 -CH2I,δ= 3.1, 出现在低场
• 判断下列化合物中Ha,Hb化学位移的大小
CH3 CH3
H C O C Hb
CH3
CH3 a
a<b
HH I C C Cl
HH ab
a<b
CH3CH2CH2I a bc
a<b<c
• 下面化合物中所标出的质子其1H NMR化学位移从低场到高场的顺序为( )
(7)溶剂效应
由于溶质分子受到不同溶剂影响而引起的化学位移变化称为溶剂效应。例 如:
O
C
.. N
CH3 b
H
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
核磁共振1H化学位移图表
质子类型 化学位移值文字需求请找字伯虎文字创意,Q为17-3125-3445
烷烃质子
(1) -C-C-H 0.9~1.5 ppm
(2) -C=C-CH
-C≡C-CH
(3)与N、S、C=O、-Ar相连 2.0~2.5 ppm
(4)与O、卤素相连 3~4 ppm
烯烃质子
4.5~8.0 ppm
利用1H-NMR可有效确定双键的取代及构型。
H=5.28+Zgem+Zcis+Ztrans
炔烃质子 4.5~8.0 ppm利用1H-NMR可有效确定双键的取代及构
型。
炔烃质子 不特征, 1.8~3.0 ppm ,与烷烃重叠,应结合IR解析。
芳烃质子 1H-NMR信息非常特征 6.5~8.0 ppm,未取代芳环
7.26 ppm,呈现单峰
1.6~2.1 ppm
C
C
Rcis
Rtrans
H
Rgem
其它质子
醛基 -CO-H 9.0~10.0 ppm
羟基 R-OH 0.5~1.0ppm (稀溶液)
4~ 5.5 ppm (浓溶液)
Ar-OH 3.5~7.7 ppm
10~16 ppm(分子内氢键)
-COOH 10.5~13 ppm
