蛋白质检验原始记录单
饲料厂各种表格

产品出入库记录
产品名称:代号:规格或等级:
产品销售记录
检验报告
检验记录
粗蛋白测定原始记录(常量法)
检测人:校核人:审核人:
现场质量巡查记录
检验仪器档案
仪器设备名称:规格型号:
危险化学品出入库记录
不合格品评价与处理记录
供应商评价记录
供应商名录
原料编号:原料名称:规格或等级:生产日期:生产企业或供应商代码:
原料垛位标识卡垛料编号:
原料垛位标识卡垛料编号:
垛位编号:
原料监控记录
班次:日期:
复核(生产主任):编制(中控员):投料员:
中间产品标识卡
设备档案
仪器名称:
设备维修记录
包装作业记录
注:本报表可复制,寄:南京市龙江小区月光广场8号901室,或传真,电话确认收到。
留样观察记录
不合格产品分析。
食品中蛋白质的测定

任务:1、请设计检验样品抽样单,并抽样,填写相关记录;2、食品中蛋白质种类及含量是标志食品营养价值的重要指标,查阅资料,了解并下载国家标准测定蛋白质的方法。
3、凯氏定氮法测定食品中蛋白质方法原理是什么?凯氏定氮法测定食品中蛋白质的原理是样品与浓硫酸、硫酸钾、硫酸铜一同加热消化, 使蛋白质分解, 其中碳和氢被氧化为二氧化碳和水逸出, 而样品中的有机氮转化为氨和硫酸结合成硫酸铵, 然后加碱蒸馏, 使氨蒸出,用硼酸吸收后再以标准盐酸溶液滴定, 根据标准酸消耗量可计算出蛋白质的含量。
4、对照国家标准,列出实验所需仪器与试剂所有试剂均为分析纯,水为蒸馏水或同等纯度的水。
硫酸铜、硫酸钾、浓硫酸;40%氢氧化钠溶液:称取40g 氢氧化钠溶于60ml 蒸馏水中;4%硼酸溶液:称取4g 硼酸溶于蒸馏水中稀释至100ml;0.050mol/l 盐酸标准滴定溶液;甲基红次甲基蓝混合指示液:将次甲基蓝乙醇溶液(1g/l)与甲基红乙醇溶液(1g/l)按1∶2 体积比混合。
实验室常规仪器及下列各项:凯氏烧瓶:500ml;可调式电炉;蒸汽蒸馏装置;绞肉机:篦孔径不超过4nm;组织捣碎机;粉碎机;研钵:玻璃或瓷质;化学消化器;凯氏定氮仪;空气滤过器5.样品在消化过程中,应加入浓硫酸、硫酸钾及硫酸铜,试分别说清他们各自的作用。
加硫酸作用:硫酸及催化剂与样品加热消化, 使蛋白质分解, 其中C、H 形成CO2和H2O 逸出, 而蛋白质中的氮则转化成( NH4 )2SO4加硫酸钾作用:在消化过程中添加硫酸钾可以提高温度加快有机物分解,它与硫酸反应生成硫酸氢钾,可提高反应温度,一般纯硫酸加热沸点330 ℃,而添加硫酸钾后,温度可达400 ℃,加速了整个反应过程。
此外,也可以加入硫酸钠,氢化钾盐类来提高沸点。
其理由随着消化过程硫酸的不断地被分解,水分的逸出而使硫酸钾的浓度增大,沸点增加。
加速了有机的分解。
但硫酸钾加入量不能太大,否则温度太高,生成的硫酸氢铵也会分解,放出氨而造成损失。
检验原始记录【范本模板】
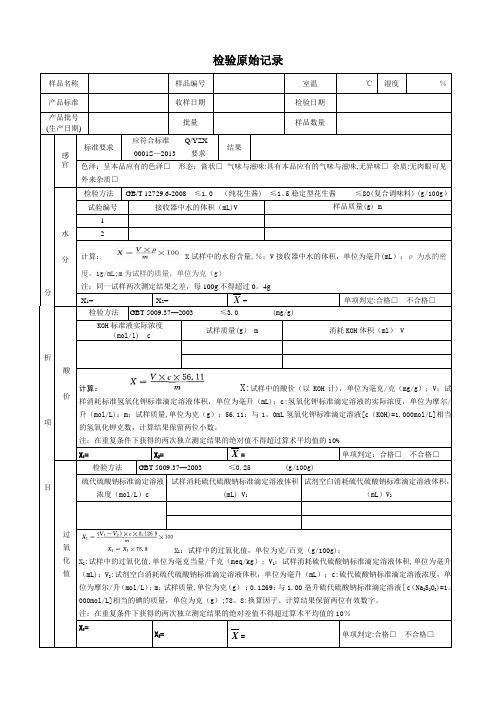
样品名称样品编号室温℃湿度%产品标准收样日期检验日期产品批号(生产日期)批量样品数量分析项目感官标准要求应符合标准Q/YZX0001S—2013 要求结果色泽:呈本品应有的色泽□形态:膏状□气味与滋味:具有本品应有的气味与滋味,无异味□杂质:无肉眼可见外来杂质□水分检验方法GB/T 12729.6-2008 ≤1.0 (纯花生酱) ≤1。
5稳定型花生酱≤80(复合调味料) (g/100g)试验编号接收器中水的体积(mL)V 样品质量(g) m12计算: X试样中的水份含量,%;V接收器中水的体积,单位为毫升(mL);ρ为水的密度,1g/mL;m为试样的质量,单位为克(g)注:同一试样两次测定结果之差,每100g不得超过0。
4gX1= X2= X= 单项判定:合格□不合格□酸价检验方法GBT 5009.37—2003 ≤3.0 (mg/g)KOH标准液实际浓度(mol/l) c试样质量(g) m 消耗KOH体积(ml) V计算:X:试样中的酸价(以KOH计),单位为毫克/克(mg/g);V:试样消耗标准氢氧化钾标准滴定溶液体积,单位为毫升(mL);c:氢氧化钾标准滴定溶液的实际浓度,单位为摩尔/升(mol/L);m:试样质量,单位为克(g);56.11:与1。
0mL氢氧化钾标准滴定溶液[c(KOH)=1.000mol/L]相当的氢氧化钾克数,计算结果保留两位小数。
注:在重复条件下获得的两次独立测定结果的绝对值不得超过算术平均值的10%X1= X2= X= 单项判定:合格□不合格□过氧化值检验方法GBT 5009.37—2003 ≤0.25 (g/100g)硫代硫酸钠标准滴定溶液浓度(mol/L)c试样消耗硫代硫酸钠标准滴定溶液体积(mL) V1试剂空白消耗硫代硫酸钠标准滴定溶液体积,(mL)V2X1:试样中的过氧化值,单位为克/百克(g/100g);X2:试样中的过氧化值,单位为毫克当量/千克(meq/kg);V1:试样消耗硫代硫酸钠标准滴定溶液体积,单位为毫升(mL);V2:试剂空白消耗硫代硫酸钠标准滴定溶液体积,单位为毫升(mL);c:硫代硫酸钠标准滴定溶液浓度,单位为摩尔/升(mol/L);m:试样质量,单位为克(g);0.1269:与1.00亳升硫代硫酸钠标准滴定溶液[c(Na2S2O3)=1。
蛋白质检测原始记录

F ——注意:(1)蛋白质含量≥1g/100g时,结果保留三位有效数字;蛋白质含量<1g/100g时, 结果保留两位有效数字。
(2)在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
样品
m
1#
2#
V1
V2
V3
X
差值 允差 平均值
C
V1 ——试样消耗硫酸或盐酸标准滴定液的体积,单位为毫升(ml); V2 ——试剂空白消耗硫酸或盐酸标准滴定液的体积,单位为毫升(ml); V3 ——吸取消化液的体积,单位为毫升(ml);
C ——硫酸或盐酸标准滴定溶液的浓度,单位为摩尔每升(mol/l); 0.0140——1.0ml硫酸【c(1/2H2SO4)=1.000mol/l】或盐酸【c(HCL)=1.000mol/l 】标准滴定溶液相当的氮的质量,单位为克(g); m ——试样的质量,单位为克(g);
F
报出结果
备注:
检验员:
审核:
年月日
编号: 样品名称:
蛋白质检测原始记录
批次:
1、检验依据:GB/T5009.5-2016(凯式定氮法)
2、范围:适用于各种食品中蛋白质的测定
3、使用主要仪器:①定氮蒸馏装置
②分析天平
4、计算公式:
式中:
X (V1 V 2)C 0.0140 F 100 mV 3 /100
X ——试样中蛋白质含量,单位为克每百克(g/100g);
蛋白质原始记录表

蛋白质原始记录表
蛋白质原始检验记录
产品名称
检测方法:
称取0.0995g±0.1005g样品于100ml容量瓶,用纯化水定容,溶解,精密量取1.0ml供试品溶液于10ml具塞刻度管,加5ml碱性铜,摇匀,室温放置10分钟,快速加入0.5ml酚试剂,摇匀,室温放置30分钟。
用分光光度计检测。
检测温度:20℃。
计算公式:平均值=(检测值A+检测值B+检测值C)÷3 蛋白含量=吸光度/稀释倍数(100)/标准曲线斜率(0.2023)/称样量批号检验号日期称样量g 检测值蛋白含量备注检测人:复核人:批号检验号日期称样量g 检测值蛋白含量备注检测人:复核人:。
蛋白质检验原始记录

15s,蒸馏 420s,吸废液 10s,清洗 45s,如果是手动加硼酸,加酸时间为 0s,结束后仪器自动
停止,将三角瓶取下。
(7) 同时做两分空白。
4 标准溶液的配制:
0.05mol/L 的盐酸:4.2ml 盐酸容于 1000ml 蒸馏水,并用碳酸钠发标定。
标定后盐酸浓度
5 结果分析
蛋白%= (V1-V2)×C×0.0893
(4) 每个样品再加入 15ml 硫酸。
(5) 消化:【01】(250 10)-【02】(280 5)
【03】(310 10)-【04】(350 10)
【05】(390 5)-【06】(420 90)
(6) 蒸馏:样品管放冷后,加 20ml 水混匀,三角瓶加入 20ml 硼酸和 3-5 滴指示剂;系统设置加碱
蛋白质含量测定
本方法适用于原料乳和乳制品中蛋白质的检测,方法结合国标 GB5009.12-2010 中凯氏定氮法。 1、原理:蛋白质是含氮的有机化合物。样品与硫酸和催化剂一同加热消化,使氮分解,分解的
氮与硫酸结合生产硫酸铵,然后碱化蒸馏使氨游离,用硼酸吸收,再用已知摩尔浓度盐酸标准溶液滴 定,根据酸的消耗量乘以换算系9.12-2010,水为 GB/T6682 规定的一级水。
仪器名称:定氮仪全自动蒸馏装置、智能消化炉;仪器型号 KND-812、HPY-314;
检定有效期 年 月 日
; 检验日期:
年
月日
样品名称:
样品批号:
称样量及编号:
样品来源:
样品名称:
样品批号:
称样量及编号:
样品来源:
样品名称:
样品批号:
称样量及编号:
样品来源:
3 样品前处理:
3.牛血清蛋白质含量检验记录
—————
样品1
样品2
结果判定:
检验人: 复核人:
蛋白质含量检验记录
文件编号:
生产编码
生产批号
生产日期
_____年_____月_____日
检验日期
_____年_____月_____日
检验依据
执行文件
《牛血清蛋白含量检验操作规程》
测定方法
双缩脲法
设备编码
试剂名称
1.双缩脲试剂:取碳酸铜(CuSO4·5H2O)3.0g、酒石酸钾钠(KNaC4H4O6·4H2O)9.0g,碘化钾5.0g,氢氧化钠24g,加水溶解并稀释至1000ml,摇匀,即得;
2.另精密量取双蒸水0.05ml,自加“双缩脲试剂4.0ml”起,同法操作,作为空白对照。
计算方法
按下式计算:蛋白质含量(W/V)=
式中:A1为样品溶液的吸光度;
A2为标准蛋白质溶液的吸光度;
C为标准蛋白质溶液的浓度,mg/ml;
测试结果
样品
测定值
平均值
标准
判定
空白对照
—————
3.5%~5.0%
□合格 □不合格
2.标准蛋白质溶液的制备:精密量取人血白蛋白(牛血白蛋白)标准品适量,用水定量稀释成每1ml含50mg的溶液;);
操作方法
1.分别精密量取待检样品与标准蛋白质溶液各0.05ml置玻璃试管中,分别加双缩脲试剂4.0ml,混匀,置37℃水浴中30分钟,在波长540nm处测定吸光度。
食品蛋白质测定原始记录GB 5009.5-2016
基苯酚指示剂溶液,摇匀后滴加氢氧化钠溶液中和至黄色,再滴加乙酸溶液至溶液无色,用水稀释至刻度,混匀试样溶液总体积为V3mL。
标准曲线的绘制:吸取0.00mL、0.05mL、0.10mL、0.20mL、0.40mL、0.60mL、0.80mL和1.00mL氨氮标准使用溶液(相当于0.00μg、5.00μg、10.0μg、20.0μg、40.0μg、60.0μg、80.0μg和100.0μg氮),分别置于10mL比色管中。加4.0mL乙酸钠-乙酸缓冲溶液及4.0mL显色剂,加水稀释至刻度,混匀。置于100℃水浴中加热15min。取出用水冷却至室温后,移入1cm比色杯内,以零管为参比,于波长400nm处测量吸光度值,根据标准各点吸光度值绘制标准曲线或计算线性回归方程。
检验结果
试样中氮含量C(g/100g)
氮换算为蛋白质的系数F
样品含量X(g/100g)
平均值(g/100g)
计算公式
X=C*F
其他说明
1.重复性条件下获得的两次独立测定结果的绝对差值不超过算术平均值的10%
2.结果保留三位有效数字
检验仪器
仪器名称
仪器编号
量值溯源状态
电子天平
氮/蛋白质分析仪
检验过程
按照仪器说明书要求称取g充分混匀的试样(精确至0.0001g),用锡箔包裹后置于样品盘上。试样进入燃烧反应炉(900℃~1200℃)后,在高纯氧(≥99.99%)中充分燃烧。燃烧炉中的产物(NOx)被载气二氧化碳或氦气运送至还原炉(800℃)中,经还原生成氮气后检测其含量。
氨氮标准使用溶液(0.1g/L):用移液管吸取10.00mL氨氮标准储备液于100mL容量瓶内,加水定容至刻度,混匀,此溶液每毫升相当于0.1mg氮。
蛋白质检测原始检验记录
HY4-04-055
烟台浩洋农业科技有限公司
蛋白质测定记录
样品编号:
样品名称:检测项目:
样品状态:检测依据、方法:
检测日期:实验室环境:室温℃,相对湿度% 标准滴定溶液、编号:滴定管名称、编号:
配制日期:标准滴定溶液浓度:
主要检测仪器□分析天平,量程0-210g,精度0.1mg。
□凯氏定氮仪
□滴定管,量程0-50ml,精度0.02ml。
样品前处理方法
□称取试样m,放入凯氏烧瓶中,加入6g硫酸钾(或硫酸钠)、0.4g硫酸铜、12mL浓硫酸和2粒玻璃珠充分混匀,加热消化至蓝色透明,定容。
取试液蒸馏、定氮。
滴定
数据
空白消耗标准液V0= mL
样品分号取样量
m
定容体
积V1
测定用
体积V2
试样消耗标准液体积
V
计算结果
X
平均值
X
相对偏
差
报告值
X
g mL mL mL g/100g g/100g % g/100g
1 2
计算公式
()
()
100
1000
/
100
/
1
2
0⨯
⨯
⨯
⨯
⨯
⨯
-
=F
V
V
m
M
c
V
V
g
g
X
X——试样中被测物质含量,以计;
c——标准溶液浓度;
M =0.014g/mol,与标准溶液相当的、以克表示氮的质量;
F——氮换算为蛋白质的平均系数:F= .审核:检验:。
蛋白质设施样品登记表Avant150
自带层析柱:□是□否
UV监测:□280nm□nm□nm
pH在线监测:□是□否
是否需配制缓冲液(若是,请填写详细的缓冲液信息,如平衡缓冲液、洗脱缓冲液等):
Doe实验填写:□筛选实验□优化实验□稳健性实验
样品信息
样品名称:
样品个数/编号:
样品体积:
可能包含的杂质分子:
蛋白浓度:
目标蛋白大致分子量:
AKTA Avant150样品登记表
用户信息
单位(院系):
实验室名称:
使用人:
实验室电话:
手机:
ail:
经费负责人(导师):
特别提示:第一次实验送交此表格时,需要经费负责人签字。负责人签字:
服务项目
□纯化收集□纯度测定□分子量测定□Doe实验
层析类型:□凝胶过滤□离子交换□亲和层析□疏水层析
上样量:
目标蛋白等电点:
目标蛋白是否带标签:
样品备注:(buffer成分,buffer pH,实验温度,可能的生物化学毒性等)
平台填写
实验日期起止时间:
操作人员:
实际使用的层析柱/填料:
是否使用上样环/样品环:
应收实验费用:
备注:
送样须知:
1.预约时,请认真填写样品登记表,尤其是蛋白浓度、分子量及buffer成分。
2.平台将对测试完的样品作定期处理,若有需要请自行取走保存。
我已经认真阅读并同意以上送样须知。
客户签字:日期:年月日
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
0.0140:氮原子的摩尔质量,gF:氮换算成粗蛋白的系数(一般食物为6.25;纯乳与纯乳制品为6.38;)
编号
样品名称
批次
样品质量m,g或mL
样液定容体积,mL
空白消耗标准溶液毫升数v0,mL
蛋白质检验原始记录单
编号:TQM(R)72-1006-0
天平编号:□□定氮仪编号:
检验依据:
环境条件: ℃ %
滴定管规格及编号:
标准溶液浓度:□(1/2)硫酸 ( )mol/L□盐酸( )mol/L
计算公式
蛋白质 y(g/100 g)=(V1-V0)×c×0.0140×F×100/m系数:□6.38 □6.25
样液消耗标准溶液毫升数v1,mL
(V1-V0)温度补偿后消耗标准溶液体积,mL
结果y,g/100 g
报出值
g/100 g
备注
检测人
检测日期校核人校源自日期
