基因沉默
基因沉默的研究及应用实例简介

用 RNaseIII 消化长片断 siRNA表 双链RNA制 siRNA表 达载体 备siRNA 达框架
体外转录
• 以DNA Oligo为模板,通过体外转录合成siRNAs, 成本相对化学合成法而言比较低,而且能够比化 学合成法更快的得到siRNAs。不足之处是实验的 规模受到限制。 • 值得一提的是体外转录得到的siRNAs毒性小,稳 定性好,效率高,只需要化学合成的siRNA量的 1/10就可以达到化学合成siRNA所能达到的效果, 从而使转染效率更高。 • 最适用于:筛选siRNAs,特别是需要制备多种 siRNAs,化学合成的价格成为障碍时。 • 不适用于:实验需要大量的,一个特定的siRNA。 长期研究
负对照
(1)一个完整的siRNA实验应该有负对照。 (2)作为负对照的siRNA应该和选中的siRNA序列有 相同的组成,但是和mRNA没有明显的同源性。 ( 3 )通常的做法是将选中的 siRNA 序列打乱,同样 要检查结果以保证它和其他基因没有同源性。
制备siRNAs的方法
化学 合成 体外 转录
策略
• 利用RNAi降解CYP17mRNA,使CYP17基因所编码蛋白 的合成明显降低,降低CYP17基因蛋白对其下游基 因的调控,在很大程度上阻断了肿瘤细胞的应答, 建立一种基因修饰前列腺癌治疗策略,提高前列腺 癌的治疗效果。
新鲜前列 腺癌标本
组织中总 RNA的提取
反转录
siRNA的 制备
siRNA
目录
1 2
基因沉默的概述 RNA干扰
3
4
基因沉默的应用实例
RNAi的生物学意义
1.基因沉默
• 定义:基因沉默(gene silencing)是指 生物体中特定基因由于种种原因不表达或 者是表达减少的现象。
RNA介导的基因沉默技术研究

RNA介导的基因沉默技术研究基因沉默是基因表达调控的一种机制,它通过阻断基因转录或抑制已经转录的mRNA的翻译来抑制基因表达。
RNA介导的基因沉默技术采用了RNA作为调控基因表达的工具。
这种技术广泛应用于基因功能研究、疾病治疗和农作物改良等领域。
RNA介导基因沉默技术主要分为siRNA、miRNA和shRNA三类。
1. siRNAsiRNA是20-25个核苷酸的双链RNA,它通过与靶基因mRNA特异性杂交,介导RNA诱导靶基因沉默。
这个过程通过小核RNA和RISC( RNA-Induced Silencing Complex)协同完成。
当siRNA与mRNA杂交后,RISC会切断mRNA形成不完整的片段,导致mRNA降解或翻译抑制。
siRNA技术可以实现精准靶向,对于多种疾病治疗具有潜在的应用价值。
但是,siRNA技术的缺点是需要选择合适的RNA靶点,并且siRNA的短寿命和难以穿透细胞膜限制了其广泛应用。
2. miRNAmiRNA是20-24个核苷酸的单链RNA,它通过特异性结合目标mRNA,同时与RISC结合,引导RISC切割目标mRNA分子。
同时,miRNA还可以通过直接结合靶标的5’端和3’端调控mRNA 的效率和速度。
miRNA广泛参与基因表达调控,可以调控20000多种基因的表达。
miRNA的缺点是具有很高的复杂性和不确定性。
miRNA靶基因的预测算法准确性存在差异,miRNA同靶基因的作用机制还需要进一步研究。
3. shRNAshRNA是基于RNA干扰技术的新型分子,可以在基因水平靶向RNA,抑制基因表达。
shRNA是单链RNA,具有RNAi引发靶基因沉默的功能。
其优点是技术简单,稳定性较好,可以长期干扰一个基因,生成稳定的RNAi信号。
但是,shRNA技术的缺点是仍然存在一些安全性问题和非特异性靶向的可能性。
实现精准稳定靶向仍然是一个需要解决的问题。
RNA介导的基因沉默技术具有广泛的研究和应用前景。
植物抗病毒的可能机制-基因沉默

植物抗病毒的可能机制——基因沉默植物抗病性是植物抵抗病原物侵染的性能。
1986年有人首次将烟草花叶病毒(TMV,下称)的衣壳蛋白(CP,下称)基因导人烟草获得了抗TMV转基因植株后,很多学者开展了转基因抗病毒的研究。
1990年Carylon等人首先报道了转基因沉默(Transgene silencing)现象。
基因沉默是指生物体中特定基因由于种种原因不表达。
它发生在两种水平上,1种是转录水平上的基因沉默,另1种是转录后基因沉默(post transcriptional gene silencing.PTGS.下称)。
转录后水平基因沉默在植物表现型上称为共抑制,是指在外源基因沉默的同时,与其同源的内源基因的表达也受到抑制的现象。
Carylon为加深花色将查尔酮合成酶基因(ehalcone synthase,CHS)转到紫花矮牵牛中,发现42%的转基因植株中不仅花色未加深,反而变为白色或紫白相间,这种转入的外源基因和内源基因共同沉默的现象就是转基因沉默。
目前认为.植物基因沉默是植物长期进化形成的用来防止外来遗传物质干扰自身基因组功能和保持稳定性的重要机制,是生物体中1种不完全的原始的生物免疫系统。
本文将从基因沉默的角度介绍植物抗病毒的可能机制。
1 RNA介导的病毒抗性和PTGS近20年来,植物抗病毒基因工程的研究逐步深入。
在CP基因介导的抗性研究中,对CP基因进行改造,插入翻译终止密码子或去掉翻译起始密码子,使其不能翻译产生CP蛋白,结果也能获得高抗病甚至免疫的转基因植株。
这种病原来源的抗性称之为RNA介导的病毒抗性(RNA mediated virus re— sistance,RMVR.下称)。
RMVR与PTGS机制类似。
两者均发生在胞质中。
PTGS与RMVR两种现象具有许多共同特征,如序列特异性、与转基因的拷贝数有关,减数分裂后沉默保持的不可预见性(George,1998),所以RMVR也是1种PTGS。
基因沉默
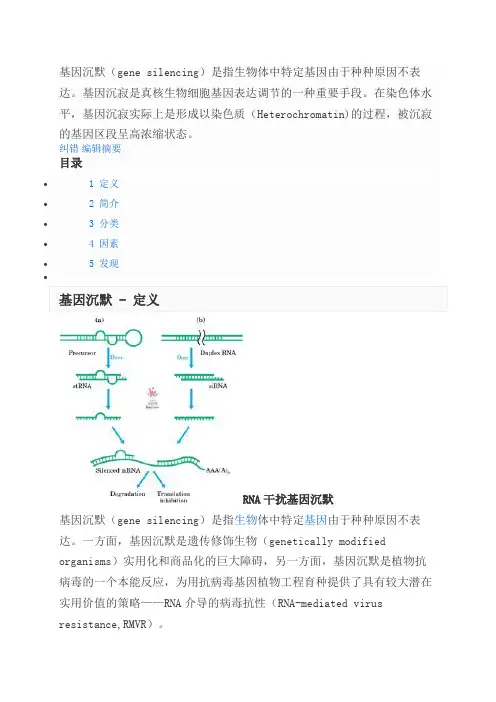
RNA干扰基因沉默基因沉默(gene silencing)是指生物体中特定基因由于种种原因不表达。
一方面,基因沉默是遗传修饰生物(genetically modified organisms)实用化和商品化的巨大障碍,另一方面,基因沉默是植物抗病毒的一个本能反应,为用抗病毒基因植物工程育种提供了具有较大潜在实用价值的策略——RNA介导的病毒抗性(RNA-mediated virus resistance,RMVR)。
转基因植物和转基因动物中往往会遇到这样的情况,外源基因存在于生物体内,并未丢失或损伤,但该基因不表达或表达量极低,这种现象称为基因沉默。
转基因沉默分为转录水平的沉默(TGS)和转录后水平的沉默(PTGS)。
TGS是指转基因在细胞核内RNA合成受到了阻止导致基因沉默,PTGS是指RNAi——基因沉默指南基因沉寂(Gene Silencing) 也可以被称为“基因沉默”。
基因沉寂是真核生物细胞基因表达调节的一种重要手段。
在染色体水平,基因沉寂实际上是形成以染色质(Heterochromatin)的过程,被沉寂的基因区段呈高浓缩状态。
基因沉寂需要经历不同的反应过程才能实现,包括组蛋白N端结构域的赖氨酸残基的去乙酰基化加工、甲基化修饰(由甲基转移酶催化,修饰可以是一价、二价和三价甲基化修饰,后者又被称为'过度’甲基化修饰(Hypermethylation) ) 、以及和甲基化修饰的组蛋白结合的蛋白质(MBP)形成“异染色质”,在上述过程中,除了部分组蛋白的N端尾部结构域需要去乙酰化、甲基化修饰之外,有时也许要在其他的组蛋白N端尾部结构域的赖氨酸或精氨酸残基上相应地进行乙酰化修饰,尽管各种修饰的最终结果会导致相应区段的基因“沉寂”失去转录活性。
这个“原则”就是目前尚没有真正完全清楚的“组蛋白密码”(Histone Code)。
能够与甲基化组蛋白结合的蛋白质有sir1/2/3/4,这是一组被称为"Silencing Informative Repressor"的蛋白,其中,Sir2就是上文中的“去乙酰化”酶,而Sir1/3/4则负责与甲基化修饰的组蛋白结合"沉寂”相应的染色质为异染色质。
基因沉默名词解释

基因沉默名词解释基因沉默,指的是抑制或抑制正常的基因功能。
基因沉默可以在多种水平上发生,从分子层次到细胞层次,从细胞层次到组织层次,再到整个机体组织水平。
基因沉默可分为三类,即转录抑制、调节抑制和调节转录抑制(TGS)。
转录抑制是指基因转录过程中的抑制,它是由转移因子介导的,通常是由抑制基因的非编码RNA、DNA复合物或其他蛋白质抑制有效的HTR导致的。
当转录因子在基因上聚集时,它们可以抑制此基因上的有效拷贝数量及其表达,从而降低或抑制基因的功能。
调节抑制是指在基因转录后的调控过程中,由抑制蛋白质通过影响mRNA或蛋白质的稳定性来抑制基因表达。
调节抑制可以在不同水平上发挥作用,例如在细胞中可以抑制mRNA和蛋白质的形成,在组织水平上可以抑制蛋白质的稳定性和细胞分化,从而抑制基因表达。
这种抑制机制可以使基因表达更加精细,可以更好地调节基因功能,从而调节机体的新陈代谢。
调节转录抑制也叫TGS,它是一种可以在基因组织水平上实现基因沉默的技术,它可以实现非编码RNA涉及的基因表达调控。
在基因水平上,TGS可以改变mRNA和蛋白质的形成方式和稳定性,从而抑制基因表达,在组织水平上,TGS可以影响细胞分化,从而抑制机体的器官及组织的新陈代谢。
此外,TGS还可以通过调控细胞的基因表达,影响细胞的生长、分化和功能,从而抑制疾病发病。
基因沉默在生物的发育过程中具有重要作用,它可以控制基因的表达,从而调节细胞的发育和机体的新陈代谢。
目前,基因沉默技术被用于各种疾病治疗,如癌症、心脏疾病和神经系统损伤等,这些技术可以改变基因表达水平,从而抑制疾病发病。
未来,基因沉默技术可能在生物医学领域展开广泛的应用,例如可以用于器官的再生、药物的研发等。
同时,基因沉默技术在生物安全性、社会安全性和科学道德上也可能引起讨论,因此,在基因沉默技术的应用时,还需要综合考虑法律、人文、社会等因素。
基因沉默是一种重要的基因调控技术,它可以影响基因表达、影响细胞发育和机体新陈代谢,还可以用于疾病治疗,因此,基因沉默技术将在未来发挥更多重要的作用。
沉默基因的原理及应用

沉默基因的原理及应用1. 沉默基因的定义沉默基因(Silencing Gene)是指可以通过RNA干涉(RNA interference, RNAi)技术降低或消除目标基因表达的基因。
RNA干涉是一种细胞内天然的基因调控机制,通过降解特定的mRNA分子来抑制目标基因的表达。
沉默基因技术的出现为基因功能研究和遗传改良提供了有力的工具。
2. 沉默基因的原理沉默基因的原理主要基于RNA干涉技术。
在细胞中,RNA干涉主要分为两个步骤:siRNA的合成和RISC(RNA-Induced Silencing Complex)的形成与作用。
2.1 siRNA的合成siRNA(small interfering RNA)是由双链RNA酶(Dicer)作用下产生的双链小分子RNA。
siRNA可以由来源于细胞内的长串RNA、预先合成的siRNA或经过外源RNA病毒转染所合成。
在细胞中,长串RNA被Dicer酶切割成约21-25个碱基对的双链siRNA,在此过程中Dicer酶与合成的siRNA共同组成RISC。
2.2 RISC的形成与作用RISC是由特殊的蛋白质组成的复合物,其中包含一个Dicer蛋白和一个Argonaute蛋白。
RISC能够识别并结合与siRNA序列互补的靶基因mRNA,在结合的过程中RISC将mRNA分子切割并降解,从而阻断目标基因的正常表达。
3. 沉默基因的应用沉默基因技术在多个领域都有重要的应用价值,主要包括基因功能研究、生物医学研究、农业遗传改良等。
3.1 基因功能研究沉默基因技术可以通过特异性地降低或消除目标基因的表达来研究基因在生物体内的功能。
通过沉默某个特定基因,研究人员能够观察到该基因缺失或受抑制后生物体的表型变化,并进一步了解该基因在生物体发育、代谢、免疫等方面的作用机制。
3.2 生物医学研究沉默基因技术在生物医学研究中的应用十分广泛。
研究人员可以通过沉默特定的致病基因来研究该基因与疾病之间的关系,并探索新的治疗方法。
引起基因沉默的原因
引起基因沉默的原因研究表明,引起基因沉默的原因很多,转基因的拷贝数和构型、在植物上的整合位点、转基因的转录水平等都与沉默有关,外界环境如过高的温度、过强的光照也会增加基因沉默发生的几率和产生时间,此外,外源基因的表达还受植物发育因子(如亲本年龄)的影响。
因此,植物转基因沉默的作用机制可能不是单一的,而是各种机制共同作用的结果,是植物本身的防御系统和外界环境因素协同作用的产物。
转基因沉默可以发生在染色体DNA水平、转录水平和转录后水平三种不同的层次上。
1.染色体DNA水平的转基因沉默发生在染色体DNA水平的转基因沉默叫做位置效应(positioneffect)。
当导入的外源基因随机地插入到宿主基因组时,如果被导入到转录活跃区,就有可能进行高水平的转录,如果外源基因插入转录不活跃区,则只能进行低水平的转录或不能转录。
按照染色质高级结构组织的环状结构模型,核基质结合区(matrixattachmentregions,MARs)作为边界元件与核基质结合,使两个MAR之间的基因片段被界定成一个独立的染色质环(1oop),并作为隔离子(insulator)阻挡邻近染色质区的顺式调控元件对环内基因的影响,使位于染色体环内的基因可作为一独立的表达调控单位而存在。
MAR可能使转基因在受体基因组整合后形成独立的环状结构,从而提高转基因的表达水平并减少转基因在不同株系表达差异2.转录水平的基因沉默发生在转录水平上的转基因沉默叫做转录失活。
反向重复的基因或转基因可以进行异位配对,配对的DNA作为信号,使DNA异染色质化或从头甲基化,这样转录过程就会受到抑制。
此外,DNA-RNA协同(association)也是造成转录水平基因沉默的原因之一。
(1)转移基因及其启动子甲基化甲基化是活细胞中最常见的一种DNA其价修饰形式,它通常发生在DNA的GC和CN G序列的C碱基上,C甲基化的频率在哺乳动物及高等植物中部比较高。
甲基化修饰在基因表达、植物细胞分化以及系统发育中起着重要的调节作用。
基因沉默
Hale Waihona Puke 共抑制• 共抑制现象普遍存在于转基因植物中。 共抑制的发生是由于外源基因编码区与 受体细胞基因间存在同源性而导致外源 基因与内源基因的表达同时受到抑制。
基因压制
• Cogoni在粗糙脉抱霉的转化实验中发现, 外源基因可以抑制自身和相应内源基因 的表达,他们把这一现象定为基因压制。 他们发现,基因压制是可逆的,而且这 种逆转会伴随有外源拷贝的丢失。基因 压制发生在转录后水平,导致已复制的 稳定态mRNA大量减少。
转录水平上的基因沉默
• 转录水平基因沉默是指对基因专一的细 胞核RNA合成的失活,它的发生主要是 由于基因无法被顺利转录成相应的RNA 而导致基因沉默。
引起转录水平基因沉默的 机制主要有以下几种:
• • • • • .基因及其启动子甲基化 基因及其启动子甲基化 同源基因间的反式失活 后成修饰作用 重复序列 位置效应
2 基因沉默的和分类及机制
• 根据作用部位和作用机理的不同,将基因 沉默分为转录水平上的基因沉默 (Transcriptional gene silen-cing,TGS) 和转录后基因沉默(Post transcriptional gene silencing,PTGS),TGS发生在细胞 核内,一般由于启动子失活而导致基因转 录无法正常进行,而PTGS则是指基因能 正常转录
转录后基因沉默
• 指基因在细胞核内能稳定转录,但在细 胞质里却无相应稳定态mRNA 存在的现 象。与转录水平基因沉默不同,转录后 水平基因沉默具有逆转性,即受抑制基 因通过减数分裂可以恢复表达活性,表 现为减数分裂不可遗传性。
已发现主要有以下几种转 录后水平基因沉默现象
• 共抑制 • 基因压制 • RNA 干扰
基因沉默技术:治疗遗传性疾病的新希望
基因沉默技术:治疗遗传性疾病的新希望在医学的广阔天空中,基因沉默技术如同一颗新星,其光芒正在逐渐照亮治疗遗传性疾病的未来。
这项技术,被科学家们形象地比喻为“分子剪刀”,能够精确地剪除或修复导致疾病的基因序列,从而为患者带来新的希望。
首先,让我们来了解什么是基因沉默技术。
简单来说,它是一种通过特定的分子机制,使特定基因的表达受到抑制或完全停止的技术。
这就像是给有问题的基因按下了“静音键”,阻止它继续制造有害的蛋白。
那么,这项技术为何能成为治疗遗传性疾病的新希望呢?让我们来看几个例子。
首先,对于一些由单一基因突变引起的疾病,如囊性纤维化、镰状细胞贫血等,基因沉默技术可以直接针对这些突变基因进行干预,从根本上解决问题。
其次,对于一些复杂的多基因疾病,如癌症、心脏病等,虽然不能直接治愈,但基因沉默技术可以作为一种辅助治疗手段,帮助减轻症状或延缓病程。
当然,任何新技术的出现都会伴随着挑战和争议。
基因沉默技术的安全问题是人们关注的焦点之一。
毕竟,我们是在对生命的基本单位——基因进行操作,稍有不慎就可能引发严重的后果。
此外,如何确保技术的准确性和有效性,也是科学家们需要不断探索的问题。
尽管如此,我仍然对基因沉默技术抱有乐观的态度。
我相信,随着科学研究的深入和技术的进步,这些问题最终将得到解决。
而且,与其他治疗方法相比,基因沉默技术具有不可比拟的优势。
它不仅可以针对病因进行治疗,还可以实现个性化医疗,根据每个患者的具体情况制定治疗方案。
在我看来,基因沉默技术就像是一把双刃剑。
一方面,它为我们提供了治疗遗传性疾病的新途径;另一方面,它也带来了新的挑战和风险。
我们需要谨慎而明智地使用这项技术,确保它真正造福于人类。
最后,我想用一个比喻来结束这篇文章:基因沉默技术就像是一艘航船,正驶向未知的海域。
虽然前方可能充满了风浪和暗礁,但只要我们坚定信念、勇往直前,就一定能够到达理想的彼岸。
在这个过程中,科学家、医生和患者都需要携手合作,共同面对挑战、分享成果。
基因沉默技术的原理及应用
基因沉默技术的原理及应用1. 引言基因沉默技术是一种用于研究基因功能和调控机制的重要方法。
它能够通过抑制特定基因的表达来观察其对细胞和生物体的影响,为我们揭示基因在生物体内的功能和相互作用提供了有效的手段。
本文将介绍基因沉默技术的原理以及其在基础研究和应用方面的相关实验技术。
2. 基因沉默技术的原理基因沉默技术主要通过RNA干扰(RNA interference,RNAi)和基因编辑技术实现。
以下将分别介绍这两种技术的原理。
2.1 RNA干扰(RNAi)RNA干扰是一种通过介导RNA分子与特定的mRNA相互作用来沉默目标基因表达的方式。
其基本原理是通过引入双链RNA(dsRNA)或小干扰RNA(siRNA)分子,利用细胞内的RNA诱导酶(RNA-induced silencing complex,RISC)将这些RNA分子切割成小片段,并通过与靶标mRNA互补序列的结合,诱导腺苷酸转化酶(adenosine deaminase,APOBEC)催化酶将目标mRNA降解,进而抑制基因的表达。
RNA干扰技术已经得到广泛应用,主要包括以下几个方面: - 基因功能研究:通过沉默特定基因,观察其对细胞生长、分化和功能的影响,从而揭示基因功能和调控机制。
- 药物筛选:利用RNA干扰技术可以高通量筛选候选药物,加速新药研发过程。
- 疾病治疗:RNA干扰技术可用于治疗基因突变引起的疾病,例如肿瘤和遗传性疾病等。
2.2 基因编辑技术基因编辑技术可以通过改变基因组DNA的序列来实现对特定基因的沉默。
CRISPR-Cas9技术是目前最常用的基因编辑技术之一。
其基本原理是利用Cas9蛋白和RNA分子形成复合物,通过与目标基因的DNA序列互补结合,引导Cas9蛋白在目标位点上产生双链切割。
随后,细胞内自身的修复机制(如非同源末端联合修复)介导修复切割部位,导致目标基因的功能缺失或沉默。
基因编辑技术在基础研究和临床应用上具有广阔的前景,如下所示: - 基因功能验证:通过编辑特定基因,验证其对生物体生理和病理过程的影响,从而鉴定相关疾病发病机制。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《细胞》:不依赖于RNAi的基因沉默机制被发现来自瑞士日内瓦大学细胞生物学系的研究人员发现了一种不依赖于RNAi(RNA干扰)的基因沉默机制,这为进一步揭示生物体中基因沉默的多样化,以及功能作用提供了重要信息。
这一研究成果公布在最新一期的《细胞》(Cell)杂志上。
RNA沉默存在两种既有联系又有区别的途径:siRNA(small interference RNA)途径和miRNA(microRNA)途径。
siRNA途径是由dsRNA(double-stranded RNA)引发的,dsRNA被一种RNaseⅢ家族的内切核酸酶(RNA- induced silencing complex,Dicer)切割成21-26nt长的siRNA,通过siRNA指导形成RISC蛋白复合物(RNA-induced silencing complex)降解与siRNA序列互补的mRNA而引发RNA沉默。
而miRNA途径中miRNA是含量丰富的不编码小RNA(21-24个核苷酸),由Dicer酶切割内源性表达的短发夹结构RNA(hairpin RNA,hpRNA)形成。
miRNA同样可以与蛋白因子形成RISC蛋白复合物,可以结合并切割特异的mRNA而引发RNA沉默。
尽管引发沉默的来源不同,但siRNA 和miRNA都参与构成结构相似的RISC,在作用方式上二者有很大的相似性。
在最近的一项研究中,来自加州大学河畔分校的研究人员发现了一种新的小RNAs分子,而这些小RNAs与近期的研究热点PIWI-interacting RNAs (piRNAs)和repeat-associated siRNAs (rasiRNAs)也不相同,这说明了小RNA家族和小RNA介导的基因调控远比之前预想的复杂。
同样在这篇文章中,研究人员也发现基因沉默机制包含有多种途径,他们最新发现酿酒酵母中,反义RNA稳定(Antisense RNA Stabilization)能通过组蛋白去乙酰化引起转录基因沉默。
在之前的研究中,酿酒酵母全基因组研究分析揭示出其转录本中包含了大量的反义RNA(antisense RNAs),以及由外切酶体元件(exosome component)Rrp6调控的基因间转录(intergenic transcripts)。
通过进一步研究,瑞士的研究人员发现当缺失了Rrp6的功能后,两个PHO84反义转录就会变得稳定,并且抑制了PHO84基因的转录。
有趣的是,研究人员在野生型中也发现了同样的现象:在时间性老化(chronological aging)的过程中Rrp6功能缺失也能稳定PHO84反义转录。
上位性和染色质免疫共沉(Epistasis and chromatin immunoprecipitation)实验结果说明Rrp6功能的缺失与PHO84基因以及邻近基因的Hda1组蛋白去乙酰化的补充有关,但是组蛋白的去乙酰化受限于PHO84基因,这又说明Hda1活性依赖于反义RNA。
因此敲除反义产物,即使是在缺失Rrp6的条件下也会阻碍PHO84基因抑制。
这些数据表明反义转录的稳定通过不同于转录干扰的一种机制导致了PHO84基因抑制,而Rrp6功能调节则通过RNA依赖性表观遗传修饰调控基因。
基因沉寂基因沉寂(Gene Silencing) 也可以被称为“基因沉默”。
基因沉寂是真核生物细胞基因表达调节的一种重要手段。
在染色体水平,基因沉寂实际上是形成异染色质(Heterochromatin)的过程,被沉寂的基因区段呈高浓缩状态。
定义RNAi与转录后基因沉默(post-transcriptional gene silencing and transgene silencing)在分子层次上被证实是同一种现象。
原理基因沉寂需要经历不同的反应过程才能实现,包括组蛋白N端结构域的赖氨酸残基的去乙酰基化加工、甲基化修饰(由甲基转移酶催化,修饰可以是一价、二价和三价甲基化修饰,后者又被称为'过度’甲基化修饰(Hypermethylation) ) 、以及和甲基化修饰的组蛋白结合的蛋白质(MBP)形成“异染色质”,在上述过程中,除了部分组蛋白的N端尾部结构域需要去乙酰化、甲基化修饰之外,有时也许要在其他的组蛋白N端尾部结构域的赖氨酸或精氨酸残基上相应地进行乙酰化修饰,尽管各种修饰的最终结果会导致相应区段的基因“沉寂”失去转录活性。
作用这个“原则”就是目前尚没有真正完全清楚的“组蛋白密码”(Histone Code)。
能够与甲基化组蛋白结合的蛋白质有sir1/2/3/4,这是一组被称为"Silencing Informative Repressor"的蛋白,其中,Sir2就是上文中的“去乙酰化”酶,而Sir1/3/4则负责与甲基化修饰的组蛋白结合"沉寂”相应的染色质为异染色质。
此外,基因沉寂也和DNA的甲基化修饰有关,比如在真核生物基因组中的许多基因的5‘端分布有长约1KB( 千碱基对)的“CpG"岛序列(CpG island),其中的“C"芳香环5位可被甲基化修饰,之后,与甲基化修饰的DNA结合蛋白形成“沉寂"区段,使其下游基因不能表达;另外,非编码的RNA分子(non-coding RNA)也参与“基因沉默”过程。
这一类型常见于含有重复DNA序列的染色质区,如着丝粒部位的基因沉寂就需要非编码RNA分子的参与。
简言之,基因沉寂或者基因沉默是涉及组蛋白甲基化、去乙酰化、乙酰化,DNA的甲基化修饰,甲基化修饰组蛋白结合蛋白Sir2/3/4,甲基化DNA结合蛋白,非编码RNA等等在内的一系列复杂组分的生理反应过程。
基因沉寂导致相应区段内的遗传信息不能被转录。
详细内容基因沉默现象首先在转基因植物中发现,接着和线虫、真菌、昆虫、原生动物以及才鼠中陆续发现。
大量的研究表明,环境因子、发育因子、DNA修饰、组蛋白乙酰化程度、基因拷贝数、位置效应、生物的保护性限制修饰以及基因的过度转录等都与基因沉默有关。
但总的看来,基因沉默发生在两种水平上,一种是由于DNA甲基化、异染色质化以及位置效应等引起的转录水平上的基因沉默(tran-scriptional gene silencing,TGS),另一种是转录后基因沉默(post-transcriptional gene silen-cing,PTGS),即在基因转录后的水平上通过对靶标RNA进行特异性降解而使基因失活。
在这两种水平上引起的基因沉默都与基因的同源性有关,称为同源依赖性的基因沉默(homology-dependent gene silencing,HDGS)。
PTGS PTGS在多种生物中有共性,对PTGS的激活和与其相关的RNA降解调控过程有了初步的认识。
也发现植物病毒在转基因植物和非转基因植物中都能和转基因一样诱发转录后基因沉默。
令人吃惊的是,转基因植物的共抑制现象(转基因与同源的内源基因一起失活)、转基因植物的病毒抗性和非转基因植物对病毒正常自然侵染的抗性、真菌的quelling现象(真菌中的共抑制)、各种动物的RNA干扰(RNA interference,RNAi)以及转座因子的转座失活等这些表面看来完全不相关的现象中竟然存在着非常相似的基因沉默机制,即PTGS。
这种基因沉默可能是生物体的本能的反应,因为无论是转基因、转座因子还是病毒,对植物而言都是诱发突变的外来侵入的核酸,植物为保护自己,在长期的生物进化中,形成了基因沉默这种限制外源核酸入侵的防卫保护机制。
在线虫Caenorhabditis elegans中,RNAi敏感性缺失突变体中转座子的转座活性增强,表明转座子的转座失活是被一种类似PTGS的过程调控的,这一过程与RNAi作用有关,是通过细胞内双链RNA互作引起同源特异性的RNA降解。
PTGS中的RNA在细胞质中的特异性降解并不需要RNA结合到核糖体上,这与通常的RNA降解代谢调控需要与翻译相关连不同。
Bass对RNAi激发的RNA特异性降解机制进了体外研究,发现通过添加外源的双链RNA或靶标mRNA可以激活PTGS,这与早期在植物中发现的双链RNA介导PTGS一致。
通过对发生PTGS的转基因植物进行嫁接实验和分析植物病毒病的恢复现象观察到,PTGS是一种系统性的过程,称为系统获得性沉默(systemic acquired silencing,SAS)。
PTGS的系统传播性在真菌和线虫中也得到了证明。
进一步研究发现,转基因或病毒侵染介导的PTGS植物中普遍存在着大量的序列特异性正义和反义的大约25个核苷酸的小分子RNA,而正常的非转基因植物和没有发生PTGS的植物中则没有。
这些小分子RNA作为信号分子,在植物中与特定的运输蛋白特异结合,防止被核酸酶的降解,通过胞间连丝和韧皮部筛管运送到植物体的各个部位,使PTGS具有系统持久性。
这一运转过程与植物病毒在植物体内的运输有着十分相近的机制。
这些-25nt RNA的积累需要转基因的转录或病毒的复制,与其它双链RNA等多种异常RNA相比,-25nt RNA对于PTGS的激发、靶标RNA的特异性降解以及PTGS的系统性维持更为重要。
病毒对RNA活性影响早在20世纪70年代初人们就发现,病毒或类病毒侵入植物后,RNA 依赖性的RNA聚合酶(RNA-dependent RNA polymerase,RdRP)的活性明显提高。
RdRP是生物体内普遍存在的一种RNA聚合酶,在体外能以单链RNA或单链DNA甚至以双链RNA 为模板,合成与模板互补RNA,合成的cRNA可长达100个核苷酸。
1993年,Lindbo等认为在PTGS植物中的RdRP与PTGS同源依赖性的RNA特异性降解有关。
最近Mour-rain 等从缺失转基因介导的PTGS拟南芥突变体中分离的sgs2(suppressor of gene silencing)和sde1(silencing defective)两个基因与番茄中的RdRP基因十分相似,支持了Lindbo的观点。
粗糙脉孢菌Neurospora crassa的qde-2(quilling-defective gene)和线虫C.elegans的rde-1(RNA interference-deficient gene)与蕃茄的RdRP基因也具有很高的同源性。
RdRP基因剔除实验证明,RdRP对RNAi和PTGS尤为重要。
这些研究结果表明,从比较低等的生物藻类、真菌到高等的植物再到动物线虫、锥虫、果蝇等中可能存在着一个由共同祖先进化来的相似的抵抗外来DNA侵入自身基因组的本能防卫机制。
RNAi引发的PTGS作为生物体中一种不完全的原始的生物免疫系统,在植物抗病毒中研究得比较详细。
