双键和硼酸的偶联
偶联剂的种类和特点及应用[资料]
![偶联剂的种类和特点及应用[资料]](https://img.taocdn.com/s3/m/cbf65c34182e453610661ed9ad51f01dc28157b6.png)
偶联剂的种类和特点及应用偶联剂的种类和特点及应用偶联剂是一种重要的、应用领域日渐广泛的处理剂,主要用作高分子复合材料的助剂。
偶联剂分子结构的最大特点是分子中含有化学性质不同的两个基团,一个是亲无机物的基团,易与无机物表面起化学反应;另一个是亲有机物的基团,能与合成树脂或其它聚合物发生化学反应或生成氢键溶于其中。
因此偶联剂被称作“分子桥”,用以改善无机物与有机物之间的界面作用,从而大大提高复合材料的性能,如物理性能、电性能、热性能、光性能等。
偶联剂用于橡胶工业中,可提高轮胎、胶板、胶管、胶鞋等产品的耐磨性和耐老化性能,并且能减小NR用量,从而降低成本。
偶联剂的种类繁多,主要有硅烷偶联剂、钛酸酯偶联剂、铝酸酯偶联剂、双金属偶联剂、磷酸酯偶联剂、硼酸酯偶联剂、铬络合物及其它高级脂肪酸、醇、酯的偶联剂等,目前应用范围最广的是硅烷偶联剂和钛酸酯偶联剂。
1 硅烷偶联剂硅烷偶联剂是人们研究最早、应用最早的偶联剂。
由于其独特的性能及新产品的不断问世,使其应用领域逐渐扩大,已成为有机硅工业的重要分支。
它是近年来发展较快的一类有机硅产品,其品种繁多,结构新颖,仅已知结构的产品就有百余种。
1945年前后由美国联碳(UC)和道康宁(DowCorning)等公司开发和公布了一系列具有典型结构的硅烷偶联剂;1955年又由UC公司首次提出了含氨基的硅烷偶联剂;从1959年开始陆续出现了一系列改性氨基硅烷偶联剂;20世纪60年代初期出现的含过氧基硅烷偶联剂和60年代末期出现的具有重氮和叠氮结构的硅烷偶联剂,又大大丰富了硅烷偶联剂的品种。
近几十年来,随着玻璃纤维增强塑料的发展,促进了各种偶联剂的研究与开发。
改性氨基硅烷偶联剂、过氧基硅烷偶联剂和叠氮基硅烷偶联剂的合成与应用就是这一时期的主要成果。
我国于20世纪60年代中期开始研制硅烷偶联剂。
首先由中国科学院化学研究所开始研制γ官能团硅烷偶联剂,南京大学也同时开始研制α官能团硅烷偶联剂[1]。
硼酸及其衍生物
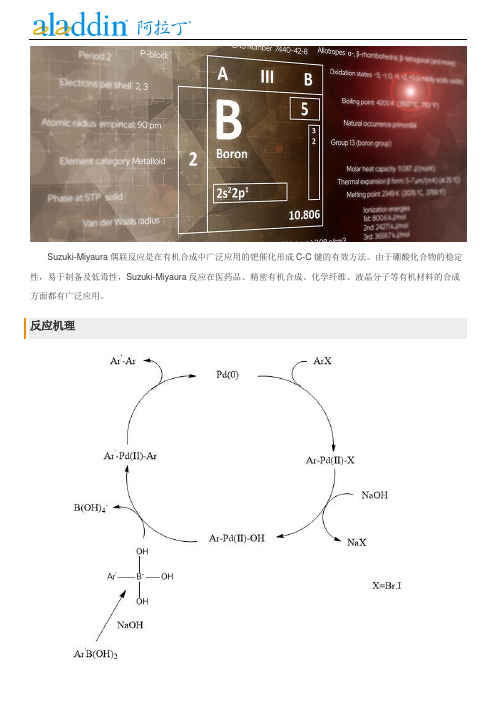
Suzuki-Miyaura偶联反应是在有机合成中广泛应用的钯催化形成C-C键的有效方法。
由于硼酸化合物的稳定性,易于制备及低毒性,Suzuki-Miyaura反应在医药品、精密有机合成、化学纤维、液晶分子等有机材料的合成方面都有广泛应用。
反应机理通常碳硼键的结合力较强(有机硼化物稳定),金属迁移不好发生。
加入碱,使生成更容易发生金属迁移的硼酸盐。
近年来随着催化剂和方法的发展,Suzuki偶联反应范围不再局限于硼酸化合物,硼酸酯、三氟硼酸钾盐和有机硼烷等都可以用来代替硼酸化合物。
硼酸√ 烷基硼酸4-三氟甲基苄基硼酸频哪醇酯475250-46-5√ 烯基硼酸√ 芳基硼酸(* 一元取代* 二元取代* 三元取代* 四元取代* 五元取代* 无取代)* 一元取代(部分):4-甲基-1-萘硼酸103986-53-4 * 二元取代(部分):4-乙氧羰基-2-硝基苯硼酸(含有数量不等的酸酐) 5785-70-6 * 三元取代(部分):2-溴-6-氟-3-丙氧基苯基硼酸849052-20-6 * 四元取代:* 五元取代:* 无取代:√ 杂环硼酸(部分)中文名称Cas硼酸酯(部分)硼酸酯参与的Suzuki-Miyaura偶联反应,可以解决与合成试剂不兼容的问题。
另外,也能避免芳基硼酸加热干燥过程中脱水形成酸酐降低产物得率的问题。
4-甲氧羰基苯硼酸频哪醇酯171364-80-0MIDA酯甲基亚氨二乙酸Methyliminodiacetic acid(MIDA)酯是可参与Suzuki-Miyaura偶联反应的一类新型试剂。
MIDA酯易于处理,在空气中是稳定的,并且可在温和的水碱性条件下容易脱保护。
MIDA酯中,sp3杂化的硼原子被两个五元环固定,极大地增加了硼酸的稳定性,利于合成复杂的分子。
中文名称Cas三氟硼酸钾盐在C-C键形成反应(如Suzuki-Miyaura)中,三氟硼酸钾盐(R-BF3K)是可有效替代有机硼酸盐的一类试剂。
suzuki偶联反应教学文案

铃木章凭借研发“有机合成中的钯催化的交叉 偶联”与美国科学家理查德赫克、日本科学家 根岸英一共同获得2010年诺贝尔化学奖。
Suzuki-Miyaura交叉偶联的反应机理
这是个普通的催化循环过程,主要包括三 个步骤,它们分别是: (1)氧化加成(oxidative addition) (2)转移金属化(transmetalation) (3)还原消除(reductive elimination)
Suzuki偶联反应的概念
Suzuki反应(铃木反应),也称作Suzuki偶联反应 、是在过渡金属催化的芳基偶联反应中,在钯配 合物Pd(PPh3)4催化下,芳基或烯基的硼酸或硼酸 酯与氯、溴、碘代芳烃或烯烃发生交叉偶联。该 反应因具有反应条件温和、可容忍多种活性官能 团、受空间位阻影响不大、产率高以及芳基硼酸 经济易得且对潮气不敏感等优越性而成为普遍适 用的C一 C键偶联方法,倍受有机及高分子合成工 作者的青睐。
Br +
N
O 2N
Pd (PPh3)4 B(O H )2
aq. N a2CO 3
benzene
M eO O C N
N O 2
J . O rg. Chem . 1984, 49, 5237.
H O
O H
BSB
H O
O H
O B
S
O B
O
O
N O 2
Br
R
O 2N
S
5% m m ol Pd(PPh3)4 K 2CO 3 D M E
4. 反应:在Suzuki芳基偶联反应中,通常要求芳基硼酸的量 相对于卤代芳烃过量10%,以保证应有的产率,因为脱硼作
用会造成芳基硼酸的损失,尤其是带吸电子的芳基硼酸这种
suzuki_-miyaura偶联反应_概述说明

suzuki -miyaura偶联反应概述说明1. 引言1.1 概述Suzuki-Miyaura偶联反应是有机合成中一种重要的偶联反应方法,它以其高效、高选择性和广泛的底物适用性而受到广泛关注。
该反应以有机卤化物和有机硼酸酯为底物,在铜盐和配体的催化下进行,生成相应的偶联产物。
该反应可以构建碳-碳键和碳-氮键,常用于构建芳香化合物、杂环化合物等复杂分子结构。
1.2 文章结构本文将首先介绍Suzuki-Miyaura偶联反应的原理,包括反应机理、催化剂和底物选择性以及该反应的发展历史与应用领域。
然后会详细说明该反应的条件与步骤,包括底物准备与选择、反应条件控制以及步骤与工艺优化。
接下来将介绍实验操作与注意事项,包括实验操作步骤、常见问题与解决方法以及安全注意事项。
最后我们将给出结论部分,总结Suzuki-Miyaura偶联反应的优势和局限性,并展望其在未来发展中的重要性,并提出研究方向和未解决问题。
1.3 目的本文的目的是介绍Suzuki-Miyaura偶联反应及其在有机合成中的重要性。
通过对该反应原理、条件与步骤以及实验操作和注意事项的详细讲解,旨在帮助读者更好地理解和应用该反应,并掌握其正确操作方法。
同时,我们也将指出该反应存在的局限性,并展望其在未来发展中的前景和研究方向,希望能够激发更多科学家对该领域的兴趣并促进相关研究的推进。
2. Suzuki-Miyaura偶联反应的原理2.1 反应机理Suzuki-Miyaura偶联反应是一种重要的C-C键形成方法,其基本反应机理可被概括为以下几个步骤。
首先,芳香环上的硼酸和卤代烷基(或烯基)底物在催化剂的存在下发生吕得霉素配合物与底物之间的交换反应,生成含有硼酸酯官能团的中间体。
接下来,中间体与有机卤化物经过还原消除反应,在钯催化剂参与下进行脱羧作用,生成新的碳-碳键以及相应的芳香环。
最后,在正常工作温度条件下,溶剂中反应产物与锡盐或锂盐等强碱进行水解,得到目标产物。
suzuki偶联反应

Suzuki-Miyaura交叉偶联反应机理及其在有机合成中的应用学院:化学学院专业:有机化学学号:姓名:一、Suzuki-Miyaura 交叉偶联反应概念Suzuki 反应(铃木反应),也称作Suzuki 偶联反应、Suzuki-Miyaura 反应(铃木-宫浦反应),是一个较新的有机偶联反应,是在钯配合物催化下,芳基或烯基的硼酸或硼酸酯与氯、溴、碘代芳烃或烯烃发生交叉偶联。
Z=Cl,Br,I自从1981年Suzuki 等报道了通过钯催化的有机硼化学物和卤代烃可以在很温和的条件下发生偶联反应制备不对称联芳烃以后,为芳-芳键的形成展开了一个新的领域[1]。
Suzuki-Miyaura 交叉偶联反应被证明是目前制备联芳基及其衍生物最为广泛利用的方法,因为其具有很强的底物适应性及官能团耐受性,常用于合成多烯烃、苯乙烯和联苯的衍生物,从而应用于众多天然产物、有机材料的合成中。
铃木章也凭借此贡献与理查德·赫克、根岸英一共同获得2010年诺贝尔化学奖。
二、Suzuki-Miyaura 交叉偶联反应机理Suzuki-Miyaura 交叉偶联的反应机理通常是一个普通的催化循环过程。
这个过程主要包括三个步骤:(1)氧化加成(oxidative addition) (2)转移金属化(transmetalation) (3)还原消除(reductive elimination)Ar-Pd-Ar 1Ar-ArPd(0)ArXArPdXArPdOHNaOHNaXB(OH)4ArB -(OH)3NaOHArB(OH)2氧化加成还原消除转移金属化ZB(OH)2BrZ+3% Pd(PPh 3)4Benzene, Na 2CO 3/H 2O首先,卤代芳烃与Pd(0)氧化加成后,与1mol 的碱生成有机钯氢氧化物中间物种,取代了键极性较弱的钯卤键,这种含有强极性的Pd-OH 的中间体具有非常强的亲电性;同时另1mol 的碱与芳基硼酸生成四价硼酸盐中间物种,具有非常强的富电性,有利于向Pd 金属中心迁移。
偶联反应

分子间Heck反应
端基烯烃与卤代芳香烃发生分子间Heck 反应,是研究最早 的一类反应。这类反应已经成为芳烃烷基化重要反应。
1.常规分子间 Heck反应
分子间Heck反应
2.不对称分子间 Heck反应
分子间Heck反应
3.非常用离去基团的 Heck反应
3.1重氮盐参与的Heck反应不需要膦催化剂和胺,条件温和,
于不需要任何碱的存在。
分子间Heck反应
Tips:
1、该类反应在卤代物中,卤素的β位的碳原子上不能有 SP3 杂化的氢原子。主要是因为这类卤代物形成烷基钯络合物时,
氢化钯的消除反应速度大于烯烃的加成反应,因此仅有消除产物。
2、当有强烈供电子基团时,芳基溴参与的反应收率也很 低。其主要原因是在反应中膦配体被季化与卤代物被还原。当使用
有机硼试剂的合成 1.通过金属有机试剂制备单取代芳基硼酸
1.1.通过Grinard试剂制备单取代芳基硼酸
1.2.通过有机锂试剂制备单取代芳基硼酸
有机硼试剂的合成
2.通过二硼烷频哪酯制备芳基硼酸酯
对于分子中带有酯基、氰基、硝基、羰基等官能团的芳香卤代物来说, 无法通过有机金属试剂来制备相应的芳基硼酸。
Suzuki偶联反应的应用
普通操作 在水的存在下,加入催化剂、碱和有机溶剂,加热回流一段合理
的时间完成反应,但反应体系必须全程严格控制在无氧的环境下。
1.普通体系Suzuki偶联反应
Suzuki偶联反应的应用
2.大位阻芳基硼酸参与Suzuki偶联反应
收率低
解决措施:
强碱水溶液如NaOH或Ba(OH)2 苯和DME为溶剂 将大位阻芳基硼酸转化为硼酸酯
间的交叉偶联反应通常被称之为Sonogashira 反应
Liebeskind_–_Srogl_偶联反应
反 应 特 点
1.Liebeskind-Srogl 去硫偶联的应用在全合成中的 优点是具有广泛的一般性和官能团容忍性。
2.大多数硼酸有对空气,水分稳定,毒性也比较 低等优点。 3.传统的 Suzuki-Miyaura 偶联中都有碱的存在, 但含氧的碱不利于Liebeskind-Srogl 反应。在本 反应中,相对于硼提出了氢键,三重态化合物作 为活泼的中间体。由于硼酸与羧酸盐之间存在的 氢键,使反应能量降低,有利于反应的进行。 4.反应条件温和,在中性条件里进行。
反 应 简 介
2000 年,Liebeskind 和 Srogl 提供了一种 在中性条件下经过渡金属催化硫酯和有机 硼酸的去硫偶联合成酮类化合物的重要方 法。由于反应可在中性条件下进行,因此 可以应用于对碱敏感的偶联体,从而拓展 了钯催化的 C-C 交叉偶联反应的应用范围。 十年来,Liebeskind-Srogl 反应得到了系 统的发展。其中,有机硫偶联体已由硫酯 被逐渐扩展到杂芳基硫醚、炔基硫醚、环 状硫代酰胺和异硫脲等。此外,对环丁烯 二酮类插烯型硫酯的 Liebeskind-Srogl 反 应也有初步报道。Liebeskind-Srogl 反应 是经钯催化在温和的条件下由硫酯和硼酸 合成酮的方法。
Liebeskind – Srogl 偶联反应
反 应 背 景
大多数偶联方法是亲电子有机金属卤 化物和亲核有机金属试剂发生偶联反应, 但也有利用有机金属硫化物作为亲核试剂。 大多数硼酸有对空气,水分稳定,毒性也 比较低等优点。因此,现在众多的偶联方 法之中,硼酸作为偶联的反应物的方法越 来越受到人们的关注。由于有机金属硫化 合物与硼酸的偶联反应能很容易的得到低 毒性的稳定分子,所以具有很高的合成价 值。
Байду номын сангаас 发 展 与 应 用
suzuki偶联反应
常用于反应的亲电试剂——卤代芳烃
1 吸电 子 基 有利于卤代芳烃与Pd(0)氧化加成
2 多卤代芳烃在反应中存在着明显的化学选择性
Suzuki反应中,卤代物的活性顺序为I>Br>Cl,碘代、溴代和氯代芳烃分 别在室温、80℃和135℃下,可与Pd(PPh3)4氧化加成,因此在多卤代物 中存在明显的活性选择性:
Suzuki反应的特点
1. 溶剂:在极性溶剂里此偶联反应的产率可以得到很大的 提高:DMSO≥ DMF > dioxane > toluene。 2. 碱:经过验证,KOAc是应用于这个反应最合适的碱,
其他的如K3PO4或K2CO3这些碱性略强的碱会进一步使原 料芳基卤发生自偶联反应的结果。
Suzuki反应的问世
日本北海道大学Akira Suzuki教授发现
B(OH)2 + Br 3% Pd(PPh3)4 Z Benzene, Na2CO3/H2O Z
N. Miyaura, T. Yanagi, and A. Suzuki. Synth. Commun, 1981, 11(7), 513-519
Bun H H + B(OH)2 Ph Br
Pd催化剂 碱
Bun Ph
+
Bun
Ph
“头”-“头”偶联
“头”-“尾”偶联
3. 催化剂:对于制备溴代物和碘代物相应的芳基硼酸酯,
Pd(dppf)Cl2一般可以得到很好的结果,又由于其具有易于 反应的后处理的优点,因此是实验室目前最常用的一类催 化剂。
4. 反应:在Suzuki芳基偶联反应中,通常要求芳基硼酸的量 相对于卤代芳烃过量10%,以保证应有的产率,因为脱硼作 用会造成芳基硼酸的损失,尤其是带吸电子的芳基硼酸这种 脱硼作用更为显著,有时候,将芳基硼酸转化为酯后再用于 偶联反应,可减少反应过程中硼酸的损失。
改性硼酸盐晶须用硼酸酯偶联剂的研制
李 玉玲 周 莉 徐 新 宇 赵 园
( 宁 石油化 工 大学 , 宁抚顺 1 3 0 ) 辽 辽 1 0 1
摘 要 :以硼酸 、 乙醇胺 、 甲基丙烯酰氯等为主要原料 , 合成 了改性硼酸盐 晶须用新型 可聚合硼酸酯偶
联剂 , 由红 外 光 谱 I 对 其进 行 表 征 和 确认 。 实验 研 究 了 原 料 配 比 、 聚剂 的选 择 对 硼酸 酯 收率 影 响 , R 阻 并
显 优 于 以 前 通 常 用 于 这 种 体 系 的 硅 烷 偶 联 剂 K 9 1 。为 了进一 步 提高对 硼 酸盐 晶须 的 改性 效 H 2
年 , 晓兰 和梁 国正 等 以硼 酸 与 乙醇 胺 的酯 化 反 胡
应合 成 了硼 酸 三 乙醇 胺 酯 ( E ) 硼 酸 酯 中 富 电 子 B 3 , 的氨基 能与 缺 电子 的硼 原子 配位 , 占据硼 的空 轨道 ,
L u ln ZHOU i XU n— u ZHAO u n I Y —ig L Xi y Y a
( io igS iu nvr t, uh n 10 1Lann C ia La nn hh a U i sy F su l3 0 ,io i ei g,hn )
A BSTRAC T :A o e oy rz b e b r t se u a t n s p e r d b o i cd,eh n lmi e a d meha — n v lp lme ia l o ae e trs r ca twa rpa e y b rc a i f t a o a n n t c r l y h o i e,a d c r c e ie n de tfe y I yo lc lrd n ha a trz d a d i n iid b R. Ex e i n a t d fr w ae i lr t n h ee to f p rme tlsu y o a m t ra a i a d t e s l cin o o poy rz to n i io e e to ha fe t h il fbo i a i se o p i g a e ti i p e e t d, n t l me iai n i h b trs lc in t te fc s t e y ed o rc c d e tr c u ln g n s m lm n e a d he
硼酸酯偶联剂的结构特点
硼酸酯偶联剂的结构特点1.引言1.1 概述硼酸酯偶联剂是一类广泛应用于有机合成和材料科学中的化合物。
它们具有独特的分子结构特点,可以在化学反应中起到连接、稳定和增强材料性能的作用。
硼酸酯偶联剂以其独特的化学性质在许多领域中被广泛研究和应用。
硼酸酯偶联剂的分子结构包含硼、氧和有机基团。
其中,硼酸酯的硼原子与三个氧原子形成一个平面三角形结构。
有机基团则通过硼原子和氧原子之间的化学键与硼酸酯分子相连。
这种结构使得硼酸酯偶联剂具有特殊的反应性和稳定性。
硼酸酯偶联剂的一个显著特点是其与羟基(OH)之间的相互作用。
由于硼酸酯分子中的硼原子和氧原子之间的化学键的极性特点,硼酸酯偶联剂可以与羟基发生氢键作用,形成稳定的配位化合物。
这种配位作用可用于控制化学反应的速率和选择性,从而实现有机合成反应的精确调控。
此外,硼酸酯偶联剂还具有较好的水溶性和热稳定性。
这些特性使得硼酸酯偶联剂可以在许多溶剂系统中有效地应用,并能在高温条件下保持其活性和稳定性。
综上所述,硼酸酯偶联剂具有独特的分子结构特点,包括硼原子与氧原子形成的平面三角形结构和与羟基之间的氢键配位作用。
这些特点使得硼酸酯偶联剂在化学反应中具有广泛的应用前景,并在有机合成和材料科学领域发挥着重要的作用。
1.2 文章结构文章结构部分的内容如下:文章结构:本文分为引言、正文和结论三个部分。
引言部分主要概述硼酸酯偶联剂的性质和应用领域,并介绍了文章的目的。
正文部分将具体讨论硼酸酯偶联剂的定义、作用,以及其结构特点。
其中,通过对硼酸酯偶联剂的化学结构进行分析,探讨其分子间键合、原子组成和空间排布等方面的特点。
结论部分将对硼酸酯偶联剂的结构特点进行总结,并展望其在未来的应用前景。
同时,还将对硼酸酯偶联剂开展可能的改进方向和研究方向进行探讨。
通过以上的文章结构,读者可以系统了解硼酸酯偶联剂的结构特点以及其在实际应用中的潜力,并为相关领域的科研工作者提供一定的参考和启示。
1.3 目的本文的主要目的是对硼酸酯偶联剂的结构特点进行详细的介绍和分析。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1111
双键和硼酸的偶联是一种化学反应,涉及将硼酸基团连接到双键上。
这种偶联反应可以通过多种方法实现,包括使用手性膦-镍络合物催化醛、二烯烃和芳基硼酸的三组分偶联反应,或者通过镍氢催化的不对称C(sp³)-C(sp³)偶联反应等。
在手性膦-镍络合物催化的反应中,醛、二烯烃和芳基硼酸三者发生偶联,生成高烯丙基醇。
而在镍氢催化的反应中,α-芳基或α-硼烷基可以稳定支链的烷基-镍中间体,从而减缓“链行走”反应速率,进而降低甚至抑制副反应的发生。
双键和硼酸的偶联反应在化学合成中具有重要的应用价值,可以用于制备各种化合物。
在实际应用中,选择合适的催化剂和反应条件对于获得良好的反应结果至关重要。
