组蛋白修饰及其功能(乙酰化,甲基化,磷酸化等)-于凯 PPT
合集下载
组蛋白修饰及其功能(乙酰化,甲基化,磷酸化等)-于凯讲解学习

组蛋白修饰及其功能
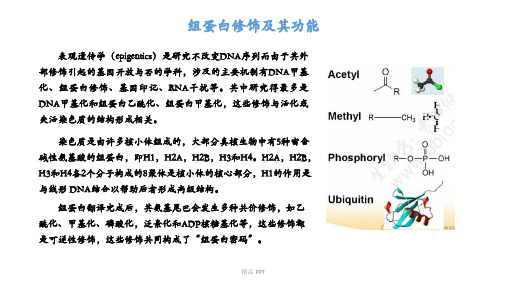
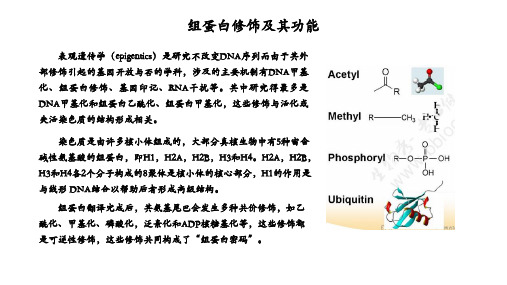
表观遗传学(epigentics)是研究不改变DNA序列而由于其外 部修饰引起的基因开放与否的学科,涉及的主要机制有DNA甲基 化、组蛋白修饰、基因印记、RNA干扰等。其中研究得最多是 DNA甲基化和组蛋白乙酰化、组蛋白甲基化,这些修饰与活化或 失活染色质的结构形成相关。
染色质是由许多核小体组成的,大部分真核生物中有5种富含 碱性氨基酸的组蛋白,即H1,H2A,H2B,H3和H4。H2A,H2B, H3和H4各2个分子构成的8聚体是核小体的核心部分,H1的作用是 与线形 DNA结合以帮助后者形成高级结构。
组蛋白翻译完成后,其氨基尾巴会发生多种共价修饰,如乙 酰化、甲基化、磷酸化,泛素化和ADP核糖基化等,这些修饰都 是可逆性修饰,这些修饰共同构成了“组蛋白密码”。
1. 组蛋白乙酰化
核心组蛋白乙酰化反应多发生在核心组蛋白 N端碱性氨基 酸集中区的特定 Lys 残基。组蛋白乙酰化由组蛋白乙酰转移酶 (histone acetyltransferase,HAT)和组蛋白去乙酰化酶(histone deacetylase,HDAC)协调进行。HAT通过将乙酰辅酶 A 的乙酰 基转移到 Lys 的NH+,中和掉一个正电荷。 HDAC使组蛋白去乙 酰化,与带负电荷的DNA紧密结合,染色质致密卷曲,基因的 转录受到抑制。
2. 组蛋白的甲基化
组蛋白甲基化是由组蛋白甲基化转移酶(histone methyl transferase,HMT)完成的。甲基化可发生在组 蛋白的赖氨酸和精氨酸残基上,而且赖氨酸残基能够 发生单、双、三甲基化,而精氨酸残基能够单、双甲 基化,这些不同程度的甲基化极大地增加了组蛋白修 饰和调节基因表达的复杂性。
局部乙酰化举例
当DNA与核小体尚未解开缠绕时,转录激活因子如糖皮质激素受体可以和DNA上相应 的反应元件(GRE)结合。当结合至GRE之后,糖皮质激素募集共激活因子如CBP到染色 体上的靶转录基因区。此时,共激活因子利用HAT活性使得结合在DNA启动子区域的核心 组蛋白乙酰化,进而使DNA与组蛋白结合减弱,核小体释放,转录因子和RNA聚合酶可以 与DNA上特异的启动子结合,启动靶基因的转录。
表观遗传学(epigentics)是研究不改变DNA序列而由于其外 部修饰引起的基因开放与否的学科,涉及的主要机制有DNA甲基 化、组蛋白修饰、基因印记、RNA干扰等。其中研究得最多是 DNA甲基化和组蛋白乙酰化、组蛋白甲基化,这些修饰与活化或 失活染色质的结构形成相关。
染色质是由许多核小体组成的,大部分真核生物中有5种富含 碱性氨基酸的组蛋白,即H1,H2A,H2B,H3和H4。H2A,H2B, H3和H4各2个分子构成的8聚体是核小体的核心部分,H1的作用是 与线形 DNA结合以帮助后者形成高级结构。
组蛋白翻译完成后,其氨基尾巴会发生多种共价修饰,如乙 酰化、甲基化、磷酸化,泛素化和ADP核糖基化等,这些修饰都 是可逆性修饰,这些修饰共同构成了“组蛋白密码”。
1. 组蛋白乙酰化
核心组蛋白乙酰化反应多发生在核心组蛋白 N端碱性氨基 酸集中区的特定 Lys 残基。组蛋白乙酰化由组蛋白乙酰转移酶 (histone acetyltransferase,HAT)和组蛋白去乙酰化酶(histone deacetylase,HDAC)协调进行。HAT通过将乙酰辅酶 A 的乙酰 基转移到 Lys 的NH+,中和掉一个正电荷。 HDAC使组蛋白去乙 酰化,与带负电荷的DNA紧密结合,染色质致密卷曲,基因的 转录受到抑制。
2. 组蛋白的甲基化
组蛋白甲基化是由组蛋白甲基化转移酶(histone methyl transferase,HMT)完成的。甲基化可发生在组 蛋白的赖氨酸和精氨酸残基上,而且赖氨酸残基能够 发生单、双、三甲基化,而精氨酸残基能够单、双甲 基化,这些不同程度的甲基化极大地增加了组蛋白修 饰和调节基因表达的复杂性。
局部乙酰化举例
当DNA与核小体尚未解开缠绕时,转录激活因子如糖皮质激素受体可以和DNA上相应 的反应元件(GRE)结合。当结合至GRE之后,糖皮质激素募集共激活因子如CBP到染色 体上的靶转录基因区。此时,共激活因子利用HAT活性使得结合在DNA启动子区域的核心 组蛋白乙酰化,进而使DNA与组蛋白结合减弱,核小体释放,转录因子和RNA聚合酶可以 与DNA上特异的启动子结合,启动靶基因的转录。
组蛋白修饰及其功能(乙酰化,甲基化,磷酸化等)(教学课件)
分子效应:乙酰化可能通过对组蛋白电荷以及相互作用蛋 白的影响,增加组蛋白与DNA的排斥力,来调节基因转录。组 蛋白的乙酰化有利于DNA与组蛋白八聚体的解离,核小体结构 松弛,从而使各种转录因子和协同转录因子能与DNA结合位点 特异性结合,激活基因的转录。同时影响泛素与组蛋白的H2A的 结合,导致蛋白质的选择性降解。
精品 PPT
3. 组蛋白的磷酸化
精品Байду номын сангаасPPT
组蛋白共价修饰间的关系
组蛋白的其他修饰方式 相对而言,组蛋白的甲基化修饰方式是最稳定的,所以最适合作为稳定的表观遗传信息。而 乙酰化修饰具有较高的动态,另外还有其他不稳定的修饰方式,如磷酸化、腺苷酸化、泛素 化、ADP核糖基化等等。这些修饰更为灵活的影响染色质的结构与功能,通过多种修饰方式 的组合发挥其调控功能。
•
12、人乱于心,不宽余请。16:10:2516 :10:251 6:10Sunday, October 18, 2020
•
13、生气是拿别人做错的事来惩罚自 己。20. 10.1820 .10.181 6:10:25 16:10:2 5October 18, 2020
•
14、抱最大的希望,作最大的努力。2 020年1 0月18 日星期 日下午4 时10分 25秒16 :10:252 0.10.18
研究表明,组蛋白精氨酸甲基化是一种相对动态 的标记,精氨酸甲基化与基因激活相关,而H3和H4精 氨酸的甲基化丢失与基因沉默相关。相反,赖氨酸甲 基化似乎是基因表达调控中一种较为稳定的标记。
精品 PPT
组蛋白甲基化的调节机制
1. H3-K9甲基化与异染色质的形成:人们曾针对异染色质的形成提出过一个模型:首先组蛋白 脱乙酰酶使H3中的K9、K14脱乙酰化,然后Suv39h1或Clr4对H32K9进行甲基化,H32K9的甲基 化再影响DNA的甲基化,随后甲基化的H32K9做为一个结合位点招募HP1或Swi6蛋白的定位, 最后HP1/Swi6通过它们的shadow染色质结合区域定位在C末端,进而形成异染色质的多聚体。 2. H32K9甲基化对常染色体中基因表达调控的影响: 3. 组蛋白其他位点上发生甲基化与基因表达的关系:大量实验表明H32K9甲基化的功能与基 因沉默有关,但其它位点甲基化可能存在激活转录作用。 4. 组蛋白甲基化与DNA甲基化:H32K9的甲基化可以直接或间接影响DNA 的甲基化,DNA 甲基化可能是组蛋白甲基化的间接结果
精品 PPT
3. 组蛋白的磷酸化
精品Байду номын сангаасPPT
组蛋白共价修饰间的关系
组蛋白的其他修饰方式 相对而言,组蛋白的甲基化修饰方式是最稳定的,所以最适合作为稳定的表观遗传信息。而 乙酰化修饰具有较高的动态,另外还有其他不稳定的修饰方式,如磷酸化、腺苷酸化、泛素 化、ADP核糖基化等等。这些修饰更为灵活的影响染色质的结构与功能,通过多种修饰方式 的组合发挥其调控功能。
•
12、人乱于心,不宽余请。16:10:2516 :10:251 6:10Sunday, October 18, 2020
•
13、生气是拿别人做错的事来惩罚自 己。20. 10.1820 .10.181 6:10:25 16:10:2 5October 18, 2020
•
14、抱最大的希望,作最大的努力。2 020年1 0月18 日星期 日下午4 时10分 25秒16 :10:252 0.10.18
研究表明,组蛋白精氨酸甲基化是一种相对动态 的标记,精氨酸甲基化与基因激活相关,而H3和H4精 氨酸的甲基化丢失与基因沉默相关。相反,赖氨酸甲 基化似乎是基因表达调控中一种较为稳定的标记。
精品 PPT
组蛋白甲基化的调节机制
1. H3-K9甲基化与异染色质的形成:人们曾针对异染色质的形成提出过一个模型:首先组蛋白 脱乙酰酶使H3中的K9、K14脱乙酰化,然后Suv39h1或Clr4对H32K9进行甲基化,H32K9的甲基 化再影响DNA的甲基化,随后甲基化的H32K9做为一个结合位点招募HP1或Swi6蛋白的定位, 最后HP1/Swi6通过它们的shadow染色质结合区域定位在C末端,进而形成异染色质的多聚体。 2. H32K9甲基化对常染色体中基因表达调控的影响: 3. 组蛋白其他位点上发生甲基化与基因表达的关系:大量实验表明H32K9甲基化的功能与基 因沉默有关,但其它位点甲基化可能存在激活转录作用。 4. 组蛋白甲基化与DNA甲基化:H32K9的甲基化可以直接或间接影响DNA 的甲基化,DNA 甲基化可能是组蛋白甲基化的间接结果
组蛋白修饰及其功能(乙酰化,甲基化,磷酸化等)-于凯
组蛋白密码学说的完善: 1. 更好地开发新药。研究组蛋白密码对药物开发具有战略
意义,多种组蛋白修饰酶已成为相关疾病治疗的靶目标。比如,组蛋白去乙酰酶
(HDACs)抑制剂已应用于临床治疗多种肿瘤; 2. 深入探讨遗传调控和表观遗传调控相互作用的网络与不同生物学表型之间的关系;
3. 在控制真核基因选择性表达的网络体系内进一步深入理解染色质结构、调控序列以
②组蛋白的N末端尾巴可与参与维持染色质高级结构的多种蛋白质相互作用,更加稳定了核
小体的结构。而组蛋白乙酰化却减弱了上述作用,阻碍了核小体装配成规则的高级结构(如 螺线管);
③组蛋白乙酰基转移酶(HAT)对相关转录因子或活化因子进行乙酰化修饰以调节基因的表
达。如 CBP/P300对P53的乙酰化可增强其特异性 DNA结合能力、转录激活能力,并延长其 半衰期。
组蛋白乙酰化调节转录的机制
组蛋白乙酰化引起染色质结构改变及基因转录活性变化的至少包括以下几个方面: ①组蛋白尾部赖氨酸残基的乙酰化能够使组蛋白携带正电荷量减少,降低其与带负电荷的 DNA链的亲和性,导致局部 DNA与组蛋白八聚体解开缠绕,从而促使参与转录调控的各种 蛋白因子与DNA特异序列结合,进而发挥转录调控作用;
及调控蛋白之间交互作用的内在机制; 4. 建立基因表达的调控网络数据库及其分析系统。总之,随着越来越多组蛋白核心结
构区域和修饰方式的确定,组蛋白密码在基因调控过程中的作用会越来越明确。
局部乙酰化举例
当DNA与核小体尚未解开缠绕时,转录激活因子如糖皮质激素受体可以和DNA上相应 的反应元件(GRE)结合。当结合至GRE之后,糖皮质激素募集共激活因子如CBP到染色
体上的靶转录基因区。此时,共激活因子利用HAT活性使得结合在DNA启动子区域的核心
组蛋白的修饰作用ppt课件

组蛋白的修饰作用
1
一、组蛋白的定义:
组蛋白是染色体的结构蛋白,与DNA构成核小体。它分为 H1、H2A、H2B、H3和H4等5种。
2
二、组蛋白的特征:
1、进化上的极端保守性: 其保守程度比较:H1<H2A 、H2B<H3 、H4;
2、无组织特异性: 鸟、鱼、两栖类的红细胞染色体不含H1而含H5,精细胞
DNA复制和重组过程发挥着直接的作用。组蛋白H1被细胞周期 蛋白依赖的激酶磷酸化是其主要的修饰作用。组蛋白H1的磷酸 化能够影响DNA二级结构的改变和染色体凝集状态的改变。另 外,组蛋白H1的磷酸化需要DNA复制,并且激活DNA复制的蛋 白激酶也促进组蛋白H1的磷酸化。因此,组蛋白H1的磷酸化与 DNA复制存在一个协同发生的机制。
12
直到1996年,James Brownell 和David Allis 成功的纯化和鉴定 了一种组蛋白乙酰转移酶(Histone acetyltransferase HAT ),该 酶是从供体乙酰辅酶A上将乙酰基团转移到核心组蛋白上。
进一步研究得出HAT的两种作用机制: 1)使组蛋白H1、H2A、H4的氨基末端乙酰化,形成α-乙酰丝氨 酸;通常组蛋白在细胞质内合成后输入细胞核之前发生这一修 饰作用。 2)在组蛋白H2A、H2B、H3 和 H4 的氨基末端区域的某些专一位 置形成N6-乙酰赖氨酸。通常发生在蛋白质的赖氨酸(K)上。如下 图1所示:
由组蛋白甲基化的特定模式识别及结合核小体的蛋白质共同产 生的,并进一步修饰染色质或直接影响转录。
2、组蛋白的甲基化对促进DNA甲基化具有一定的作用。 DNA甲基化在转录水平可影响基因表达、参与真核生物胚胎发 育调节、参与基因组印记和X染色体失活及影响DNA与蛋白质 的相互作用。
1
一、组蛋白的定义:
组蛋白是染色体的结构蛋白,与DNA构成核小体。它分为 H1、H2A、H2B、H3和H4等5种。
2
二、组蛋白的特征:
1、进化上的极端保守性: 其保守程度比较:H1<H2A 、H2B<H3 、H4;
2、无组织特异性: 鸟、鱼、两栖类的红细胞染色体不含H1而含H5,精细胞
DNA复制和重组过程发挥着直接的作用。组蛋白H1被细胞周期 蛋白依赖的激酶磷酸化是其主要的修饰作用。组蛋白H1的磷酸 化能够影响DNA二级结构的改变和染色体凝集状态的改变。另 外,组蛋白H1的磷酸化需要DNA复制,并且激活DNA复制的蛋 白激酶也促进组蛋白H1的磷酸化。因此,组蛋白H1的磷酸化与 DNA复制存在一个协同发生的机制。
12
直到1996年,James Brownell 和David Allis 成功的纯化和鉴定 了一种组蛋白乙酰转移酶(Histone acetyltransferase HAT ),该 酶是从供体乙酰辅酶A上将乙酰基团转移到核心组蛋白上。
进一步研究得出HAT的两种作用机制: 1)使组蛋白H1、H2A、H4的氨基末端乙酰化,形成α-乙酰丝氨 酸;通常组蛋白在细胞质内合成后输入细胞核之前发生这一修 饰作用。 2)在组蛋白H2A、H2B、H3 和 H4 的氨基末端区域的某些专一位 置形成N6-乙酰赖氨酸。通常发生在蛋白质的赖氨酸(K)上。如下 图1所示:
由组蛋白甲基化的特定模式识别及结合核小体的蛋白质共同产 生的,并进一步修饰染色质或直接影响转录。
2、组蛋白的甲基化对促进DNA甲基化具有一定的作用。 DNA甲基化在转录水平可影响基因表达、参与真核生物胚胎发 育调节、参与基因组印记和X染色体失活及影响DNA与蛋白质 的相互作用。
蛋白质分子的化学修饰课件

磷酸酶
催化去磷酸化反应的酶,将蛋白 质上的磷酸基团去除。
蛋白质磷酸化修饰 磷酸化修饰的种类
调节蛋白质活性
磷酸化修饰可改变蛋白质 的构象或活性位点,从而 调节其功能。
参与信号转导
磷酸化修饰在细胞信号转 导过程中起着关键作用, 可影响细胞生长、分化、 代谢等过程。
蛋白质稳定性
磷酸化修饰可影响蛋白质 的稳定性,通过调节蛋白 质降解途径来影响细胞内 蛋白质水平。
2023
PART 04
蛋白质甲基化修饰
REPORTING
甲基化修饰的种类
赖氨酸甲基化
赖氨酸残基的ε-氨基上加上甲基 基团,包括单甲基化、二甲基化
和三甲基化。
蛋氨酸甲基化
蛋氨酸残基的α-氨基上加上甲基基 团,通常为N-甲基化。
精氨酸甲基化
精氨酸残基的胍基上加上甲基基团 ,包括N-甲基化和N,N-二甲基化。
2023
PART 03
蛋白质糖基化修饰
REPORTING
糖基化修饰的种类
O-糖基化
糖基磷脂化
发生在蛋白质的丝氨酸或苏氨酸的羟 基上,由糖苷酶催化。
将糖基连接到脂质分子上,形成糖脂 。
N-糖基化
发生在蛋白质的氨基上,由糖苷酶催 化。
糖基化修饰的酶类
糖基转移酶
催化糖基从供体转移到受体上。
糖苷酶
催化糖苷键的断裂,释放出糖基 。
泛素化
泛素化是指将泛素分子加到蛋 白质的特定位点上,可以调节 蛋白质的降解和功能。
甲基化
甲基化是指将甲基基团加到蛋 白质的特定位点上,可以调节 蛋白质的构象和与其他蛋白质
的相互作用。
蛋白质分子化学修饰的功能
调节蛋白质活性
调节蛋白质稳定性
催化去磷酸化反应的酶,将蛋白 质上的磷酸基团去除。
蛋白质磷酸化修饰 磷酸化修饰的种类
调节蛋白质活性
磷酸化修饰可改变蛋白质 的构象或活性位点,从而 调节其功能。
参与信号转导
磷酸化修饰在细胞信号转 导过程中起着关键作用, 可影响细胞生长、分化、 代谢等过程。
蛋白质稳定性
磷酸化修饰可影响蛋白质 的稳定性,通过调节蛋白 质降解途径来影响细胞内 蛋白质水平。
2023
PART 04
蛋白质甲基化修饰
REPORTING
甲基化修饰的种类
赖氨酸甲基化
赖氨酸残基的ε-氨基上加上甲基 基团,包括单甲基化、二甲基化
和三甲基化。
蛋氨酸甲基化
蛋氨酸残基的α-氨基上加上甲基基 团,通常为N-甲基化。
精氨酸甲基化
精氨酸残基的胍基上加上甲基基团 ,包括N-甲基化和N,N-二甲基化。
2023
PART 03
蛋白质糖基化修饰
REPORTING
糖基化修饰的种类
O-糖基化
糖基磷脂化
发生在蛋白质的丝氨酸或苏氨酸的羟 基上,由糖苷酶催化。
将糖基连接到脂质分子上,形成糖脂 。
N-糖基化
发生在蛋白质的氨基上,由糖苷酶催 化。
糖基化修饰的酶类
糖基转移酶
催化糖基从供体转移到受体上。
糖苷酶
催化糖苷键的断裂,释放出糖基 。
泛素化
泛素化是指将泛素分子加到蛋 白质的特定位点上,可以调节 蛋白质的降解和功能。
甲基化
甲基化是指将甲基基团加到蛋 白质的特定位点上,可以调节 蛋白质的构象和与其他蛋白质
的相互作用。
蛋白质分子化学修饰的功能
调节蛋白质活性
调节蛋白质稳定性
表观遗传学 第三章 组蛋白修饰 ppt课件

HAT识别底物的分子机制
r A. ‘hit-and-run’ model;
物 om r B. & C. attract-and生 .c hit’ models
做 oo r D. ‘targeted action’ 心 bi model
秀 r E. ‘relay’ model: 两个 物 - 专.b w HAT先后修饰底物
表观遗传学
第三章 组蛋白修饰
DNA Packing
r 1. 如何将10,000公里长的蚕
丝(半径~10-5米)装入一个篮 球中。
r 2. 蚕丝的体积:3.14*10-3m3
生物.com
r 3. 折叠、缠绕…
心做bioo
物秀- 专.b w
生 ww
染色体上不同的区域
r Euchromatin: 常染色质; r Heterochromatin: 异染色
5mC 物秀- 专.b w H4 乙酰化
H3 乙酰化
生 ww
组蛋白共价修饰的功能
r 基因转录、DNA损伤修复、DNA复制、染色体凝聚等
心做b生io物 生物w秀w- 专.b w
内容纲要
r 一、组蛋白的乙酰化
r r r r
r
六二 三 四 五、、 、 、 、组组 组 组 组蛋蛋 蛋 蛋 蛋白白白白白物密的的的的秀码甲磷泛SU-基酸素M专.化化化Ob心化w做b生io物
Gcn5/PCAF
Br, bromodomain;
物 om Nr, nuclear receptor生 .c interacting box; 做 oo CH, cysteine/histidine心 rich module; 秀 bi KIX, phospho-CREB 物 - 专.b w interacting module;
组蛋白修饰及其功能(乙酰化,甲基化,磷酸化等)-于凯资料
组蛋白修饰的生物学意义
尤其是组蛋白乙酰化、甲基化修饰能为相关调控蛋白提供其在组蛋白上的附着位点,改变染色质结 构和活性。一般来说,组蛋白乙酰化能选择性的使某些染色质区域的结构从紧密变得松散,开放某 些基因的转录,增强其表达水平。而组蛋白甲基化既可抑制也可增强基因表达。乙酰化修饰和甲基 化修饰往往是相互排斥的。在细胞有丝分裂和凋亡过程中,磷酸化修饰能调控组蛋白共价修饰间的关系
组蛋白的其他修饰方式 相对而言,组蛋白的甲基化修饰方式是最稳定的,所以最适合作为稳定的表观遗传信息。而 乙酰化修饰具有较高的动态,另外还有其他不稳定的修饰方式,如磷酸化、腺苷酸化、泛素 化、ADP核糖基化等等。这些修饰更为灵活的影响染色质的结构与功能,通过多种修饰方式 的组合发挥其调控功能。
组蛋白修饰及其功能(乙酰化,甲基化,磷酸化 等)-于凯
组蛋白乙酰化调节转录的机制
组蛋白乙酰化引起染色质结构改变及基因转录活性变化的至少包括以下几个方面: ①组蛋白尾部赖氨酸残基的乙酰化能够使组蛋白携带正电荷量减少,降低其与带负电荷的 DNA链的亲和性,导致局部 DNA与组蛋白八聚体解开缠绕,从而促使参与转录调控的各种 蛋白因子与DNA特异序列结合,进而发挥转录调控作用; ②组蛋白的N末端尾巴可与参与维持染色质高级结构的多种蛋白质相互作用,更加稳定了核 小体的结构。而组蛋白乙酰化却减弱了上述作用,阻碍了核小体装配成规则的高级结构(如 螺线管); ③组蛋白乙酰基转移酶(HAT)对相关转录因子或活化因子进行乙酰化修饰以调节基因的表 达。如 CBP/P300对P53的乙酰化可增强其特异性 DNA结合能力、转录激活能力,并延长其 半衰期。
2. 组蛋白的甲基化
组蛋白甲基化是由组蛋白甲基化转移酶(histone methyl transferase,HMT)完成的。甲基化可发生在组 蛋白的赖氨酸和精氨酸残基上,而且赖氨酸残基能够 发生单、双、三甲基化,而精氨酸残基能够单、双甲 基化,这些不同程度的甲基化极大地增加了组蛋白修 饰和调节基因表达的复杂性。
组蛋白的修饰ppt课件
组蛋白赖氨酸甲基化 组蛋白精氨酸甲基化
最新编辑ppt
4
组蛋白上的甲基化修饰
组蛋白赖氨酸甲基化 组蛋白精氨酸甲基化
最新编辑ppt
5
组蛋白赖氨酸甲基化修饰位点
组 蛋 白 赖 氨 酸 甲 基 化 主 要 发 生 在 组 蛋 白 H3 和H4上。目前研究较多的有6个位点, 其中 有5个存在于H3组蛋白,它们分别位于N-末端 (H3K4、H3K9、H3K27 和H3K36)和球状区域 中(H3K79),另一个位于H4组蛋白赖氨酸N 末 端的K20,还可发生在H1的N端。
最新编辑ppt
12
组蛋白精氨酸甲基化
催化组蛋白精氨酸去甲基酶主要有两个:一个是肽基精氨
酸去亚胺基酶4(peptide
arginine
deiminase
4,PADI/PAD4),它能将蛋白质内单甲基化的精氨酸脱去加
甲基和亚胺基,进而转化为瓜氨酸,因此这一过程常被称
为ቤተ መጻሕፍቲ ባይዱ亚胺基化(demination)或瓜氨酸化(citrullination)
最新编辑ppt
14
组蛋白 赖氨酸甲基 化似乎是基 因表达调控 较为稳定的 修饰,作用 也较复杂。
最新编辑ppt
15
组蛋白甲基化与组蛋白乙酰化 及DNA 甲基化的联系
关于组蛋白修饰与DNA甲基化之间的相互作用, 目 前 有 以 下 几 种 推 测 : 甲 基 化 的 CpG 连 接 蛋 白 (MBD)募集组蛋白去乙酰化酶复合物,使得组蛋 白尾端便于被HMTs甲基化;染色体上,组蛋白被 高度乙酰化,含有MBD的HMTs可直接结合组蛋白 并将其甲基化;甲基化的组蛋白尾端可募集 DNMTs,导致DNA甲基化,使基因长期沉默。
最新编辑ppt
最新编辑ppt
4
组蛋白上的甲基化修饰
组蛋白赖氨酸甲基化 组蛋白精氨酸甲基化
最新编辑ppt
5
组蛋白赖氨酸甲基化修饰位点
组 蛋 白 赖 氨 酸 甲 基 化 主 要 发 生 在 组 蛋 白 H3 和H4上。目前研究较多的有6个位点, 其中 有5个存在于H3组蛋白,它们分别位于N-末端 (H3K4、H3K9、H3K27 和H3K36)和球状区域 中(H3K79),另一个位于H4组蛋白赖氨酸N 末 端的K20,还可发生在H1的N端。
最新编辑ppt
12
组蛋白精氨酸甲基化
催化组蛋白精氨酸去甲基酶主要有两个:一个是肽基精氨
酸去亚胺基酶4(peptide
arginine
deiminase
4,PADI/PAD4),它能将蛋白质内单甲基化的精氨酸脱去加
甲基和亚胺基,进而转化为瓜氨酸,因此这一过程常被称
为ቤተ መጻሕፍቲ ባይዱ亚胺基化(demination)或瓜氨酸化(citrullination)
最新编辑ppt
14
组蛋白 赖氨酸甲基 化似乎是基 因表达调控 较为稳定的 修饰,作用 也较复杂。
最新编辑ppt
15
组蛋白甲基化与组蛋白乙酰化 及DNA 甲基化的联系
关于组蛋白修饰与DNA甲基化之间的相互作用, 目 前 有 以 下 几 种 推 测 : 甲 基 化 的 CpG 连 接 蛋 白 (MBD)募集组蛋白去乙酰化酶复合物,使得组蛋 白尾端便于被HMTs甲基化;染色体上,组蛋白被 高度乙酰化,含有MBD的HMTs可直接结合组蛋白 并将其甲基化;甲基化的组蛋白尾端可募集 DNMTs,导致DNA甲基化,使基因长期沉默。
最新编辑ppt
组蛋白修饰及其功能(乙酰化,甲基化,磷酸化等)-于凯
组蛋白翻译完成后,其氨基尾巴会发生多种共价修饰,如乙 酰化、甲基化、磷酸化,泛素化和ADP核糖基化等,这些修饰都 是可逆性修饰,这些修饰共同构成了“组蛋白密码”。
1
1. 组蛋白乙酰化
核心组蛋白乙酰化反应多发生在核心组蛋白 N端碱性氨基 酸集中区的特定 Lys 残基。组蛋白乙酰化由组蛋白乙酰转移酶 (histone acetyltransferase,HAT)和组蛋白去乙酰化酶(histone deacetylase,HDAC)协调进行。HAT通过将乙酰辅酶 A 的乙酰 基转移到 Lys 的NH+,中和掉一个正电荷。 HDAC使组蛋白去 乙酰化,与带负电荷的DNA紧密结合,染色质致密卷曲,基因 的转录受到抑制。
7
3. 组蛋白的磷酸化
8
组蛋白共价修饰间的关系
组蛋白的其他修饰方式 相对而言,组蛋白的甲基化修饰方式是最稳定的,所以最适合作为稳定的表观遗传信息。而 乙酰化修饰具有较高的动态,另外还有其他不稳定的修饰方式,如磷酸化、腺苷酸化、泛素 化、ADP核糖基化等等。这些修饰更为灵活的影响染色质的结构与功能,通过多种修饰方式 的组合发挥其调控功能。
通常,异染色质结构域组蛋白呈低乙酰化,常染色质结构 域组蛋白呈高乙酰化。
酵母组蛋白乙酰化与去乙酰化的调节
2
组蛋白乙酰化调节转录的机制
组蛋白乙酰化引起染色质结构改变及基因转录活性变化的至少包括以下几个方面: ①组蛋白尾部赖氨酸残基的乙酰化能够使组蛋白携带正电荷量减少,降低其与带负电荷的 DNA链的亲和性,导致局部 DNA与组蛋白八聚体解开缠绕,从而促使参与转录调控的各种 蛋白因子与DNA特异序列结合,进而发挥转录调控作用; ②组蛋白的N末端尾巴可与参与维持染色质高级结构的多种蛋白质相互作用,更加稳定了核 小体的结构。而组蛋白乙酰化却减弱了上述作用,阻碍了核小体装配成规则的高级结构(如 螺线管); ③组蛋白乙酰基转移酶(HAT)对相关转录因子或活化因子进行乙酰化修饰以调节基因的表 达。如 CBP/P300对P53的乙酰化可增强其特异性 DNA结合能力、转录激活能力,并延长其 半衰期。
1
1. 组蛋白乙酰化
核心组蛋白乙酰化反应多发生在核心组蛋白 N端碱性氨基 酸集中区的特定 Lys 残基。组蛋白乙酰化由组蛋白乙酰转移酶 (histone acetyltransferase,HAT)和组蛋白去乙酰化酶(histone deacetylase,HDAC)协调进行。HAT通过将乙酰辅酶 A 的乙酰 基转移到 Lys 的NH+,中和掉一个正电荷。 HDAC使组蛋白去 乙酰化,与带负电荷的DNA紧密结合,染色质致密卷曲,基因 的转录受到抑制。
7
3. 组蛋白的磷酸化
8
组蛋白共价修饰间的关系
组蛋白的其他修饰方式 相对而言,组蛋白的甲基化修饰方式是最稳定的,所以最适合作为稳定的表观遗传信息。而 乙酰化修饰具有较高的动态,另外还有其他不稳定的修饰方式,如磷酸化、腺苷酸化、泛素 化、ADP核糖基化等等。这些修饰更为灵活的影响染色质的结构与功能,通过多种修饰方式 的组合发挥其调控功能。
通常,异染色质结构域组蛋白呈低乙酰化,常染色质结构 域组蛋白呈高乙酰化。
酵母组蛋白乙酰化与去乙酰化的调节
2
组蛋白乙酰化调节转录的机制
组蛋白乙酰化引起染色质结构改变及基因转录活性变化的至少包括以下几个方面: ①组蛋白尾部赖氨酸残基的乙酰化能够使组蛋白携带正电荷量减少,降低其与带负电荷的 DNA链的亲和性,导致局部 DNA与组蛋白八聚体解开缠绕,从而促使参与转录调控的各种 蛋白因子与DNA特异序列结合,进而发挥转录调控作用; ②组蛋白的N末端尾巴可与参与维持染色质高级结构的多种蛋白质相互作用,更加稳定了核 小体的结构。而组蛋白乙酰化却减弱了上述作用,阻碍了核小体装配成规则的高级结构(如 螺线管); ③组蛋白乙酰基转移酶(HAT)对相关转录因子或活化因子进行乙酰化修饰以调节基因的表 达。如 CBP/P300对P53的乙酰化可增强其特异性 DNA结合能力、转录激活能力,并延长其 半衰期。
表观遗传学和磷酸化-蛋白质磷酸化-分子生物学课件.ppt
DNA甲基化是指在甲基化酶的作用下,将一个 甲基添加在DNA分子的碱基上。
DNA甲基化修饰决定基因表达的模式,即决定 从亲代到子代可遗传的基因表达状态。
DNA甲基化的部位通常在CpG岛的胞嘧啶
胞嘧啶
DNMT1
S-腺苷 甲硫氨 酸SAM
5-甲基胞嘧啶
胞嘧啶甲基 化反应
真核生物细胞内存在两种甲基化酶活性:
组蛋白甲基化可以与基因抑制有关,也 可以与基因的激活相关,这往往取决于 被修饰的赖氨酸处于什么位置。
组蛋白修饰主要是氨基端的甲基化修饰和(或) 乙酰化修饰,特定组蛋白的氨基酸残基被甲基 化和(或)乙酰化可以最终激活基因的表达,反 之则抑制基因的表达。
特定组蛋白羧基端的泛素化同样影响蛋白质的 降解过程,从而也可调节基因的表达。
(2)糖原合成酶—P—失活
使许多蛋白质磷酸化 (1)核中组蛋白磷酸化—加速核酸的复制,转录。 (2)核糖体蛋白质磷酸化—加速蛋白质合成通性。 (3)使膜蛋白磷酸化—加速物质的转运。
蛋白质磷酸化在细胞信号转导中的作用
(1). 在胞内介导胞外信号时具有专一应答特点。与信号传递有关的蛋白激酶类主要受控于 胞内信使,
根据是否有调节物来分又可分成两大类: 信使依赖性蛋白质激酶(messenger-dependent protein
kinase),包括胞内第二信使或调节因子依赖性蛋白激酶及激 素(生长因子)依赖性激酶两个亚类;非信使依赖型蛋白激酶。
蛋白激酶的催化作用: 使调节酶磷酸化 (1)磷酸化酶激酶—P—激活
基因表达的重新编程
已完全分化的细胞,其基因组在特定条件下经 历表观遗传修饰重建而为胚胎发育中的基因表 达重新编程(reprogramming)并赋予发育全能 性,为胚胎发育和分化发出正确的指令。
DNA甲基化修饰决定基因表达的模式,即决定 从亲代到子代可遗传的基因表达状态。
DNA甲基化的部位通常在CpG岛的胞嘧啶
胞嘧啶
DNMT1
S-腺苷 甲硫氨 酸SAM
5-甲基胞嘧啶
胞嘧啶甲基 化反应
真核生物细胞内存在两种甲基化酶活性:
组蛋白甲基化可以与基因抑制有关,也 可以与基因的激活相关,这往往取决于 被修饰的赖氨酸处于什么位置。
组蛋白修饰主要是氨基端的甲基化修饰和(或) 乙酰化修饰,特定组蛋白的氨基酸残基被甲基 化和(或)乙酰化可以最终激活基因的表达,反 之则抑制基因的表达。
特定组蛋白羧基端的泛素化同样影响蛋白质的 降解过程,从而也可调节基因的表达。
(2)糖原合成酶—P—失活
使许多蛋白质磷酸化 (1)核中组蛋白磷酸化—加速核酸的复制,转录。 (2)核糖体蛋白质磷酸化—加速蛋白质合成通性。 (3)使膜蛋白磷酸化—加速物质的转运。
蛋白质磷酸化在细胞信号转导中的作用
(1). 在胞内介导胞外信号时具有专一应答特点。与信号传递有关的蛋白激酶类主要受控于 胞内信使,
根据是否有调节物来分又可分成两大类: 信使依赖性蛋白质激酶(messenger-dependent protein
kinase),包括胞内第二信使或调节因子依赖性蛋白激酶及激 素(生长因子)依赖性激酶两个亚类;非信使依赖型蛋白激酶。
蛋白激酶的催化作用: 使调节酶磷酸化 (1)磷酸化酶激酶—P—激活
基因表达的重新编程
已完全分化的细胞,其基因组在特定条件下经 历表观遗传修饰重建而为胚胎发育中的基因表 达重新编程(reprogramming)并赋予发育全能 性,为胚胎发育和分化发出正确的指令。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
通常,异染色质结构域组蛋白呈低乙酰化,常染色质结构 域组蛋白呈高乙酰化。
酵母组蛋白乙酰化与去乙酰化的调节
组蛋白乙酰化调节转录的机制
组蛋白乙酰化引起染色质结构改变及基因转录活性变化的至少包括以下几个方面: ①组蛋白尾部赖氨酸残基的乙酰化能够使组蛋白携带正电荷量减少,降低其与带负电荷的 DNA链的亲和性,导致局部 DNA与组蛋白八聚体解开缠绕,从而促使参与转录调控的各种 蛋白因子与DNA特异序列结合,进而发挥转录调控作用; ②组蛋白的N末端尾巴可与参与维持染色质高级结构的多种蛋白质相互作用,更加稳定了核 小体的结构。而组蛋白乙酰化却减弱了上述作用,阻碍了核小体装配成规则的高级结构(如 螺线管); ③组蛋白乙酰基转移酶(HAT)对相关转录因子或活化因子进行乙酰化修饰以调节基因的表 达。如 CBP/P300对P53的乙酰化可增强其特异性 DNA结合能力、转录激活能力,并延长其 半衰期。
2. 组蛋白的甲基化
组蛋白甲基化是由组蛋白甲基化转移酶(histone methyl transferase,HMT)完成的。甲基化可发生在组 蛋白的赖氨酸和精氨酸残基上,而且赖氨酸残基能够 发生单、双、三甲基化,而精氨酸残基能够单、双甲 基化,这些不同程度的甲基化极大地增加了组蛋白修 饰和调节基因表达的复杂性。
大家学习辛苦了,还是要坚持
继续保持安静
组蛋白修饰的生物学意义
尤其是组蛋白乙酰化、甲基化修饰能为相关调控蛋白提供其在组蛋白上的附着位点,改变染色质结 构和活性。一般来说,组蛋白乙酰化能选择性的使某些染色质区域的结构从紧密变得松散,开放某 些基因的转录,增强其表达水平。而组蛋白甲基化既可抑制也可增强基因表达。乙酰化修饰和甲基 化修饰往往是相互排斥的。在细胞有丝分裂和凋亡过程中,磷酸化修饰能调控蛋白质复合体向染色 质集结。
Hale Waihona Puke 组蛋白密码学说的完善: 1. 更好地开发新药。研究组蛋白密码对药物开发具有战略 意义,多种组蛋白修饰酶已成为相关疾病治疗的靶目标。比如,组蛋白去乙酰酶
局部乙酰化举例
当DNA与核小体尚未解开缠绕时,转录激活因子如糖皮质激素受体可以和DNA上相应 的反应元件(GRE)结合。当结合至GRE之后,糖皮质激素募集共激活因子如CBP到染色 体上的靶转录基因区。此时,共激活因子利用HAT活性使得结合在DNA启动子区域的核心 组蛋白乙酰化,进而使DNA与组蛋白结合减弱,核小体释放,转录因子和RNA聚合酶可以 与DNA上特异的启动子结合,启动靶基因的转录。
研究表明,组蛋白精氨酸甲基化是一种相对动态 的标记,精氨酸甲基化与基因激活相关,而H3和H4精 氨酸的甲基化丢失与基因沉默相关。相反,赖氨酸甲 基化似乎是基因表达调控中一种较为稳定的标记。
组蛋白甲基化的调节机制
1. H3-K9甲基化与异染色质的形成:人们曾针对异染色质的形成提出过一个模型:首先组蛋白 脱乙酰酶使H3中的K9、K14脱乙酰化,然后Suv39h1或Clr4对H32K9进行甲基化,H32K9的甲基 化再影响DNA的甲基化,随后甲基化的H32K9做为一个结合位点招募HP1或Swi6蛋白的定位, 最后HP1/Swi6通过它们的shadow染色质结合区域定位在C末端,进而形成异染色质的多聚体。 2. H32K9甲基化对常染色体中基因表达调控的影响: 3. 组蛋白其他位点上发生甲基化与基因表达的关系:大量实验表明H32K9甲基化的功能与基 因沉默有关,但其它位点甲基化可能存在激活转录作用。 4. 组蛋白甲基化与DNA甲基化:H32K9的甲基化可以直接或间接影响DNA 的甲基化,DNA 甲基化可能是组蛋白甲基化的间接结果
有丝分裂过程也与特异性组蛋白修饰有显著的相关性。在有丝分裂过程中,有数个组蛋白磷酸化反 应,其中大多数由Aurora B激酶催化。特异性组蛋白修饰可在有丝分裂的不同阶段检测到,在细胞 核分裂中发挥多种功能。
组蛋白修饰还参与DNA损伤和凋亡。在凋亡的级联反应中,激酶(包括CHK1和CHK2)的主要底 物之一是组蛋白衍生物H2A.X ,H2A.X的磷酸化是凋亡早期最早标志之一。在凋亡后期,Caspase激 活蛋白激酶Mst1, Mst1使组蛋白H2B的14位丝氨酸磷酸化。这一修饰在染色质浓缩步骤中可检测到, 是凋亡途径良好的标记物。
3. 组蛋白的磷酸化
组蛋白共价修饰间的关系
组蛋白的其他修饰方式 相对而言,组蛋白的甲基化修饰方式是最稳定的,所以最适合作为稳定的表观遗传信息。而 乙酰化修饰具有较高的动态,另外还有其他不稳定的修饰方式,如磷酸化、腺苷酸化、泛素 化、ADP核糖基化等等。这些修饰更为灵活的影响染色质的结构与功能,通过多种修饰方式 的组合发挥其调控功能。
组蛋白不同修饰之间的关系 乙酰化一般是活性染色质的标志,而甲基化和磷酸化则在活性染 色质和非活性染色质中都存在。组蛋白H3K9的甲基化在调节基因 表达、染色质组装和异染色质形成过程发挥重要作用。H3S10的 短暂磷酸化足以使H3K9甲基化引起的染色质浓缩变得疏松。这是 一个两种组蛋白同时调节染色质组装状态的例子:稳定的甲基化 和动态的磷酸化标记。
1. 组蛋白乙酰化
核心组蛋白乙酰化反应多发生在核心组蛋白 N端碱性氨基 酸集中区的特定 Lys 残基。组蛋白乙酰化由组蛋白乙酰转移酶 (histone acetyltransferase,HAT)和组蛋白去乙酰化酶(histone deacetylase,HDAC)协调进行。HAT通过将乙酰辅酶 A 的乙酰 基转移到 Lys 的NH+,中和掉一个正电荷。 HDAC使组蛋白去乙 酰化,与带负电荷的DNA紧密结合,染色质致密卷曲,基因的 转录受到抑制。
分子效应:乙酰化可能通过对组蛋白电荷以及相互作用蛋 白的影响,增加组蛋白与DNA的排斥力,来调节基因转录。组 蛋白的乙酰化有利于DNA与组蛋白八聚体的解离,核小体结构 松弛,从而使各种转录因子和协同转录因子能与DNA结合位点 特异性结合,激活基因的转录。同时影响泛素与组蛋白的H2A的 结合,导致蛋白质的选择性降解。
酵母组蛋白乙酰化与去乙酰化的调节
组蛋白乙酰化调节转录的机制
组蛋白乙酰化引起染色质结构改变及基因转录活性变化的至少包括以下几个方面: ①组蛋白尾部赖氨酸残基的乙酰化能够使组蛋白携带正电荷量减少,降低其与带负电荷的 DNA链的亲和性,导致局部 DNA与组蛋白八聚体解开缠绕,从而促使参与转录调控的各种 蛋白因子与DNA特异序列结合,进而发挥转录调控作用; ②组蛋白的N末端尾巴可与参与维持染色质高级结构的多种蛋白质相互作用,更加稳定了核 小体的结构。而组蛋白乙酰化却减弱了上述作用,阻碍了核小体装配成规则的高级结构(如 螺线管); ③组蛋白乙酰基转移酶(HAT)对相关转录因子或活化因子进行乙酰化修饰以调节基因的表 达。如 CBP/P300对P53的乙酰化可增强其特异性 DNA结合能力、转录激活能力,并延长其 半衰期。
2. 组蛋白的甲基化
组蛋白甲基化是由组蛋白甲基化转移酶(histone methyl transferase,HMT)完成的。甲基化可发生在组 蛋白的赖氨酸和精氨酸残基上,而且赖氨酸残基能够 发生单、双、三甲基化,而精氨酸残基能够单、双甲 基化,这些不同程度的甲基化极大地增加了组蛋白修 饰和调节基因表达的复杂性。
大家学习辛苦了,还是要坚持
继续保持安静
组蛋白修饰的生物学意义
尤其是组蛋白乙酰化、甲基化修饰能为相关调控蛋白提供其在组蛋白上的附着位点,改变染色质结 构和活性。一般来说,组蛋白乙酰化能选择性的使某些染色质区域的结构从紧密变得松散,开放某 些基因的转录,增强其表达水平。而组蛋白甲基化既可抑制也可增强基因表达。乙酰化修饰和甲基 化修饰往往是相互排斥的。在细胞有丝分裂和凋亡过程中,磷酸化修饰能调控蛋白质复合体向染色 质集结。
Hale Waihona Puke 组蛋白密码学说的完善: 1. 更好地开发新药。研究组蛋白密码对药物开发具有战略 意义,多种组蛋白修饰酶已成为相关疾病治疗的靶目标。比如,组蛋白去乙酰酶
局部乙酰化举例
当DNA与核小体尚未解开缠绕时,转录激活因子如糖皮质激素受体可以和DNA上相应 的反应元件(GRE)结合。当结合至GRE之后,糖皮质激素募集共激活因子如CBP到染色 体上的靶转录基因区。此时,共激活因子利用HAT活性使得结合在DNA启动子区域的核心 组蛋白乙酰化,进而使DNA与组蛋白结合减弱,核小体释放,转录因子和RNA聚合酶可以 与DNA上特异的启动子结合,启动靶基因的转录。
研究表明,组蛋白精氨酸甲基化是一种相对动态 的标记,精氨酸甲基化与基因激活相关,而H3和H4精 氨酸的甲基化丢失与基因沉默相关。相反,赖氨酸甲 基化似乎是基因表达调控中一种较为稳定的标记。
组蛋白甲基化的调节机制
1. H3-K9甲基化与异染色质的形成:人们曾针对异染色质的形成提出过一个模型:首先组蛋白 脱乙酰酶使H3中的K9、K14脱乙酰化,然后Suv39h1或Clr4对H32K9进行甲基化,H32K9的甲基 化再影响DNA的甲基化,随后甲基化的H32K9做为一个结合位点招募HP1或Swi6蛋白的定位, 最后HP1/Swi6通过它们的shadow染色质结合区域定位在C末端,进而形成异染色质的多聚体。 2. H32K9甲基化对常染色体中基因表达调控的影响: 3. 组蛋白其他位点上发生甲基化与基因表达的关系:大量实验表明H32K9甲基化的功能与基 因沉默有关,但其它位点甲基化可能存在激活转录作用。 4. 组蛋白甲基化与DNA甲基化:H32K9的甲基化可以直接或间接影响DNA 的甲基化,DNA 甲基化可能是组蛋白甲基化的间接结果
有丝分裂过程也与特异性组蛋白修饰有显著的相关性。在有丝分裂过程中,有数个组蛋白磷酸化反 应,其中大多数由Aurora B激酶催化。特异性组蛋白修饰可在有丝分裂的不同阶段检测到,在细胞 核分裂中发挥多种功能。
组蛋白修饰还参与DNA损伤和凋亡。在凋亡的级联反应中,激酶(包括CHK1和CHK2)的主要底 物之一是组蛋白衍生物H2A.X ,H2A.X的磷酸化是凋亡早期最早标志之一。在凋亡后期,Caspase激 活蛋白激酶Mst1, Mst1使组蛋白H2B的14位丝氨酸磷酸化。这一修饰在染色质浓缩步骤中可检测到, 是凋亡途径良好的标记物。
3. 组蛋白的磷酸化
组蛋白共价修饰间的关系
组蛋白的其他修饰方式 相对而言,组蛋白的甲基化修饰方式是最稳定的,所以最适合作为稳定的表观遗传信息。而 乙酰化修饰具有较高的动态,另外还有其他不稳定的修饰方式,如磷酸化、腺苷酸化、泛素 化、ADP核糖基化等等。这些修饰更为灵活的影响染色质的结构与功能,通过多种修饰方式 的组合发挥其调控功能。
组蛋白不同修饰之间的关系 乙酰化一般是活性染色质的标志,而甲基化和磷酸化则在活性染 色质和非活性染色质中都存在。组蛋白H3K9的甲基化在调节基因 表达、染色质组装和异染色质形成过程发挥重要作用。H3S10的 短暂磷酸化足以使H3K9甲基化引起的染色质浓缩变得疏松。这是 一个两种组蛋白同时调节染色质组装状态的例子:稳定的甲基化 和动态的磷酸化标记。
1. 组蛋白乙酰化
核心组蛋白乙酰化反应多发生在核心组蛋白 N端碱性氨基 酸集中区的特定 Lys 残基。组蛋白乙酰化由组蛋白乙酰转移酶 (histone acetyltransferase,HAT)和组蛋白去乙酰化酶(histone deacetylase,HDAC)协调进行。HAT通过将乙酰辅酶 A 的乙酰 基转移到 Lys 的NH+,中和掉一个正电荷。 HDAC使组蛋白去乙 酰化,与带负电荷的DNA紧密结合,染色质致密卷曲,基因的 转录受到抑制。
分子效应:乙酰化可能通过对组蛋白电荷以及相互作用蛋 白的影响,增加组蛋白与DNA的排斥力,来调节基因转录。组 蛋白的乙酰化有利于DNA与组蛋白八聚体的解离,核小体结构 松弛,从而使各种转录因子和协同转录因子能与DNA结合位点 特异性结合,激活基因的转录。同时影响泛素与组蛋白的H2A的 结合,导致蛋白质的选择性降解。
