第2章 离子聚合-阴离子聚合
合集下载
阴离子聚合

CH2 CH
CH2 CH CH CH2
CH2 C CH CH2 CH3
苯乙烯
丁二烯
异戊二烯
5
二、阴离子聚合的机理和动力学
1.阴离子聚合的引发体系 阴离子聚合的引发剂是电子给体(亲核试剂),
属碱类物质(碱金属,有机金属化合物以及三级胺 等)。根据引发机理可分为电子转移引发和阴离子 引发两类。
6
(1)碱金属 Li、Na、K等碱金属原子最外层近一个价电子,
2
一、阴离子聚合的单体
烯类、羰基化合物、三元含氧杂环和含氮杂环 都有可能进行阴离子聚合,本节主要讨论烯烃的阴 离子聚合。
原则上讲,带有π—π共轭体系的单体都能进 行阴离子聚合。如果同时具有吸电子基,则更易进 行阴离子聚合。吸电子基减少双键上电子云密度, 有利于阴离子进攻,并使形成的碳阴离子的电子云 密度分散而稳定。
12
(3)其他 ROH,H2O ,R3P, R3N等中性亲核试剂中都
含有未共用电子对,能引发很活泼的单体阴离子聚 合,如硝基乙烯、偏二腈乙烯、α—氰基丙烯酸酯 等等。
CN CH2 C C O CH3
O
α—氰基丙烯酸甲酯
13
(4) 阴离子聚合引发剂与单体的匹配 阴离子聚合的单体和引发剂都具有很强的选择
31
7. 丁基锂的缔合现象和定向聚合作用 丁基锂是目前应用最广的阴离子聚合引发剂。
实践中发现若溶剂体系选择不当,丁基锂的引发活 性很低,这可能是由于丁基锂的缔合作用引起。
丁基锂在特定条件下对聚合产物具有定向作用。 (1)丁基锂的缔合现象
丁基锂在非极性溶剂如苯、甲苯、己烷中存在缔 合现象,缔合度2 ~6不等。缔合分子无引发活性。
在增长反应中,单体的加成方向受离子对的限 制,产物的立构规整性较自由基聚合强,但尚不能 控制。
离子型聚合物

❖ 单体、溶剂中的杂质会使引发剂失活;杂质的存在会影响聚合反
应的速率、聚合物的相对分子质量、相对分子质量分布以及聚合物的
微观结构,其结果必然会影响产品的质量。
❖
单体中的H2O和O2能与引发剂中的金属有机化合物激烈反应,使
引发剂失去活性。其它杂质允许含量以10-6计。因此,原料、反应系
统中设备和管道必须经脱氧、脱水处理,使H2O和O2含量在10-6以下。 ❖
③溶剂的选用要与引发剂匹配 采用Co系和Ti系引发剂时以苯或甲苯作溶剂;采用
Ni-三元引发剂时,采用芳烃和烷烃的混合物作溶剂。 我国因采用Ni-三元引发剂
[(CH2)nCOO]2 Ni/BF3.O(C2H5)2 /Al(i-C4H9)3
溶剂选用抽余油或加氢汽油。
• 其优点:来源丰富、毒性小、回收费用低、容易分离,因而 成本低。
❖ ②溶剂的选择 ❖ 聚合用溶剂国外主要采用苯或甲苯或烷烃和芳烃的混合物。 ❖ 用苯作溶剂的优点是其对单体和聚合物的溶解性能好、沸点低容
易回收和分离;其缺点是聚合物溶液粘度大对传热不利,且冰点低 (5℃)要求管道保温,毒性大。 ❖ 用甲苯作溶剂的优点是其对单体和聚合物的溶解性能好,反应平 稳;其缺点是由于沸点高(110℃)回收时蒸气消耗量大, ❖ 聚合物溶液粘度大传热和搅拌都有困难,毒性也大。采用烷烃和 芳烃的混合物,既可以使聚合物溶液粘度降低,又可以调节聚合物的 相对分子质量。
此外,如丙二烯、丁二烯、甲基乙炔等对聚合反应和聚 合物的立构规整性都是有害的;
饱和烃如乙烷和丙烷如含量高会降低单体的分压,影响 聚合速率,如有积累需定期排除。
因此,聚合用原料和助剂中杂质的含量必须减少到允许 的范围以下。聚合用丙烯的纯度>99.6%,其它杂质允许含 量以10-6计。
阴离子聚合反应课件

功能性聚合物的制备
1 2 3
功能高分子
阴离子聚合反应可以用于制备功能性高分子材料 ,如导电聚合物、荧光聚合物、吸附分离聚合物 等。
导电聚合物
通过阴离子聚合反应可以合成聚苯胺、聚吡咯等 导电聚合物,这些材料在电子器件、传感器等领 域具有广泛的应用。
荧光聚合物
利用阴离子聚合反应可以合成荧光聚合物,这些 材料在生物成像、荧光探针等领域具有潜在的应 用价值。
反应机理
引发阶段
01
阴离子聚合反应通常由活性阴离子引发,这些阴离子可以由相
应的阳离子引发剂产生。
增长阶段
02
增长链以负离子形式存在,与单体进行加成反应,不断延长增
长链。
终止阶段
03
当增长链上的活性中心被消去或被其他因素钝化时,聚合反应
终止。
02
CATALOGUE
阴离子聚合反应的影响因素
引发剂
引发剂种类
02
03
04
混合单体和引发剂
按照规定的比例混合单体和引 发剂,确保混合均匀。
加热和搅拌
将混合物加热至规定温度,并 保持适当的搅拌速度以促进反
应进行。
聚合反应监测
通过定时取样和分析,监测聚 合反应的进程和产物性能。
终止反应
当聚合反应达到预定程度时, 加入终止剂终止反应。
安全注意事项与防护措施
防爆措施
特点
阴离子聚合反应具有高活性、高 选择性、高聚合度等优点,广泛 应用于合成高分子材料、功能性 高分子材料等领域。
历史与发展
历史
阴离子聚合反应最早可追溯到20世纪50年代,随着科技的不 断进步,人们对阴离子聚合反应的机理和应用研究越来越深 入。
发展
5.阴离子聚合反应

2 CH2 CHNa
NaCH CH2 CH2 CHNa (双阴离子)
4.3
阴离子聚合
用烷基金属化合物作引发剂形成单阴离子,体系为均相反应。
而用碱金属作引发剂形成双阴离子,体系为非均相反应。
图4.2 用碱金属作引发剂 的链引发反应示意图
4.3
阴离子聚合
•
⑶ 用碱金属配合物作引发剂的链引发反应 在醚类溶剂(如四氢呋喃)中,钠与萘形成配合物
4.3
阴离子聚合
• ⒊ 链终止反应和链转移反应 • 阴离子聚合的一个重要特点是在适当条件下: • 没有空气、醇、酸等极性物质时 ,不发生链终止反应 ,而形成 活性聚合物。 • 原因: • ⑴ 阴离子活性增长链中心离子具有相同电荷 ,相同电荷的排 斥作用,不像自由基聚合那样可以双基终止。 • ⑵ 阴离子聚合中,阴离子活性增长链的反离子常为金属阳离 子,中心离子为碳负离子二者之间离解度大 ,不能发生中心离子和 反离子的结合反应。 • ⑶ 阴离子活性增长链也不容易发生向单体转移反应。 • 因为,这种转移反应需脱除H(-)需要较高的能量,而阴离子聚合 往往是在低温(0℃以下)进行。 • 但在某些条件下 ,阴离子活性增长链发生链转移反应而终止:
1,1,4,4-四苯基丁基二锂;
Li C CH2 CH2 C Li
碱金属中主要有Li、Na和K等。 烷基金属化合物和碱金属的碱性最强,聚合活性最大,可以 引发各种能进行阴离子聚合的烯类单体。
4.3
阴离子聚合
⒉ 碱金属配合物
+ Na [ ] Na 萘-钠配合物
⒊ 活性聚合物
先制备一个活性聚合物做为种子,然后用它引发第二单体。
4.3
阴离子聚合
该聚合体系的聚合速率方程为
阴离子聚合
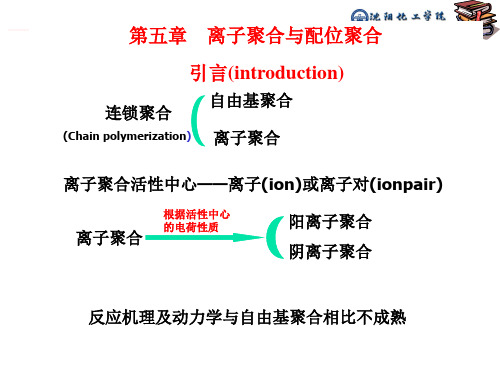
丙烯腈 甲基丙烯腈 甲基丙烯酮
偏二氰乙烯
a-氰基丙烯酸乙酯
硝基乙烯
单体活性
低
中
较高
高
苯乙烯在自由基聚合是活性单体,在阴离子聚合成低活性单体?
四. 阴离子聚合机理
1.机理:引发、增长、終止。
链引发:I
链增长: 链終止:
极快
M-
慢 M nM M n1M
M n1M 难終止
烷基卤化镁RMgX由于其C-Mg键极性弱,不能直 接引发阴离子聚合,但制成格氏试剂后使C-Mg键的 极性增大,可以引发活性较大的单体聚合。
以丁基锂和萘钠最为重要也最为常用的引用剂。
三. 阴离子聚合引发剂和单体的匹配
阴离子聚合与自由基聚合相比,单体对引发剂 有较强的选择性,只有当引发剂与单体活性相 匹配才能得到所需的聚合物。
甲基丙烯酸甲酯
CH3
H2C CH CH CH2
H2C C
CH CH2
苯乙烯
甲基苯乙烯
丁二烯
异戊二烯
乙烯基单体,取代基的吸电子能力越强,双键上的电子云密度 越低,越易与阴离子活性中心加成,聚合反应活性越高。
二. 阴离子聚合引发体系和引发 阴离子聚合引发剂——电子给体,即亲核 试剂,属于碱类。
直接转移引发
一. 阴离子聚合的单体 (1)带吸电子取代基的乙烯基单体
一方面,吸电子性能能使双基上电子云密度降低,有利 于阴离子的进攻,另一方面,形成的碳阴离子活性中心由于 取代基的共轭效应而稳定,因而易阴离子聚合:
H2C CH X
降低电子云密度,易 与富电性活性种结合
H2C CH X
H R CH2 C X
分散负电性,稳定活性中心
强碱性高活性引发剂能引发各种活性的单体,而弱碱 性低活性引发剂只能引发高活性的单体。
第一二章活性自由基聚合阴离子聚合详解演示文稿

第三十九页,共92页。
举例:
第四十页,共92页。
可逆加成-断裂链转移可控自由基聚合
1998年,Rizzardo在第37届国际高分子会议上作了“Tailored Polymers by
Free
Radical processes”提出了RAFT.
RAFT (Reversible Addition-Fragmentation Transfer)聚合:在AIBN等引
(1)反应机理
与光引发iniferter有本质不同 光引发iniferter:C-S键的光降解产生一个高活性的碳自由基与一个低 活性的硫自由基,高活性的碳自由基引发单体聚合,增长的活性链与 低活性的硫自由基反应而终止。
N,N-二乙基二硫代氨基
甲酸苄酯(BDC)
RAFT与TEMPO均源于经典引发剂的热分解。 RAFT关键是自由基向链转移剂分子中C=S的可逆加成,断裂S-R形
活性聚合的基本概念 引发反应速度远远大于增长反应速度, 而且不存在
链转移和链终止的聚合反应称为活性聚合。
第五页,共92页。
活性聚合的特征
➢定义:不存在链转移和链终止的聚合称为活性聚合。 ➢特征:
(1)聚合产物的数均聚合度等于消耗掉的单体浓度与引 发剂的初始浓度之比
Xn = [M]0×Conversion / [I]0
控自由基聚合。
第三十七页,共92页。
.
第三十八页,共92页。
TEMPO体系 •温度高,速度慢,达到高转化率所需时间较长。 •主要用于苯乙烯类单体的活性聚合,对MMA等极性单 体不适用。
在该体系中加入少量酸性物质,可加速反应的聚合速率。
近年来发现一系列酰化试剂如乙酰丙酮、乙酸酐丙二酸乙二酯等可改善苯乙烯聚合速率。
举例:
第四十页,共92页。
可逆加成-断裂链转移可控自由基聚合
1998年,Rizzardo在第37届国际高分子会议上作了“Tailored Polymers by
Free
Radical processes”提出了RAFT.
RAFT (Reversible Addition-Fragmentation Transfer)聚合:在AIBN等引
(1)反应机理
与光引发iniferter有本质不同 光引发iniferter:C-S键的光降解产生一个高活性的碳自由基与一个低 活性的硫自由基,高活性的碳自由基引发单体聚合,增长的活性链与 低活性的硫自由基反应而终止。
N,N-二乙基二硫代氨基
甲酸苄酯(BDC)
RAFT与TEMPO均源于经典引发剂的热分解。 RAFT关键是自由基向链转移剂分子中C=S的可逆加成,断裂S-R形
活性聚合的基本概念 引发反应速度远远大于增长反应速度, 而且不存在
链转移和链终止的聚合反应称为活性聚合。
第五页,共92页。
活性聚合的特征
➢定义:不存在链转移和链终止的聚合称为活性聚合。 ➢特征:
(1)聚合产物的数均聚合度等于消耗掉的单体浓度与引 发剂的初始浓度之比
Xn = [M]0×Conversion / [I]0
控自由基聚合。
第三十七页,共92页。
.
第三十八页,共92页。
TEMPO体系 •温度高,速度慢,达到高转化率所需时间较长。 •主要用于苯乙烯类单体的活性聚合,对MMA等极性单 体不适用。
在该体系中加入少量酸性物质,可加速反应的聚合速率。
近年来发现一系列酰化试剂如乙酰丙酮、乙酸酐丙二酸乙二酯等可改善苯乙烯聚合速率。
离子聚合

CH3 CH2 CH CH CH3 CH2 CH CH CH3 CH3
二级碳阳离子(仲碳阳离子) 三级碳阳离子(叔碳阳离子)
CH3 CH2 CH2 C CH3
阳离子聚合
3. 链转移和链终止
离子聚合的活性种带有电荷,无法双基终止,因此只能 通过单基终止和链转移终止,也可人为添加终止剂终止。 自由基聚合的链转移一般不终止动力学链,而阳离子聚 合的链转移则有可能终止动力学链。因此阳离子聚合的链终 止只可分为动力学链不终止的链终止反应和动力学链终止的 链终止反应两类。
+ XA
ktr,s kp
HMnMA + XCR HMnM NR3(CR)
+
NR3
阳离子聚合
CH3 CH3 (BF3OH) + H2O CH3 CH3 OH + H (BF3OH) H 2O H [ CH2 C ] n CH2 C CH3 CH3 H [ CH2 C ] n CH2 C CH3 CH3
离子聚合
引言
离子聚合是又一类连锁聚合。它的活性中心为离子。根 据活性中心的电荷性质,可分为阳离子聚合和阴离子聚合。 多数烯烃单体都能进行自由基聚合,但是离子聚合却有 极高的选择性。原因是离子聚合对阳离子和阴离子的稳定性 要求比较严格。例如只有带有1,1—二烷基、烷氧基等强推 电子的单体才能进行阳离子聚合;带有腈基、羰基等强吸电 子基的单体才能进行阴离子聚合。但含有共轭体系的单体, 如苯乙烯、丁二烯等,则由于电子流动性大,既可进行阳离 子聚合,也能进行阴离子聚合。
离子聚合
离子聚合的发展导致了活性聚合的诞生。这是高分子发 展史上的重大转折点。通过阴离子活性聚合,可实现高分子 的分子设计,制备预定结构和分子量的聚合物。 阴离子活性聚合在制备特殊结构的嵌段共聚物、接枝共 聚物、星状聚合物等方面有十分重要的作用。 目前,活性聚合领域已扩展到阳离子聚合、自由基聚合 和基团转移聚合。 配位聚合在本质上属于阴离子聚合。
二级碳阳离子(仲碳阳离子) 三级碳阳离子(叔碳阳离子)
CH3 CH2 CH2 C CH3
阳离子聚合
3. 链转移和链终止
离子聚合的活性种带有电荷,无法双基终止,因此只能 通过单基终止和链转移终止,也可人为添加终止剂终止。 自由基聚合的链转移一般不终止动力学链,而阳离子聚 合的链转移则有可能终止动力学链。因此阳离子聚合的链终 止只可分为动力学链不终止的链终止反应和动力学链终止的 链终止反应两类。
+ XA
ktr,s kp
HMnMA + XCR HMnM NR3(CR)
+
NR3
阳离子聚合
CH3 CH3 (BF3OH) + H2O CH3 CH3 OH + H (BF3OH) H 2O H [ CH2 C ] n CH2 C CH3 CH3 H [ CH2 C ] n CH2 C CH3 CH3
离子聚合
引言
离子聚合是又一类连锁聚合。它的活性中心为离子。根 据活性中心的电荷性质,可分为阳离子聚合和阴离子聚合。 多数烯烃单体都能进行自由基聚合,但是离子聚合却有 极高的选择性。原因是离子聚合对阳离子和阴离子的稳定性 要求比较严格。例如只有带有1,1—二烷基、烷氧基等强推 电子的单体才能进行阳离子聚合;带有腈基、羰基等强吸电 子基的单体才能进行阴离子聚合。但含有共轭体系的单体, 如苯乙烯、丁二烯等,则由于电子流动性大,既可进行阳离 子聚合,也能进行阴离子聚合。
离子聚合
离子聚合的发展导致了活性聚合的诞生。这是高分子发 展史上的重大转折点。通过阴离子活性聚合,可实现高分子 的分子设计,制备预定结构和分子量的聚合物。 阴离子活性聚合在制备特殊结构的嵌段共聚物、接枝共 聚物、星状聚合物等方面有十分重要的作用。 目前,活性聚合领域已扩展到阳离子聚合、自由基聚合 和基团转移聚合。 配位聚合在本质上属于阴离子聚合。
阴离子聚合要点课件

05
阴离子聚合的应用与实例
高分子合成中的应用
合成橡胶
阴离子聚合可用于合成橡胶,如 丁基橡胶、异戊橡胶等,具有高
弹性、耐油、耐老化等特性。
合成纤维
通过阴离子聚合可以制备高性能纤 维,如聚酯纤维、聚酰胺纤维等, 具有高强度、高模量等特点。
合成粘合剂
阴离子聚合可以合成各种粘合剂, 如聚氨酯、环氧树脂等,具有粘附 力强、耐久性好等特点。
如丙烯、异丁烯等,由于 它们具有不饱和碳-碳双键 ,能够进行阴离子聚合。
共轭烯烃单体
如苯乙烯、丁二烯等,这 些单体在阴离子聚合条件 下可以生成高分子量聚合 物。
环状单体
如环己烯、环戊烯等,这 些单体在阴离子聚合条件 下可以生成环状聚合物。
阴离子聚合的引发剂
烷基锂引发剂
如正丁基锂、苯基锂等, 是常用的阴离子聚合引发 剂。
03
在使用引发剂时,应遵循安全操作规程,避免与空 气和水接触,以免发生危险。
04
阴离子聚合的影响因素
温度的影响
温度对阴离子聚合速率有显著影响。 随着温度的升高,聚合速率通常会增 加,因为高温可以促进活性种的生成 和链增长。
然而,过高的温度可能导致聚合体系 不稳定,引发链转移反应和链断裂, 从而降低聚合物分子量和分子量分布 。
结合形成增长链。
阴离子聚合的机理具有高度的可逆性, 这使得聚合反应可以在较低的温度下进 行,同时也有利于控制聚合产物的分子
量和分子量分布。
阴离子聚合的活性中心可以通过不同的 引发剂来控制,例如有机金属化合物、
碱金属和碱金属化合物等。
阴离子聚合的动力学
阴离子聚合的动力学主要受聚合温度、单体浓度、引发剂浓度等 因素的影响。在聚合过程中,聚合速率随着单体浓度的增加而增 加,但同时也受到引发剂浓度的限制。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
H2C CH
H2C
CH3 C CO
H2C CH CH CH2
O CH3
AN 硝基乙烯 St MMA
BD
吸电子基团并不具有-共轭体系,则不能进行阴 离子聚合,如VC,因p-共轭效应和诱导效应相反,削 弱了双键电子云密度下降的程度,不利于阴离子进攻。
3
二. 引发体系及引发作用
1. 碱金属引发 碱金属外层只有一个价电子,容易直接转移给单体
CH2
CH2
CH - Na +
双阴离子 活性中心
6
(2) 电子间接转移引发
碱金属将电子转移给中间体,形成自由基-阴离子,再将
活性中心转移给单体,例如:萘钠在四氢呋喃(THF)
中引发苯乙烯(St)
Na +
[
ห้องสมุดไป่ตู้
]
-
. Na
+
(绿色)萘钠
(自由基-阴离子)
e
complex (greenish blue color)
引发剂种类
自由基聚合
偶氮类
采用受热易产生自由基的物质作为 过氧类
引发剂
氧化还原体系
引发剂的性质只影响引发反应,用量影响 Rp和
离子聚合
采用容易产生活性离子的物质作为引发剂 阳离子聚合:亲电试剂,主要是Lewis酸,需共引发剂
阴离子聚合:亲核试剂,主要是碱金属及金属有机化合物
17
引发剂中的一部分,在活性中心近旁成为反离子 其形态影响聚合速率、分子量、产物的立构规整性
带正电荷的Li+则作为反离子与带部分负电荷的碳原子形 成离子对,从而完成链引发过程。丁基锂属于单阴离子引发 。
9
三、阴离子聚合机理无终止聚合 阴离子聚合反应是一种连锁聚合反应,也包括
链引发、链增长和链终止三个基元反应。 1 链引发
(1) 阴离子加成引发
按引发阴离子与阳离子的离解程度,分2种:
(i)自由离子
11
2 链增长 (1)阴离子聚合的链增长反应
α-烯烃分子
离子对
阴离子活性链
经过极化的α-烯烃分子“插入”碳负离子与反离子(即引发剂碱金属阳 离子)之间形成的离子对,从而完成一步加成聚合过程,这样的加成聚合反 应不间断地反复进行下去即生成聚合度很高的阴离子活性链。不过,由于 在不同极性的溶剂中起引发作用的活性阴离子存在不同的离子形态,所以 它们引发的阴离子聚合链增长反应方式有所不同。
单体结构
自由基聚合 带有弱吸电子基的乙烯基单体 共轭烯烃
离子聚合 对单体有较高的选择性
阳离子聚合:带有强推电子取代基的烯类单体 共轭烯烃(活性较小)
阴离子聚合:带有强吸电子取代基的烯类单体 共轭烯烃 环状化合物、羰基化合物
18
溶剂的影响
自由基聚合
向溶剂链转移,降低分子量 笼蔽效应,降低引发剂效率 f 溶剂加入,降低了[M],Rp略有降低 水也可作溶剂,进行悬浮、乳液聚合
由于阴离子聚合反应活性中心具有与活泼氢(质子) 反应的强烈倾向,因此凡是含有活泼氢的物质如醇、 酸、水等均能够使活性阴离子链发生转移反应而终止 。向质子性物质转移终止,例如:
13
生成活性低于原来使用的引发剂(如LiBu)的醇锂 或氢氧化锂,起阻聚剂的作用而使反应停止。
因此,对于理想的阴离子聚合体系如果不外加链终止剂 或链转移剂,一般不存在链转移反应与链终止反应。
烷、四氢呋喃等(既可以进行阴离子聚合,也可以进 行阳离子聚合)。 以第一、二种是最重要和最常见的。
2
具有吸电子取代基的烯类单体原则上可以进行 阴离子聚合,能否聚合取决于两种因素
是否具有-共轭体系
带有吸电子基团并具有-共轭体系的单体能够进
行阴离子聚合,如:
H2C CH CN
H2C CH
N OO
本科●
Macromolecular
Chemistry & Physics
高分子化学与物理
主讲:化学化工学院 聂康明 教授
教材:董炎明主编《高分子科学简明教程》
1
2.4 阴离子聚合
一、阴离子聚合单体
(1) 带吸电子取代基的α-烯烃; (2) 带共轭取代基的α-烯烃; (3) 某些含杂原子(如O、N杂环)的化合物如环氧乙
14
为什么阴离子聚合可为活性聚合?
在阴离子聚合反应中,带相同电荷的活性链离 子不能发生双基终止;
活性链负碳离子的反离子常为金属离子,而不是 原子团,它一般不能夺取链中的某个原子或H+而终 止,活性链通过脱去H-离子发生链终止又很困难, 所以当体系中没有引起链转移或链终止的杂质时, 实际上是无终止聚合,即活性聚合。
萘和钠在THF溶剂中反应生成萘钠;萘钠在极性
溶剂中是均相体系,碱金属的利用率高。
7
2. 有机金属化合物引发
(1)金属氨基化合物
是研究得最早的一类阴离子聚合引发剂,重要通过 自由阴离子方式引发聚合反应,主要有 NaNH2- 液氨、KNH2 -液氨体系
2 K + 2 NH3
2 KNH2 + H2
KNH2
阻聚剂种类
自由基聚合:氧、DPPH、苯醌 阳离子聚合:极性物质水、醇,碱性物质,苯醌 阴离子聚合:极性物质水、醇,酸性物质,CO2
21
12
3 链终止
自由基聚合中,因为带有独电子的活泼自由基
具有配对成键的强烈倾向,其链终止反应多以双基
歧化或双基偶合的方式进行;
在阴离子聚合反应中,由于带有相同负电荷 的两个阴离子之间不可能进行双基终止,所以只 能与体系中的其他杂质进行所谓“单基终止”, 即发生转移反应而终止。这是离子型聚合链终止 反应与自由基聚合链终止反应的最大区别。
或中间体,生成阴离子引发聚合,叫电子转移引发。 按引发机理,具体可分为: 电子直接转移引发和电子间接转移引发。
4
(1) 电子直接转移引发
Na + CH2 CH X
Na CH2 CH X
Na CH CH2
X
单体自由基-阴离子
Na原子最外层电子转移给单体,生成单体自由 基-阴离子;
2 Na CH CH2
15
微量杂质,如水、氧、二氧化碳,都易使碳 阴离子终止,因此,阴离子聚合必须在高真 空或惰性气氛下、试剂和玻璃器皿非常洁净 的条件下进行。
在聚合末期,加入链转移剂(水、醇、酸、胺) 可使活性聚合物终止 有目的的加入CO2、环氧乙烷、二异氰酸酯可获 得指定端基聚合物。
16
离子聚合与自由基聚合特征区别
离子聚合
溶剂的极性和溶剂化能力,对活性种的形态有较 大影响:离子对、自由离子
影响到 Rp、Xn 和产物的立构规整性 溶剂种类 阳:卤代烃、CS2、液态SO2、CO2
阴:液氨、醚类 (THF、二氧六环)
19
反应温度
自由基聚合:取决于引发剂的分解温度,50 ~ 80 ℃
离子聚合:引发活化能很小
为防止链转移、重排等副反应,在低温聚合 阳离子聚合常在-70 ~ -100 ℃进行
Na CH CH2 CH2 CH Na
X
X
X
双阴离子活性中心
2个自由基末端迅速偶合终止,生成双阴离 子,而后从两端阴离子引发单体聚合。
5
碱金属不溶于溶剂,属非均相体系,利用率低
例如:
e
Na + H2C CH
electron transfer
. CH2 CH- Na +
苯乙烯自由 基-阴离子
dimerize Na + -CH radical couple
[
] .- Na + + H2C CH
electron transfer
. CH2 CH- Na + +
萘钠阴离子将电子转移给苯乙烯,苯乙烯自由基-阴离子(红色)
radical couple Na + -CH CH2 CH2 CH - Na + dimerize
2个苯乙烯自由基-阴离子 再偶合成苯乙烯双阴离子
K + NH2
NH2 + CH2 CH
H2N CH2 CH
形成自由阴离子 聚合引发体系, 属于单阴离子
8
(2)金属烷基化合物
——最常用的阴离子聚合引发剂
CH3CH2CH2CH2
Li +
(n-BuLi)
initiation
β+ α-
+ H2C CH
n-BuCH2 CH - Li +
具有共价键的碱金 属烷基化合物在溶剂 的作用下,带负电荷 的烷基进攻α-烯烃分 子中带有部分正电荷 的β碳原子;
Nu + CH2=CHX
Nu CH2 CH X
如在极性溶剂中,引发阴离子与单体的简单加成产 生,引发剂主要以自由离子的形式存在:
10
(ii)紧密离子对
R Li + CH2=CHX
R Li CH2 CHX
R CH2 CHL i X
π-复合物
如在非极性溶剂中,引发剂主要以紧离子对 的形式存在,一般认为其引发反应先形成引发 剂与单体的π-复合物,再引发聚合。
聚合机理
自由基聚合:多为双基终止 双基偶合 Rp [I] 1/2
双基歧化
离子聚合:具有相同电荷,不能双基终止 阳:向单体、反离子、链转移剂终止
无自加速现象 Rp [C]
阴:往往无终止,活性聚合物,添加其它试剂终止
20
机理特征:
自由基聚合:慢引发、快增长、速终止、可转移 阳离子聚合:快引发、快增长、易转移、难终止 阴离子聚合:快引发、慢增长、无终止
