(完整版)电化学曲线极化曲线阻抗谱分析
电化学曲线极化曲线阻抗谱分析

交流电导法:通过测量电导来 计算阻抗
阻抗谱的等效电路分析
等效电路的概念和组成 电容、电感、电阻等元件的特性与作用 等效电路的阻抗谱分析方法 阻抗谱在等效电路分析中的应用实例
05 应用实例与案例分析
阻抗谱在电化学反应中的应用
阻抗谱在电化学反应中的应用:阻抗谱可以用于研究电化学反应的动力学 过程,如电极反应速率常数、电荷传递系数等。
阻抗谱分析可以 用于评估不同电 极材料和电解质 的性能,为电池 材料的选择提供 依据
阻抗谱在电镀和金属表面处理中的应用
阻抗谱用于研究电镀过程中电 化学反应的动力学
阻抗谱能够评估金属表面处理 的效率和效果
阻抗谱在电镀和金属表面处理 中应用的实际案例分析
阻抗谱在电镀和金属表面处理 中的优势和局限性
06 实验技术与实践操作
极化类型与反应机理
极化类型:电化 学极化、浓差极 化、化学极化
反应机理:电化 学反应过程和影 响因素
测定方法:线性 扫描伏安法、循 环伏安法、计时 电流法等
分析方法:根据测 定的极化曲线,分 析电化学反应速率 常数、反应机理等
04 阻抗谱分析原理与技术
阻抗谱基本概念
定义:阻抗谱分 析是一种电化学 测量技术,通过 测量电极系统的 阻抗随正弦波频 率变化来研究电 极系统的电化学
实验设备与试剂准备
实验设备:电化学工作站、电解池、电极等 试剂准备:电解质溶液、参比电极、辅助电极等 注意事项:确保设备完好、试剂纯度及浓度准确 实验前准备:清洗电极、检查电解池密封性等
实验操作流程与注意事项
实验前准备:检查仪器设 备是否完好,准备所需试 剂和电极
数据采集:按照预设条件 进行实验,记录实验数据
未来发展方向:结合人工智能和机器学习算法,实现阻抗谱数据的快速 处理和解析 展望:阻抗谱技术将在电化学测量领域发挥越来越重要的作用,为解决 能源、环境等问题提供有力支持
电化学阻抗谱分析PPT课件

• 定义
以小振幅的正弦波电势(或电流)为扰动信 号,使电极系统产生近似线性关系的响应, 测量电极系统在很宽频率范围的阻抗谱,以 此来研究电极系统的方法就是电化学阻抗法 (AC Impedance),现称为电化学阻抗谱。
哈尔滨工业大学(威海)
引言
• 定义
G
X
Y
G=Y/X
对于一个稳定的线性系统M,如以一个角频 率为ω的正弦波电信号X(电压或电流)输入 该系统,相应的从该系统输出一个角频率为 ω的正弦波电信号Y(电流或电压),此时电 极系统的频响函数G就是电化学阻抗。
在腐蚀科学研究中的应用
以小振幅的正弦波电势(或电流)为扰动信号,使电极系统产生近似线性关系的响应,测量电极系统在很宽频率范围的阻抗谱,以此
元件外面的括号总数为奇数时,该元件的第一层运 来研究电极系统的方法就是电化学阻抗法(AC Impedance),现称为电化学阻抗谱。
一般认为,出现这种半圆向下压扁的现象,亦即通常说的阻抗半圆旋转现象的原因与电极/电解液界面性质的不均匀性有关。
哈尔滨工业大学(威海)
6.1 有关复数和电工学知识-复数
1 复数的概念
(1)复数的模
Z Z '2 Z ''2
(2)复数的辐角(即相位角)
arctg Z ''
Z'
哈尔滨工业大学(威海)
6.1 有关复数和电工学知识-复数
(3)虚数单位乘方
j 1 j2 1 j3 j
(4)共轭复数
Z Z ' jZ '' Z Z ' jZ ''
6·3平面电极的有限层扩散阻 抗(等效元件0) 6·4平面电极的阻挡层扩散阻 抗(等效元件T) 6·5球形电极W
电化学曲线极化曲线阻抗谱分析
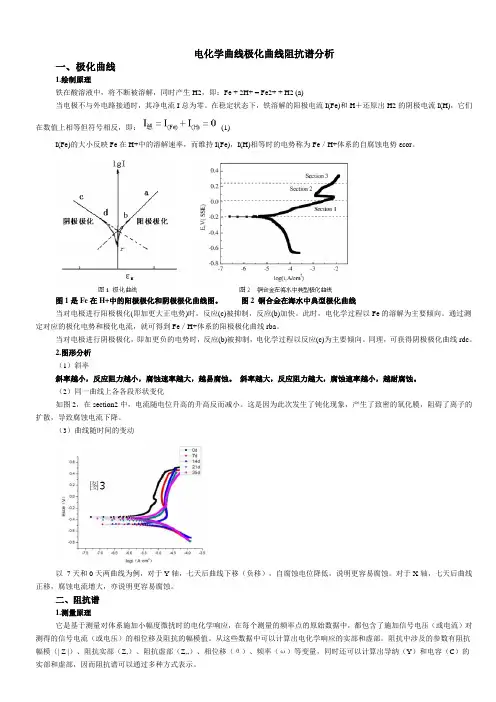
电化学曲线极化曲线阻抗谱分析一、极化曲线1.绘制原理铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流I(Fe)和H+还原出H2的阴极电流I(H),它们在数值上相等但符号相反,即:(1)I(Fe)的大小反映Fe在H+中的溶解速率,而维持I(Fe),I(H)相等时的电势称为Fe/H+体系的自腐蚀电势εcor。
图1是Fe在H+中的阳极极化和阴极极化曲线图。
图2 铜合金在海水中典型极化曲线当对电极进行阳极极化(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以Fe的溶解为主要倾向。
通过测定对应的极化电势和极化电流,就可得到Fe/H+体系的阳极极化曲线rba。
当对电极进行阴极极化,即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
同理,可获得阴极极化曲线rdc。
2.图形分析(1)斜率斜率越小,反应阻力越小,腐蚀速率越大,越易腐蚀。
斜率越大,反应阻力越大,腐蚀速率越小,越耐腐蚀。
(2)同一曲线上各各段形状变化如图2,在section2中,电流随电位升高的升高反而减小。
这是因为此次发生了钝化现象,产生了致密的氧化膜,阻碍了离子的扩散,导致腐蚀电流下降。
(3)曲线随时间的变动以7天和0天两曲线为例,对于Y轴,七天后曲线下移(负移),自腐蚀电位降低,说明更容易腐蚀。
对于X轴,七天后曲线正移,腐蚀电流增大,亦说明更容易腐蚀。
二、阻抗谱1.测量原理它是基于测量对体系施加小幅度微扰时的电化学响应,在每个测量的频率点的原始数据中,都包含了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值。
从这些数据中可以计算出电化学响应的实部和虚部。
阻抗中涉及的参数有阻抗幅模(| Z |)、阻抗实部(Z,)、阻抗虚部(Z,,)、相位移(θ)、频率(ω)等变量,同时还可以计算出导纳(Y)和电容(C)的实部和虚部,因而阻抗谱可以通过多种方式表示。
电化学阻抗谱原理应用及谱图分析

电化学阻抗谱原理应用及谱图分析电化学阻抗谱原理应用及谱图分析电化学阻抗谱(Electrochemical Impedance Spectroscopy,EIS)是一种测量电化学系统的电化学行为的方法,它通过测量系统对于正弦电压或电流的响应,来研究电化学反应过程中的阻抗变化。
EIS广泛应用于材料科学、化学工程、电池研究、腐蚀研究和生物医学等领域。
EIS的原理是利用正弦电压或电流去激励待测电化学系统,并测量响应信号的振幅和相位,然后将这些数据在频率域或时间域中进行分析,从而得到电化学系统的等效电路模型,如电阻、电容、电感等等,这些参数可以反映出系统的结构、特性和电化学反应的动力学信息。
EIS的主要作用是在电化学反应的过程中研究电荷传递、离子传输、质量传递等复杂的反应机理,可以通过建立电化学反应动力学模型,分析电极表面化学反应动力学参数,优化电极材料和电解液配方,提高电化学反应效率。
以下是两个例子,说明EIS的应用及注意事项:锂离子电池的研究:EIS广泛应用于电池的研究和开发中,通过测量电池的电化学阻抗谱来评估电池的性能和寿命。
例如,在锂离子电池中,电解质的性质和电极材料的表面形貌对电池性能有很大影响。
利用EIS可以评估电池的内部电阻、扩散系数等参数,进而优化电池设计和材料配方。
注意事项是,需要确保电池在测量时处于稳态,并控制好测量温度和电压等参数。
金属腐蚀的研究:EIS也被广泛应用于金属腐蚀的研究中,通过测量金属表面的电化学阻抗谱,可以评估金属表面的保护膜的质量和稳定性,了解金属腐蚀的机制,同时也可以评估防腐涂层的性能。
注意事项是,需要确保测量条件稳定,避免干扰,同时应选择合适的电解液和电极材料。
电化学阻抗谱(EIS)的谱图是通过测量电化学系统对于正弦电压或电流的响应所得到的。
谱图提供了电化学系统的等效电路模型,这些参数可以反映出系统的结构、特性和电化学反应的动力学信息。
在谱图的分析过程中,需要注意以下几点:峰的位置和形状:电化学阻抗谱中的峰代表电化学体系中不同的特征和反应机理。
电化学阻抗谱分析详解68页PPT

56、死去何所道,托体同山阿。 57、春秋多佳日,登高赋新诗。 58、种豆南山下,草盛豆苗稀。晨兴 理荒秽 ,带月 荷锄归 。道狭 草木长 ,夕露 沾我衣 。衣沾 不足惜 ,但使 愿无违 。 59、相见无杂言,但道桑麻长。 60、迢迢新秋夕,亭亭月将圆。
56、书不仅是生活,而且是现在、过 去和未 来文化 生活的 源泉。 ——库 法耶夫 57、生命不可能有两次,但许多人连一 次也不 善于度 过。— —吕凯 特 58、问渠哪得清如许,为有源头活水来 。—— 朱熹 59、我的努力求学没有得到别的好处, 只不过 是愈来 愈发觉 自己的 无知。 ——笛 卡儿
拉
60、生活的道路一旦选定,
最新电化学曲线极化曲线阻抗谱分析
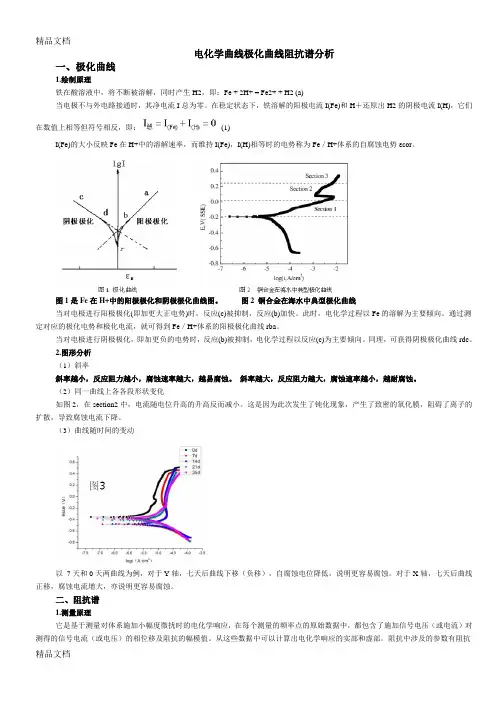
电化学曲线极化曲线阻抗谱分析一、极化曲线1.绘制原理铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流I(Fe)和H+还原出H2的阴极电流I(H),它们在数值上相等但符号相反,即:(1)I(Fe)的大小反映Fe在H+中的溶解速率,而维持I(Fe),I(H)相等时的电势称为Fe/H+体系的自腐蚀电势εcor。
图1是Fe在H+中的阳极极化和阴极极化曲线图。
图2 铜合金在海水中典型极化曲线当对电极进行阳极极化(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以Fe的溶解为主要倾向。
通过测定对应的极化电势和极化电流,就可得到Fe/H+体系的阳极极化曲线rba。
当对电极进行阴极极化,即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
同理,可获得阴极极化曲线rdc。
2.图形分析(1)斜率斜率越小,反应阻力越小,腐蚀速率越大,越易腐蚀。
斜率越大,反应阻力越大,腐蚀速率越小,越耐腐蚀。
(2)同一曲线上各各段形状变化如图2,在section2中,电流随电位升高的升高反而减小。
这是因为此次发生了钝化现象,产生了致密的氧化膜,阻碍了离子的扩散,导致腐蚀电流下降。
(3)曲线随时间的变动以7天和0天两曲线为例,对于Y轴,七天后曲线下移(负移),自腐蚀电位降低,说明更容易腐蚀。
对于X轴,七天后曲线正移,腐蚀电流增大,亦说明更容易腐蚀。
二、阻抗谱1.测量原理它是基于测量对体系施加小幅度微扰时的电化学响应,在每个测量的频率点的原始数据中,都包含了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值。
从这些数据中可以计算出电化学响应的实部和虚部。
阻抗中涉及的参数有阻抗幅模(| Z |)、阻抗实部(Z,)、阻抗虚部(Z,,)、相位移(θ)、频率(ω)等变量,同时还可以计算出导纳(Y)和电容(C)的实部和虚部,因而阻抗谱可以通过多种方式表示。
电化学阻抗谱及其数据处理与解析ppt课件
线性条件
由于电极过程的动力学特点,电极过程速度随 状态变量的变化与状态变量之间一般都不服从 线性规律。只有当一个状态变量的变化足够小, 才能将电极过程速度的变化与该状态变量的关 系作线性近似处理。故为了使在电极系统的阻 抗测量中线性条件得到满足,对体系的正弦波 电位或正弦波电流扰动信号的幅值必须很小, 使得电极过程速度随每个状态变量的变化都近 似地符合线性规律,才能保证电极系统对扰动 的响应信号与扰动信号之间近似地符合线性条 件。
电化学阻抗谱方法是一种以小振幅的 正弦波电位(或电流)为扰动信号的电化 学测量方法。由于以小振幅的电信号对体 系扰动,一方面可避免对体系产生大的影 响,另一方面也使得扰动与体系的响应之 间近似呈线性关系,这就使测量结果的数 学处理变得简单。
同时,电化学阻抗谱方法又是一种频 率域的测量方法,它以测量得到的频率范 围很宽的阻抗谱来研究电极系统,因而能 比其他常规的电化学方法得到更多的动力 学信息及电极界面结构的信息。
规则(1):
凡由等效元件串联组成 的复合元件,将这些等 效元件的符号并列表示; 凡由等效元件并联组成 的复合元件,用括号内 并列等效元件的符号表 示。如图中的复合等效 元 件 , 可 以 用 符 号 RLC 或CLR表示 。
规则(2):
凡由等效元件并联组成的 复合元件,用括号内并列 等效元件的符号表示。例 如图中的复合等效元件以 符号(RLC)表示。
Circuit Description Code (CDC)
阻纳数据的非线性最小二乘法拟合原理
一般数据的非线性拟合的最小二乘法
非线若性函G是数变,量且X已和知m函个数参的量具C体1,表C达2,式:…,Cm的
G = G( X,C1,C2,…,Cm )
测 线到性在n拟个控合测制就量变是值量要(X根n的据>数这m值n)个为:测Xg1量,1,值Xg来22,,估……定,,mXg个nn时参。, 非量
(完整版)电化学曲线极化曲线阻抗谱分析
电化学曲线极化曲线阻抗谱分析一、极化曲线1.绘制原理铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流I(Fe)和H+还原出H2的阴极电流I(H),它们在数值上相等但符号相反,即:(1)I(Fe)的大小反映Fe在H+中的溶解速率,而维持I(Fe),I(H)相等时的电势称为Fe/H+体系的自腐蚀电势εcor。
图1是Fe在H+中的阳极极化和阴极极化曲线图。
图2 铜合金在海水中典型极化曲线当对电极进行阳极极化(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以Fe的溶解为主要倾向。
通过测定对应的极化电势和极化电流,就可得到Fe/H+体系的阳极极化曲线rba。
当对电极进行阴极极化,即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
同理,可获得阴极极化曲线rdc。
2.图形分析(1)斜率斜率越小,反应阻力越小,腐蚀速率越大,越易腐蚀。
斜率越大,反应阻力越大,腐蚀速率越小,越耐腐蚀。
(2)同一曲线上各各段形状变化如图2,在section2中,电流随电位升高的升高反而减小。
这是因为此次发生了钝化现象,产生了致密的氧化膜,阻碍了离子的扩散,导致腐蚀电流下降。
(3)曲线随时间的变动以7天和0天两曲线为例,对于Y轴,七天后曲线下移(负移),自腐蚀电位降低,说明更容易腐蚀。
对于X轴,七天后曲线正移,腐蚀电流增大,亦说明更容易腐蚀。
二、阻抗谱1.测量原理它是基于测量对体系施加小幅度微扰时的电化学响应,在每个测量的频率点的原始数据中,都包含了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值。
从这些数据中可以计算出电化学响应的实部和虚部。
阻抗中涉及的参数有阻抗幅模(| Z |)、阻抗实部(Z,)、阻抗虚部(Z,,)、相位移(θ)、频率(ω)等变量,同时还可以计算出导纳(Y)和电容(C)的实部和虚部,因而阻抗谱可以通过多种方式表示。
化学检验工常见电化学涂层性能测试方法
化学检验工常见电化学涂层性能测试方法电化学涂层是一种常见的表面处理方法,可用于增加材料的耐腐蚀性能、改善导电性能等。
为了确保电化学涂层的质量,需要进行一系列的性能测试。
本文将介绍几种常见的电化学涂层性能测试方法。
1. 腐蚀性能测试电化学腐蚀测试是评估电化学涂层耐腐蚀性能的重要方法之一。
常用的测试方法包括极化曲线法和电化学阻抗谱法。
(1)极化曲线法极化曲线法是一种通过测量极化曲线来评估电化学涂层在腐蚀环境中的抗腐蚀性能的方法。
通过应用一定电位范围内的电流,可以观察到电流随电位的变化关系,从而评估涂层的耐腐蚀性能。
(2)电化学阻抗谱法电化学阻抗谱法是一种通过测量电化学阻抗谱曲线来评估电化学涂层耐腐蚀性能的方法。
该方法可以得到频率范围内的电阻和电容数值,通过分析这些数据可以评估涂层的耐腐蚀性能。
2. 导电性能测试导电性能是衡量电化学涂层质量的关键指标之一。
常用的测试方法有四探针法和电阻率测量法。
(1)四探针法四探针法是一种通过测量电阻来评估电化学涂层导电性能的方法。
在该方法中,四个探针被插入涂层中,通过测量电流和电阻的关系,可以计算涂层的电导率和电阻率。
(2)电阻率测量法电阻率测量法是一种通过测量涂层材料的电阻来评估导电性能的方法。
该方法使用导电传感器在涂层表面上测量电阻,通过计算电阻率可以评估涂层的导电性能。
3. 附着力测试附着力是评估电化学涂层质量的重要指标之一。
常用的测试方法包括划伤测试、拉伸测试和冲击测试。
(1)划伤测试划伤测试是一种通过使用硬度指针在涂层表面划伤,从而评估涂层与基材之间的附着力的方法。
通过观察划痕形状和痕迹深度,可以评估涂层的附着力。
(2)拉伸测试拉伸测试是一种通过施加拉伸力来评估涂层与基材之间的附着力的方法。
通过在涂层上施加力并测量力的变化,可以计算涂层与基材的附着力。
(3)冲击测试冲击测试是一种通过施加冲击力来评估涂层与基材之间的附着力的方法。
常用的冲击测试方法包括钢球落锤测试和冲击炮测试,通过观察涂层破损情况可以评估附着力。
电化学曲线极化曲线阻抗谱分析
电化学曲线极化曲线阻抗谱分析一、极化曲线1.绘制原理铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流在数值上相等但符号相反,即: 1 1 - 12.图形分析(1)斜率斜率越小,反应阻力越小,腐蚀速率越大,越易腐蚀。
(2)同一曲线上各各段形状变化如图2,在section2中,电流随电位升高的升高反而减小。
这是因为此次发生了钝化现象,产生了致密的氧化膜,阻碍了离子的扩散,导致腐蚀电流下降。
(3)曲线随时间的变动以7天和0天两曲线为例,对于Y轴,七天后曲线下移(负移),自腐蚀电位降低,说明更容易腐蚀。
对于X轴,七天后曲线正移,腐蚀电流增大,亦说明更容易腐蚀。
二、阻抗谱1.测量原理它是基于测量对体系施加小幅度微扰时的电化学响应,在每个测量的频率点的原始数据中,都包含了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值。
从这些数据中可以计算出电化学响应的实部和虚部。
阻抗中涉及的参数有阻抗幅模(I Z |)、阻抗实部(Z,)、阻抗虚部(乙,)、相位移(B )、频率(3)等变量,同时还可以计算出导纳(Y)和电容(C)的实部和虚部,因而阻抗谱可以通过多种方式表示。
I(Fe)的大小反映而维持I(Fe), I(H)相等时的电势称为Fe/H+体系的自腐蚀电势& corFe在H+中的溶解速率,图丄极化曲线图1是Fe在H+中的阳极极化和阴极极化曲线图。
当对电极进行阳极极化定对应的极化电势和极化电流,当对电极进行阴极极化,图2铜合金在海水中典型极化曲线(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以就可得到Fe/ H+体系的阳极极化曲线rba。
即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
Fe的溶解为主要倾向。
通过测同理,可获得阴极极化曲线rdc。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电化学曲线极化曲线阻抗谱分析
一、极化曲线
1.绘制原理
铁在酸溶液中,将不断被溶解,同时产生H2,即:Fe + 2H+ = Fe2+ + H2 (a)
当电极不与外电路接通时,其净电流I总为零。
在稳定状态下,铁溶解的阳极电流I(Fe)和H+还原出H2的阴极电流I(H),它们在数值上相等但符号相反,即:(1)
I(Fe)的大小反映Fe在H+中的溶解速率,而维持I(Fe),I(H)相等时的电势称为Fe/H+体系的自腐蚀电势εcor。
图1是Fe在H+中的阳极极化和阴极极化曲线图。
图2 铜合金在海水中典型极化曲线
当对电极进行阳极极化(即加更大正电势)时,反应(c)被抑制,反应(b)加快。
此时,电化学过程以Fe的溶解为主要倾向。
通过测定对应的极化电势和极化电流,就可得到Fe/H+体系的阳极极化曲线rba。
当对电极进行阴极极化,即加更负的电势时,反应(b)被抑制,电化学过程以反应(c)为主要倾向。
同理,可获得阴极极化曲线rdc。
2.图形分析
(1)斜率
斜率越小,反应阻力越小,腐蚀速率越大,越易腐蚀。
斜率越大,反应阻力越大,腐蚀速率越小,越耐腐蚀。
(2)同一曲线上各各段形状变化
如图2,在section2中,电流随电位升高的升高反而减小。
这是因为此次发生了钝化现象,产生了致密的氧化膜,阻碍了离子的扩散,导致腐蚀电流下降。
(3)曲线随时间的变动
以7天和0天两曲线为例,对于Y轴,七天后曲线下移(负移),自腐蚀电位降低,说明更容易腐蚀。
对于X轴,七天后曲线正移,腐蚀电流增大,亦说明更容易腐蚀。
二、阻抗谱
1.测量原理
它是基于测量对体系施加小幅度微扰时的电化学响应,在每个测量的频率点的原始数据中,都包含了施加信号电压(或电流)对测得的信号电流(或电压)的相位移及阻抗的幅模值。
从这些数据中可以计算出电化学响应的实部和虚部。
阻抗中涉及的参数有阻抗幅模(| Z |)、阻抗实部(Z,)、阻抗虚部(Z,,)、相位移(θ)、频率(ω)等变量,同时还可以计算出导纳(Y)和电容(C)的实部和虚部,因而阻抗谱可以通过多种方式表示。
2. Bode图
Bode图是阻抗幅模的对数log| Z |和相角θ对相同时间的横坐标频率的对数logf的图。
图4 Bode图
阻抗:如果X是角频率为ω的正弦波电流信号,则Y即为角频率也是ω的正弦电势信号。
此时Y/X既称为系统的阻抗,用Z表示。
1.溶液电阻(Rs)
2.双电层电容(Cdl)
3.极化阻抗(Rp)
4.电荷转移电阻(Rct)
5.扩散电阻(Zw)
6.界面电容(C)
7.电感(L)
图6 两个时间常数
3. Nyquist图
电极的交流阻抗由实部z’和虚部z”组成,z=z’+j z”.Nyquist图是以阻抗虚部(-z”)对阻抗实部(z’)作的图。
对纯电阻,在Nyquist图上表现为z’轴上的一点,该点到原点的距离为电阻值的大小;对纯电容体系,表现为与z”轴重合的一条直线。
图中的半圆弧就是容抗弧;后面的斜线是W扩散;感抗是低频的时候一个向下的收缩环。
圆弧半径越大,也就是极化电阻越大,耐腐蚀越好。
圆弧半径越小,也就是极化电阻越小,耐腐蚀越差。
通过控制电极电位或者电流密度的值,测定相应的电流密度或者电位的变化而得到的电极电位与电流密度的关系曲
线,被称为极化曲线。
1.典型的、用来测试电极腐蚀速度的动电位极化曲线包括线性极化区、弱极化区和强极化区。
在强极化区,极化曲线(e-logi 图)基本是条直线,这条直线可以用来得到电极的腐蚀速度,而强极化区又叫Tafel区,所以,在不严格的说法中(通常是学生之间进行交流),说“做个强极化曲线”、“做个Tafel曲线”(只在小木虫听到),意思是做个动电位极化曲线,而曲线要极化程度够大,进入Tafel区。
2.在不同体系中,动电位极化曲线的形状是不同的。
比如,某些金属的动电位极化曲线在NaCl溶液中,阳极极化80mV就可以进入Tafel区,而在碱性溶液中,却表现出随着极化电位的增加(阳极极化同样超过80mV),极化电流密度反而减少的现象,即进入了钝化区。
动电位极化曲线会有“钝化区”。
这个钝化区和tafel区一样,是动电位极化曲线上的,具有某种特性的一段区间。
极化曲线获取信息
1.腐蚀电位(E corr),腐蚀电流(icorr)
2.获得Tafel参数(阴极极化斜率ba,阳极极化斜率bk)
3.研究防腐蚀机理,可以知道是阳极机制剂、阴极抑制剂或者是混合型抑制剂。
4.通过腐蚀电流可以计算腐蚀抑制效率(IE%=1-i1.corr/i2.corr)
由于本人电化学还不是特别了解,但是最近投了一篇文章,然后收到评委的回信,其内容是:
评委意见:Authors should remove the Ba value of CrN coating in T able 3, which is 1.218 V/dec because of the reliable T afel region is not seen in related figure due to passivation process.
但是看图的话,我感觉阳极有比较明显的塔菲尔区,现在不知如何是好,恳请大家给给意见和对图的看法!非常感谢
塔菲尔的关系是beta = dE/ d(log i)。
但是不能因为E-logi是直线关系就判断塔菲尔区。
正常的塔菲尔斜率应该在0.12V / n 左右。
n是(速率控制步的)电子传递数。
也就是说,beta 最大不会远大于0.12V。
观察阳极曲线,0 ~0.5V 这个区段。
虽然看上去是直线,但是这个斜率有0.5V 那么高,显然已经不是简单的塔菲尔关系了。
而是因为表面钝化(产生氧化/氢氧化膜)而拔高了过电位。
所以,让你去掉阳极的塔菲尔斜率,是因为它不是真正的塔菲尔区。
阻抗谱半径越大说明阻抗越大,相应的腐蚀电流就应该相对较小。
做极化时可能会出现阳极钝化,EIS对电极表面影响很小,是不会产生钝化的。
从我的极化曲线结果图中看不到阳极有钝化现象。
扫描范围看需要,只是为了确定腐蚀电位,腐蚀电流这样的就可以在开路电压正负300mv就差不多了,根据实际测试效果再调整一下。
扫速一般要求比较慢,可能毫伏/秒这样吧,具体可以看看文献是多大。
上至10mV/s,下到0.1mV/s都有的。
工作电极最好能够固定裸露面积,圆形,方形都有,我觉得主要是保证每次测试的浸入面积一样
自腐蚀电流越小,耐蚀性越好,其对应的阻抗谱的弧越大
阻抗测试对样品影响不大而极化会对样品造成破坏,1、一般先测试腐蚀电位,2、做交流阻抗,电位10mv 3、再做极化曲线。
